2. 农业部甘肃耕地保育与农业环境科学观测实验站, 兰州 730070;
3. 土壤与农业可持续发展国家重点实验室(中国科学院南京土壤研究所), 南京 210008
酸性土壤几乎占据了全球可耕地土壤的50%,随着土壤酸化过程的继续进行,面积还在扩大[1-2]。我国南方热带和亚热带地区分布有大面积的酸性土壤,近30年来由于铵态氮肥的过量施用和酸沉降的持续影响,土壤酸化呈加速发展趋势[3-8]。土壤酸化是土壤退化的一个重要方面,是热带亚热带酸性土壤地区制约土壤生产力的主要限制因素。土壤酸化增加了Al毒和Mn毒对作物的危害,降低了P、Mo、B等元素的有效性,造成Ca、Mg、K等盐基性养分离子的亏缺[9]。近年来研究发现,由生物质热解制备的生物质炭是一种高效的酸化土壤改良剂[10-17]。
生物质炭一般呈碱性,具有提高酸化土壤pH和降低土壤酸度的作用[18-19]。它不仅能通过增强酸性土壤自身的抗酸化能力而阻止酸性土壤的复酸化,而且可以降低复酸化过程中Al毒的潜在危害[20]。生物质炭含有丰富的C及作物所需的N、P、K、Ca、Mg等营养元素,可以提高土壤Ca、Mg、K、Na等盐基离子含量而减小土壤酸化带来的危害[21-22]。生物质炭改良酸化土壤过程中,生物质炭的碱性物质中和土壤H+的同时其中的盐基离子会释放出来与交换性H+和交换性Al3+发生阳离子交换反应,使部分交换性Al3+释放进入土壤溶液中,此时生物质炭中的碱中和由于Al3+水解产生的H+,促进溶液中的活性形态铝转变为惰性的Al(OH)3,这是生物质炭增加酸化土壤交换性盐基离子含量、降低土壤交换性酸的主要机制,也是生物质炭改良土壤酸度的主要机制[23]。
经生物质炭改良后的酸性土壤中的盐基离子主要来源于所施用的生物质炭,生物质炭中盐基离子的含量和存在形态影响其改良酸性土壤的能力,但机制尚不明确。为此,本研究通过3个热解温度下制备的玉米秸秆炭对酸性土壤为期1年的改良试验,旨在研究热解温度对玉米秸秆炭盐基离子含量和存在形态的影响,揭示盐基离子K、Na、Ca、Mg在玉米秸秆炭改良酸性土壤中的作用机制,为生物质炭作为高效酸性土壤改良剂的应用提供理论支持。
1 材料与方法 1.1 玉米秸秆炭的制备玉米秸秆采自南京市郊区农田。将秸秆于室温下自然风干,粉碎过1 mm筛后装入陶瓷坩埚中,装满压实,盖上盖子置于马弗炉中于300、500和700 ℃下进行厌氧热解,升温速率为20 ℃/min,热解过程持续4 h[24],待自然冷却至室温后取出研磨过1 mm筛备用,热解过程进行3次重复。
1.2 玉米秸秆炭物理化学性质测定玉米秸秆炭的总K、总Na、总Ca、总Mg含量采用干灰化-酸溶法提取[25],具体操作步骤为:称取0.200 0 g的玉米秸秆炭置于坩埚中,每个处理3次重复。将坩埚盖上盖子置于马弗炉中以20 ℃/min的升温速率加热至200 ℃,并维持1 h,接着以20 ℃/min的升温速率加热至500 ℃,并维持4 h,待马弗炉温度降至室温时取出样品。将灰化产物溶于25.0 ml 1.0 mol/L的标准HCl溶液中,摇匀后过滤备用。取过滤后的酸溶液,火焰光度计法测定K、Na含量,原子吸收分光光度计法测定Ca、Mg含量。玉米秸秆炭的水溶性盐基离子和交换性盐基离子采用文献报道的方法测定[26],具体操作步骤为:称取0.200 0 g的玉米秸秆炭,先用100 ml的去离子水淋洗5次,每次所用去离子水为20 ml,收取滤液并测定其中的K、Na、Ca、Mg含量,即为水溶性盐基离子含量;接着用100 ml 1.0 mol/L的乙酸钠溶液(pH 7)淋洗5次,每次所用乙酸钠溶液为20 ml,收取滤液并测定其中的K、Ca、Mg含量,即为交换性盐基离子含量。
1.3 供试土壤基本性质供试土壤采自安徽郎溪(119°8'E,31°6'N),为第四纪红黏土,0 ~ 10 cm表层土壤,风干过2 mm筛。采用1:2.5的土水比测得土壤的pH为4.31,土壤有机质为16.5 g/kg,CEC为9.36 cmol/kg,交换性H+、Al3+、K+、Na+、Ca2+和Mg2+分别为0.20、5.97、0.53、0.68、4.92和0.35 cmol/kg。
1.4 土壤培养试验玉米秸秆炭的加入量为风干土的1.65%,土壤与炭混合均匀后置于塑料杯中,按田间持水量的70%加入去离子水。塑料杯用保鲜膜封口,并在膜中间留一小孔,以便气体交换并减少水分损失。将塑料杯置于25 ℃的恒温培养箱中培养,每隔3 d称重1次并补充水分,以保持土壤含水量恒定。每个处理重复3次,并设不加玉米秸秆炭的处理作为对照。培养试验持续1年,培养结束后将土壤样品取出风干,研磨过2 mm筛备用。
1.5 土壤交换性酸和交换性盐基测定土壤交换性酸用1.0 mol/L氯化钾(pH 7.0)溶液淋洗,碱滴定法测定[27]。土壤交换性盐基用1.0 mol/L醋酸铵(pH 7.0)浸提,浸提液中的K、Na用火焰光度法测定,Ca、Mg用原子吸收分光光度法测定[27]。
1.6 数据处理数据采用SPSS 15.0软件进行统计分析。
2 结果 2.1 K、Na、Ca、Mg含量玉米秸秆炭中总K、总Na、总Ca、总Mg含量均随热解温度升高显著增加(表 1)。与300 ℃相比,500和700 ℃下总K含量显著增加了50.8%和117%,总Na含量显著增加了16.4%和116%,总Ca含量显著增加了47.4%和136%,总Mg含量显著增加了57.0%和157%。水溶性K、Na和Ca含量随热解温度升高显著增加,水溶性Mg含量随热解温度升高先增加(500 ℃)后下降(700 ℃)。与300 ℃相比,500和700 ℃下水溶性K含量显著增加了72.1%和149%,水溶性Na含量显著增加了67.7%和444%,水溶性Ca含量显著增加了76.1%和134%,水溶性Mg含量显著增加了64.4%和15.6%。交换性K含量随热解温度升高先增加(500 ℃)后下降(700 ℃),交换性Ca和Mg含量随热解温度升高显著增加。与300 ℃相比,500和700 ℃下交换性K含量显著增加了29.3%和18.8%,交换性Ca含量显著增加了31.9%和84.6%,交换性Mg含量显著增加了75.4%和82.1%。
|
|
表 1 300、500和700 ℃下玉米秸秆炭不同形态盐基离子含量 Table 1 Contents of base cations in different forms in corn straw biochars under 300, 500 and 700 ℃ |
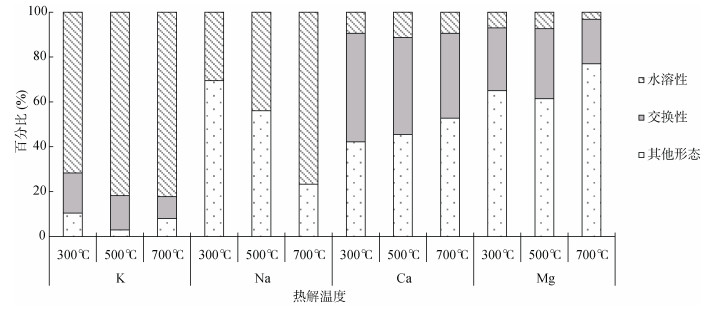
水溶性、交换性和其他形态K、Na、Ca、Mg分别占总K、总Na、总Ca、总Mg的比例见图 1。随热解温度升高,水溶性K和Na所占比例分别从71.7%升高到82.2%和从30.5%升高到76.7%。水溶性Ca和Mg所占比例从300 ℃到500 ℃表现为增加,分别从9.45%升高到11.3%和从7.03%升高到7.36%,500 ℃时所占比例最大;从500 ℃到700 ℃时表现为降低,700 ℃时所占比例降至最低,分别为9.39%和3.17%。随热解温度升高,交换性K和Ca所占比例分别从17.9%降低到9.78%和从48.3%降低到37.8%。交换性Mg所占比例从300 ℃到500 ℃时表现为增加,从28.0%增加到31.2%,500 ℃时所占比例最大;从500 ℃到700 ℃时表现为降低,700 ℃时所占比例降至最低,为19.8%。
|
图 1 不同形态盐基离子占某一盐基离子总量比例 Fig. 1 Percentages of base cations in different forms to the corresponding total base cation |
3个热解温度下,水溶性K、Na、Ca、Mg分别占总K、总Na、总Ca、总Mg的比例范围为71.7% ~ 82.2%、30.5% ~ 76.7%、9.39% ~ 11.3%、3.17% ~ 7.36%,平均78.6%的K、50.4%的Na、10.0%的Ca和5.85%的Mg以水溶态存在;交换性K、Ca、Mg所占比例范围为9.78% ~ 17.9%、37.8% ~ 48.3%、19.8% ~ 31.2%,平均14.3%的K、43.1%的Ca和26.4%的Mg以交换态存在;以其他形态存在的K、Ca、Mg所占比例范围为2.89% ~ 10.4%、42.2% ~ 52.8%、65.0% ~ 77.0%,平均7.10%的K、46.8%的Ca和67.8%的Mg以其他形态存在。以水溶态和交换态存在的盐基离子是最容易被植物吸收利用的离子形态,二者之和能反映玉米秸秆炭中有效态盐基离子的占比情况。4种盐基离子中,K、Ca和Mg为植物生长所需营养元素,其中K为大量营养元素,Ca和Mg为中量营养元素。3个热解温度下,水溶性和交换性K、Ca、Mg之和所占比例范围为89.6% ~ 97.1%、47.2% ~ 57.8%、23.0% ~ 38.6%,平均92.9%的K、53.2%的Ca和32.2%的Mg为植物有效态。
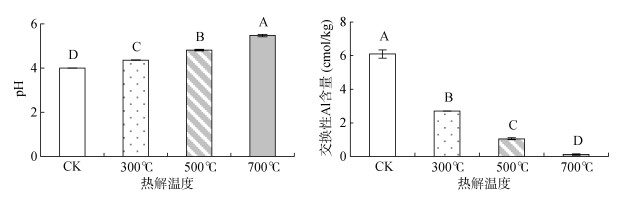
2.3 K、Na、Ca、Mg与玉米秸秆炭改良土壤酸度的关系与对照相比,300、500和700 ℃下玉米秸秆炭分别将酸性土壤的pH极显著提高了0.363、0.816和1.48个pH单位,提高程度随热解温度升高极显著增加;分别将酸性土壤的交换性Al3+含量极显著降低了55.6%、82.7%和98.0%,降低幅度随热解温度升高极显著增加(图 2)。
|
(图柱上方大写字母不同表示处理间差异达到P < 0.01显著水平) 图 2 不同生物质炭处理下土壤pH和交换性Al Fig. 2 Soil pH and exchangeable Al contents under different biochar treatments |
为考察各形态盐基离子在玉米秸秆炭提高酸性土壤pH和降低交换性Al3+中的作用,采用逐步回归分析法将300、500和700 ℃下玉米秸秆炭的总K、总Na、总Ca、总Mg、水溶性K、水溶性Na、水溶性Ca、水溶性Mg、交换性K、交换性Ca、交换性Mg、水溶性K +交换性K、水溶性Ca +交换性Ca、水溶性Mg +交换性Mg、总K +总Na +总Ca +总Mg、水溶性K +水溶性Na +水溶性Ca +水溶性Mg、交换性K +交换性Ca +交换性Mg、水溶性K +水溶性Na+水溶性Ca +水溶性Mg +交换性K +交换性Ca +交换性Mg含量分别与改良后土壤pH、交换性Al3+含量进行逐步回归分析。结果显示,总K +总Na +总Ca +总Mg含量与土壤pH之间呈极显著线性正相关,多元线性回归方程为:y= 0.010x + 3.451(校正判定系数R2 = 0.988,P = 0.000),其中,y为土壤pH,x为总K +总Na +总Ca +总Mg含量(标准化回归系数Beta = 0.995, P = 0.000)。4种盐基离子总量能解释98.8%玉米秸秆炭提高土壤pH的原因,在玉米秸秆炭提高土壤pH中的作用为99.5%。
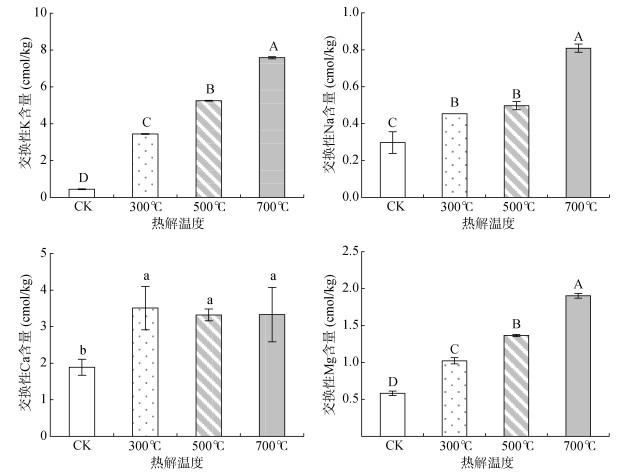
2.4 K、Na、Ca、Mg提高酸性土壤交换性盐基的作用与对照相比,300、500和700 ℃下玉米秸秆炭分别将酸性土壤的交换性K含量极显著提高了338%、1 069%和1 589%,提高程度随热解温度升高极显著增加;分别将交换性Na含量极显著提高了52.2%、67.2%和172%,提高程度随热解温度升高极显著增加,其中300和500 ℃之间差异不显著;分别将交换性Ca含量显著提高了85.8%、75.9%和76.2%,其中300、500和700 ℃之间差异不显著;分别将交换性Mg含量极显著提高了75.6%、134%和227%,提高程度随热解温度升高极显著增加(图 3)。分别将土壤交换性盐基总量显著提高了162%、224%和323%,提高程度随热解温度升高显著增加(P < 0.05)。
|
(图柱上方小写字母不同表示处理间差异达到P < 0.05显著水平,大写字母不同表示处理间差异达到P < 0.01显著水平) 图 3 不同生物质炭处理下土壤交换性盐基离子含量 Fig. 3 Contents of soil exchangeable base cations under different biochar treatments |
将300、500和700 ℃下玉米秸秆炭的总K、总Na、总Ca、总Mg、水溶性K、水溶性Na、水溶性Ca、水溶性Mg、交换性K、交换性Ca、交换性Mg、水溶性K +交换性K、水溶性Ca +交换性Ca、水溶性Mg +交换性Mg、总K +总Na +总Ca +总Mg、水溶性K +水溶性Na +水溶性Ca +水溶性Mg、交换性K +交换性Ca +交换性Mg、水溶性K +水溶性Na +水溶性Ca +水溶性Mg +交换性K +交换性Ca +交换性Mg含量分别与改良后土壤交换性K、交换性Na、交换性Ca、交换性Mg、交换性盐基总量进行逐步回归分析。结果显示,总K含量与土壤交换性K含量呈极显著线性正相关,多元线性回归方程为:y = 0.052x-0.076(R2 = 0.998,P = 0.000),其中,y为土壤交换性K含量,x为总K含量(Beta = 0.999, P = 0.000)。总K含量能解释99.8%土壤交换性K含量升高的原因,在提高土壤交换性K含量中的作用为99.9%。总Na含量与土壤交换性Na含量呈极显著线性正相关,多元线性回归方程为:y = 0.176x + 0.142(R2 = 0.976,P = 0.000),其中,y为土壤交换性Na含量,x为总Na含量(Beta = 0.989, P = 0.000)。总Na含量能解释97.6%土壤交换性Na含量升高的原因,在提高土壤交换性Na含量中的作用为98.9%。交换性Ca含量与土壤交换性Mg含量呈极显著线性正相关,多元线性回归方程为:y = 0.139x-0.015(R2 = 0.985,P = 0.000),其中,y为土壤交换性Mg含量,x为交换性Ca含量(Beta = 0.993,P = 0.000)。交换性Ca含量能解释98.5%土壤交换性Mg含量升高的原因,在提高土壤交换性Mg含量中的作用为99.3%。交换性Ca含量与土壤交换性盐基总量呈极显著线性正相关,多元线性回归方程为:y = 0.820x + 2.294(R2 = 0.861,P = 0.000),其中,y为土壤交换性盐基总量,x为交换性Ca含量(Beta = 0.937,P = 0.000)。交换性Ca含量能解释86.1%土壤交换性盐基总量升高的原因,其在提高土壤交换性盐基总量中的作用为93.7%。
3 讨论 3.1 热解温度对K、Na、Ca、Mg含量和存在形态的影响玉米秸秆炭中K、Na、Ca、Mg总量、水溶态和交换态含量均随热解温度升高呈显著增加趋势,这主要是因为在热解原料相同的情况下,生物质炭中元素含量和存在形态主要受热解温度影响[28-29]。随热解温度升高,原料中的元素会在生物质炭中发生富集[22],从而增加了各形态盐基离子含量。玉米秸秆炭中78.6%的K以水溶态存在,主要是因为生物质炭中的K主要以易溶性的KCl形态存在,容易被水淋洗[30-31]。Na在生物质炭中的存在形态与K相似,主要以易溶性的NaCl形态存在[30-31]。玉米秸秆炭中只有10.0%的Ca和5.85%的Mg以水溶态存在,主要是因为Ca和Mg在生物质炭中主要以CaCO3、CaMg(CO3)2等难溶性化合物形态存在,不容易被水淋洗[13]。水溶性K和Na所占比例随热解温度升高而增加,主要是因为生物质炭中K和Na主要以离子态存在,随热解温度增加生物质炭灰分增加,K和Na发生富集而提高了含量[13, 22]。水溶性Ca和Mg所占比例随热解温度升高先增加后下降,主要是由于当热解温度高于500 ℃时,生物质炭中的Ca和Mg化合物向晶体态转变并且溶解性下降[13, 22]。交换性K、Ca、Mg所占比例随热解温度升高而下降,主要是由于它们主要以静电作用吸附在生物质炭表面的羧基官能团上,随热解温度升高羧基官能团呈下降趋势,导致交换性K、Ca、Mg所占比例下降[13]。此外,随热解温度升高形成的Ca和Mg难溶性化合物的增加是导致水溶性和交换性Ca、Mg所占比例下降的另一个原因。
3.2 K、Na、Ca、Mg与玉米秸秆炭改良土壤酸度的关系以往的研究表明,生物质炭中碱性物质的主要存在形态为碳酸盐和有机阴离子[13],当将生物质炭施入酸性土壤时,这些碱性物质可与土壤溶液中的活性酸H+、Al3+和CO2等发生反应生成碳酸氢盐,碳酸氢盐会进一步与酸反应释放出CO2,反应过程中释放出的Ca、Mg、K、Na等盐基阳离子与土壤交换性H+和交换性Al3+发生交换反应,降低它们的含量,提高土壤pH[2, 34]。本研究结果表明,玉米秸秆炭所含4种盐基离子总量与土壤pH之间呈极显著线性正相关性,能解释98.8%玉米秸秆炭提高土壤pH的原因,在玉米秸秆炭提高土壤pH中的作用为99.5%。说明,盐基离子总量可以作为衡量玉米秸秆炭提高酸性土壤pH能力的间接指标,盐基离子总量越高,玉米秸秆炭提高酸性土壤pH的能力越强,这和生物质炭的盐基离子浓度与其所含的碱性呈强的正相关性[35]的研究结果相一致。需要指出的是,决定生物质炭改良酸性土壤能力的是其所含的碱性物质的量的大小[10-13]。K、Na、Ca、Mg不能起到直接中和土壤酸度和提高土壤pH的作用。
3.3 K、Na、Ca、Mg提高酸性土壤交换性盐基的作用机制经生物质炭改良后的酸性土壤中的盐基离子主要来源于生物质炭带入的盐基离子,生物质炭自身盐基离子含量的高低往往决定改良后酸性土壤中的盐基离子含量[13, 36]。本研究同样表明了3个温度下的玉米秸秆炭均极显著或显著提高了酸性土壤交换性K、Na、Ca、Mg含量和交换性盐基总量。本研究表明,玉米秸秆炭的总K含量与土壤交换性K含量呈极显著线性正相关,能解释99.8%土壤交换性K含量升高的原因,在提高土壤交换性K含量中的作用为99.9%;玉米秸秆炭的总Na含量与土壤交换性Na含量呈极显著线性正相关,能解释97.6%土壤交换性Na含量升高的原因,在提高土壤交换性Na含量中的作用为98.9%。在玉米秸秆炭中,K和Na主要以KCl和NaCl等易溶盐化合物存在,极易被醋酸铵溶解,改良后土壤的交换性K和Na很大部分是溶解于醋酸铵溶液中的K和Na离子,玉米秸秆炭中K和Na的含量决定了改良后土壤中交换性K和Na的量。因此,土壤交换性K和Na含量主要取决于玉米秸秆炭中总K和总Na含量。玉米秸秆炭的交换性Ca含量与土壤交换性Mg含量呈极显著线性正相关,能解释98.5%土壤交换性Mg含量升高的原因,在提高土壤交换性Mg含量中的作用为99.3%;玉米秸秆炭的交换性Ca含量与土壤交换性盐基总量呈极显著线性正相关,能解释86.1%土壤交换性盐基总量升高的原因,在提高土壤交换性盐基总量中的作用为93.7%。玉米秸秆炭的交换性Ca取代土壤表面吸附的Al3+后,随着土壤交换性Al3+的降低和pH的升高,土壤表面的负电荷大量增加,为K+、Na+和Mg2+等阳离子创造了更多的吸附点位,从而增加了阳离子在土壤表面的吸附量,提高了土壤的交换性盐基总量,这是玉米秸秆炭的交换性Ca含量能极显著提高土壤交换性Mg和交换性盐基总量的主要原因。
4 结论由于热解过程对元素的富集作用,玉米秸秆炭中总K、总Na、总Ca、总Mg含量均随热解温度升高显著增加。玉米秸秆炭中K和Na主要以离子态存在,随热解温度增加K和Na发生富集,水溶态离子含量显著增加。由于随温度增加玉米秸秆炭中Ca、Mg化合物向晶体态的转变,造成约50%的Ca和70%的Mg以其他形态(主要为难溶态)存在。K、Na、Ca、Mg可以作为间接指标衡量玉米秸秆炭提高酸性土壤pH的能力。玉米秸秆炭总K和总Na含量是提高土壤交换性K和Na含量的决定因素。玉米秸秆炭交换性Ca含量在提高土壤交换性Mg和交换性盐基总量中起决定作用。
| [1] |
Kochian L V, Piñeros M A, Liu J P, et al. Plant adaptation to acid soils: The molecular basis for crop aluminum resistance[J]. Annual Review of Plant Biology, 2015, 66: 571-598 DOI:10.1146/annurev-arplant-043014-114822 (  0) 0) |
| [2] |
Dai Z M, Zhang X J, Tang C, et al. Potential role of biochars in decreasing soil acidification—A critical review[J]. Science of the Total Environment, 2017, 581/582: 601-611 DOI:10.1016/j.scitotenv.2016.12.169 (  0) 0) |
| [3] |
Vogt R D, Seip H M, Larssen T, et al. Potential acidifying capacity of deposition-experiences from regions with high NH4+ and dry deposition in China[J]. Science of the Total Environment, 2006, 367(1): 394-404 DOI:10.1016/j.scitotenv.2005.12.018 (  0) 0) |
| [4] |
Zhao Y, Duan L, Xing J, et al. Soil acidification in China: Is controlling SO2 emissions enough?[J]. Environmental Science and Technology, 2009, 43(21): 8021-8026 DOI:10.1021/es901430n (  0) 0) |
| [5] |
Guo J H, Liu X J, Zhang Y, et al. Significant acidification in major Chinese croplands[J]. Science, 2010, 327(5968): 1008-1010 DOI:10.1126/science.1182570 (  0) 0) |
| [6] |
徐仁扣. 秸秆生物质炭对红壤酸度的改良作用:回顾与展望[J]. 农业资源与环境学报, 2016, 33(4): 303-309 (  0) 0) |
| [7] |
周碧青, 邱龙霞, 张黎明, 等. 基于灰色关联-结构方程模型的土壤酸化驱动因子研究[J]. 土壤学报, 2018, 55(5): 1233-1242 (  0) 0) |
| [8] |
徐仁扣. 土壤酸化及其调控研究进展[J]. 土壤, 2015, 47(2): 238-244 (  0) 0) |
| [9] |
袁金华, 徐仁扣. 生物质炭对酸性土壤改良作用的研究进展[J]. 土壤, 2012, 44(4): 541-547 DOI:10.3969/j.issn.0253-9829.2012.04.003 (  0) 0) |
| [10] |
Yuan J H, Xu R K. The amelioration effects of low temperature biochar generated from nine crop residues on an acidic Ultisol[J]. Soil Use and Management, 2011, 27(1): 110-115 DOI:10.1111/sum.2011.27.issue-1 (  0) 0) |
| [11] |
Yuan J H, Xu R K, Qian W, et al. Comparison of the ameliorating effects on an acidic Ultisol between four crop straws and their biochars[J]. Journal of Soils and Sediments, 2011, 11(5): 741-750 DOI:10.1007/s11368-011-0365-0 (  0) 0) |
| [12] |
Yuan J H, Xu R K, Wang N, et al. Amendment of acid soils with crop residues and biochars[J]. Pedosphere, 2011, 21(3): 302-308 DOI:10.1016/S1002-0160(11)60130-6 (  0) 0) |
| [13] |
Yuan J H, Xu R K, Zhang H. The forms of alkalis in the biochar produced from crop residues at different temperatures[J]. Bioresource Technology, 2011, 102(3): 3488-3497 DOI:10.1016/j.biortech.2010.11.018 (  0) 0) |
| [14] |
袁金华, 徐仁扣. 稻壳制备的生物质炭对红壤和黄棕壤酸度的改良效果[J]. 生态与农村环境学报, 2010, 26(5): 472-476 DOI:10.3969/j.issn.1673-4831.2010.05.013 (  0) 0) |
| [15] |
袁金华, 徐仁扣. 生物质炭的性质及其对土壤环境功能影响的研究进展[J]. 生态环境学报, 2011, 20(4): 779-785 DOI:10.3969/j.issn.1674-5906.2011.04.034 (  0) 0) |
| [16] |
索龙, 潘凤娥, 胡俊鹏, 等. 秸秆及生物质炭对砖红壤酸度及交换性能的影响[J]. 土壤, 2015, 47(6): 1157-1162 (  0) 0) |
| [17] |
李九玉, 赵安珍, 袁金华, 等. 农业废弃物制备的生物质炭对红壤酸度和油菜产量的影响[J]. 土壤, 2015, 47(2): 334-339 (  0) 0) |
| [18] |
Chan K Y, Van Zwieten L, Meszaros I, et al. Agronomic values of greenwaste biochar as a soil amendment[J]. Australian Journal of Soil Research, 2007, 45(8): 629-634 DOI:10.1071/SR07109 (  0) 0) |
| [19] |
Novak J M, Lima I, Xing B S, et al. Characterization of designer biochar produced at different temperatures and their effects on a loamy sand[J]. Annals of Environmental Science, 2009, 3: 195-206 (  0) 0) |
| [20] |
Shi R Y, Li J Y, Jiang J, et al. Incorporation of corn straw biochar inhibited the re-acidification of four acidic soils derived from different parent materials[J]. Environmental Science and Pollution Research, 2018, 25(10): 9662-9672 DOI:10.1007/s11356-018-1289-7 (  0) 0) |
| [21] |
Bruun S, Harmer S, Bekiaris G, et al. The effect of different pyrolysis temperatures on the speciation and availability in soil of P in biochar produced from the solid fraction of manure[J]. Chemosphere, 2017, 169: 377-386 DOI:10.1016/j.chemosphere.2016.11.058 (  0) 0) |
| [22] |
Xu X Y, Zhao Y H, Sima J K, et al. Indispensable role of biochar-inherent mineral constituents in its environmental applications: A review[J]. Bioresource Technology, 2017, 241: 887-899 DOI:10.1016/j.biortech.2017.06.023 (  0) 0) |
| [23] |
Shi R Y, Hong Z N, Li J Y, et al. Mechanisms for increasing the pH buffering capacity of an acidic Ultisol by crop residue-derived biochars[J]. Journal of Agricultural and Food Chemistry, 2017, 65(37): 8111-8119 DOI:10.1021/acs.jafc.7b02266 (  0) 0) |
| [24] |
Chun Y, Sheng G Y, Chiou C T, et al. Compositions and sorptive properties of crop residue-derived chars[J]. Environmental Science and Technology, 2004, 38(17): 4649-4655 DOI:10.1021/es035034w (  0) 0) |
| [25] |
Slattery W J, Ridley A M, Windsor S M. Ash alkalinity of animal and plant products[J]. Australian Journal of Experimental Agriculture, 1991, 31(3): 321-324 DOI:10.1071/EA9910321 (  0) 0) |
| [26] |
Gaskin J W, Steiner C, Harris K, et al. Effect of low-temperature pyrolysis conditions on biochar for agricultural use[J]. Transactions of the ASABE, 2008, 51(6): 2061-2069 DOI:10.13031/2013.25409 (  0) 0) |
| [27] |
Pansu M, Gautheyrou J. Handbook of soil analysis- mineralogical, organic and inorganic methods[M]. Heidelberg: Springer-Verlag, 2006
(  0) 0) |
| [28] |
Zhao L, Cao X D, Masek O, et al. Heterogeneity of biochar properties as a function of feedstock sources and production temperatures[J]. Journal of Hazardous Materials, 2013, 256/257: 1-9 DOI:10.1016/j.jhazmat.2013.04.015 (  0) 0) |
| [29] |
Zhao L, Cao X D, Zheng W, et al. Endogenous minerals have influences on surface electrochemistry and ion exchange properties of biochar[J]. Chemosphere, 2015, 136: 133-139 DOI:10.1016/j.chemosphere.2015.04.053 (  0) 0) |
| [30] |
Limwikran T, Kheoruenromne I, Suddhiprakarn A, et al. Dissolution of K, Ca, and P from biochar grains in tropical soils[J]. Geoderma, 2018, 312(15): 139-150 (  0) 0) |
| [31] |
Li M, Lou Z J, Wang Y, et al. Alkali and alkaline earth metallic (AAEM) species leaching and Cu(Ⅱ) sorption by biochar[J]. Chemosphere, 2015, 119: 778-785 DOI:10.1016/j.chemosphere.2014.08.033 (  0) 0) |
| [32] |
Cao X D, Harris W. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation[J]. Bioresource Technology, 2010, 101(14): 5222-5228 DOI:10.1016/j.biortech.2010.02.052 (  0) 0) |
| [33] |
Kong Z Y, Liaw S B, Gao X P, et al. Leaching characteristics of inherent inorganic nutrients in biochars from the slow and fast pyrolysis of mallee biomass[J]. Fuel, 2014, 128(128): 433-441 (  0) 0) |
| [34] |
Van Zwieten L, Kimber S, Morris S, et al. Effects of biochar from slow pyrolysis of paper mill-waste on agronomic performance and soil fertility[J]. Plant and Soil, 2010, 327(1/2): 235-246 (  0) 0) |
| [35] |
Fidel R B, Laird D A, Thompson M L, et al. Characterization and quantification of biochar alkalinity[J]. Chemosphere, 2017, 167: 367-373 DOI:10.1016/j.chemosphere.2016.09.151 (  0) 0) |
| [36] |
Yuan J H, Xu R K. Effects of biochars generated from crop residues on chemical properties of acid soils from tropical and subtropical China[J]. Soil Research, 2012, 50(7): 570-578 DOI:10.1071/SR12118 (  0) 0) |
2. Gansu Scientific Observing and Experimental Station of Agro-Environment and Arable Land Conservation, Ministry of Agriculture, Lanzhou 730070, China;
3. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2019, Vol. 51
2019, Vol. 51

