2. 重庆市地下水资源利用与环境保护实验室,重庆 401147
根据国际标准化组织(ISO)的定义,土壤为具有矿物质、有机质、水分、空气和生命有机体的地球表层物质。土壤不仅分布于自然界,也分布于城市、工业、交通和矿区,可出现在混凝土等覆盖层的下部。随着工业化的发展和人类活动的影响,土壤受到的各种污染(如无机污染、有机污染、核辐射等)对活动在其上的人类及动植物造成了巨大的威胁[1-2],各国对土壤污染状况的调查和控制越来越重视,我国在2018年分别发布了农用地和建设用地土壤环境质量标准,与1995版相比,农用地所检测污染物从10项增加到了12项,建设用地所检测污染物增加到了85项,美国制定的土壤环境基准中所考虑的污染物种类多达110项[3]。目前,土壤中无机污染物的检测对象主要为重金属元素和有机物,建设用地环境质量标准仅对氰化物含量有限值要求[4],测定土壤中的各种阴离子含量,对了解土壤污染状况和其他科研试验都有重要意义[5-7]。
土壤中阴离子的检测方法主要有分光光度法[8-9]、离子选择性电极法[8]、电位滴定法[10]、重量法[11]、毛细管电泳法[12],由于离子色谱法分离性好、干扰小、准确度高、操作简单、分析速度快、检出限低、可以同时检测多种阴离子等优点在土壤阴离子的检测中得到了广泛应用[13-15],有报道采用离子色谱法测定了固废和水质中的CN-和BrO3-[16-18],已报道的离子色谱法测定土壤中阴离子的方法主要检测几种常规无机阴离子。
本文采用超声提取-离子色谱法测定了土壤中F-、CN-、BrO3-、Cl-、NO2-、Br-、NO3-、PO43-、SO42-、C2O42-等10种水溶性阴离子含量,该方法分析速度快、成本低、准确度和精密度较高,可以满足环境质量监测需求,对相关领域的科学研究也具有很好的指导作用。
1 材料与方法 1.1 仪器与试剂Eco IC型离子色谱仪(瑞士万通),配863型自动进样器、A5-250型阴离子色谱柱、电导检测器;VP30型隔膜真空泵(北京莱伯泰科仪器股份有限公司),配2 L抽滤瓶,0.45 μm(φ60 mm)过滤膜,用于淋洗液真空脱气;VP-1型旋片式真空泵(台州正空泵业有限公司),配1 L抽滤瓶,0.22 μm(φ45 mm)微孔滤膜,用于试样过滤;GW-1008-40TL型超声波清洗机(中山市广威超声设备科技有限公司),超声波频率40 kHZ,最高温度90 ℃;TDL-50型电动离心机(江苏金怡仪器科技有限公司),离心管体积50 ml,转速0 ~ 4 000 r/min。
F-、Cl-、NO2-、Br-、NO3-、PO43-、SO42-标准溶液:1 000 μg/ml(国家有色金属及电子材料分析测试中心);CN-标准溶液:50 μg/ml(中国计量科学研究院);BrO3-标准溶液:1 000 μg/ml(中国计量科学研究院),以上标准溶液均为国家有证标准溶液,使用时根据需要逐级稀释到合适浓度。
C2O42-标准溶液:1 000 μg/ml,称取0.152 2 g草酸钠于100 ml烧杯中,用水溶解后转移到100 ml容量瓶定容。
淋洗液配制:称取6.783 9 g碳酸钠和1.680 1 g碳酸氢钠于100 ml烧杯中,用水溶解后转移到250 ml容量瓶中,定容至刻度摇匀,配制成淋洗液储备溶液,使用时,移取25 ml淋洗液储备溶液于2 L容量瓶中,用水定容至刻度,配制成浓度为3.2 mmol/L Na2CO3 + 1.0 mmol/L NaHCO3淋洗液使用溶液,使用前用真空过滤装置脱气,以防淋洗液中溶解的气泡造成高压泵压力波动而影响测定。
再生液:0.5%硫酸溶液,移取10 ml浓硫酸(98%)于2 L水中,搅拌均匀。
草酸钠、碳酸钠、碳酸氢钠均为优级纯,使用前在105 ℃下烘干2 h,浓硫酸为优级纯,实验用水为高纯水(18.2 MΩ)。
1.2 离子色谱条件Metrosep A Supp 5-250/4.0阴离子色谱柱,长度250.0 mm,内径4.0 mm,粒径5 μm;Metrosep A Supp 5 Guard保护柱,长度50.0 mm,内径4.0 mm;淋洗液:3.2 mmol/L Na2CO3+1.0 mmol/L NaHCO3,流速为0.7 ml/min;进样量为20 μl;电导检测器,池常数15.9 cm-1,控温装置40 ℃。
1.3 试验方法 1.3.1 标准溶液系列配制按表 1所列浓度配制各阴离子混合标准溶液系列Std1 ~ Std6,用水稀释和定容。
|
|
表 1 标准溶液系列 |
称取过0.15 mm(100目)筛的风干土壤样品5.000 0 g于50 ml离心管中,用水定容至50 ml,摇匀,盖上离心管盖,固定于离心管架上,然后于30 ℃下超声提取30 min,超声频率40 kZH,取出后在离心机中以4 000 r/min转速下离心15 min,离心后的上清液经0.22 μm微孔滤膜过滤于洁净干燥的50 ml比色管中,用于测定。
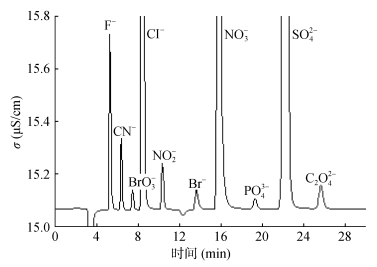
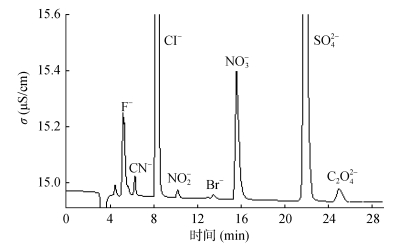
2 结果与讨论 2.1 色谱行为按离子色谱条件测定混合标准溶液和样品,图 1为标准系列Std3的色谱图,图 2为2#样品的色谱图。
|
图 1 标准溶液色谱图 |
|
图 2 2#样品色谱图 |
试验了不同固液比(1︰5、1︰10、1︰15、1︰20),不同提取温度(10、20、30、40、50 ℃)和不同超声提取时间(10、20、30、40、50 min)对测定结果的影响,试验发现:当固液比为1︰10、提取温度为30 ℃、提取时间为30 min时,各离子测定浓度趋于稳定,所以选择此条件为各离子提取条件。
2.3 校准曲线和检出限在离子色谱测定条件下测定各标准溶液系列,以峰面积A(μS/(cm·min))为纵坐标,质量浓度ρ(mg/L)为横坐标绘制校准曲线。由于方法检出限和仪器检出限差别较大,本实验采用空白加低浓度标准溶液,加标浓度为预期方法检出限的1 ~ 5倍,如果加标浓度小于所计算方法检出限或大于所计算检出限的5倍,则调整到合适浓度重新测定,平行测定11次,3倍标准偏差对应的质量分数方法的检出限,10倍标准偏差对应的质量分数为方法的定量限。校准曲线、检出限和定量限数据见表 2。
|
|
表 2 校准曲线及检出限 |
按实验方法,称取2个不同的土壤样品,每个样品平行称取两份,其中一份直接按样品处理方法进行前处理,另一份在样品前处理之前加入标准溶液,计算加标回收率验证准确度,加标样品平行测定7次计算精密度。试验数据见表 3,2#样品的色谱图见图 2。由表 3可知:2个土壤样品中BrO3-和PO43-测定值均低于检出限,不同样品各阴离子加标回收率在84.0% ~ 112%之间,各阴离子7次测定的相对标准偏差在0.09% ~ 4.3%。
|
|
表 3 准确度和精密度试验结果 |
本文采用超声波振荡提取-离子色谱法测定了土壤中10种水溶性阴离子含量,通过大量实验优化了提取条件和测定条件,通过实验发现:此方法的准确度和精密度较高,实际土壤样品加标回收率可以满足环境监测和科研中对准确度的要求,自动化程度高,分析速度快,可以满足大批量检测需求。
| [1] |
王炜炜, 田丽, 杨明. 我国土壤污染成因分析与防治对策研究[J]. 工业安全与环保, 2016, 42(5): 48-51 DOI:10.3969/j.issn.1001-425X.2016.05.015 (  0) 0) |
| [2] |
张桃林. 科学认识和防治耕地土壤重金属污染[J]. 土壤, 2015, 47(3): 435-439 (  0) 0) |
| [3] |
张耀丹, 邱琳琳, 杜文超, 等. 土壤环境基准的研究现状及展望[J]. 南京大学学报(自然科学), 2017, 53(2): 209-217 (  0) 0) |
| [4] |
中华人民共和国生态环境部.土壤环境质量建设用地土壤污染风险管控标准(试行): GB 36600—2018[S].北京: 中国标准出版社, 2018
(  0) 0) |
| [5] |
王祖伟, 弋良朋, 高文燕, 等. 碱性土壤盐化过程中阴离子对土壤中镉有效态和植物吸收镉的影响[J]. 生态学报, 2012, 32(23): 7512-7518 (  0) 0) |
| [6] |
邢维芹, 王亚莉, Scheckel K G, 等. 不同阴离子对水溶性磷酸盐稳定污染土壤中重金属的影响[J]. 环境科学学报, 2013, 33(10): 2814-2820 (  0) 0) |
| [7] |
李广之, 陈银节, 尹红军, 等. 近地表土壤中可溶态阴离子的石油地质意义[J]. 物探与化探, 2011, 35(2): 198-202 (  0) 0) |
| [8] |
刘彬, 王霞. 土壤中氟离子的测定方法对比[J]. 广东化工, 2017, 44(13): 256-258 DOI:10.3969/j.issn.1007-1865.2017.13.119 (  0) 0) |
| [9] |
韩康芹, 张云肖, 冯敏英. 土壤中有害氰化物的检测方法[J]. 安徽农业科学, 2014, 42(3): 729-730 DOI:10.3969/j.issn.0517-6611.2014.03.034 (  0) 0) |
| [10] |
孙又宁, 余梅玲. 自动电位滴定法测定肥料和土壤中氯离子含量[J]. 中国土壤与肥料, 2007(2): 75-77 DOI:10.3969/j.issn.1673-6257.2007.02.019 (  0) 0) |
| [11] |
龙希建. 浅析土壤中可溶性硫酸盐的测定[J]. 世界有色金属, 2016(12): 124-125, 127 (  0) 0) |
| [12] |
蒋倩, 韩勇, 孙晓丽, 等. 离子色谱法和毛细管电泳法测定土壤中氯离子、硫酸根及其差异性[J]. 土壤, 2016, 48(2): 343-348 (  0) 0) |
| [13] |
王红斌, 谢静, 丁雪梅, 等. 正交试验优化土壤萃取法及常见无机阴离子的离子色谱分析[J]. 分析试验室, 2012, 31(6): 103-107 (  0) 0) |
| [14] |
李庆霞, 刘亚轩, 陈卫明, 等. 离子色谱法检测土壤样品水溶态中的七种阴离子[J]. 物探与化探, 2012, 36(3): 418-421 (  0) 0) |
| [15] |
杨春霞, 李彩虹, 赵银宝. 离子色谱法测定土壤中无机阴阳离子含量[J]. 理化检验-化学分册, 2012, 48(10): 1199-1202 (  0) 0) |
| [16] |
林冬, 郭晶晶, 王鑫. 安倍检测-离子色谱法测定固废中痕量氰根离子[J]. 广州华工, 2017, 45(18): 95-97 (  0) 0) |
| [17] |
李朦, 于泓, 郑秀荣. 离子色谱-紫外检测法同时分析碘酸根、碘离子、溴酸根和溴离子[J]. 色谱, 2014, 32(3): 299-303 (  0) 0) |
| [18] |
黄选忠, 邹大喜, 杜宏山. 离子色谱法测定纯净水中F-、BrO3-等6种阴离子[J]. 化学分析计量, 2016, 25(4): 53-56 DOI:10.3969/j.issn.1008-6145.2016.04.014 (  0) 0) |
2. Laboratory of Chongqing Groundwater Resource Utilization and Environmental Protection, Chongqing 401147, China
 2019, Vol. 51
2019, Vol. 51

