2. 中国科学院大学,北京 100049
红壤是我国南方地区的主要土壤类型和重要土壤资源[1]。红壤酸性强,其酸害、铝毒和低肥力严重限制了该地区的农作物生长和农林业生产[2-3]。近年来,由于酸沉降和铵态氮肥的过量施用等原因,红壤的酸化速率加快,酸化范围进一步加大[4-7]。因此,需要对酸化红壤进行改良,并采取有效措施提高土壤抗酸化能力以减缓酸化速率,恢复并增强其生产力。施用石灰性物质是改良红壤酸度的传统措施[8-9],虽然其对土壤酸度的改良效果很好,但它不能对土壤的再酸化发挥阻控作用,因此需要研发新型改良剂。近年来,生物质炭作为新型改良剂被用于酸性土壤改良[10-11],生物质炭不仅能有效中和土壤酸度,而且能提高土壤的酸缓冲容量,从而提高土壤的抗酸化能力,阻控土壤的再酸化[12]。
富里酸是土壤腐殖质的组分之一,是动植物残体经微生物分解、转化和聚合形成的含芳香环结构、非晶质天然高分子有机化合物[13-14],在自然界中广泛分布。富里酸具有很高的CEC[15],含羧基、羟基、羰基、醌基、甲氧基等众多有机官能团[14],其中的弱酸性官能团能够通过解离产生大量负电荷[16],因此,富里酸具有较强的离子交换能力和吸附能力,不仅能增加土壤对养分保持能力,改良土壤理化性质,还能提高土壤对酸碱变化的缓冲能力[15]。此外,富里酸能与铝离子发生络合作用[17]。富里酸在土壤中与矿质颗粒结合形成有机无机复合胶体而稳定存在[18-19]。因此,可以预期富里酸不仅可以改良土壤酸度,减轻土壤铝对植物的毒害,还可以提高土壤的抗酸化能力,对土壤酸化具有一定的阻控作用。本文研究了富里酸对由第四纪红黏土和第三纪红砂岩发育的两种红壤酸度的改良效果,并初步分析了富里酸对红壤酸化的阻控作用,研究结果可为红壤酸化阻控措施的研发提供参考。第四纪红色黏土和第三纪红砂岩发育的红壤在我国南方地区广泛分布,且两种红壤在黏粒含量、CEC和pH缓冲容量(pHBC)等方面具有明显差异,本文选择这两种土壤用于比较研究。
1 材料与方法 1.1 供试土壤与富里酸第四纪红黏土发育的红壤(红黏土)采自安徽省郎溪县(31°3′N, 119°5′E),第三纪红砂岩发育的红壤(红砂土)采自江西省鹰潭市(28°14′N, 116°55′E)。土样采自0 ~ 20 cm耕作层,去除石块和残根后,风干、研磨、过2 mm筛,用于土壤培养试验。两种土壤的基本性质列于表 1中。土壤有机质采用重铬酸钾滴定法测定,CEC则采用醋酸铵法(pH 7.0)测定[20]。用LS13320激光粒度分析仪(Beckman Coulter Inc., Fullerton, CA, USA)测定土壤粒度分布,并根据黏粒(直径 < 2 μm)、粉粒(直径2 ~ 20 μm)、砂粒(直径 > 20 μm)的分数计算土壤粒度分布。
|
|
表 1 两种红壤的基本性质 Table 1 Basic physiochemical properties of two tested red soils |
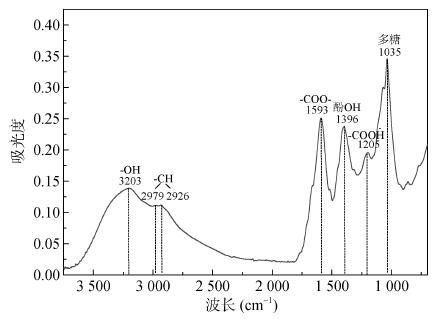
所用富里酸购自江西省萍乡市红土地腐植酸有限公司。采用复合pH电极配pH计(Orion Star A211)测得的富里酸pH为4.91(固液比为1︰25),用元素分析仪(Vario Max CN)测得的C和N含量分别为335和50.5 g/kg。将富里酸用HCl-HNO3-HClO4消煮后用HPLC-ICP-MS联用仪(7700x)测定P、Ca、Mg、K、Na等元素含量分别为1.94、13.83、7.46、79.86和0.94 g/kg。用傅里叶变换红外光谱仪(Nicolet 8700)测定富里酸的红外光谱,结果列于图 1中。
|
图 1 供试富里酸的红外光谱图 Fig. 1 ATR-FTIR of fulvic acid used |
分别称取300 g土壤样品至500 ml一次性塑料杯中,按10、20和50 g/kg土的比例添加富里酸进行培养试验,每个处理设置3次重复。然后加入适量去离子水,使含水量为土壤田间持水量的60%。待水分充分湿润土壤后,将其搅拌均匀,用保鲜膜覆盖杯口,并在其中间扎2 mm小孔以保持空气交换并减少水分散发。将土壤放置在25 ℃恒温培养箱中培养30 d,每3 ~ 5 d添加去离子水维持水分含量基本恒定。培养结束后,将土壤样品取出,风干、磨细后过60目筛,用于测定土壤pH、土壤pHBC和进行模拟酸化试验。本研究中富啡酸的添加量根据文献调研确定,一般室内培养试验中腐殖物质的用量在5.0 ~ 25.0 g/kg[21],本文中10和20 g/kg添加量与之相似,同时设置较高添加量(50 g/kg)用于比较研究。
采用滴定法测定土壤pHBC [22]:分别称取4.00 g土壤样品于10个50 ml塑料离心管中,然后加入适量的去离子水,再加入不同体积的0.04 mol/L(标定)HCl或NaOH,使溶液总体积达到20 ml,并形成pH梯度。为维持土壤悬液的离子强度基本恒定,向每个离心管中加入1.0 ml 0.04 mol/L CaCl2溶液;每个离心管中还加入0.25 ml的氯仿以抑制微生物活动。将土壤悬液放置在25 ℃环境下振荡24 h,再平衡6 d,期间每天振荡2 min。7 d后,测定离心管中土壤悬液的pH,绘制土壤pH与酸碱加入量之间的关系曲线,计算土壤pHBC。
1.3 模拟酸化试验土壤培养试验结束后,土壤pH提高,因此,在进行模拟酸化试验前,需要用Ca(OH)2将不加富里酸对照处理的土壤pH调节至与添加富里酸处理相似的值。根据目标土壤pH和土壤pHBC计算调节土壤pH所需的Ca(OH)2量。Ca(OH)2添加至土壤后,将两者充分混合,然后采用与添加富里酸处理相似方法进行为期30 d的培养试验。培养结束,将土壤样品风干、磨细过60目筛。
称取4.00 g培养后的土壤样品至50 ml塑料离心管中,加入20 ml不同浓度的HNO3,拧紧管盖,在25 ℃下振荡24 h,再平衡6 d,期间每天振荡2 min再静置,共耗时7 d。7 d后,用Orion 720 pH计与带有双盐桥(LiCl)的玻璃电极和参比电极测定土壤悬液pH[12]。然后将离心管连同悬液在4 500 r/min条件下离心5 min,分离上层清液,将离心管中的土壤样品放置在50 ℃下烘干,烘干后磨细,并过60目筛,用于测定土壤交换性铝含量。交换性铝采用1 mol/L KCl浸提[20]、0.01 mol/L NaOH滴定法测定。
1.4 统计分析所有数据均以3个重复的平均值±标准差的形式表示。处理间的差异性分析采用单因素方差分析法进行(ANOVA),单因素方差分析后用LSD和邓肯分析法(Duncan’s multiple range)进行显著性分析,(P < 0.05)。
2 结果与讨论 2.1 富里酸对不同母质发育红壤酸度的影响由表 2可知,与对照相比,培养前,添加富里酸使两种土壤pH均略有下降,这可能是由于富里酸中羧基发生解离释放出H+,使土壤pH下降。但培养结束后,添加富里酸均显著提高两种土壤的pH (P < 0.05),并且提升效果随富里酸加入量的增加而增加。这主要是由于在培养过程中,富里酸中部分活性有机物分解,有机阴离子发生脱羧反应释放CO2,消耗土壤中的H+,致使土壤pH上升[23-24]。两种土壤相比,添加10和20 g/kg富里酸对红砂土pH的提升效果优于红黏土。比如,添加10 g/kg富里酸后,红砂土的pH比对照提高0.55个pH单位,而红黏土的pH比对照提高0.23个pH单位。这主要因为红砂土的CEC、有机质和黏粒含量均显著低于红黏土,因而其pHBC也显著低于红黏土,对富里酸等改良剂的添加更敏感。因此,富里酸对两种不同母质发育的红壤的酸度均有很好的改良效果,对红砂土的改良效果更显著。
|
|
表 2 添加富里酸对土壤pH和土壤pH缓冲容量的影响 Table 2 Effects of fulvic acid on soil pH and soil pH buffering capacity |
从表 2中可以看出,与土壤pH变化趋势相似,与对照相比,添加富里酸均显著增加了土壤pHBC(P < 0.05),并且增幅随富里酸添加量的增加而增加,这与前人观测到的土壤pHBC随土壤有机质含量增加而增加的结果相似[25]。与添加10 g/kg富里酸处理相比,添加20 g/kg和50 g/kg的富里酸对两种红壤pHBC的提升效果尤为显著。相同添加量下,富里酸对红砂土pHBC提升效果显著优于红黏土。如添加50 g/kg富里酸处理,红砂土pHBC由对照的7.78 mmol/(kg·pH)增加至23.30 mmol/(kg·pH),增加了1.99倍;相同添加量下,红黏土的pHBC由对照的20.73 mmol/(kg·pH)增加至35.31 mmol/(kg·pH),增加了0.70倍。这主要是由于红砂土本身的pHBC远低于红黏土。富里酸是一种弱酸,含丰富的有机官能团[15]。这些官能团的质子化和去质子化是富里酸增加土壤pHBC的主要原因。由此可见,添加富里酸不仅能改良土壤酸度,还能提升土壤对酸的缓冲能力。
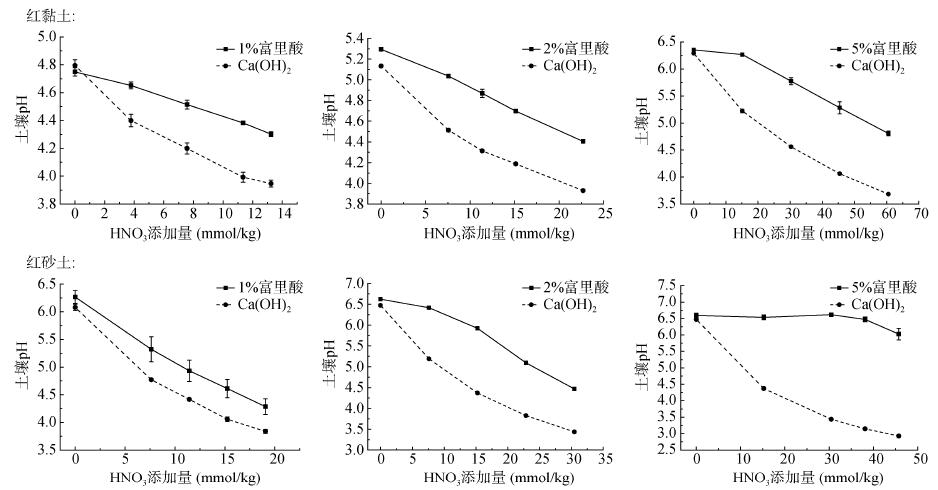
2.3 添加富里酸对红壤酸化的阻控效果一般来说,土壤抗酸化能力会随土壤pHBC的增加而增加。为了验证这一假设,通过模拟酸化试验,研究了添加富里酸对两种红壤抗酸化能力的影响。用Ca(OH)2将不添加富里酸的对照处理的土壤pH调节至与添加富里酸处理相近的值,然后加入不同浓度的HNO3进行模拟酸化试验,结果列于图 2中。可以看出,加入相同量HNO3的情况下,添加富里酸处理的红砂土的pH下降幅度显著小于添加Ca(OH)2处理的,说明添加富里酸提高了土壤的抗酸化能力,添加50 g/kg富里酸处理的效果更显著。添加富里酸对红黏土的抗酸化能力有相似的提升效果,添加20 g/kg和50 g/kg富里酸处理的效果更显著。添加富里酸对红砂土抗酸化能力的提升效果优于红黏土。当加入30 mmol/kg HNO3后,红黏土和红砂土添加5%富里酸处理的土壤pH分别比添加Ca(OH)2处理的高1.21和3.13个pH单位,这与添加富里酸对两种土壤pHBC的提升效果一致。因此,添加富里酸能有效提升土壤的pHBC,从而提高土壤的抗酸化能力,对土壤pHBC较低的土壤,富里酸对其抗酸化能力的提升效果更为明显。
|
图 2 模拟酸化过程中,两种土壤添加富里酸/Ca(OH)2处理土壤pH随HNO3加入量的变化 Fig. 2 pH changes of soils added with fulvic acid or Ca(OH)2 with increasing HNO3 addition during simulated acidification |
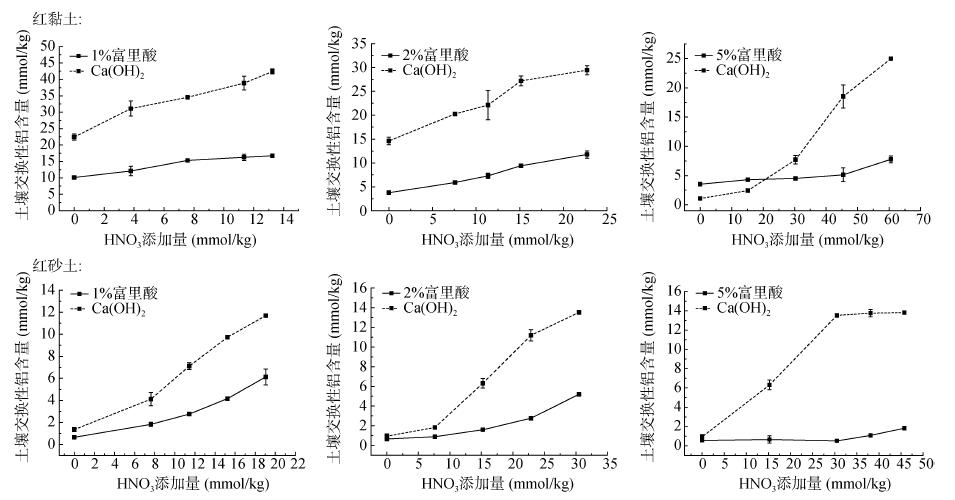
除了土壤pH下降外,土壤酸化的另一个负面效应是土壤铝的活化,尤其是土壤交换性铝的大量产生。从图 3可看出,两种土壤所有处理中交换性铝含量随土壤pH的降低而逐渐增加。但与添加Ca(OH)2处理相比,加入相同量HNO3的情况下,添加富里酸显著抑制了土壤交换性铝含量的增加。原因主要有两方面,添加富里酸抑制了模拟酸化过程中土壤pH的下降,从而减少了交换性铝的产生,因为酸性土壤的pH与交换性铝呈此消彼涨的关系;另一方面,富里酸分子中羧基和酚羟基等有机官能团与铝离子形成稳定络合物,从而减少了土壤中交换性铝的量。对红黏土而言,添加10和20 g/kg富里酸对交换性铝的抑制效果差异不大,但50 g/kg富里酸的抑制效果较前两者显著。比如,模拟酸化达最低pH时,与Ca(OH)2处理相比,10和20 g/kg富里酸使红黏土交换性铝分别减少了60.6%和60.0%,而50 g/kg富里酸使土壤交换性铝减少了68.9%。富里酸对红砂土交换性铝的抑制作用更显著,模拟酸化达最低pH时,添加10、20和50 g/kg富里酸使土壤交换性铝相较Ca(OH)2处理分别减少了47.6%、61.6%和86.8%。
|
图 3 模拟酸化过程中,两种土壤添加富里酸/Ca(OH)2处理土壤交换性铝随HNO3加入量的变化 Fig. 3 Exchangeable Al3+ changes of soils added with fulvic acid or Ca(OH)2 with increasing HNO3 addition during simulated acidification |
土壤与富里酸混合培养过程中部分活性有机物发生分解,消耗土壤中的H+,因此,添加富里酸能显著提高酸性红壤的pH,对红壤酸度有一定的改良效果。同时,富里酸是一种含有大量有机官能团和很高阳离子交换量的弱酸,添加富里酸能增加土壤对酸碱变化的缓冲能力,提高红壤的抗酸化能力,抑制红壤交换性铝的产生。因此,富里酸具有改良红壤酸度及阻控红壤酸化的双重功效,但实际改良和阻控效果还有待田间试验的进一步验证。
| [1] |
李庆逵. 中国红壤[M].
科学出版社, 北京, 1983
(  0) 0) |
| [2] |
张桃林. 中国红壤退化机制与防治[M].
中国农业出版社, 北京, 1999
(  0) 0) |
| [3] |
孙波, 董元华, 徐明岗, 等. 加强红壤退化分区治理, 促进东南红壤丘陵区现代高效生态农业发展[J]. 土壤, 2015, 47(2): 204-209 (  0) 0) |
| [4] |
吴甫成, 彭世良, 王晓燕, 等. 酸沉降影响下近20年来衡山土壤酸化研究[J]. 土壤学报, 2005, 42(2): 219-224 (  0) 0) |
| [5] |
孟红旗, 刘景, 徐明岗, 等. 长期施肥下我国典型农田耕层土壤的pH演变[J]. 土壤学报, 2013, 50(6): 1109-1116 DOI:10.11766/trxb201211070459 (  0) 0) |
| [6] |
Guo J H, Liu X J, Zhang Y, et al. Significant acidification in major Chinese croplands[J]. Science, 2010, 327(5968): 1008-1010 DOI:10.1126/science.1182570 (  0) 0) |
| [7] |
张忠启, 茆彭, 于东升, 等. 近25年来典型红壤区土壤pH变化特征——以江西省余江县为例[J]. 土壤学报, 2018, 55(6): 1545-1553 (  0) 0) |
| [8] |
Adams F. Soil acidity and liming[M].
American Society of Agronomy, Crop Science Society of America, Soil Science Society of America, Madison, WI, USA, 1984
(  0) 0) |
| [9] |
徐仁扣. 土壤酸化及其调控研究进展[J]. 土壤, 2015, 47(2): 238-244 (  0) 0) |
| [10] |
袁金华, 徐仁扣. 生物质炭对酸性土壤改良作用的研究进展[J]. 土壤, 2012, 44(4): 541-547 (  0) 0) |
| [11] |
李九玉, 赵安珍, 袁金华, 等. 农业废弃物制备的生物质炭对红壤酸度和油菜产量的影响[J]. 土壤, 2015, 47(2): 334-339 (  0) 0) |
| [12] |
Shi R Y, Hong Z N, Li J Y, et al. Mechanisms for increasing the pH buffering capacity of an acidic ultisol by crop residue-derived biochars[J]. Journal of Agricultural and Food Chemistry, 2017, 65(37): 8111-8119 DOI:10.1021/acs.jafc.7b02266 (  0) 0) |
| [13] |
郑平. 煤炭腐植酸的生产和应用[M].
化学工业出版社, 北京, 1991
(  0) 0) |
| [14] |
Stevenson F J. Humus chemistry: Genesis, composition, reactions(2nd ed)[M].
Wiley, New York, 1994
(  0) 0) |
| [15] |
窦森. 土壤有机质[M].
科学出版社, 北京, 2010
(  0) 0) |
| [16] |
Campitelli P, Velasco M I, Ceppi S. Charge development and acid-base characteristics of soil and compost humic acids[J]. Journal of the Chilean Chemical Society, 2003, 48(3): 91-96 DOI:10.4067/S0717-97072003000300018 (  0) 0) |
| [17] |
Browne B, Driscoll C T. pH-dependent binding of aluminum by a fulvic acid[J]. Environmental Science & Technology, 1993, 27(5): 915-922 DOI:10.1021/es00042a014 (  0) 0) |
| [18] |
Rodríguez F J, Schlenger P, García-Valverde M. Monitoring changes in the structure and properties of humic substances following ozonation using UV-Vis, FTIR and (1)H NMR techniques[J]. The Science of the Total Environment, 2016, 541: 623-637 DOI:10.1016/j.scitotenv.2015.09.127 (  0) 0) |
| [19] |
赵世翔, 于小玲, 李忠徽, 等. 不同温度制备的生物质炭对土壤有机碳及其组分的影响:对土壤腐殖物质组成及性质的影响[J]. 环境科学, 2017, 38(2): 769-782 DOI:10.13227/j.hjkx.201604059 (  0) 0) |
| [20] |
Pansu M, Gautheyrou J. Handbook of soil analysis[M].
Springer Berlin Heidelberg, Berlin, Heidelberg, 2006
(  0) 0) |
| [21] |
隽英华, 陈利军, 武志杰, 等. 尿素氮形态转化对腐殖酸的响应[J]. 土壤通报, 2011, 42(1): 112-116 (  0) 0) |
| [22] |
Xu R K, Zhao A Z, Yuan J H, et al. pH buffering capacity of acid soils from tropical and subtropical regions of China as influenced by incorporation of crop straw biochars[J]. Journal of Soils and Sediments, 2012, 12(4): 494-502 DOI:10.1007/s11368-012-0483-3 (  0) 0) |
| [23] |
Haynes R J, Mokolobate M S. Amelioration of Al toxicity and P deficiency in acid soils by additions of organic residues: a critical review of the phenomenon and the mechanisms involved[J]. Nutrient Cycling in Agroecosystems, 2001, 59(1): 47-63 DOI:10.1023/A:1009823600950 (  0) 0) |
| [24] |
Tang C, Yu Q. Legume materials and amelioration of soil acidity[J]. Plant and Soil, 1999, 215: 29-38 DOI:10.1023/A:1004704018912 (  0) 0) |
| [25] |
Magdoff F R, Bartlett R J, Ross D S. Acidification and pH buffering of forest soils[J]. Soil Science Society of America Journal, 1987, 51(5): 1384-1386 DOI:10.2136/sssaj1987.03615995005100050053x (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China
 2020, Vol. 52
2020, Vol. 52


