2. 中国科学院大学, 北京 100049
钾(K)是作物生长发育所必需的关键矿质营养元素。作为含量最丰富的阳离子,植物细胞内的钾离子浓度通常在100 mmol/L以上,占植物体干重的2%~10%。在钾营养充足的条件下,植物体内的含钾量一般可高达其干重的4% 以上[1],而富钾植物如空心莲子草等,植株含钾量甚至可达13%[2]。与另外两种大量营养元素氮、磷不同,钾不直接参与植物体内蛋白质、核酸、多糖等生命物质的组成,其生理功能主要体现在基于该离子的运动和平衡所产生的调控作用上。细胞内钾浓度直接控制细胞的体积和膨压,对细胞、组织的伸长及韧性有重要调控作用,与植物体内水分的保持和抗旱性关系极为密切,并且对病虫害等侵害提供物理屏障和机械抗性[3]。与钾素作为重要调控元素的生理作用相对应,植物钾素营养的关键环节除了根系从土壤中吸收、获取钾素之外,钾素在植株体内各部位的高效转运和分配过程也尤为重要。
土壤是植物根系获取钾营养的主要来源。我国土壤钾素及有效钾含量随地形、土壤质地、气候条件和土壤发育程度呈由北至南而递减的趋势[4]。我国耕地土壤缺钾面积达60% 左右,南方水稻主产区由于高温多雨、淋溶作用等土壤缺钾面积高达70% 以上,其中近90% 的水稻土处于钾亏缺状态[5-6]。土壤供钾不足会导致作物产量和品质的降低[7-8]、根系早衰和抗逆性下降,易感染病虫害和出现倒伏现象[9-10]。因此,保证钾素供应是水稻等作物高产和优质的重要环节。诸多研究表明,稻田增施钾肥能够显著提高水稻产量及品质[11-12]。在我国钾肥资源供应严重不能自给的背景下,通过生理学研究和分子生物学手段,掌握作物的钾素营养规律,针对钾素利用的关键环节挖掘关键基因资源,是目前钾素养分优化管理以及对作物进行钾高效分子调控的重要环节之一。
通常,植物对土壤钾素的吸收、利用过程可分为3个阶段:①根系表皮吸收土壤中的钾离子;②钾在根内及根-地上部的传输;③钾在地上各组织部位的分配及行使调控功能(如气孔运动)[13]。这些过程分别由定位于细胞质膜上的相应钾转运体和钾离子通道来承担。在模式植物拟南芥中,根系从土壤中吸收钾离子及钾由根表向内部组织的转运主要是通过钾转运系统如高亲和钾转运体(KUP)及钾离子通道基因AKT1来完成[14-15];其中,KUP主要负责根系从土壤吸收钾离子[14],而AKT1主要介导钾离子在植物根内的转运[15-16]。外排型钾通道拟南芥AtSKOR基因主要定位于根的韧皮部,其作用是将根中的钾由韧皮部分泌至木质部,进而实现钾离子经由木质部的根-茎长距离运输[17]。缺失该通道活性导致拟南芥植株地上部含钾量降低约50%[17]。此外,AtSKOR基因的表达丰度受脱落酸(ABA)抑制,随着ABA处理时间的延长,几乎检测不到AtSKOR基因的存在,暗示ABA有可能参与钾离子所介导的渗透调节且在调控植物生长方面起着重要作用[17]。在地上部,钾的再运输或分配主要由双向整流型钾通道基因AKT2/3负责。AKT2/3主要在拟南芥包括根、茎、叶柄、花及叶片的韧皮部表达,通过介导钾离子在其中的装载和卸载从而实现钾离子在植株各部位的分配[18]。作为钾离子调控功能的典型例证,拟南芥保卫细胞中的KAT1和KAT2基因共同介导钾离子的吸收,其运作的结果使得保卫细胞钾离子积累,细胞膨压增大而促使气孔开放[19]。与此相反,外排型钾通道GORK的运作则降低保卫细胞的钾浓度从而关闭气孔[20]。
上述过程在拟南芥中已经比较明晰,而在水稻中目前仅限于类似的推测,还缺乏相应的实验证据。同时,与拟南芥相比,水稻中的KUP和钾通道蛋白则更为众多,预示其作用机制可能更为复杂。本文通过水培试验研究了不同供钾强度对4种基因型水稻日本晴(NB)、武育粳18(WYJ18)、南光(NG)及桂单4号(GD4)生长特性及养分吸收的影响,同时通过分根试验探究了根系局部供钾条件下水稻的生长状况,进而以日本晴为材料通过实时荧光定量PCR研究了水稻钾传输/转运通道基因OsKAT1;1、OsSKOR和OsAKT2/3的表达定位及其对外界供钾水平的响应特征,通过伤流试验探索了低钾条件下水稻根茎钾传输能力与OsSKOR基因之间存在的可能关联,为理解水稻钾的体内转运过程提供有益的依据。
1 材料与方法 1.1 试验材料及培养条件试验所用的4种基因型水稻品种分别为模式品种日本晴(NB)和生产品种武育粳18(WYJ18)、南光(NG)及桂单4号(GD4)。水稻种子经NaClO (2.5%,V/V)溶液消毒30 min,再用蒸馏水清洗6~8次去除种子表面的消毒液,于37℃培养箱浸种24 h使种子充分吸水后,均匀放置于尼龙网上暗处萌发6 d;挑选长势一致的幼苗,3颗1束移栽于盛有8 L国际水稻完全营养液(IRRI营养液)的周转箱中培养1周。周转箱四周及底部喷黑漆,以防藻类生长。IRRI营养液配方:1.25 mmol/L NH4NO3, 0.3 mmol/L KH2 PO4,0.5 mmol/L K2SO4,1 mmol/L CaCl2,1 mmol/L MgSO4·7H2O,0.5 mmol/L Na2SiO3·9H2O,20 μmol/L EDTA-Fe,20 μmol/L H3BO3,0.32 μmol/L CuSO4·5H2O,9 μmol/L MnCl2·4H2O,0.77 μmol/L ZnSO4·7H2O和0.39 μmol/L Na2MoO4·2H2O,用HCl调pH至5.5[21]。
温室培养条件:27℃/25℃(昼/夜),16 h/8 h(光照/黑暗),相对湿度70%,光强为400 μmol/(m2·s)。并于移苗后的第3天、第5天及第7天更换营养液,第7天选则长势一致的水稻苗分别于1 mmol/L CaSO4溶液(1 min)及蒸馏水中冲洗,以除去附着于根表面的离子,然后置于装有不同钾处理的IRRI营养液的1.2 L PVC桶中进行培养,每桶4穴。
1.2 试验设计水培试验:设置3个钾水平处理:低钾(LK,0.1 mmol/L K+),即在缺钾的IRRI营养液中加入所需浓度的KCl,并用NaH2PO4代替KH2PO4,其他成分保持不变,其余处理钾处理方式相同;高钾(HK,5 mmol/L K+);正常钾(MK,1 mmol/L K+),即中钾,为对照。每2 d更换1次营养液,处理10 d后收样。样品根系用1 mmol/L CaSO4及蒸馏水依次清洗干净,每处理收3个重复,将地上部和根部剪开,在烘箱中105 ℃杀青30 min,接着75 ℃左右烘72 h,称干重后再粉碎样品,用于钾含量测定。
分根试验:取上述正常钾浓度培养条件下生长1周且长势一致的水稻苗用于分根试验。水稻苗生长于IRRI营养液(不含钾),两侧根系处理分别为:①+K(5 mmol/L KCl);②-K(5 mmol/L NaCl),其他养分均同完全营养液。每个分根培养箱种6穴,每穴8棵苗。分根处理两侧营养液均为6 L,每2 d换1次,处理10 d后取样测定总根长和根表面积。
基因表达试验:取上述正常钾浓度培养条件下生长1周且长势一致的日本晴水稻苗进行低钾(LK,0.1 mmol/L K+)、正常钾(MK,1 mmol/L K+)、高钾(HK,5 mmol/L K+)处理4 d和7 d后,将水稻地下部样品分整体根、根段(0~1.5、1.5~3.0、>3.0 cm)及根茎连接处收样;并于处理当天早上9:00对样品进行ABA处理(完全营养液中加入ABA至浓度为10 μmol/L),分别于处理0、2、4、8、12、24、72 h不同时间点收取水稻根样,迅速置于液氮中速冻,-80 ℃保存备用,用于进行不同钾离子通道基因在各个部位的表达试验。
伤流试验:收集水培试验中低钾处理4 d和7 d的水稻伤流液。具体为:于当日17:00距离根茎结合处约2 cm处用刀割去上部水稻茎秆,并用脱脂棉擦干切口液后,再用装有脱脂棉的自封袋套于剩余茎秆上,并保持脱脂棉和切口充分接触,放于黑暗环境中收集,于次日早上9:00取回称重。脱脂棉吸收伤流液前后重量差即为伤流量[22]。于装有脱脂棉的自封袋中加入适量蒸馏水,揉捏混匀后,用带有滤芯的注射器挤出伤流液保存,用于进一步分析伤流液中ABA含量和钾含量。
1.3 测定项目及方法 1.3.1 ABA含量及钾含量的测定伤流液中的ABA含量使用MALLBIO公司提供的植物激素脱落酸(ABA)试剂盒MBE21031进行测定。不同基因型水稻在不同钾浓度处理下地上部、根部钾含量及伤流液中钾含量通过HG-5型火焰光度计(北京检测仪器有限公司)测定[23]。
1.3.2 水稻根系活力的测定用伤流强度评估根系活力,计算公式为:伤流强度=伤流液中钾的含量/(烘干根重×时间)。伤流液的收集时间为16 h,伤流液收集完成后将根系放于烘箱烘至恒重并称量。
1.3.3 根表面积及根长的测定通过Epson根系扫描仪获取分根试验中+K和-K处理10 d的水稻根系图像,通过WinRHIZO软件分析获得其根长及根表面积指标。
1.3.4 水稻钾通道基因检索与引物设计从水稻基因组网站(http://rice.plantbiology.msu.edu)检索得到OsAKT2/3, OsKAT1;1及OsSKOR的cDNA序列,采用Primer 5软件及NCBI网站Primer-BLAST工具设计引物(表 1)。采用Plant CARE (http://bioin-formatics.psb.ugent.be/webtools/plantcare/html/)[24]对水稻SKOR启动子顺式作用元件进行预测分析。
|
|
表 1 OsKAT1;1、OsAKT2/3和OsSKOR基因表达丰度检测引物 Table 1 Primers used to amplify OsKAT1;1, OsAKT2/3, OsSKOR genes of rice for testing expressive abundance |
用Trizol法提取不同钾浓度及ABA处理基因表达试验水稻各个部位样品RNA,使用超微量核酸蛋白测定仪Nanodrop 2000(北京芯起点基因科技) 测定RNA浓度,并用甲醛变性胶电泳检测RNA质量。甲醛变性胶的制备:称取0.72 g Agarose于三角瓶中,加入Running buffer(10×)及DEPC水,于微波炉溶解,待降温至60 ℃,于通风橱中加入甲醛溶液,此时溶液体积约60 ml,充分摇匀后倒板。RNA电泳样品制备:于1.5 ml离心管中加0.5 μg RNA样品及5 μl的Mix混合液,并用DEPC水补充至13 μl,混匀后65 ℃金属浴加热10 min,冰上冷却后用于电泳检测。电泳条件:80 V,1 h。
反转录及基因扩增:采用Prime Script RT reagent Kit (Takara)将RNA反转录为cDNA,用于基因转录表达的半定量及定量检测。用2×Phanta Master Mix(Vazyme)进行半定量的PCR扩增检测,用LightCycler480Ⅱ荧光定量PCR仪(罗氏公司)对基因表达进行定量检测,内参基因选用Actin (Os03g 50885),基因相对表达量用2-ΔΔCt公式计算。
1.4 数据处理数据统计分析使用SPSS 16.0,用T-test进行显著性检验,采用Sigma Plot 13.0软件作图。
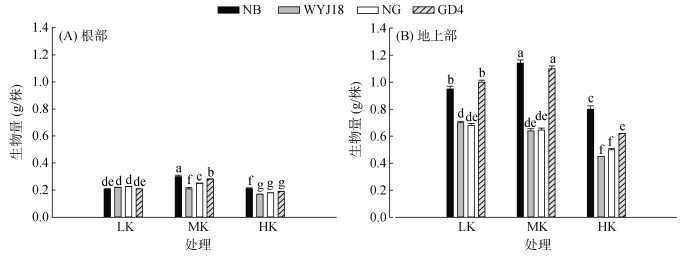
2 结果与分析 2.1 不同供钾水平对4种基因型水稻生长的影响不同供钾水平的水培试验结果表明,高钾条件(HK)对4种基因型水稻的生长都有不同程度的抑制作用,地上部和根部生物量与正常供钾条件(MK)相比均显著降低(图 1)。高钾条件下根部生物量降低的幅度在不同基因型水稻中差异不大,均为30.0% 左右(图 1A)。地上部生物量降低幅度最大的是GD4,达43.6%,降低幅度最小的是NB,为22.4%(图 1B)。与高钾条件相比,WYJ18及NG在低钾及正常供钾条件下的生物量较低,而NB和GD4在3个钾水平下生物量均较高(图 1)。
|
(图中LK为低钾处理,MK为中钾处理,HK为高钾处理;柱图上方不同小写字母表示不同钾水平及基因型水稻下处理差异在P < 0.05水平显著;下同) 图 1 不同基因型水稻在不同供钾水平下根部及地上部生物量 Fig. 1 Biomass of roots and shoots of rice genotypes under different K supplying levels |
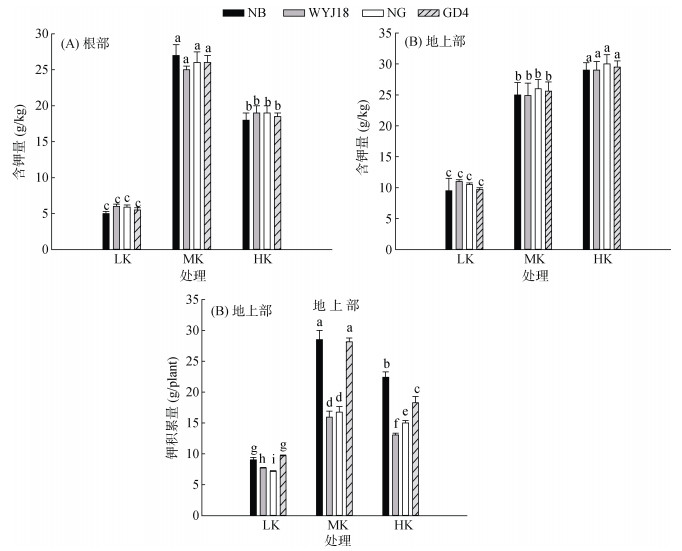
图 2A结果表明,4种基因型水稻根部的含钾量在正常供钾条件下最高,而在高钾和低钾条件下其含钾量都明显下降。与正常供钾相比,低钾处理时4种水稻的根部含钾量均降低了约4.5倍;而高钾处理的根系含钾量降低约40%(图 2A)。然而4种基因型水稻的地上部含钾量则随外界供钾浓度的增加呈现出较一致的显著增加趋势(图 2B)。其中正常供钾时,4种水稻的含钾量是低钾条件时的2.5倍;继续增加供钾浓度(HK),地上部含钾量仅呈略有增加趋势(增幅均15%)(图 2B)。这一结果表明,水稻根系对供钾浓度较为敏感,缺钾或过量供钾不利于水稻生长。在同一供钾水平下,无论是在根部还是地上部,4种水稻的含钾量均无显著差异(图 2A和2B)。而在钾素利用效率方面,4种水稻在正常供钾条件下的钾积累量达到最高,其中NB和GD4的钾积累量较WYJ18和NG增加了近1倍(图 2C),结合图 1B结果,NB及GD4在低钾条件下即可保持较好的生长,推测NB和GD4较WYJ18和NG有更强的钾吸收及转运能力。
|
图 2 不同基因型水稻在不同处理条件下的含钾量 Fig. 2 Potassium content of different rice genotypes in response to different growth conditions |
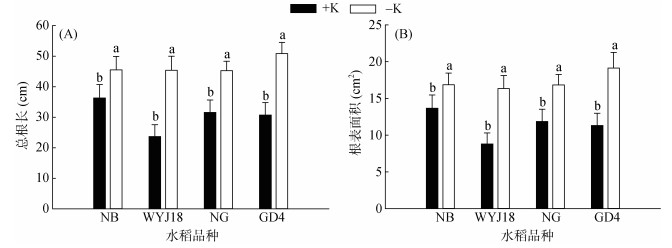
将在正常供钾条件下生长一周的水稻苗根系均分为两部分置于分根根系生长箱中,一侧供钾(5 mmol/L K+),一侧缺钾处理10 d,结果表明,缺钾一侧4种基因型水稻的根系生长均比供钾侧更快。与供钾侧相比,不同基因型水稻在缺钾侧的总根长均显著增加(图 3A)。同时根表面积的变化趋势与总根长的变化趋势一致,缺钾侧的根表面积显著大于供钾一侧(图 3B),而分侧供钾时地上部的生物量与全根供钾时没有显著差异(同图 1B),说明根部分侧供钾对地上部生长的影响非常小,根系局部供钾即可满足水稻生长需求。
|
(柱图上方不同小写字母表示同一水稻品种下处理间差异显著(P < 0.05)) 图 3 分根试验中不同基因型水稻的总根长及根表面积 Fig. 3 Total root lengths and root surface areas of different rice genotypes in split-root experiments |
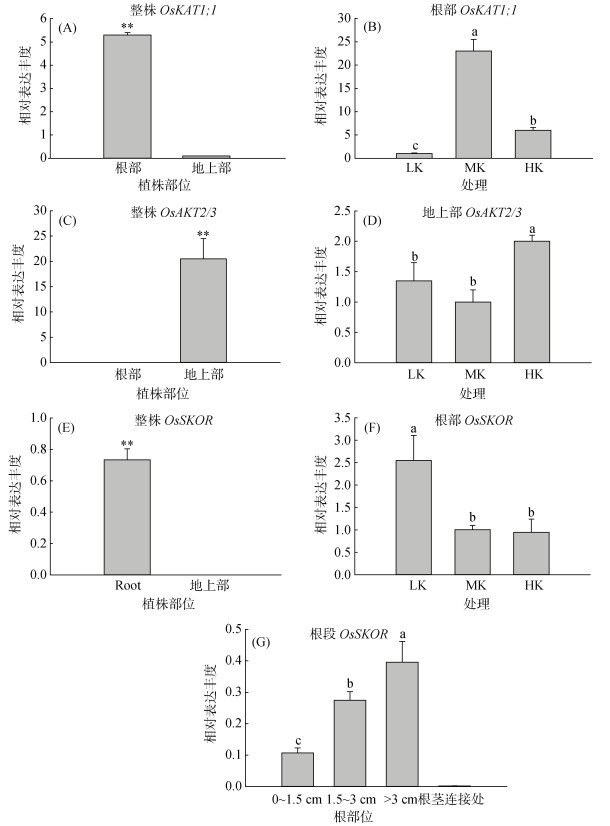
以NB为研究材料,通过实时定量PCR研究表明,内向型钾离子通道基因OsKAT1;1主要定位于根部(图 4A),OsAKT2/3基因主要定位于地上部(图 4C),其中OsAKT2/3基因在地上部的表达丰度受高钾的诱导,增幅约1倍,而在低钾下的表达丰度与对照相比无显著差异(图 4D)。在根部,OsKAT1;1基因在正常供钾条件下的表达丰度最高(图 4B)。而外向型钾离子通道OsSKOR则主要在水稻的根系表达(图 4E),进一步的根系分段定量PCR结果表明,OsSKOR基因主要在距根尖大于1.5 cm的成熟区表达(图 4G),且在根部的表达丰度受低钾诱导(图 4F),而对高钾的响应不敏感,推测OsSKOR很可能是一个在低钾环境中起重要作用的钾离子通道基因。
|
(柱图上方**或不同小写字母表示植株不同部位或不同处理间差异在P < 0.05水平显著) 图 4 不同供钾水平下水稻钾离子通道OsKAT1;1、OsAKT2/3及OsSKOR基因响应 Fig. 4 Responses of OsKAT1;1, OsAKT2/3 and OsSKOR genes of rice to different K supplying levels |
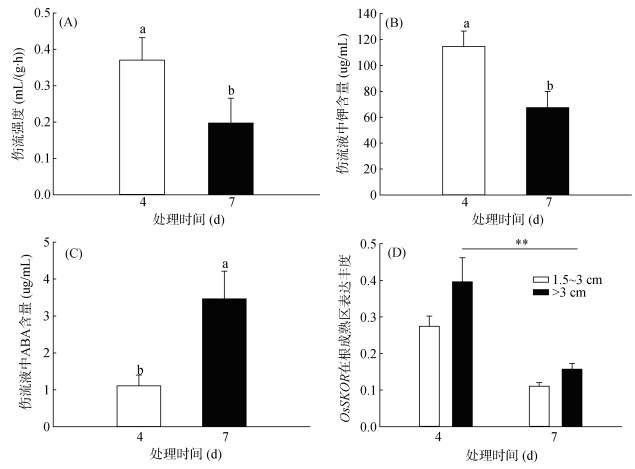
在拟南芥中,SKOR基因在根茎钾传输过程中发挥着极其关键的作用[17]。为进一步了解OsSKOR基因在低钾条件下可能发挥的作用,本研究通过伤流试验评估了NB水稻在低钾处理后的根系活力,同时测定了伤流液组分中的ABA含量及钾含量。结果表明,随着低钾处理时间的延长,根系活力逐渐降低,与处理4 d相比,处理7 d后的水稻根系活力降低了约50%(图 5A);低钾处理7 d后,伤流液中ABA含量是低钾处理4 d的3倍(图 5C),而钾含量比低钾处理4 d降低约1倍(图 5B),随低钾处理时间的延长,伤流液中ABA含量与钾含量呈相反的变化趋势。与此同时,OsSKOR基因的表达丰度却随着低钾处理时间的推移而下降(图 5D),暗示缺钾条件下,水稻体内积累的ABA可能与参与钾离子从根向茎传输过程中的钾离子通道基因OsSKOR存在紧密联系。
|
(柱图上方**或不同小写字母表示不同处理时间间差异在P < 0.05水平显著;下同) 图 5 低钾处理下不同时间水稻伤流强度(A)、钾(B) 伤流液组分中ABA(C)、含量及OsSKOR在根成熟区的表达丰度(D) Fig. 5 Bleeding sap intension (A), K (B) and ABA (C) contents in bleeding saps in different time under low K condition and relative expression (D) of OsSKOR in maturation zone of root |
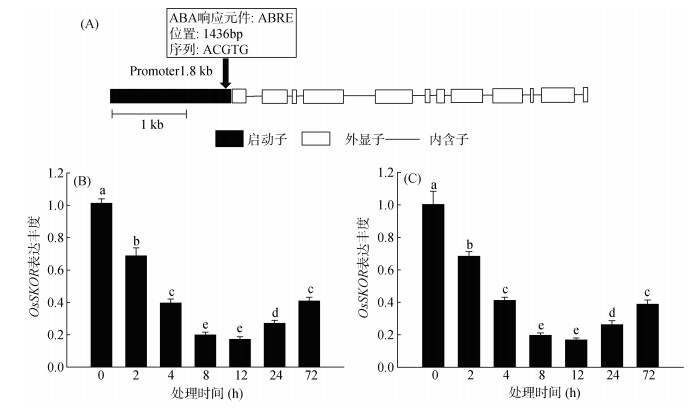
启动子作为调控基因表达的重要顺式作用元件,在基因表达过程中具有重要作用。本研究使用启动子分析软件对OsSKOR基因起始密码子ATG上游1.8 kb的序列进行了预测,结果显示,OsSKOR基因启动子内除含有必需的核心元件CAAT-box和TATA-box外,还存在对ABA响应的ABRE元件(图 6A),预测ABA可能调控SKOR基因的转录水平。ABA作为一种胁迫激素,在低温、高温、干旱和盐害等多种胁迫下,植物体ABA含量大幅度升高。进而,为进一步证实ABA含量与OsSKOR基因转录丰度的直接关系,本研究在正常供钾水平(对照)中添加10 μmol/L ABA,研究ABA处理不同时间后水稻根系样品OsSKOR基因表达量的变化。提取RNA并通过定量PCR研究发现,与对照相比,使用两对引物的平行定量试验结果均表明,ABA显著抑制OsSKOR基因的表达,随着处理时间的延长,其表达丰度显著降低(图 6B和6C)。这些结果表明,低钾条件下,ABA很可能在钾从水稻根部向地上部的传输过程中扮演着重要角色,相关研究需要进一步证实。
|
(A:OsSKOR的基因结构;B:外源ABA处理不同时间水稻根系SKOR相对表达丰度(第一对引物);C:外源ABA处理不同时间水稻根系SKOR相对表达丰度(第二对引物)) 图 6 OsSKOR基因结构及其对ABA的响应特征 Fig. 6 Structure (A) of OsSKOR gene and expression (B and C exogenous sources) of root-specific SKOR gene in response to ABA |
钾是植物生长最关键的矿质营养元素之一,在植物生长发育的各个时期都发挥着关键作用。在我国耕地土壤普遍缺钾的背景下,由于长期耕作过程中施肥量、肥料种类及施肥方式的差异,促使土壤钾的供应强度及空间分布存在非均匀性[4]。
本研究以日本晴(NB)、武育粳18(WYJ18)、南光(NG)及桂单4号(GD4)四种基因型水稻为材料模拟根系钾不均匀分布状况,发现4种不同基因型水稻缺钾一侧的根系总根长和根表面积均显著高于供钾侧,这与王为木等[8]研究发现水稻根系在缺钾时变长且侧根增多结果一致。不均匀供钾时水稻地上部生物量与全根供钾没有显著差异,根系局部供钾即可满足水稻正常的生长需求,由此可以说明,田间施肥方式侧施等不影响水稻的生长。通过水培试验对4种基因型水稻供应不同钾水平的研究发现,4种水稻在正常供钾(1 mmol/L K+)条件下生物量达到最高,这与薛欣欣和李小坤[25]报道的水稻品种丰两优香1号和两优6326在中等钾肥供应水平下其地上部干物质量即可达到较高水平的结果一致;钾积累量在正常供钾条件下达到最高,而高钾(5 mmol/L K+)条件反而抑制水稻生长及钾的积累,由于NB和GD4在低钾及正常供钾条件下均能保持较高的生物量,推测NB和GD4具有高效利用养分产生生物量的能力。
植物通过根系从土壤中吸收获取钾营养,再将钾分配到各个部位,主要是由定位于细胞膜上的钾转运体及钾通道完成[26]。本研究以NB为研究材料,初步分析了水稻钾离子通道OsKAT1;1, OsSKOR及OsAKT2/3基因的定位及其对外界不同供钾状态的响应特征,结果表明,OsAKT1;1基因主要定位于根部,其表达受高钾和低钾抑制,在正常供钾条件下表达丰度最高。OsAKT2/3基因在地上部的表达丰度受高钾供应的诱导,其作用机理有待进一步深入研究。而OsSKOR基因与已经报道的AtSKOR基因高度同源[17],在根部特异性表达,与Kim等[27]对其定位研究结果一致,且其表达丰度受外界低钾的诱导,推测是一个在外界低钾环境中起关键作用的基因。根系伤流不仅可以作为根系活力的重要指标,也是植物体内溶质从根向茎传输能力的体现[28],本研究通过伤流试验初步探讨了低钾条件下水稻的根系活力及伤流钾含量与OsSKOR基因之间的关系,发现随低钾处理时间的延长伤流液中ABA含量增加;同时伤流强度及钾离子含量随处理时间的延长而降低,OsSKOR基因的表达量也同步降低。一方面,长时间缺钾会影响根系活力,OsSKOR基因的表达丰度降低,导致从根部转运到地上部的钾减少,暗示OsSKOR基因在水稻根茎钾传输过程中起关键作用,很可能与已经报道的AtSKOR基因的功能一致[17];另一方面,长时间缺钾导致ABA含量大幅度增加,而外源添加ABA显著降低了OsSKOR基因的表达丰度。推测在水稻中,ABA很可能参与调控了OsSKOR基因介导的根茎钾传输过程。水稻伤流液中含钾量与ABA含量之间的变化关系与本研究发现OsSKOR基因在低钾下起着更关键的作用及前人研究发现SKOR基因钾外排能力受ABA抑制的结果相吻合[17],推测水稻伤流液中观察到的现象可能与OsSKOR基因的功能有关。鉴于OsSKOR基因在根茎钾传输环节及其在低钾胁迫中可能发挥的重要作用,进一步深入研究其功能并充分发挥其用钾能力很可能是一项行之有效的提高作物钾素利用效率的措施。
4 结论1) 高钾条件可抑制4种基因型水稻地上部和根部生物量,根部生物量降低幅度均为30% 左右,地上部生物量降低幅度最大的是GD4,达43.6%,降低幅度最小的是NB,为22.4%。与高钾条件相比,WYJ18及NG在低钾及正常供钾条件下的生物量较低,而NB和GD4在3个钾水平下生物量均较高;与正常供钾相比,4种基因型水稻低钾处理时根部含钾量均降低了约4.5倍,高钾处理的根系含钾量降低约40%,地上部含钾量随外界供钾浓度的增加呈现出较一致的显著增加趋势;4种不同基因型水稻不均匀供钾时缺钾一侧的根系总根长和根表面积均显著高于供钾侧。
2) NB水稻钾离子通道OsKAT1;1基因主要定位于根部,其表达受高钾和低钾抑制,在正常供钾条件下表达丰度最高;OsAKT2/3基因在地上部的表达丰度受高钾供应的诱导;OsSKOR基因在根部特异性表达,且其表达丰度受外界低钾的诱导。
3) 低钾处理时间延长,根系活力逐渐降低,处理7 d比处理4 d的水稻根系活力降低了约50%,低钾处理7 d后,伤流液中ABA含量是低钾处理4 d的3倍,钾含量比低钾处理4 d降低约1倍,OsSKOR基因的表达丰度却随着低钾处理时间的推移而下降。
4) OsSKOR基因启动子内存在对ABA响应的ABRE元件,随着ABA处理时间的延长,OsSKOR基因的表达丰度显著降低。
| [1] |
Leigh R A, WYN JONES R G. A hypothesis relating critical potassium concentrations for growth to the distribution and functions of this ion in the plant cell[J]. New Phytologist, 1984, 97(1): 1-13 DOI:10.1111/j.1469-8137.1984.tb04103.x (  0) 0) |
| [2] |
Song Z Z, Su Y H. Distinctive potassium-accumulation capability of alligatorweed (alternanthera philoxeroides) links to high-affinity potassium transport facilitated by K+-uptake systems[J]. Weed Science, 2013, 61(1): 77-84 DOI:10.1614/WS-D-12-00100.1 (  0) 0) |
| [3] |
Maathuis F J M, Amtmann A. K+ Nutrition and Na+ toxicity: The basis of cellular K+/Na+ ratios[J]. Annals of Botany, 1999, 84(2): 123-133 DOI:10.1006/anbo.1999.0912 (  0) 0) |
| [4] |
朱向东, 王宏庭. 土壤钾素管理研究进展[J]. 山西农业科学, 2013, 41(11): 1274-1281 (  0) 0) |
| [5] |
黄绍文, 金继运. 土壤钾形态及其植物有效性研究进展[J]. 土壤肥料, 1995(5): 23-28 (  0) 0) |
| [6] |
陈防, 郑圣先. 我国南方作物高效施钾技术的研究进展[J]. 土壤肥料, 2004(6): 28-32 (  0) 0) |
| [7] |
胡泓, 王光火, 张奇春. 田间低钾胁迫条件下水稻对钾的吸收和利用效率[J]. 中国水稻科学, 2004, 18(6): 527-532 (  0) 0) |
| [8] |
王为木, 杨肖娥, 李华, 等. 低钾胁迫对两个耐钾能力不同水稻品种养分吸收和分配的影响[J]. 中国水稻科学, 2003, 17(1): 52-56 (  0) 0) |
| [9] |
Mengel K, Kirkby E A. Principles of plant nutrition(4th Edition)[M].
International Potash Institute, Bern Switzerland, 1987: 687
(  0) 0) |
| [10] |
Mengel K, Kirkby E A, Kosegarten H, et al. Potassium[M]//Principles of Plant Nutrition. Dordrecht: Springer Netherlands, 2001: 481-511.
(  0) 0) |
| [11] |
林咸永, 孙義. 不同水稻品种对钾的吸收及其对钾肥的反应[J]. 土壤学报, 1995, 32(1): 77-83 (  0) 0) |
| [12] |
李华, 杨肖娥, 罗安程. 不同氮钾条件下水稻基因型氮、钾积累利用差异[J]. 中国水稻科学, 2002, 16(1): 86-88 (  0) 0) |
| [13] |
Besford R T. Effect of replacing nutrient potassium by sodium on uptake and distribution of sodium in tomato plants[J]. Plant and Soil, 1978, 50(1/2/3): 399-409 (  0) 0) |
| [14] |
Kim E J, Kwak J M, Uozumi N, et al. AtKUP1:an Arabidopsis gene encoding high-affinity potassium transport activity[J]. The Plant Cell, 1998, 10(1): 51-62 DOI:10.1105/tpc.10.1.51 (  0) 0) |
| [15] |
Xu J, Li H D, Chen L Q, et al. A protein kinase, interacting with two calcineurin B-like proteins, regulates K+ transporter AKT1 in Arabidopsis[J]. Cell, 2006, 125(7): 1347-1360 DOI:10.1016/j.cell.2006.06.011 (  0) 0) |
| [16] |
徐赫韩, 侯国媛, 李洋, 等. 植物钾离子通道AKT1的研究进展[J]. 生物技术, 2018, 28(2): 200-205 (  0) 0) |
| [17] |
Gaymard F, Pilot G, Lacombe B, et al. Identification and disruption of a plant shaker-like outward channel involved in K+ release into the xylem Sap[J]. Cell, 1998, 94(5): 647-655 DOI:10.1016/S0092-8674(00)81606-2 (  0) 0) |
| [18] |
Lacombe B, Pilot G, Michard E, et al. A shaker-like K+ channel with weak rectification is expressed in both source and sink phloem tissues of Arabidopsis[J]. The Plant Cell, 2000, 12(6): 837-851 (  0) 0) |
| [19] |
Pilot G, Lacombe B, Gaymard F, et al. Guard cell inward K+ Channel activity inArabidopsisInvolves expression of the twin channel subunits KAT1 and KAT2[J]. Journal of Biological Chemistry, 2001, 276(5): 3215-3221 DOI:10.1074/jbc.M007303200 (  0) 0) |
| [20] |
Schroeder J I. Knockout of the guard cell K+ out channel and stomatal movements[J]. PNAS, 2003, 100(9): 4976-4977 DOI:10.1073/pnas.1031801100 (  0) 0) |
| [21] |
Yang S Y, Hao D L, Song Z Z, et al. RNA-Seq analysis of differentially expressed genes in rice under varied nitrogen supplies[J]. Gene, 2015, 555(2): 305-317 DOI:10.1016/j.gene.2014.11.021 (  0) 0) |
| [22] |
郭士伟, 夏士健, 朱虹霞, 等. 水稻根系活力测定方法及超级稻两优培九生育后期根系活力研究[J]. 土壤, 2012, 44(2): 308-311 (  0) 0) |
| [23] |
王敬, 王火焰, 周健民, 等. 盐酸提取-火焰光度计法测定黑麦草中钾含量的可行性研究[J]. 土壤通报, 2013, 44(3): 624-627 (  0) 0) |
| [24] |
Lescot M, Déhais P, Thijs G, et al. PlantCARE, a database of plant cis-acting regulatory elements and a portal to tools for in silico analysis of promoter sequences[J]. Nucleic Acids Research, 2002, 30(1): 325-327 DOI:10.1093/nar/30.1.325 (  0) 0) |
| [25] |
薛欣欣, 李小坤. 施钾量对水稻干物质积累及吸钾规律的影响[J]. 江西农业大学学报, 2018, 40(5): 905-913 (  0) 0) |
| [26] |
Véry A A, Sentenac H. Molecularmechanisms andregulation of K+ transport inhigherplants[J]. Annual Review of Plant Biology, 2003, 54(1): 575-603 DOI:10.1146/annurev.arplant.54.031902.134831 (  0) 0) |
| [27] |
Kim H Y, Choi E H, Min M K, et al. Differential gene expression of two outward-rectifying shaker-like potassium channels OsSKOR and OsGORK in rice[J]. Journal of Plant Biology, 2015, 58(4): 230-235 DOI:10.1007/s12374-015-0070-4 (  0) 0) |
| [28] |
黄沆, 陈光辉. 水稻根系育种的研究现状及展望[J]. 湖南农业大学学报(自然科学版), 2009, 35(z1): 35-39 (  0) 0) |
2. University of Chinese Academy of Science, Beijing 100049, China
 2021, Vol. 53
2021, Vol. 53


