2. 水利部山洪地质灾害防治工程技术研究中心, 武汉 430010;
3. 中南安全环境技术研究院股份有限公司, 武汉 430071
生物土壤结皮简称生物结皮,是由微观(藻类、细菌、真菌等)和宏观(地衣类、苔藓类)变水生物体与土壤表层颗粒胶结而成的厚度几毫米至几厘米的特殊复合体[1-2]。生物结皮广泛分布于各类气候和生境,是陆地生态系统地表景观的重要组成部分,在不同生物气候区的土壤–水文–侵蚀过程中发挥着重要作用[3-4],如改良土壤属性[5]、调控土壤水热特性[6]、增强土壤稳定性从而提高土壤抗侵蚀能力[7-8]、影响土壤水文过程[9-10]等。普遍认为生物结皮增强土壤抗侵蚀能力的作用是其最重要的生态功能之一,目前在许多生态区均有证实[11-13]。
土壤侵蚀包括土壤分离、泥沙输移和泥沙沉积,土壤分离是指在降雨击溅或径流冲刷作用下,土壤颗粒脱离土体、发生位移的过程[14-15]。国际上对径流驱动的土壤分离过程的研究,大多基于一种“临界”思想,即水流剪切力超过临界剪切力时土壤发生分离[16],如国际上极具代表性的水蚀预报计划(WEPP)模型[17]。对给定的水动力条件,土壤分离主要受控于土壤内在属性,与地表粗糙度[18]、植物茎秆覆盖[19]、枯落物[20]、生物结皮[21]、植物根系[22-23]等近地表特性密切相关。
作为近地表特征的重要组分[23-24],生物结皮的存在可通过影响外在水力特性(侵蚀动力或水流侵蚀力)和内在土壤属性(侵蚀阻力或土壤可蚀性)来影响土壤侵蚀过程[16]。尽管目前生物结皮在增强土壤抗侵蚀能力方面的作用已得到普遍共识[7, 25],但其作用机理仍不清楚。杨凯等[26]发现生物结皮的强稳定层状结构是其具有较强抗侵蚀能力的根本原因,而有研究指出生物结皮是通过削弱侵蚀动力来减轻侵蚀[27]。Knapen等[28]认为,植被、作物残茬、枯落物、生物结皮、砾石等地表覆盖要素严格讲都不属于土壤侵蚀阻力概念,其减蚀作用是通过影响侵蚀动力而不是影响土壤属性。Gao等[12]的研究则表明生物结皮是通过其地表覆盖的直接物理保护作用和改善土壤属性的间接作用来提高土壤抗侵蚀性的。Chaudhary等[29]也指出生物结皮覆盖对土壤抗侵蚀作用是其他因子的3倍。可见,关于生物结皮如何影响土壤侵蚀的变化仍存争议。
目前有关生物结皮影响土壤分离过程的研究非常薄弱,且主要集中于干旱半干旱地区。Wang等[30]对黄土高原的研究指出,土壤分离能力与生物结皮发育程度呈负指数关系,其抑制土壤分离的水流剪切力阈值为11 Pa[24]。有研究显示生物结皮通过地表覆盖、假根及菌丝的物理捆绑和分泌物的化学胶结作用影响土壤分离过程[31],且其盖度达到50% 后,生物结皮将不再被水流冲刷破坏[32]。然而,仍有一些问题尚未解决:生物结皮覆盖/盖度如何影响土壤分离过程?土壤分离与生物结皮盖度间的关系如何?此外,生物结皮可以改变土壤内在属性,那么体现土壤性质的哪些具体变量与土壤分离能力或土壤侵蚀阻力密切相关?生物结皮是否通过改变这些土壤属性间接影响土壤分离过程?解决这些问题有助于进一步理清生物结皮在抗侵蚀方面的重要作用,进而深入理解生物结皮对土壤分离的影响机制。
三峡库区是长江上游重要的生态屏障,也是我国土壤侵蚀最为严重的区域之一。为治理水土流失,自20世纪80年代起该区开始大力实施水土保持生态建设工程[33-34],植被得到迅速恢复,侵蚀环境发生变化,生物结皮也因此广泛发育,继而对整个植物群落及地表过程产生深刻影响[35-36]。鉴于此,开展三峡库区生物结皮对土壤分离过程的影响机制研究,既是对国内外生物结皮生态功能认知的重要补充,也为深入理解土壤侵蚀过程机理,构建或完善土壤侵蚀过程模型提供理论参考。
1 材料与方法 1.1 研究区概况研究区位于三峡库区秭归县王家桥小流域(110°40′ ~ 110°47′E,31°04′ ~ 31°15′N),是长江二级支流,出口距三峡大坝约50 km,流域总面积16.7 km2。流域坡度陡峭,为典型的山区小流域,海拔184 ~ 1 180 m。气候属亚热带大陆性季风气候,温和湿润,年均气温18 ℃,年均降水量1 016 mm,主要集中在5—9月,占全年降雨总量的70% 以上。流域内土壤类型主要是紫色土,是由白垩纪和侏罗纪的紫色砂页岩发育而成的一种岩性土,土层浅薄,砾石含量高[37]。紫色土极易发生侵蚀,侵蚀模数达4 887 t/(km2·a),其中由集中水流引起的细沟侵蚀在泥沙输移中占主导地位[38]。植被属亚热带常绿林,主要为次生混交林,林下有灌草分布。该区生物结皮群落以苔藓类为优势种,且在退耕地及人为干扰较少的梯田(柑橘等经济林)发育较好,在海拔较高的区域也有藻类和苔藓混生结皮。
1.2 土样采集与测定采样时间为2019年9月,在王家桥小流域选取以苔藓为优势种的结皮样地,设计5个盖度等级(1% ~ 20%、20% ~ 40%、40% ~ 60%、60% ~ 80% 和80% ~ 100%),以无结皮覆盖的裸地作为对照。采用网格法[21]对结皮盖度进行近似测量,并用数码相机拍照,室内通过图片处理软件逐个验证,以确定生物结皮的准确盖度。结皮厚度用游标卡尺“S”型布点原位测定,每个处理重复20次。在每个采样点附近,利用便携式剪切仪(Durham Geo-enterprises, Inc., UK)测定土壤黏结力,每个处理测定15次。用环刀(100 cm3)取样测定土壤容重和土壤水分,每个处理重复3次。用剖面刀采集0 ~ 5 cm土样5个,混匀风干后过2 mm筛,用于测定以下土壤属性指标:土壤质地通过马尔文MS2000型激光粒度仪测定;pH采用酸度计测定(水土比为1:2.5);有机碳的测定采用重铬酸钾外加热法。此外,用铝盒采集不同处理原状土样各3次,用于测定土壤水稳性团聚体,团聚体稳定性用平均重量直径(MWD)进行评价,通过下式计算:
| $ {\rm{MWD}} = \sum\limits_{i = 1}^n {({x_i}{w_i})} $ | (1) |
式中:MWD为平均重量直径(mm),xi是两个相邻筛孔的平均直径(mm),wi是剩余在第i级筛子上的团粒质量占土样总质量的百分比。
1.3 土壤分离冲刷试验土壤分离样品采集器为直径9.8 cm、高5.0 cm的不锈钢环,采样时,选取较为平整的地面,小心剪除杂草,同时用软毛刷扫去地表枯落物,将不锈钢环垂直压入土壤,使土体完整进入环刀。当环刀上沿与土壤表面平齐时,盖好顶盖,用剖面刀剖出土样环,削去下部多余土壤,盖上底盖。
冲刷试验在长4 m、宽0.4 m的变坡水槽内进行,坡度可在0 ~ 60% 之间调节。在水槽底部粘一层试验用土壤,以模拟相似的地表粗率。流量由阀门组控制并通过流量计观测,距水槽底端0.5 m处为直径10 cm的圆形放样室。水流表面流速通过染色法测定,记录染色水流流过距水槽出水口0.6 m以上2 m的测区所需时间,重复10次取平均值作为平均表面流速。同时测定水温,以计算水流运动黏滞系数和雷诺数,根据流态将表面流速乘以修正系数即为平均流速[39]。水流深度和剪切力通过下式计算:
| $ h = \frac{Q}{{VB}} $ | (2) |
| $ \tau = \rho ghS $ | (3) |
式中:h为水深(m),Q为流量(m3/s),V为平均流速(m/s),B为水槽宽度(m),τ为水流剪切力(Pa),ρ为水的密度(kg/m3),g为重力加速度(9.8 m/s2),S为坡度(m/m)。通过不同流量和坡度的组合,本研究选取6组水动力条件进行冲刷试验,水流剪切力介于4.89 ~ 17.99 Pa(表 1),每组侵蚀动力下重复冲刷5个土样,则每个处理需取30个土样,共采集并冲刷180个土样。
|
|
表 1 土壤分离试验坡面流水动力学特性 Table 1 Hydraulic parameters for soil detachment tests |
进行冲刷试验时,调整流量和坡度到设计值,将充分饱和后的土样移置放样室,保持土样表面与槽底平齐,待土样冲刷大约2 cm深度时停止试验[14],并记录冲刷时间;将冲刷后的土样放置于烘箱,105 ℃下烘至恒重,以冲刷前后土样的质量差除以土样面积和冲刷时间,即可得到土壤分离能力。根据WEPP模型[40]:
| $ {D_{\rm{c}}} = {K_{\rm{r}}}(\tau -{\tau _{\rm{c}}}) $ | (4) |
式中:Dc为土壤分离能力(kg/(m2·s));Kr为细沟可蚀性(s/m);τ和τc分别为水流剪切力(Pa)和临界剪切力(Pa)。以水流剪切力为横坐标、以实测的土壤分离能力为纵坐标,进行线性拟合,则拟合直线的斜率为细沟可蚀性(Kr),而拟合直线在横坐标上的截距为临界剪切力(τc)[16];Kr和τc又被称为土壤侵蚀阻力参数[15-16]。
1.4 数据统计分析数据的正态性检验采用K-S检验方法。不同处理土壤分离能力、土壤属性的差异性检验采用单因素方差分析,通过独立样本t检验比较结皮土壤与裸地之间相关指标的差异。通过简单回归分析拟合土壤分离能力与水流剪切力、生物结皮特性(盖度、厚度)或土壤属性之间的关系,通过非线性逐步回归拟合土壤分离能力、生物结皮特性和土壤属性之间的关系,回归拟合优度用决定系数(R2)和纳什效率系数(NSE)评估。此外,利用Pearson相关分析探寻土壤分离与生物结皮和土壤属性之间的相关性,进一步采用通径分析识别影响土壤分离的关键因素并确定其直接和间接作用。数据的统计分析均采用SPSS18.0软件进行,显著性水平0.05。
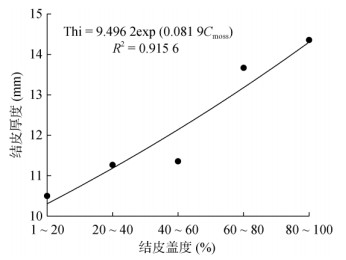
2 结果 2.1 生物结皮盖度对结皮厚度及土壤属性的影响本研究中结皮厚度最小值为8.24 ~ 11.74 mm,最大值为12.26 ~ 16.51 mm,平均厚度为10.50 ~ 14.36 mm,呈低到中度变异(表 2)。方差分析显示结皮盖度显著影响其厚度(P=0.000),高盖度处理(60% ~ 80% 和80% ~ 100%)下的结皮厚度明显大于中低盖度(1% ~ 20%、20% ~ 40% 和40% ~ 60%),但高盖度处理间及中低盖度处理间差异不显著。回归分析显示生物结皮厚度(Thi)随其盖度(Cmoss)呈指数增加(图 1):
|
|
表 2 不同处理苔藓结皮厚度统计描述 Table 2 Statistical descriptive of measured moss-crust thickness for different coverages |
|
图 1 结皮厚度与盖度之间的关系 Fig. 1 Relationship between biocrust thickness and coverage |
对于土壤属性,方差分析显示各处理土壤pH差异不显著(表 3),而其他土壤属性指标受结皮盖度显著影响(P < 0.05)。土壤黏结力、黏粒含量和水稳性团聚体随结皮盖度增大而显著增加,土壤容重、粉粒、砂粒、平均重量直径和有机碳含量呈无规律变化。独立样本t检验发现,除土壤pH和粉粒含量,结皮土壤属性与对照之间存在显著差异(P < 0.05)。与对照处理相比,结皮土壤的黏结力、pH、黏粒、粉粒、水稳性团聚体、平均重量直径和有机碳平均增加18.7%、1.9%、15.5%、4.7%、6.6%、15.6% 和16.1%,而砂粒含量和容重平均减小4.5% 和3.3%(表 3)。
|
|
表 3 不同处理土壤属性 Table 3 Soil properties under different moss crust coverages |
方差分析表明生物结皮盖度显著影响土壤分离能力(P=0.000,表 4)。土壤分离能力随生物结皮盖度的增加逐渐减小,从对照裸地的0.160 kg/(m2·s)减小到80% ~ 100% 盖度的0.008 kg/(m2·s)。独立样本t检验表明结皮土壤的平均土壤分离能力显著低于裸地(P < 0.05),与对照相比,不同盖度下的土壤分离能力减小了50% ~ 95%(表 4)。
|
|
表 4 不同盖度下土壤分离能力统计特征 Table 4 Descriptive statistics of soil detachment capacity (Dc) |
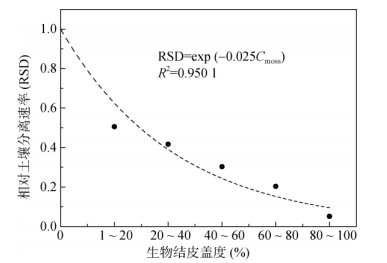
相对土壤分离速率(relative soil detachment,RSD)为有结皮覆盖的土壤分离能力与裸地土壤分离能力的比值,回归分析发现随着生物结皮盖度的增大,RSD呈指数衰减(图 2)。
|
图 2 相对土壤分离速率与结皮盖度的回归关系 Fig. 2 Relative soil detachment (RSD) rate as a function of moss coverage (Cmoss) |
通过公式(4)拟合土壤侵蚀阻力参数(细沟可蚀性和临界剪切力),发现结皮土壤的细沟可蚀性介于0.009 5 ~ 0.000 9 s/m,低于对照裸地细沟可蚀性(0.018 7 s/m)的2倍~ 20倍(表 5)。与对照相比,60% ~ 80% 和80% ~ 100% 盖度水平的细沟可蚀性分别降低了80% 和95%。回归分析显示随着结皮盖度的增加,细沟可蚀性呈指数衰减(图 4),拟合关系如下:
|
|
表 5 不同处理下细沟可蚀性和临界剪切力 Table 5 Rill erodibilities (Kr) and critical shear stresses (τc) under different treatments |

|
图 3 本研究和前人研究中细沟可蚀性(Kr)与结皮盖度(Cmoss)的回归方程 Fig. 3 Comparison of rill erodibility (Kr) as a function of moss coverage (Cmoss) in this and previous study |
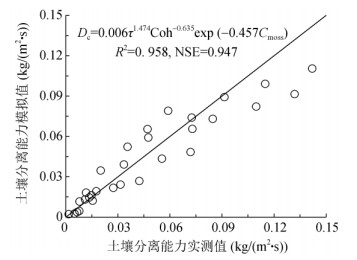
|
图 4 土壤分离能力实测值与模拟值之间的比较 Fig. 4 Comparison between observed and simulated soil detachment capacity (Dc) |
本研究中临界剪切力(τc)为3.000 ~ 3.193 Pa,回归分析显示不同处理间无显著差异。
2.4 土壤分离过程的影响因素及模拟相关分析显示,土壤分离能力和细沟可蚀性与生物结皮特性和土壤属性相关,而临界剪切力与生物结皮和土壤属性相关性不显著,土壤pH与其他指标之间亦不相关(表 6)。对于生物结皮指标,土壤分离能力与生物结皮盖度和厚度均显著相关,相关系数分别为–0.746和–0.612(P < 0.01);细沟可蚀性与生物结皮盖度和厚度同样呈显著相关,相关系数分别为–0.940和–0.969(P < 0.01)。此外,结皮盖度和厚度之间呈显著正相关,相关系数0.834(P < 0.01)。对于土壤属性指标,土壤黏结力、黏粒含量、水稳性团聚体、平均重量直径、有机碳含量与土壤分离能力和细沟可蚀性呈显著负相关,土壤容重和砂粒含量与这两个指标呈正相关。除了土壤pH,其他土壤属性指标间及其与生物结皮指标间均密切相关。
|
|
表 6 土壤分离、生物结皮、土壤属性相关系数矩阵 Table 6 Correlation coefficient matrix of soil detachment, biocrust and soil properties |
由此可见,生物结皮与土壤属性间可能存在相关或者因果关系进而影响土壤分离过程,本研究进一步通过逐步回归和通径分析来确定影响土壤分离的主要因素及其作用过程。
对于土壤分离能力(Dc),逐步回归分析显示结皮盖度(Cmoss)、土壤黏结力(Coh)和砂粒含量(Sand)最终进入方程,得到如下关系式:
| $ \begin{array}{l} {D_{\rm{c}}} = - 55.332 - 1.073{C_{{\rm{moss}}}} + 0.596{\rm{Coh}} + \\ \;\;\;\;\;\;\;0.227S{\rm{and}}\;({R^2} = 0.956, P = 0.000) \end{array} $ | (5) |
通径分析显示结皮盖度和黏结力对土壤分离能力为负影响,砂粒含量对土壤分离能力为正影响(表 7),说明结皮盖度或土壤黏结力降低、砂粒含量增加会加重土壤分离。从表 7还可以看到,土壤黏结力的总间接作用最大,为–1.861,其次为结皮盖度(0.812)和砂粒含量(0.194),而直接作用和总作用均表现为Cmoss > Coh > Sand。决策系数表现为Cmoss > Sand > Coh,说明结皮盖度为土壤分离能力的决策因子;黏结力的决策系数最低而且为负,因此为主要限制因子。尽管黏结力的直接作用不是最大(1.198),但其通过结皮盖度的间接作用最大(–1.491),且砂粒含量通过黏结力的间接作用也相对较高(–1.096)。剩余因子的通径系数和决策系数分别为0.210和0.044,说明还有其他未考虑的因子影响土壤分离能力,如其他近地表特征要素、观测误差等。
|
|
表 7 生物结皮和土壤属性对土壤分离能力影响的通径分析 Table 7 Path analysis of biocrust and soil properties on soil detachment capacity (Dc) |
除了生物结皮和土壤属性,作为侵蚀外力,水流剪切力(τ)也会对土壤分离能力产生深刻影响,回归分析发现二者符合幂函数关系:
| $ {D_{\rm{c}}} = 0.000{\rm{ }}8{\tau ^{1.519}}\;\;\;\;({R^2} = 0.741, P = 0.002) $ | (6) |
综合考虑侵蚀外力、生物结皮和土壤属性因子,非线性逐步回归分析表明土壤分离能力(Dc)可用水流剪切力(τ)、黏结力(Coh)和结皮盖度(Cmoss)的幂函数进行很好地模拟(图 4)。
对于细沟可蚀性(Kr),线性逐步回归分析显示结皮盖度(Cmoss)和土壤容重(BD)最终进入方程,得到如下回归关系:
| $ \begin{array}{l} {K_{\rm{r}}} = - 1.879 - 0.474{C_{{\rm{moss}}}} + 0.0013{\rm{BD}}\\ \;\;\;\;({R^2} = 0.877, P = 0.001) \end{array} $ | (7) |
同样进行通径分析来识别影响细沟可蚀性的关键因子(表 8),结果表明结皮盖度对细沟可蚀性表现为负影响(r=−0.940,P < 0.01),且其直接作用及通过土壤容重的间接作用均为负(−0.689和−0.251);然而,土壤容重对细沟可蚀性表现为正影响(r=0.980,P < 0.01),其直接作用和通过结皮盖度的间接作用亦为正(0.370和0.610)。结皮盖度的决策系数(0.821)高于土壤容重(0.588),因而可作为细沟可蚀性的决策因子。剩余因子的通径系数和决策系数分别为0.351和0.123,同样说明尚存其他未考虑的因素影响细沟可蚀性。
|
|
表 8 生物结皮和土壤属性对细沟可蚀性影响的通径分析 Table 8 Path analysis of moss crust and soil properties on rill erodibility (Kr) |
细沟可蚀性(部分反映土壤可蚀性)和临界剪切力是基于WEPP模型的推导参数,反映的是土壤对集中水流侵蚀的抵抗能力[16-17],也有学者采用土壤抗冲性表示土壤侵蚀阻力[12, 32]。细沟可蚀性和土壤侵蚀阻力均受控于土壤内在属性[16, 23],因而间接地受驱动土壤属性变化的诸多因素的影响,如土地利用[41]、植被覆盖[42]、枯落物[20]、生物结皮[11, 21]和植物根系[22]。
生物结皮盖度和生物量是最常用来表示生物结皮发育程度或演替阶段的两个指标[7, 12-13],本研究同样采用结皮盖度并测定相应盖度下的结皮厚度来表征生物结皮发育,因为结皮厚度也是反映近地表特性变化的一个重要指标[23-24],对土壤属性、土壤侵蚀阻力或土壤可蚀性具有潜在影响[40-41]。本研究中苔藓结皮厚度介于8.24 ~ 16.51 mm,我国黄土高原地区苔藓结皮厚度为10.87 ~ 15.43 mm[9],二者在同一数量级。此外,本研究发现结皮厚度随结皮盖度显著增加,二者的关系可用指数方程描述,而且这两个指标呈显著正相关(P < 0.01),与大部分土壤属性指标及土壤分离能力和细沟可蚀性亦显著相关,说明生物结皮厚度在一定程度上代表了生物结皮的发育程度,在今后研究生物结皮的影响机制时应予以考虑。一些研究已量化或证实了生物结皮厚度与土壤分离能力和土壤侵蚀阻力/土壤可蚀性之间的密切关系[30, 41-43],然而,未来仍需开展大量研究以系统、深入了解在一定的外部环境条件下,生物结皮发育演替的表征参数,如形态、组成、覆盖度、生物量、厚度或宏观结构及其与土壤内在属性间的相互作用等,如何控制生物结皮对土壤抗侵蚀性能的影响。
3.1.2 生物结皮–土壤属性–土壤抗侵蚀性能本研究发现生物结皮的发育显著增加了土壤黏结力、黏粒和有机碳含量,改善土壤团粒结构,减小土壤容重和砂粒含量,这与前人的很多研究一致[5, 44-45]。不同演替阶段的生物结皮土壤中,真菌菌丝、蓝藻菌丝或苔藓根状体交织在一起,形成网状结构,加之苔藓锚固结构,不仅能促进土壤稳定性,还能维持其自身动态[21]。生物结皮中的光合自养生物能够通过光合固碳、胞外分泌和残余分解等作用增加土壤有机碳[46],有利于团聚体形成从而稳定土壤[44]。此外,生物结皮的粗糙表面及生物化学风化作用使其不断捕获、累积细颗粒[7, 47],细颗粒和有机质的增加以及容重的降低同样有利于土壤团聚体形成,从而增强土壤稳定,不易被侵蚀[41, 43]。而本研究中土壤分离能力和细沟可蚀性与土壤容重呈正相关,这可能意味着土壤结构在生物发育演替过程中得到了改善(水稳性团聚体和平均重量直径增加,容重减少),土壤抗侵蚀能力大大增强[23, 30]。因此,生物结皮土壤与裸土之间土壤可蚀性的差异,可能不仅仅是生物结皮赋予的物理保护,也可能是对土壤属性变化的响应,生物结皮的存在只是特定土壤属性变量的媒介[28]。
3.2 生物结皮对土壤分离的影响机制土壤分离是土壤侵蚀的起始阶段,是由降雨击溅和径流冲刷两种侵蚀力引起的,前者是细沟间侵蚀,后者是细沟侵蚀。无论是野外天然降雨还是室内径流小区上的模拟降雨,下垫面都是可侵蚀的(侵蚀动床);而本研究是在固定水槽(侵蚀静床)上对小面积(0.007 8 m2)样品进行冲刷试验,因此整个过程中水动力特性几乎保持不变,生物结皮的作用则仅仅体现在它们对土壤的影响,即土壤分离速率或土壤侵蚀阻力,而不是体现在它们对径流侵蚀力的影响。
研究表明,生物结皮对土壤侵蚀过程的调控作用受演替阶段和地表覆盖度的影响[13, 32]。本研究发现不同结皮盖度下临界剪切力并无显著差异,临界剪切力与结皮厚度和土壤属性亦不相关;而土壤分离能力和细沟可蚀性与结皮盖度显著相关,相关系数分别为–0.746和–0.940(P < 0.01),且二者均与结皮厚度和多数土壤属性指标显著相关。作为地表覆盖物,生物结皮的存在似乎应增加发生土壤分离需克服的外力,并且一旦土壤表面被切开,分离速率将不再与裸土不同[28];因此,可以假定生物结皮会对临界剪切力产生影响,而不是对细沟可蚀性,但本研究结果并没有证实这一点。Liu等[21]对黄土高原的研究同样发现无论是苔藓结皮还是藻类–苔藓混生结皮,不同盖度下临界剪切力差异不显著,但该研究未对结皮厚度进行测定。对于这两项研究结果的解释,我们认为可能是对生物结皮和土壤属性的细微差异,临界剪切力不如细沟可蚀性敏感,亦或是由于临界剪切力本身具有很大的随机性和不确定性。Wang等[30]发现临界剪切力随结皮厚度增加而增大,但在他们的研究中,生物结皮只是响应植被恢复年限的地表特性要素之一,并且只测量了厚度。因此,后续研究仍需深入探索临界剪切力的影响因素和机制。
本研究中相对土壤分离速率和细沟可蚀性均随结皮盖度的增大呈指数衰减,拟合指数分别为0.025和0.028,Liu等[21]对黄土高原的研究得到的拟合指数分别为0.057和0.047。由于这两个研究的试验设计和方法大体相同,如水槽长度、冲刷样品的形状和大小,因此相对土壤分离能力和细沟可蚀性的不同可从气候、土壤、结皮本身、水流剪切力(他们的研究采用7.15 ~ 24.08 Pa)等几个方面来解释。本研究在亚热带湿润气候区开展,这既不同于Liu等[21]也不同于已有的大量有关干旱半干旱地区生物结皮生态功能的研究,可能是因为在这些地区水分有效性是维管植物的限制因素。本研究的试验土壤为紫色土,是由紫色砂质页岩发育而成的岩性土,土层较浅(通常小于50 cm),蓄水能力较差;而Liu等[21]研究的土壤为黄土,是由黄土母质发育而成的沉积土,具有较厚的沉积层(约300 m)和较好的蓄水能力。由于气候、土壤、生境条件的多样性,生物结皮群落自身及其与下伏土壤的相互作用在响应、适应、功能和反馈等方面不可避免地会发生变化,从而导致不同的土壤过程。指数衰减方程早有报道,用来定量评价植被、作物残茬、砾石、枯落物或生物结皮等地表覆盖类型的减蚀作用,其拟合指数代表作用效果[28]。关于植被覆盖的减蚀效力,Gyssels等[48]文献综述得到细沟侵蚀和细沟间侵蚀的指数为0.049(0.017 ~ 0.082),雨滴溅蚀的指数为0.035(0.025 ~ 0.477)。本研究的结果表明,生物结皮覆盖的减蚀作用可达到植被覆盖的作用效果,因此,在生态重建的过程中,生物结皮可作为一种恢复模式,实现土壤侵蚀防控。
如前所述,生物结皮和土壤属性之间可能存在密切的相关性或因果关系,生物结皮可通过改变土壤属性影响土壤分离过程。本研究采用通径分析进一步探析生物结皮的直接和间接影响,发现结皮盖度、土壤黏结力和砂粒含量是影响土壤分离能力的主要因素,结皮盖度和土壤容重是影响细沟可蚀性的主要因素。结皮盖度是土壤分离能力和细沟可蚀性的决策因子,黏结力是土壤分离能力的限制因子;结皮盖度对土壤分离能力和细沟可蚀性的直接影响也最大,黏结力和容重分别对土壤分离能力和细沟可蚀性的间接影响最大;且黏结力、容重和砂粒含量通过结皮盖度的绝对间接影响远大于其直接影响。这些结果表明,生物结皮不仅通过直接的物理覆盖保护影响土壤分离,还通过间接地改善土壤属性影响土壤分离,但二者不可分。
4 结论1) 三峡库区生物结皮的发育显著增强了土壤侵蚀阻力,减小了土壤分离,与无结皮土壤相比,不同结皮盖度下的土壤分离能力和细沟可蚀性分别减小了1.9倍~ 21.0倍和2.0倍~ 20.0倍。
2) 相对土壤分离速率和细沟可蚀性均随生物结皮盖度的增加呈指数衰减,土壤分离能力可用水流剪切力、土壤黏结力和生物结皮盖度的幂函数进行模拟(R2=0.958,P=0.000,NSE=0.947)。
3) 结皮盖度、土壤黏结力和砂粒含量是影响土壤分离能力的主要因素,结皮盖度和土壤容重是影响细沟可蚀性的主要因素;三峡库区生物结皮通过直接的物理覆盖保护和间接地改变土壤属性来抑制土壤分离。
| [1] |
Belnap J, Weber B, Büdel B. Biological soil crusts as an organizing principle in drylands//Weber B, Büdel B, Belnap J. Biological soil crusts: An organizing principle in drylands[M]. Cham: Springer International Publishing, 2016: 3-13.
(  0) 0) |
| [2] |
孙福海, 肖波, 姚小萌, 等. 黄土高原生物结皮斥水性及其沿降水梯度变化特征研究[J]. 农业机械学报, 2020, 51(7): 304-312 (  0) 0) |
| [3] |
Rodríguez-Caballero E, Castro A J, Chamizo S, et al. Ecosystem services provided by biocrusts: From ecosystem functions to social values[J]. Journal of Arid Environments, 2018, 159: 45-53 DOI:10.1016/j.jaridenv.2017.09.005 (  0) 0) |
| [4] |
张冠华, 胡甲均. 生物结皮土壤-水文-侵蚀效应研究进展[J]. 水土保持学报, 2019, 33(1): 1-8 (  0) 0) |
| [5] |
Kakeh J, Gorji M, Sohrabi M, et al. Effects of biological soil crusts on some physicochemical characteristics of rangeland soils of Alagol, Turkmen Sahra, NE Iran[J]. Soil and Tillage Research, 2018, 181: 152-159 DOI:10.1016/j.still.2018.04.007 (  0) 0) |
| [6] |
Xiao B, Ma S, Hu K L. Moss biocrusts regulate surface soil thermal properties and generate buffering effects on soil temperature dynamics in dryland ecosystem[J]. Geoderma, 2019, 351: 9-24 DOI:10.1016/j.geoderma.2019.05.017 (  0) 0) |
| [7] |
Belnap J, Büdel B. Biological soil crusts as soil stabilizers//Weber B, Büdel B, Belnap J. Biological soil crusts: An organizing principle in drylands[M]. Cham: Springer International Publishing, 2016: 305-320.
(  0) 0) |
| [8] |
Sepehr A, Hassanzadeh M, Rodriguez-Caballero E. The protective role of cyanobacteria on soil stability in two Aridisols in northeastern Iran[J]. Geoderma Regional, 2019, 16: e00201 DOI:10.1016/j.geodrs.2018.e00201 (  0) 0) |
| [9] |
Wang H, Zhang G H, Liu F, et al. Effects of biological crust coverage on soil hydraulic properties for the Loess Plateau of China[J]. Hydrological Processes, 2017, 31(19): 3396-3406 DOI:10.1002/hyp.11263 (  0) 0) |
| [10] |
Whitney K M, Vivoni E R, Duniway M C, et al. Ecohydrological role of biological soil crusts across a gradient in levels of development[J]. Ecohydrology, 2017, 10(7): e1875 DOI:10.1002/eco.1875 (  0) 0) |
| [11] |
Gao L Q, Bowker M A, Xu M X, et al. Biological soil crusts decrease erodibility by modifying inherent soil properties on the Loess Plateau, China[J]. Soil Biology and Biochemistry, 2017, 105: 49-58 DOI:10.1016/j.soilbio.2016.11.009 (  0) 0) |
| [12] |
Gao L Q, Sun H, Xu M X, et al. Biocrusts resist runoff erosion through direct physical protection and indirect modification of soil properties[J]. Journal of Soils and Sediments, 2020, 20(1): 133-142 DOI:10.1007/s11368-019-02372-w (  0) 0) |
| [13] |
Gao L Q, Bowker M A, Sun H, et al. Linkages between biocrust development and water erosion and implications for erosion model implementation[J]. Geoderma, 2020, 357: 113973 DOI:10.1016/j.geoderma.2019.113973 (  0) 0) |
| [14] |
张光辉. 土壤分离能力测定的不确定性分析[J]. 水土保持学报, 2017, 31(2): 1-6 (  0) 0) |
| [15] |
Wang B, Zhang G H. Quantifying the binding and bonding effects of plant roots on soil detachment by overland flow in 10 typical grasslands on the loess plateau[J]. Soil Science Society of America Journal, 2017, 81(6): 1567-1576 DOI:10.2136/sssaj2017.07.0249 (  0) 0) |
| [16] |
张冠华, 胡甲均. 径流驱动土壤分离过程的影响因素及机制研究进展[J]. 水科学进展, 2019, 30(2): 294-304 (  0) 0) |
| [17] |
Knapen A, Poesen J, Govers G, et al. Resistance of soils to concentrated flow erosion: A review[J]. Earth-Science Reviews, 2007, 80(1/2): 75-109 (  0) 0) |
| [18] |
Zhu P Z, Zhang G H, Zhang B J, et al. Variation in soil surface roughness under different land uses in a small watershed on the Loess Plateau, China[J]. CATENA, 2020, 188: 104465 DOI:10.1016/j.catena.2020.104465 (  0) 0) |
| [19] |
Mu H L, Yu X J, Fu S H, et al. Effect of stem cover on hydraulic parameters of overland flow[J]. Journal of Hydrology, 2019, 577: 123964 DOI:10.1016/j.jhydrol.2019.123964 (  0) 0) |
| [20] |
Sun L, Zhang G H, Liu F, et al. Effects of incorporated plant litter on soil resistance to flowing water erosion in the Loess Plateau of China[J]. Biosystems Engineering, 2016, 147: 238-247 DOI:10.1016/j.biosystemseng.2016.04.017 (  0) 0) |
| [21] |
Liu F, Zhang G H, Sun L, et al. Effects of biological soil crusts on soil detachment process by overland flow in the Loess Plateau of China[J]. Earth Surface Processes and Landforms, 2016, 41(7): 875-883 DOI:10.1002/esp.3870 (  0) 0) |
| [22] |
Wang B, Zhang G H, Yang Y F, et al. Response of soil detachment capacity to plant root and soil properties in typical grasslands on the Loess Plateau[J]. Agriculture, Ecosystems & Environment, 2018, 266: 68-75 (  0) 0) |
| [23] |
Wang H, Zhang G H, Li N N, et al. Soil erodibility as impacted by vegetation restoration strategies on the Loess Plateau of China[J]. Earth Surface Processes and Landforms, 2019, 44(3): 796-807 DOI:10.1002/esp.4531 (  0) 0) |
| [24] |
Wang B, Zhang G H, Zhang X C, et al. Effects of near soil surface characteristics on soil detachment by overland Flow in a natural succession grassland[J]. Soil Science Society of America Journal, 2014, 78: 589-597 DOI:10.2136/sssaj2013.09.0392 (  0) 0) |
| [25] |
Rodríguez-Caballero E, Cantón Y, Chamizo S, et al. Effects of biological soil crusts on surface roughness and implications for runoff and erosion[J]. Geomorphology, 2012, 145/146: 81-89 DOI:10.1016/j.geomorph.2011.12.042 (  0) 0) |
| [26] |
杨凯, 赵允格, 马昕昕. 黄土丘陵区生物土壤结皮层水稳性[J]. 应用生态学报, 2012, 23(1): 173-177 (  0) 0) |
| [27] |
李林, 赵允格, 王一贺, 等. 不同类型生物结皮对坡面产流特征的影响[J]. 自然资源学报, 2015, 30(6): 1013-1023 (  0) 0) |
| [28] |
Knapen A, Poesen J, Galindo-Morales P, et al. Effects of microbiotic crusts under cropland in temperate environments on soil erodibility during concentrated flow[J]. Earth Surface Processes and Landforms, 2007, 32(12): 1884-1901 DOI:10.1002/esp.1504 (  0) 0) |
| [29] |
Chaudhary V B, Bowker M A, O'dell T E, et al. Untangling the biological contributions to soil stability in semiarid shrublands[J]. Ecological Applications, 2009, 19(1): 110-122 DOI:10.1890/07-2076.1 (  0) 0) |
| [30] |
Wang B, Zhang G H, Shi Y Y, et al. Effect of natural restoration time of abandoned farmland on soil detachment by overland flow in the Loess Plateau of China[J]. Earth Surface Processes and Landforms, 2013, 38(14): 1725-1734 DOI:10.1002/esp.3459 (  0) 0) |
| [31] |
Liu F, Zhang G H, Sun F B, et al. Quantifying the surface covering, binding and bonding effects of biological soil crusts on soil detachment by overland flow[J]. Earth Surface Processes and Landforms, 2017, 42(15): 2640-2648 DOI:10.1002/esp.4213 (  0) 0) |
| [32] |
冉茂勇, 赵允格, 刘玉兰. 黄土丘陵区不同盖度生物结皮土壤抗冲性研究[J]. 中国水土保持, 2011(12): 43-45, 67 (  0) 0) |
| [33] |
Su X L, Nilsson C, Pilotto F, et al. Soil erosion and deposition in the new shorelines of the Three Gorges Reservoir[J]. Science of the Total Environment, 2017, 599/600: 1485-1492 DOI:10.1016/j.scitotenv.2017.05.001 (  0) 0) |
| [34] |
Teng M J, Huang C B, Wang P C, et al. Impacts of forest restoration on soil erosion in the Three Gorges Reservoir area, China[J]. Science of the Total Environment, 2019, 697: 134164 DOI:10.1016/j.scitotenv.2019.134164 (  0) 0) |
| [35] |
马洁, 陈先江, 侯扶江. 草地生物土壤结皮[J]. 草业科学, 2016, 33(7): 1243-1252 (  0) 0) |
| [36] |
庄伟伟, 张元明. 生物结皮对荒漠草本植物群落结构的影响[J]. 干旱区研究, 2017, 34(6): 1338-1344 (  0) 0) |
| [37] |
Chen X Y, Huang Y H, Zhao Y, et al. Analytical method for determining rill detachment rate of purple soil as compared with that of loess soil[J]. Journal of Hydrology, 2017, 549: 236-243 DOI:10.1016/j.jhydrol.2017.03.065 (  0) 0) |
| [38] |
Li T Y, Li S Y, Liang C, et al. Erosion vulnerability of sandy clay loam soil in Southwest China: Modeling soil detachment capacity by flume simulation[J]. CATENA, 2019, 178: 90-99 DOI:10.1016/j.catena.2019.03.008 (  0) 0) |
| [39] |
Luk S H, Merz W. Use of the slat tracing technique to determine the velocity of overlan-flow[J]. Soil Technology, 1992, 5(4): 289-301 (  0) 0) |
| [40] |
Foster G R, Flanagan D C, Nearing M A, et al. Hillslope erosion component//Flanagan D C, Nearing M A. USDA water erosion prediction project, hillslope profile and watershed model documentation[M]. West Lafayette, Ind. : USDA-ARS National Soil Erosion Research Laboratory, 1995.
(  0) 0) |
| [41] |
Wang H, Zhang G H, Li N N, et al. Variation in soil erodibility under five typical land uses in a small watershed on the Loess Plateau, China[J]. CATENA, 2019, 174: 24-35 DOI:10.1016/j.catena.2018.11.003 (  0) 0) |
| [42] |
Zhang B J, Zhang G H, Yang H Y, et al. Soil resistance to flowing water erosion of seven typical plant communities on steep gully slopes on the Loess Plateau of China[J]. CATENA, 2019, 173: 375-383 (  0) 0) |
| [43] |
Wang H, Zhang G H, Li N N, et al. Soil erodibility influenced by natural restoration time of abandoned farmland on the Loess Plateau of China[J]. Geoderma, 2018, 325: 18-27 (  0) 0) |
| [44] |
Chamizo S, Cantón Y, Miralles I, et al. Biological soil crust development affects physicochemical characteristics of soil surface in semiarid ecosystems[J]. Soil Biology and Biochemistry, 2012, 49: 96-105 (  0) 0) |
| [45] |
He M Z, Hu R, Jia R L. Biological soil crusts enhance the recovery of nutrient levels of surface dune soil in arid desert regions[J]. Ecological Indicators, 2019, 106: 105497 (  0) 0) |
| [46] |
Adessi A, Cruz de Carvalho R, De Philippis R, et al. Microbial extracellular polymeric substances improve water retention in dryland biological soil crusts[J]. Soil Biology and Biochemistry, 2018, 116: 67-69 (  0) 0) |
| [47] |
Souza-Egipsy V, Wierzchos J, Sancho C, et al. Role of biological soil crust cover in bioweathering and protection of sandstones in a semi-arid landscape (Torrollones de Gabarda, Huesca, Spain)[J]. Earth Surface Processes and Landforms, 2004, 29(13): 1651-1661 (  0) 0) |
| [48] |
Gyssels G, Poesen J, Bochet E, et al. Impact of plant roots on the resistance of soils to erosion by water: A review[J]. Progress in hysical Geography: Earth and Environment, 2005, 29(2): 189-217 (  0) 0) |
2. Research Center on Mountain Torrent & Geologic Disaster Prevention of Ministry of Water Resources, Wuhan 430010, China;
3. Central-Southern Safety & Environment Technology Institute Co., Ltd., Wuhan 430071, China
 2021, Vol. 53
2021, Vol. 53

