2. 内蒙古自治区土壤质量与养分资源重点实验室, 呼和浩特 010011;
3. 农业部环境保护科研监测所, 天津 300191
由于几十年来人为活动,如农业施肥、化石燃料燃烧以及过度放牧等,导致全球活性氮沉降量不断增加[1-2]。有研究表明,近40年我国氮沉降量增加迅速、氮沉降强度甚至超过欧美[3]。氮沉降可以作为一种新的肥料来源促进草原植被的生长[4],但同时,也对人类健康产生一定的影响,过多的氮沉降会导致一系列的环境问题,如有机质矿化、土壤酸化、水体富营养化,以及对全球气候系统的破坏[5],进而影响草地生态系统结构和功能,使生物多样性丧失[6]。氮沉降还可能影响生态系统碳循环,Hungate等[7]研究发现氮沉降增加了不同植物物种的碳储蓄量,而氮沉降和大气中CO2升高可能具有协调作用。
中小型土壤节肢动物在陆地生态系统起着重要的作用,是地下物质循环的重要参与者,它们在凋落物分解、促进养分循环、改善土壤结构和土壤肥力方面发挥着重要作用[8]。土壤环境与土壤动物群落之间的关系错综复杂,Murray等[9]在旱地草地系统施用氮肥对植物与土壤生物之间的关系研究表明,植物与土壤生物之间存在自上而下的控制机制,同时发现土壤动物与土壤环境之间既涉及正反馈,又涉及负反馈。Pollierer等[10]通过碳氮稳定同位素比值分析对土壤动物食物网进行研究,结果发现土壤动物食物资源的数量和质量可能会随着氮素添加的影响发生改变,从而间接导致了氮素添加对土壤动物群落的影响。在世界范围内,气候变化对土壤生态的影响已成为研究主题[11],Eisenhauer等[12]在美国明尼苏达州长期草原研究结果发现,地下食物网对全球气候变化应激源有着缓冲作用。García-Palacios等[13]发现土壤动物群落结构的变化可以反映和预测全球气候的变化。因此,更好地了解中小型土壤节肢动物对气候变化的响应将有助于预测未来陆地生态系统的状态。
全球大气氮沉降的增加对草地生态系统稳定产生了影响,并引起了国内外学者的关注。目前,主要研究集中于氮沉降对草地植物及土壤微生物多样性的影响[14],而关于氮沉降对草甸草原中小型土壤节肢动物群落结构的影响尚不明确。内蒙古草甸草原氮沉降量速率约为N 10 ~ 15 kg/(hm2·a) [15]。而在这种氮沉降背景值较低的地区展开研究,将有利于反映氮沉降对草地生态系统的初始影响。贝加尔针茅(Stipa baicalensis)草原是草甸草原的代表类型之一,在中国畜牧业生产中占有重要地位[16]。基于此,本文以贝加尔针茅草甸草原为研究对象进行了长期模拟氮沉降定点试验,研究模拟氮沉降背景下中小型土壤节肢动物群落的变化情况,以期为氮沉降对草地生态系统的影响提供分析和评估的基础资料。
1 材料与方法 1.1 试验地概况试验地位于大兴安岭西麓,内蒙古自治区呼伦贝尔市鄂温克自治旗伊敏河镇境内,试验在贝加尔针茅草甸草原围封样地进行,地理位置为48°27′ ~ 48°35′ N,119°35′ ~ 119°41′ E,地势平坦,海拔约765 m。贝加尔针茅(Stipa baicalensis)为建群种,羊草(Leymus chinensis)为优势种。该区气候属于温带大陆性气候,昼夜温差大,年平均气温-2.4 ~ 2.2 ℃,年均降水量350 ~ 400 mm,降水主要集中在6-9月,年均无霜期为100 d左右。土壤类型为暗栗钙土。
1.2 试验设计试验地区于2010年6月份围封,并开展模拟氮沉降试验,采用随机区组试验,设4个重复,8个施氮水平,依次为N 0、15、30、50、100、150、200和300 kg/(hm2·a),分别用N0(对照),N15、N30、N50、N100和N150(低氮处理),N200(中氮处理)和N300(高氮处理)表示。小区面积8 m × 8 m,小区间设2 m隔离带,重复间设5 m隔离带。每年6月中旬和7月中旬分两次将氮肥等量溶于水施入,氮肥为NH4NO3。
1.3 样品采集根据试验区草场返青期、生长期和枯黄期进行样品采集[17],于2019年5月和8月的中旬以及9月下旬采集。采用5 cm直径的环刀,在每个试验小区选取2个未被扰动的点,按土壤深度0 ~ 10 cm和10 ~ 20 cm自上而下进行取样,即每月取8个处理,每个处理取3个重复,每个重复取2层共计48个样品供土壤动物分离。采用Tullgern干漏斗法将样品中的中小型土壤节肢动物进行48 h分离,并将收集到的中小型土壤节肢动物装在盛有75% 的酒精溶液瓶并贴上标签[18]。土壤动物采样的同时,采集各层土样进行土壤理化性质指标的分析。
1.4 测定方法中小型土壤节肢动物依据尹文英等《中国土壤动物检索图鉴》[18]在显微镜(Olympus CKX41)和体视显微镜(SZ78系列)下对收集到的土壤动物标本进行鉴定,鉴定到科的水平。各类群等级划分为:个体数占总个体数的10% 以上为优势类群;个体数占总个体数的1% ~ 10% 为常见类群;个体数占总个体数的1% 以下为稀有类群[19]。
土壤有机质采用重铬酸钾容量法测定;土壤pH采用STARTER 2100型酸度计(土: 液=1:5)测定;土壤含水量采用烘干称重法测定;土壤全氮采用凯氏定氮仪测定(K9840凯氏定氮仪),全磷采用氢氧化钠熔融-钼锑抗比色法测定;全钾采用氢氧化钠熔融-火焰光度法测定;采用氯化钙浸提法和流动分析仪测定土壤NO3--N、NH4+-N[20]。土壤理化性质见表 1。
|
|
表 1 长期不同施氮水平对土壤理化性质的影响 Table 1 Soil physicochemical properties under long-term different simulated nitrogen depositions |
选取Shannon多样性指数(H′)、Simpson优势度指数(C)、Pielou均匀度指数(E)、Margalef丰富度指数(D)和群落相似性指数作为氮素添加下中小型土壤节肢动物群落特征指标[21],对不同处理间陆生土壤节肢动物特征指标分析采用单因素方差分析(One-way ANOVA)和多重比较法(LSD)分析。采用主成分分析(PCA)对中小型土壤节肢动物优势类群及常见类群对氮沉降的响应进行分析[22]。采用冗余分析(RAD)对中小型土壤节肢动物优势类群和常见类群个体数与环境之间进行相关性分析[23]。数据分析处理与作图使用Excel 2003、SigmaPlot 12.5、SAS 9.0与CANOCO 5.0进行。其计算公式如下:
| $ H′= - \sum\limits_{i = 1}^s {Pi\ln Pi} $ | (1) |
| $ C=\sum\limits_{i = 1}^s {(ni/} N{)^2} $ | (2) |
| $ E = H/{\rm{ln}}S $ | (3) |
| $ D = (S - 1)/{\rm{ln}}N $ | (4) |
式中:Pi=ni/N为第i个物种的相对多度;S为类群数;N为群落中所有物种总个体数;ni为第i个物种个体数。
2 结果与分析 2.1 模拟氮沉降对贝加尔针茅草甸草原中小型土壤动物的影响由表 2可知,试验区共捕获中小型土壤节肢动物977只,隶属于10目49个类群。其中,优势类群为蚁科、微离螨科和球角䖴科,占总捕获量49.03%。微离螨科随着施氮量的提高而个体数增加,在N300高氮处理下个体数明显高于其他处理;蚁科个体数随着施氮量的增加呈减少趋势;而球角䖴科个体数则随着施氮量的增加先增加,于N200中氮处理后开始减少。常见类群共有13类,为前气门亚目的矮蒲螨科、肉食螨科和小黑螨科,中气门亚目的厉螨科、寄螨科和厚厉螨科,甲螨亚目的奥甲螨科和若甲螨科,弹尾目的等节䖴科、棘䖴科和跳虫科,缨翅目的管蓟马科以及鳞翅目幼虫夜娥科,占总捕获量的40.04%。其余33个类群为稀有类群,其捕获个体数占总捕获量的10.93%。而优势类群与常见类群构成了氮添加试验样地中小型土壤节肢动物的主体,其个体数占总捕获量的89.07%。
|
|
表 2 不同氮添加水平下中小型土壤节肢动物群落组成 Table 2 Meso-micro soil fauna communities under different simulated nitrogen depositions |
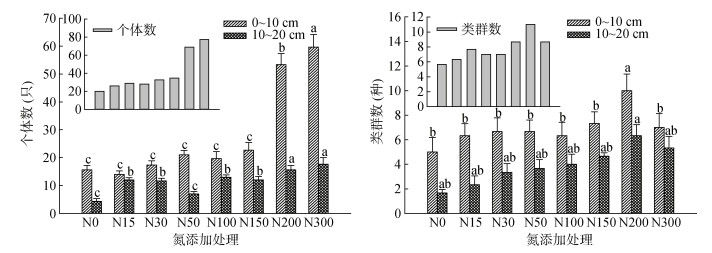
由图 1发现,贝加尔针茅草甸草原中小型节肢土壤动物群落具有明显的表聚特征。土壤动物的类群数和个体数在0 ~ 10 cm土层均高于10 ~ 20 cm土层。随着施氮量的增加,土壤动物个体数随之增加,且N200和N300处理土壤动物个体数显著高于对照N0和其他处理(P < 0.05)。而类群数则随施氮量增加先上升后下降,且在N200处理出现拐点,且类群数显著高于其他处理(P < 0.05)。随施氮量的增加土壤动物群落水平有向深层土壤迁移的趋势。
|
(图中小写字母不同表示同一土层不同氮添加处理间差异显著(P < 0.05)。个体数和类群数表示每个处理所捕获土壤动物个体数和类群总和) 图 1 不同氮添加处理中小型土壤节肢动物的垂直分布 Fig. 1 Vertical distributions of meso-micro soil faunas under different simulated nitrogen depositions |
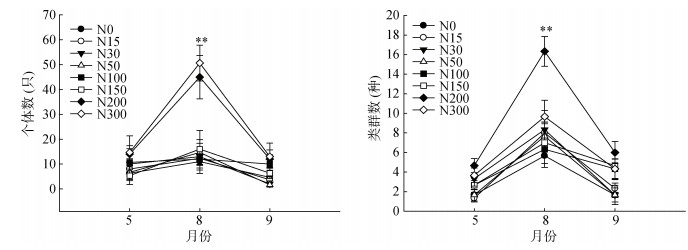
由图 2可知,N200和N300处理中小型土壤节肢动物个体数和类群数在草场返青期(5月份)、生长期(8月份)和枯黄期(9月底)均高于对照N0和其他处理。对照N0及氮添加处理下土壤动物个体数和类群数均在8月出现最大值,且显著高于其他月份(P < 0.05)。其中,N200处理和N300处理土壤动物个体数在8月份显著高于其他处理(P < 0.05),且N200处理土壤动物类群数显著高于其他处理(P < 0.05)。
|
(**表示处理间个体数和类群数差异显著(P < 0.05)) 图 2 模拟氮沉降下草甸草原中小型土壤节肢动物群落的月动态变化 Fig. 2 Monthly dynamic changes of meso-micro soil fauna communities under different simulated nitrogen depositions |
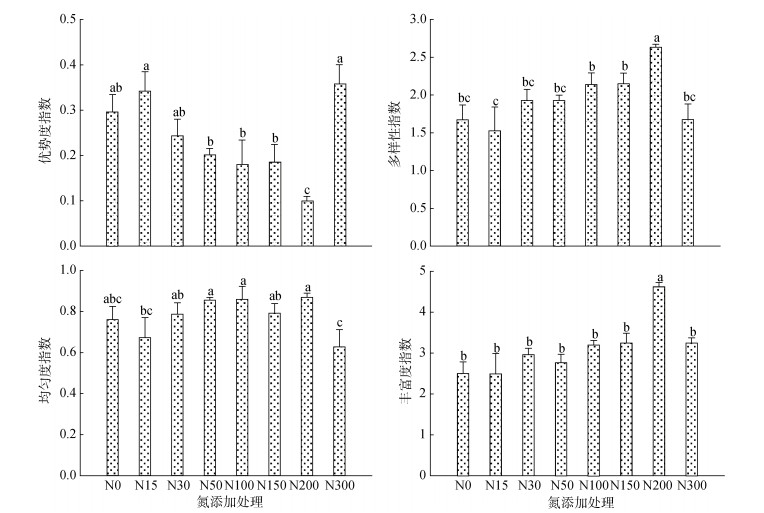
由图 3可知,氮沉降土壤动物群落的多样性指数和丰富度指数随施氮量增加呈先上升后下降的趋势,峰值均出现在N200处理,且多样性指数和丰富度指数在N200处理显著高于对照N0以及其他处理(P < 0.05)。随着施氮量的增加,优势度指数呈先下降后上升的趋势,其中拐点出现在N200处理,最高值出现在N300处理,且N200处理的优势度指数显著低于N0以及其他处理(P < 0.05)。而随着施氮量的增加,土壤动物群落的均匀度指数呈增加的趋势,并于N200处理后开始下降,且均匀度指数在N300处理显著低于N30 ~ N200处理(P < 0.05)。
|
(图中小写字母不同表示处理间差异显著(P < 0.05)) 图 3 模拟氮沉降对中小型土壤节肢动物群落多样性变化 Fig. 3 Diversities of meso-micro soil fauna communities under different simulated nitrogen depositions |
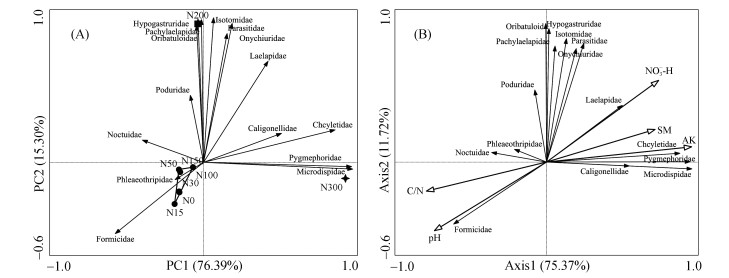
对土壤动物优势类群和常见类群进行主成分分析(PCA)(图 4A),以了解贝加尔针茅草甸草原在不同施氮量下中小型土壤节肢动物群落组成分布情况。两个排序轴累计贡献率达到91.75%,通过土壤动物优势类群和常见类群分布情况可以有效地将氮梯度划分为3组,第一组为对照N0和N15 ~ N150低氮处理,第二组和第三组分别为N200和N300处理。与第一组相关性较大的类群为3种,与第二组相关的类群为8种,与第三组相关的类群为4种。
|
(SM:含水量;AK:速效钾;NO3--N:硝态氮;C/N:土壤碳氮比值;微离螨科:Microdispidae;球角䖴科:Hypogastruridae;蚁科:Formicidae;矮蒲螨科:Pygmephoridae;肉食螨科:Cheylrtidae;小黑螨科:Caligonellidae;厉螨科:Laelapidae;寄螨科:Parasitidae;厚厉螨科:Pachylaelapidae;奥甲螨科:Oppiidae;若甲螨群:Oribatuloide;等节䖴科:Isotomidae;棘䖴科:Onychiuridae;跳虫科:Poduridae;夜娥科:Noctuidae;管蓟马科:Phloeothripidae) 图 4 模拟氮沉降下中小型土壤节肢动物和解释环境变量的主成分分析(A)及冗余分析(B) Fig. 4 Principal component analysis(A) and redundancy analysis(B) of meso-micro soil faunas and explanatory environmental variables under different simulated nitrogen depositions |
土壤环境因子中的NH4+-N和有效磷对土壤动物群落组成影响不显著,因此排除在环境因子对土壤动物的影响之外,而冗余分析RDA(图 4B)结果可以显示出土壤环境因子对土壤动物群落组成的影响。第一排序轴和第二排序轴的特征值分别为75.37% 和11.72%,累计方差解释度达到了71.9%,剔除后的土壤环境因子能够较好地解释对土壤动物的影响。由表 3可知,速效钾和土壤C/N对土壤动物群落变异的解释度分别为73.4% 和51.2%,可以认为是驱动群落变异的主要环境因子。而NO3--N、pH和含水量对群落变异的解释度均大于30%,且P值均小于0.05,可以认为对土壤群落变异有一定的影响。RDA第一排序轴的正半轴相关性较大的土壤环境因子有速效钾和含水量,与第一排序轴负半轴相关性较大的土壤环境因子为pH和土壤C/N,即第一轴可以代表以上环境因子的梯度变化。微离螨科、矮蒲螨科、肉食螨科和小黑螨科与第一排序轴正半轴相关性较大,即与第一轴正半轴代表的环境因子梯度变化呈显著正相关,与第一轴负半轴代表的环境因子的梯度变化呈显著负相关,而蚁科和管蓟马科则与pH和土壤C/N均呈显著正相关。第二排序轴的正半轴相关性较大的土壤环境因子为NO3--N,与第二轴正半轴显著相关的土壤动物类群有厉螨科、寄螨科、厚厉螨科、若甲螨科、等节䖴科、球角䖴科、棘䖴科和跳虫科,这说明NO3--N与这些土壤动物类群呈显著正相关。
|
|
表 3 冗余分析(RDA)各土壤环境因子对土壤动物群落变异的解释度 Table 3 Explanatory degrees of soil fauna community variation of various soil environmental factors by redundancy analysis |
研究结果表明,随着施氮量的增加改变了中小型土壤节肢动物群落结构,这说明氮素影响土壤动物群落组成,且在地下生态系统中起着重要的调节作用[24]。我们发现中小型土壤节肢动物个体数和类群数均随施氮量增加而增加,施氮量较高的处理下捕获的土壤动物个体数和类群数显著高于对照和施氮量较低处理。但当施氮量达到300 kg/(hm2·a) 时,所捕获土壤动物个体数达到最大,而类群数则相对于施氮量200 kg/(hm2·a) 处理时有所下降,其中微离螨科个体数相对于其他处理显著增加,这是由于土壤动物对氮素的嗜好不同而引起了种间竞争从而改变了土壤动物群落结构,使得群落趋向单一化[25]。而土壤动物生活和繁衍与其生活的环境和食物来源密不可分,长期的氮沉降改变了土壤环境,进而影响了土壤生物群落的结构。适量的氮沉降会使土壤中的NH4+-N和NO3--N含量增加,有利于微生物的生长,进而可以促进有机物分解,为土壤动物提供充足的食物来源。同时氮沉降会使土壤pH降低,当氮沉降量超过限度时,则会造成土壤酸化,抑制土壤微生物酶活性和木质素分解,从而降低了土壤微生物量,降低了食微生物的土壤动物多度[26]。与徐国良等[27]研究结果一致,适当的氮沉降对土壤动物可能是有利的,而当氮沉降量超陆地生态系统氮限制后则会对土壤动物产生负面的影响,此结果符合中度干扰理论。
贝加尔针茅草甸草原中小型土壤节肢动物最适生存月份在8月份,也是当地牧场植被生长期,8月份良好的水热条件使地上植物生长旺盛,根系较返青期和枯黄期发达[17],使得土壤孔隙度变大,有利于加快土壤中气体的流动,为土壤动物生存和繁衍提供了良好的有氧环境。这与Vreeken-Buijs等人[28]认为节肢动物群落密度与孔隙呈正相关的研究较一致。由土壤动物垂直变化可知,贝加尔针茅草甸草原中小型土壤节肢动物群落的分布具有明显的表聚特征。随着土层的加深,土壤动物个体数和类群数下降。这与叶贺等人[23]在荒漠草原草地生态系统土壤动物群落垂直分布一致。Briones等人[29]研究结果表明,草原表层土壤温度可以影响土壤动物的垂直分布。丁玲玲等人[30]研究发现草原地上植物根系分布密集,从而决定了根系分泌物分布在土壤表层,根系是植物吸收营养的主要区域,也是土壤生物最为活跃的区域,且表层土壤相对疏松,通气性较好[31],可以为土壤动物生存提供生活环境和充足的营养物质,更适宜土壤动物的生存。而受氮沉降的影响,土壤动物群落水平有向下迁移的趋势。徐国良等人[32]研究发现,过高的氮输入会对土壤动物产生负面的影响,最终使表层土壤动物向土壤深层趋避。
3.2 氮素添加对中小型土壤节肢动物多样性变化和阈值效应氮沉降可以通过改变土壤环境因子组分,进而影响地上植物群落结构和土壤动物的丰度及多样性,最终对地下生态系统产生一定的影响[33]。适量的氮素添加可以被土壤动物有效利用,而过度氮素添加则会对草原地下生态系统造成负效应[32]。本研究通过土壤动物多样性变化可以发现,土壤动物多样性指数和丰富度指数均随着施氮量的增加呈先增加后降低的趋势,在氮沉降量达到200 kg/(hm2·a) 时出现拐点,说明氮沉降量低于200 kg/(hm2·a) 时有利于土壤动物群落发展,与上述结论一致。而优势度指数则随施氮量的增加呈先下降后上升的趋势,在200 kg/(hm2·a) 处理处出现拐点,且在氮沉降量为300 kg/(hm2·a) 时达最大。殷秀琴等[34]研究认为,优势度指数越大表明该群落中某个类群的土壤动物密度占该类群总数比例越高,使该类群的优势度增加而均匀度下降。而本研究优势物种微离螨科的个体数在氮沉降量达到300 kg/(hm2·a) 时突出,类群数减少。环境变化对属于氮限制陆地生态系统的贝加尔针茅草甸草原影响敏感[35]。通过主成分分析(PCA)可将氮梯度有效地划分为3组,而施氮量200 kg/(hm2·a) 处理为独立一组,且50% 的优势类群和常见类群与其显著相关。程建伟等人[36]发现短期氮沉降对土壤动物的影响主要通过植物变化,而在较长时间上的影响主要通过改变土壤理化性质。由冗余分析(RDA)结果可知,速效钾、NO3--N、pH、含水量和土壤C/N比值是氮沉降驱动土壤动物群落变异的主要环境因子。环境因子中的pH和土壤C/N比值对土壤动物群落生活有负效应,而NO3--N对土壤动物群落生活起着正面效应。本研究中NO3--N含量在高氮处理显著高于低氮处理,pH随着氮梯度的增加呈下降趋势。过量的NO- 3会使土壤酸化,土壤中的Al3+被交换出来,造成土壤铝毒效应[14],而pH是影响土壤动物群落分布重要的限制因素,土壤酸化会使土壤动物数量减少,代谢以及繁殖能力衰退[37]。土壤C/N比值是土壤质量的敏感指标,通常被看作是土壤氮素矿化的标志,本研究中氮沉降降低了土壤C/N比值,加快了土壤氮素矿化过程,同时长期的氮素输入则会降低土壤有机碳的矿化,有利于有机质的积累,从而为土壤动物提供了一定食物资源,与Ochoa-Hueso等[38]认为土壤动物丰富度与土壤C/N比值呈负相关一致。我们通过主成分分析(PCA)划分结果以及冗余分析(RDA)结果发现,氮沉降量达到200 kg/(hm2·a)后,土壤环境将会对土壤动物生存产生消极的影响。
已有研究表明一定限度氮沉降对草地生态系统中植物和微生物是有益的,但过量氮沉降则会产生负面影响[32],即氮素输入的增加,存在着阀值效应。贝加尔针茅草甸草原适量的氮素添加对土壤动物群落水平有促进作用,但当氮素添加超过草原生态系统氮限制临界点时,则会呈现出一定的负面影响。本研究结果显示,氮沉降量达到200 kg/(hm2·a) 时,是限制中小型土壤节肢动物群落发展的一个拐点,土壤动物类群数及各项多样性指标均显著高于对照、低氮处理和300 kg/(hm2·a)高氮处理。说明当氮沉降量达到200 kg/(hm2·a) 时,接近或达到了贝加尔针茅草甸草原氮饱和的限度,可以认为本研究中氮沉降对土壤动物群落水平影响的阈值为200 kg/(hm2·a)。
4 结论大气氮沉降对草地生态系统稳定产生了影响,氮沉降通过改变土壤动物食物来源和生存环境影响着中小型土壤节肢动物群落分布。本研究区位于氮沉降背景值较低的内蒙古呼伦贝尔市鄂温克旗贝加尔草甸草原,而在这种背景值较低的地区展开模拟氮沉降试验将更清晰地反映氮沉降对草地生态系统初始反应。本研究结果表明,草原植被生长期适合草甸草原中小型土壤节肢动物群落发展,且土壤动物群落分布具有明显的表聚特征,但随着模拟氮沉降量的增加,土壤动物群落向深层趋避。氮沉降使草地土壤环境因子发生改变,进而影响土壤动物群落繁衍和生存。氮沉降对中小型土壤节肢动物群落发展存在阈值效应,适量氮沉降有利于中小型土壤动物群落发展,当氮沉降量超过草甸草原氮饱和限度,将会抑制土壤动物群落发展。
| [1] |
Liu X J, Duan L, Mo J M, et al. Nitrogen deposition and its ecological impact in China: An overview[J]. Environmental Pollution, 2011, 159(10): 2251-2264 DOI:10.1016/j.envpol.2010.08.002 (  0) 0) |
| [2] |
郑裕雄, 曹际玲, 杨智杰, 等. 氮沉降对亚热带常绿阔叶天然林不同季节土壤微生物群落结构的影响[J]. 土壤学报, 2018, 55(6): 1534-1544 (  0) 0) |
| [3] |
Ackerman D, Millet D B, Chen X. Global estimates of inorganic nitrogen deposition across four decades[J]. Global Biogeochemical Cycles, 2019, 33(1): 100-107 DOI:10.1029/2018GB005990 (  0) 0) |
| [4] |
Fowler D, Pyle J A, Raven J A, et al. The global nitrogen cycle in the twenty-first century: Introduction[J]. Philosophical Transactions of the Royal Society of London Series B, Biological Sciences, 2013, 368(1621): 20130165 DOI:10.1098/rstb.2013.0165 (  0) 0) |
| [5] |
Erisman J W, Galloway J, Seitzinger S, et al. Reactive nitrogen in the environment and its effect on climate change[J]. Current Opinion in Environmental Sustainability, 2011, 3(5): 281-290 DOI:10.1016/j.cosust.2011.08.012 (  0) 0) |
| [6] |
Song L, Bao X M, Liu X J, et al. Impact of nitrogen addition on plant community in a semi-arid temperate steppe in China[J]. Journal of Arid Land, 2012, 4(1): 3-10 DOI:10.3724/SP.J.1227.2012.00003 (  0) 0) |
| [7] |
Hungate B A, Dukes J S, Shaw M R, et al. Nitrogen and climate change[J]. Science, 2003, 302(5650): 1512-1513 DOI:10.1126/science.1091390 (  0) 0) |
| [8] |
严珺, 吴纪华. 植物多样性对土壤动物影响的研究进展[J]. 土壤, 2018, 50(2): 231-238 (  0) 0) |
| [9] |
Murray P J, Cook R, Currie A F, et al. Interactions between fertilizer addition, plants and the soil environment: Implications for soil faunal structure and diversity[J]. Applied Soil Ecology, 2006, 33(2): 199-207 DOI:10.1016/j.apsoil.2005.11.004 (  0) 0) |
| [10] |
Pollierer M M, Langel R, Scheu S, et al. Compartmentalization of the soil animal food web as indicated by dual analysis of stable isotope ratios (15N/14N and 13C/12C)[J]. Soil Biology and Biochemistry, 2009, 41(6): 1221-1226 DOI:10.1016/j.soilbio.2009.03.002 (  0) 0) |
| [11] |
Eisenhauer N, Antunes P M, Bennett A E, et al. Priorities for research in soil ecology[J]. Pedobiologia, 2017, 63: 1-7 DOI:10.1016/j.pedobi.2017.05.003 (  0) 0) |
| [12] |
Eisenhauer N, Cesarz S, Koller R, et al. Global change belowground: Impacts of elevated CO2, nitrogen, and summer drought on soil food webs and biodiversity[J]. Global Change Biology, 2012, 18(2): 435-447 DOI:10.1111/j.1365-2486.2011.02555.x (  0) 0) |
| [13] |
García-Palacios P, Maestre F T, Kattge J, et al. Climate and litter quality differently modulate the effects of soil fauna on litter decomposition across biomes[J]. Ecology Letters, 2013, 16(8): 1045-1053 DOI:10.1111/ele.12137 (  0) 0) |
| [14] |
Farrer E C, Suding K N. Teasing apart plant community responses to N enrichment: The roles of resource limitation, competition and soil microbes[J]. Ecology Letters, 2016, 19(10): 1287-1296 DOI:10.1111/ele.12665 (  0) 0) |
| [15] |
顾峰雪, 黄玫, 张远东, 等. 1961-2010年中国区域氮沉降时空格局模拟研究[J]. 生态学报, 2016, 36(12): 3591-3600 (  0) 0) |
| [16] |
赵帅, 张静妮, 赖欣, 等. 放牧与围栏内蒙古针茅草原土壤微生物生物量碳、氮变化及微生物群落结构PLFA分析[J]. 农业环境科学学报, 2011, 30(6): 1126-1134 (  0) 0) |
| [17] |
张玉静, 杨秀春, 郭剑, 等. 呼伦贝尔草原物候变化及其与气象因子的关系[J]. 干旱区地理, 2019, 42(1): 144-153 (  0) 0) |
| [18] |
尹文英. 中国土壤动物检索图鉴[M].
科学出版社, 北京, 1998
(  0) 0) |
| [19] |
Xin W D, Yin X Q, Song B. Contribution of soil fauna to litter decomposition in Songnen sandy lands in northeastern China[J]. Journal of Arid Environments, 2012, 77: 90-95 DOI:10.1016/j.jaridenv.2011.10.001 (  0) 0) |
| [20] |
鲍士旦. 土壤农化分析[M].
中国农业出版社, 北京, 2000
(  0) 0) |
| [21] |
王文东, 红梅, 赵巴音那木拉, 等. 不同培肥措施对黑土区农田中小型土壤动物群落的影响[J]. 应用与环境生物学报, 2019, 25(6): 1344-1351 (  0) 0) |
| [22] |
毛妙, 张欣, 王磊, 等. 有机种植模式土壤动物多样性的调查研究[J]. 土壤, 2019, 51(4): 698-707 (  0) 0) |
| [23] |
叶贺, 红梅, 赵巴音那木拉, 等. 水氮控制对荒漠草原中小型土壤动物的影响[J]. 中国环境科学, 2018, 38(11): 4325-4333 DOI:10.3969/j.issn.1000-6923.2018.11.043 (  0) 0) |
| [24] |
刘鹏飞, 红梅, 美丽, 等. 不同玉米秸秆还田量的土壤大型动物夏季群落动态特征[J]. 土壤学报, 2020, 57(3): 760-772 (  0) 0) |
| [25] |
吴廷娟. 全球变化对土壤动物多样性的影响[J]. 应用生态学报, 2013, 24(2): 581-588 (  0) 0) |
| [26] |
许凯, 徐钰, 张梦珊, 等. 氮添加对苏北沿海杨树人工林土壤活性有机碳库的影响[J]. 生态学杂志, 2014, 33(6): 1480-1486 (  0) 0) |
| [27] |
徐国良, 莫江明, 周国逸. N沉降下土壤动物群落的响应: 1年研究结果总述[J]. 北京林业大学学报, 2006, 28(3): 1-7 (  0) 0) |
| [28] |
Vreeken-Buijs M J, Hassink J, Brussaard L. Relationships of soil microarthropod biomass with organic matter and pore size distribution in soils under different land use[J]. Soil Biology and Biochemistry, 1998, 30(1): 97-106 DOI:10.1016/S0038-0717(97)00064-3 (  0) 0) |
| [29] |
Briones M J I, Ostle N J, McNamara N P, et al. Functional shifts of grassland soil communities in response to soil warming[J]. Soil Biology and Biochemistry, 2009, 41(2): 315-322 DOI:10.1016/j.soilbio.2008.11.003 (  0) 0) |
| [30] |
丁玲玲, 祁彪, 尚占环, 等. 东祁连山不同高寒草地型土壤微生物数量分布特征研究[J]. 农业环境科学学报, 2007, 26(6): 2104-2111 DOI:10.3321/j.issn:1672-2043.2007.06.019 (  0) 0) |
| [31] |
吴东辉, 尹文英, 卜照义. 松嫩草原中度退化草地不同植被恢复方式下土壤线虫的群落特征[J]. 生态学报, 2008, 28(1): 1-12 (  0) 0) |
| [32] |
徐国良, 莫江明, 周国逸, 等. 模拟氮沉降对苗圃地土壤动物群落的影响[J]. 生态环境, 2004, 13(4): 487-492 (  0) 0) |
| [33] |
Lu H H, Wu W X, Chen Y X, et al. Soil microbial community responses to Bt transgenic rice residue decomposition in a paddy field[J]. Journal of Soils and Sediments, 2010, 10(8): 1598-1605 DOI:10.1007/s11368-010-0264-9 (  0) 0) |
| [34] |
殷秀琴, 安静超, 陶岩, 等. 拉萨河流域健康湿地与退化湿地大型土壤动物群落比较研究[J]. 资源科学, 2010, 32(9): 1643-1649 (  0) 0) |
| [35] |
Ren J Z, Hu Z Z, Zhao J, et al. A grassland classification system and its application in China[J]. The Rangeland Journal, 2008, 30(2): 199 (  0) 0) |
| [36] |
程建伟, 郝百惠, 刘新民, 等. 氮添加对内蒙古典型草原土壤动物的影响[J]. 草业科学, 2018, 35(5): 1254-1265 (  0) 0) |
| [37] |
Stevens C J, Manning P, van den Berg L J L, et al. Ecosystem responses to reduced and oxidised nitrogen inputs in European terrestrial habitats[J]. Environmental Pollution, 2011, 159(3): 665-676 (  0) 0) |
| [38] |
Ochoa-Hueso R, Rocha I, Stevens C J, et al. Simulated nitrogen deposition affects soil fauna from a semiarid Mediterranean ecosystem in central Spain[J]. Biology and Fertility of Soils, 2014, 50(1): 191-196 DOI:10.1007/s00374-013-0838-y (  0) 0) |
2. Inner Mongolia Key Laboratory of Soil Quality and Nutrient Resources, Huhhot 010011, China;
3. Agro-Environmental Protection Institute, Ministry of Agriculture, Tianjin 300191, China
 2021, Vol. 53
2021, Vol. 53


