2. 土壤与农业可持续发展国家重点实验室(中国科学院南京土壤研究所), 南京 210008
1984年Mehlich[1]开发了一种Mehlich 3(M3)提取剂,实现了土壤和沉积物中P、K、Ca、Mg、Al、Fe、Zn、Mn、Cu等多种元素有效态的一次提取,极大地提高了土壤检测的效率;并且M3方法可适用于各种土壤,是一种“通用”型土壤有效元素提取剂[2]。尤其对磷元素而言,它参与从太阳辐射能到化学能(光合作用)的基本传递过程,并维持植物根系的发育,是植物必需的大量元素。高度风化土壤中P主要以铁铝结合态存在,而钙质土壤中主要以磷酸钙存在,相应的土壤有效态磷分别通过HCl-NH4F(Bray法)和pH 8.5的NaHCO3(Olsen法)提取[3-4]。美国各地的区域土壤测试委员会于20世纪80年代末开始开展了大量研究,目标是将M3提取剂作为土壤通用型有效元素提取试剂,并取得了理想的效果[5]。
M3提取剂的配方为0.2 mol/L HOAc, 0.015 mol/L NH4F, 0.013 mol/L HNO3, 0.001 mol/L EDTA和0.25 mol/L NH4NO3,调节提取溶液pH至2.5±0.1。其中,HOAc有分解磷灰石的作用,并且它的解离常数低(pKa=1.76×10–5),表现出很强的酸碱缓冲能力。F–对P有很强的取代能力,需要在提取环境pH低于2.9时,才能发挥最大提取效能。HNO3的作用在于预先调节提取液pH。EDTA是金属元素Mn、Cu、Zn等的强烈螯合剂,可提高这些金属元素的提取效率[1]。而试剂中NH4NO3作为惰性电解质,主要起着缓冲提取液pH和取代被提取元素的作用。
但是试剂NH4NO3在持续受热条件下具有热失控特性,在使用、存储和运输过程中容易发生爆炸[6-7]。澳大利亚于2004年协议达成一个全国性的方案,除特许使用者外,全面禁止其他人获取危及安全的NH4NO3[8]。2019年联合国《关于危险货物运输的建议书—试验和标准手册》[9]中强调,NH4NO3乳胶、悬浮液或凝胶是制作炸药的中间产物,高纯度NH4NO3需要作为危险货物运输。我国国标GB/T 29879—2013《硝酸铵类物质危险特性分类方法》[10]中规定,除特殊用途外,全面禁止其他人获取危及人身安全的NH4NO3。由于NH4NO3的管制,尤其对县级和乡镇的农业技术推广中心而言,虽然承担了全国大部分土壤质量调研工作,M3方法的使用却受到很大限制;而对土壤有效养分和重金属元素进行快速、准确监测和检测是维持土壤健康的重要一环。
另外,我国土壤资源丰富,钙质土壤、高度风化土壤、水耕人为土壤等都有大面积分布,这些土壤中P元素赋存形态存在很大差异。有效P提取一般首先需要确定土壤pH范围,对酸性、中性和碱性土壤分别采用Bray法和Olsen法进行提取,方法差异造成土壤有效P含量的定量比较在不同土壤之间存在技术难题。另外对酸性和碱性土壤进行改良时,添加碱性和酸性改良剂后土壤pH变化很大,如生物质炭的加入极大提高酸性土壤pH和补充土壤中Ca2+[11-13],此时需要一种同时兼顾不同pH土壤有效P的测定方法,才能定量评价土壤的改良效果。而M3法同时兼顾了酸性土壤中Fe/Al-P的提取,又考虑到了碱性土壤中Ca-P的提取,该方法适用于各种土壤中有效P的提取测定。
因此,本文目的在于用安全化学试剂惰性电解质NH4Cl取代易制爆NH4NO3,研究NH4Cl替代NH4NO3 M3法(NH4Cl-M3法)提取土壤中P、K、Ca、Mg、Al、Fe、Zn、Mn、Cu等元素的效果,并对NH4Cl-M3法提取的有效P含量与Bray和Olsen法获得的有效P含量进行相关性分析,进而运用NH4Cl-M3法进行定量评价改良土壤中P有效性,以期找出一种通用型土壤有效元素高效提取方法。
1 材料与方法 1.1 土壤基本性质选取全国28种表层(0~20 cm)土壤,pH范围4.71~9.22,有机质含量介于3.31~54.71 g/kg,阳离子交换量介于4.87~33.41 cmol/kg,基本上涵盖了我国主要土壤类型;另外选取土壤有效态成分分析标准物质GBW07416、GBW07459进行数据质量控制。
土壤pH在土水比为1:2.5(m: V)的悬液中用pH计(Orion 3Star,热电,美国)测定;醋酸铵法测定土壤阳离子交换容量[4];重铬酸钾氧化–外加热法测定土壤中的有机质;游离氧化铁、铝用连二亚硫酸钠–柠檬酸钠–重碳酸钠溶液提取后,电感耦合等离子发射光谱(ICP-AES, VISTA-MPX,瓦里安,美国)测定[14]。供试土壤基本性质列于表 1。
|
|
表 1 2种标准土壤样品和28种供试表土基本性质(部分数据来源于文献[15]) Table 1 Basic properties of 2 certified reference materials and 28 tested topsoils. |
选取了海南、广东和河北3个地区的砖红壤、红壤和酸污染潮土,分别添加不同碱性改良剂,其中海南砖红壤分别添加1% 400 ℃下制备的稻草秸秆炭、花生秸秆炭、大豆秸秆炭、油菜秸秆炭以及活性炭[16];广东红壤添加4 g/kg生物质灰、2 g/kg骨渣和2 g/kg碱渣混合改良剂处理[17];河北潮土分别添加5% 400 ℃制备的花生秸秆炭和大豆秸秆炭。在70% 田间持水量和25 ℃下培养56 d后,风干研磨过60目筛(0.25 mm)后,供土壤P有效性的改良效果评价用。
1.2 NH4Cl-M3法、M3法、Olsen和Bray法测定土壤有效磷按0.2 mol/L HOAc, 0.015 mol/L NH4F, 0.013 mol/L HNO3, 0.001 mol/L EDTA和0.25 mol/L NH4NO3(或NH4Cl),按比例配制M3法或NH4Cl-M3法试剂,此时溶液pH约为3.1,用5 mol/L HNO3(或HCl)调节提取溶液pH至2.5±0.1;按0.025 mol/L HCl和0.03 mol/L NH4F配制Bray提取剂,配制0.5 mol/L NaHCO3(pH=8.5)的Olsen提取剂。以上所用试剂均为沪试或南化试剂公司提供分析纯试剂。
称取2.000 g过60目筛上述30种风干土壤样品于50 ml的离心管中,分别加入20 ml的上述M3法和NH4Cl-M3法浸提液,在旋转振荡仪(QB-128,其林贝尔,中国)上以80 r/min振荡30 min后,4 500 r/min离心5min,过滤,ICP-AES测定提取液中P、K、Ca、Mg、Al、Fe、Zn、Mn、Cu等元素浓度。
分别称取2.000 g过60目筛上述10种酸性(pH < 6.0)土壤样品,或1.000 g过60目筛上述20种碱性(pH≥6.0)土壤样品于50 ml的离心管中,分别加入20 ml Bray和Olsen提取剂,在旋转振荡仪上以80 r/min振荡30 min后,4 500 r/min离心5min,过滤[18-19],磷钼蓝比色法在700 nm处测定提取液中P浓度(UV-3000,美谱达,中国)。根据以上提取液中各种元素有效态浓度,计算得出土壤中该元素有效态含量。
1.3 数据质量控制与统计分析数据质量控制通过以下方法保证数据的可信度:所有实验重复2次,当平行样品间分析结果差异超过5% 时,增加样品分析;无论是磷钼蓝比色法还是ICP-AES测定时,标准曲线均超过99.9%;ICP-AES测定过程中,每隔10个样品监测一次质控样,保证测定误差控制在5% 以内。采用单因素方差分析(One-Way ANOVA)中Duncan多重比较进行样本间差异显著性分析,统计NH4Cl-M3法、Bray法以及Olsen法获得的有效P在不同土壤中是否存在显著差异。Pearson相关分析研究NH4Cl-M3法分别和M3法、Bray法、Olsen法测定土壤有效P、K、Ca、Mg、Fe、Al、Cu、Zn和Mn元素含量之间的相关性。
2 结果与讨论 2.1 M3法和NH4Cl-M3法测定土壤中元素有效态含量与有效态成分分析标准物质认定值之间的比较表 2所示为土壤有效态成分分析标准物质GBW07416和GBW07459认定值,以及用M3法和NH4Cl-M3法测定GBW07416和GBW07459的元素有效态含量,可以看出,土壤有效态成分分析标准物质GBW07416和GBW07459的认定值与M3法和NH4Cl-M3法所获的数值接近。譬如,土壤有效态成分分析标准物质GBW07416认定值,通过M3法和NH4Cl-M3法得到的有效P含量分别为0.5、1.07和1.51 mg/kg,GBW07459有效P含量分别为15.7、31.28和28.63 mg/kg。可以看出M3法和NH4Cl-M3法提取有效P效率高于标准样品的认定值。刘婷娜等人[20]也发现M3法浸提P效果高于常规浸提方法,原因主要在于M3法以及NH4Cl-M3法提取剂中F–可调控从Al、Fe等无机P源中解吸,同时pH=2.5的强酸缓冲条件满足提取Ca-P的需求,使得M3法和NH4Cl-M3法比标准样品中P的认定值要高。因此,未来我们利用NH4Cl-M3法进行土壤有效P评估时,需要注意由于该方法不仅可以提取Fe/Al-P,还能提取Ca-P,提取效率高于Olsen或Bray等方法,当进行历史数据比较时,需要进行更加详尽的数据分析,以确保数据的可比性。另外,造成两种M3方法样品间分析结果差异的原因可能是多方面的:①提取效率差异(包括提取试剂性质不同、供试土壤性质差异、实验室操作环境的差异、提取间隔时间略有不同等);②ICP-AES测定过程中引起的误差(包括样品放置时间的差异、分析过程中仪器检测噪声影响等)。以上原因大多源自于实验过程中不可避免的试剂差异、人员操作误差、仪器误差等。
|
|
表 2 土壤有效态成分分析标准物质认定值和M3法、NH4Cl-M3法获得有效元素含量(mg/kg)比较 Table 2 Comparison of certified values of reference materials and soil available element contents (mg/kg) determined by M3 and NH4Cl-M3 methods |
同时,M3法和NH4Cl-M3法得到的有效态Cu、Zn、Fe、Mn含量介于用DTPA、HCl和NaNO3溶液提取的认定值之间。具体而言,两种M3方法得到的有效态含量低于HCl提取态,高于DTPA和NaNO3提取态含量。GBW07459中用M3法和NH4Cl-M3法测定有效态Cu、Zn、Fe、Mn含量均高于其认定值,主要是由于该土壤有效态金属认定值分别通过DTPA提取剂(pH=7.3)或NaNO3溶液提取,提取效率较低。EDTA对有效态金属Cu、Zn、Fe、Mn的提取效率高于DTPA,并且EDTA对Cu和Zn等金属的提取具有明显的pH依赖性,pH越低提取效率越高[21-22]。因此,NH4Cl-M3法在酸性条件下(pH=2.5),可提取更多钙质土壤中的金属元素。
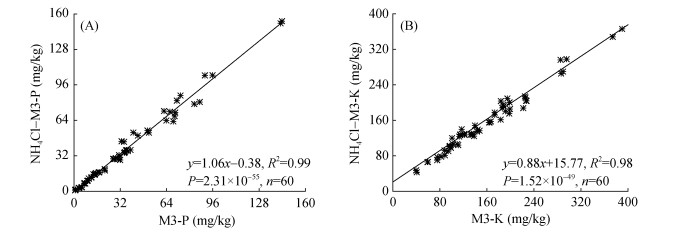
图 1为28种供试土壤和2种标准物质用M3法和NH4Cl-M3法测定得到的有效态P、速效K含量。结果表明,M3法和NH4Cl-M3法测定土壤中的有效P和速效K含量极显著相关(P=2.31×10–55、1.52×10–49, n=60)。M3法中试剂NH4NO3作为惰性电解质,主要起着缓冲提取悬液pH和取代被提取元素的作用,用NH4Cl替代NH4NO3尽可能还原了M3法体系中NH4NO3的作用。同时,M3法和NH4Cl-M3法中有效P的提取,主要源于F–络合取代能力强于P,增强了FePO4、AlPO4中P的提取[5],所以两种方法获得的有效P存在极显著相关。M3法和NH4Cl-M3法中速效K的提取,主要源于0.25 mol/L NH4NO3或NH4Cl与0.2 mol/L HOAc形成了pH=2.5的强缓冲体系,使得土壤中速效K的提取能力显著提高。
|
图 1 M3法和NH4Cl-M3法测定30种土壤有效P(A)、速效K(B)结果比较 Fig. 1 Comparison of available phosphorus (A) and potassium (B) in 30 tested topsoils determined by M3 and NH4Cl-M3 methods |
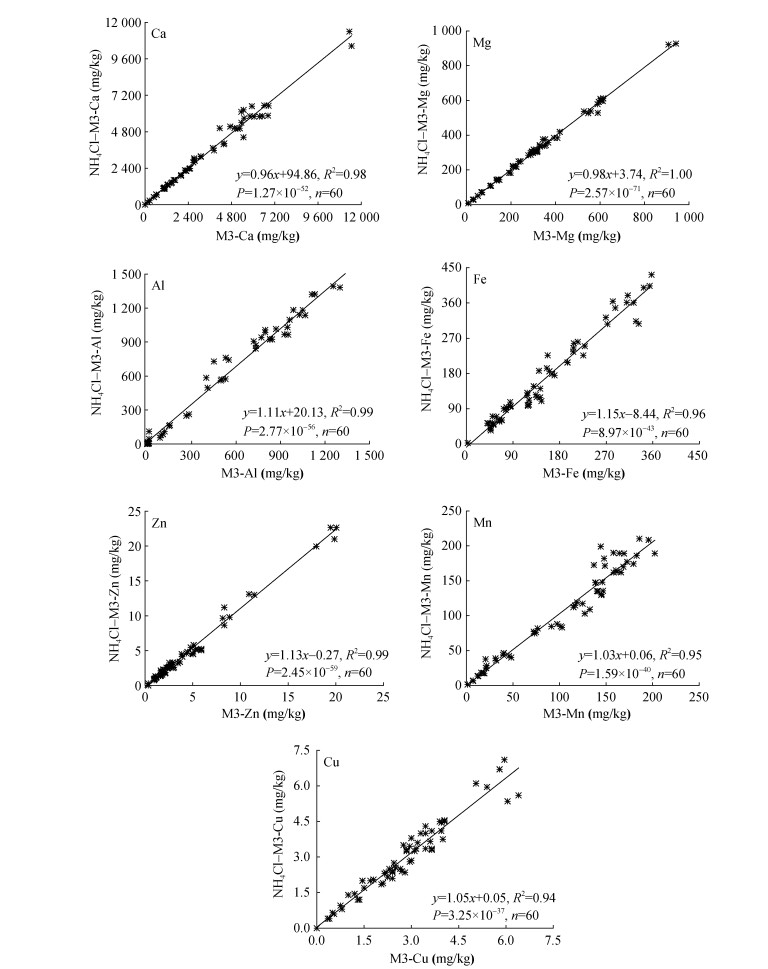
M3法和NH4Cl-M3法提取土壤中多种金属元素含量的相关关系,如图 2所示。从中可以看出两种方法测得的Ca、Mg、Al、Fe、Zn、Mn和Cu含量呈极显著相关,决定系数R2分别为0.98、1.00、0.99、0.96、0.99、0.95、0.94;P分别为1.27×10–52、2.57×10–71、2.77×10–56、8.97×10–43、2.45×10–59、1.59×10–40、3.25×10–37。因此,NH4Cl-M3法适用于各种土壤有效P和速效K的提取,也可满足Ca、Mg、Al、Fe、Zn、Mn和Cu等多种金属元素提取的需要[5]。
|
图 2 M3法和NH4Cl-M3法测定30种土壤有效态Ca、Mg、Al、Fe、Zn、Mn、Cu的结果比较 Fig. 2 Comparison of available elements of Ca, Mg, Al, Fe, Zn, Mn and Cu in 30 tested topsoils determined by M3 and NH4Cl-M3 methods |
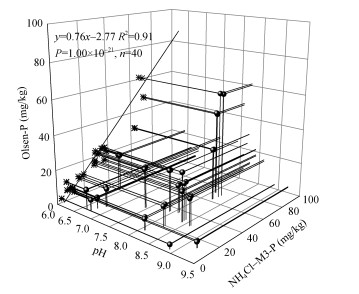
将从21个省获取的28种土样和2种土壤有效态成分分析标准物质以pH = 6为界,分别采用Bray以及Olsen法提取土壤中的有效P,结果表明,pH < 6的10种酸性土壤,Bray法和NH4Cl-M3法提取的有效P结果极显著相关(图 3,P=1.42×10–15,n=20)。Sawyer和Mallarino[23]研究也表明,在酸性土壤中,M3-P和Bray-P的结果相似。Olsen法和NH4Cl-M3法提取pH≥6的20种中性和碱性土壤有效P结果也极显著相关(图 4,P=1.00×10–21,n=40)。这与Sawyer和Mallarino[23]研究结果也一致,即石灰性土壤中M3法和Olsen法测定结果显著相关。

|
图 3 10种酸性土壤NH4Cl-M3-P和Bray-P相关性 Fig. 3 Correlation between available P contents of 10 tested acid soils determined by NH4Cl-M3 and Bray methods |
|
图 4 20种中性和碱性土壤NH4Cl-M3-P和Bray-P相关性 Fig. 4 Correlation between available P contents of 20 tested neutral and alkaline topsoils determined by NH4Cl-M3 and Olsen methods |
Bray法提取酸性土壤有效P,一是通过NH4F中的F–和Fe-P、Al-P中的Fe、Al在酸性条件下形成络合物从而释放有效P;二是通过稀酸溶解部分P,因此这种方法适用于酸性土壤而不适于石灰性土壤[24]。Olsen法主要适用于石灰性土壤,其提取液中的HCO3-在碱性条件下可以和土壤溶液中的Ca2+形成CaCO3沉淀,降低Ca2+活度而使某些活性较大的Ca-P被浸提出来。正如上文所述,NH4Cl-M3法可提取Al、Fe、Ca等各种结合形态P,因此NH4Cl-M3法比Bray法和Olsen法所提取的有效P含量更高(图 3和图 4),Mehlich[1]和Tan等[25]比较M3法与Bray和Olsen法测定土壤有效P也观察到了相似的结果。因此,NH4Cl-M3法可用于不同pH土壤有效P含量的测定。
2.3 运用NH4Cl-M3法评价土壤改良效果分别选取pH为5.04、4.56和5.40的海南砖红壤、广东红壤和河北潮土进行改良土壤有效P评价,添加改良剂后,3种土壤的pH分别提高至6.13~7.52,6.33和7.05~7.57,如果按常规实验室操作需要对酸性、中性和碱性(pH 6.0为界)土壤分别进行Bray和Olsen法提取,可以发现2种方法提取的有效P含量不完全一致(表 3)。譬如,Bray法和Olsen法测定的改良广东红壤有效P含量相差1.43倍;又如受酸污染的河北潮土,Bray法提取的有效P含量是Olsen法的1.23倍~ 2.27倍;再譬如酸性原土样品中有效P测定结果存在较大差异,海南砖红壤、广东红壤和河北潮土等3种酸性原土样品NH4Cl-M3-P分别为1.5、2.1和283.5 mg/kg,显著高于Bray法得到的有效P含量(分别为1.1、0.2和227.5 mg/kg)。其中的原因正如上文所述,NH4Cl-M3方法提取有效P效率更高;另外,海南砖红壤和广东红壤这2种土壤本身的有效P含量较低,不同方法得到的土壤有效P含量绝对值差异较大。对河北潮土而言,它是一个酸污染土壤,由于土壤pH较低(pH=5.4),采用Bray法测定其有效P含量,但土壤本身的铁铝氧化物含量又不高,用Bray法提取铁铝结合态P(227.5 mg/kg)比NH4Cl-M3法所得有效P含量(283.5 mg/kg)低很多;再者河北潮土属于钙质土壤,未污染土壤pH一般在7.6~8.5[26],理论上需要用Olsen法测定其有效P含量,但提取过程中大部分碱用于中和土壤酸度,提取的有效P效率更低(69.6 mg/kg)。因此,不同pH土壤的有效P提取方法各异,可能导致评价改良土壤有效P提升的效果存在疑议。
|
|
表 3 NH4Cl-M3法测试土壤改良效果(部分数据来源于文献[16-17]) Table 3 Available P contends in amended acid soils determined by NH4Cl-M3 method |
兼顾Fe/Al-P和Ca-P的NH4Cl-M3法得到的海南砖红壤改良结果表明,尤其是对花生秸秆炭改良土壤而言,相比于原始土壤,有效P含量提高了44.1倍;而NH4Cl-M3法得到的广东红壤和其改良土壤有效P含量分别为2.1和64.3 mg/kg,有效P提高了29.6倍;再以受酸污染的河北潮土为例,NH4Cl-M3法表明添加5% 的花生秸秆炭和大豆秸秆炭,可分别提高有效P含量28.4% 和36.7%。因此,NH4Cl-M3法测定土壤有效P结果表明,本文中所涉及的改良土壤中的有效P含量均显著增加。
3 结论1) NH4Cl-M3法不仅可以代替M3法测定不同地区土壤的有效P和速效K含量,而且也可以提取Ca、Mg、Al、Fe、Zn、Mn和Cu等金属元素。
2) NH4Cl-M3法与Bray和Olsen法提取有效P结果比较发现,NH4Cl-M3法不仅可以提取酸性土壤,也可提取中性和石灰性土壤中的有效P,解决了Bray和Olsen法分别不适用于碱性和酸性土壤有效P提取的问题,并且可同时提取有效K、Ca、Mg、Al、Fe、Zn、Mn和Cu等元素。
因此,NH4Cl-M3法适用于所有酸性、中性和碱性土壤有效P、速效K等营养元素测定,也适用于有效态重金属Zn、Cu等元素测定,是一种高效、通用型土壤有效元素提取方法。
| [1] |
Mehlich A. Mehlich 3 soil test extractant: A modification of Mehlich 2 extractant[J]. Communications in Soil Science and Plant Analysis, 1984, 15(12): 1409-1416 DOI:10.1080/00103628409367568 (  0) 0) |
| [2] |
刘肃, 李西开. Mehlich3通用浸提剂的研究[J]. 土壤学报, 1995, 32(2): 132-141 DOI:10.3321/j.issn:0564-3929.1995.02.010 (  0) 0) |
| [3] |
卜玉山, Magdoff F R. 十种土壤有效磷测定方法的比较[J]. 土壤学报, 2003, 40(1): 140-146 DOI:10.3321/j.issn:0564-3929.2003.01.020 (  0) 0) |
| [4] |
Pansu M, Gautheyrou J. Handbook of soil analysis: Mineralogical, organic and inorganic methods[M]. Springer Science & Business Media, 2007.
(  0) 0) |
| [5] |
Sims J T. Comparison of mehlich 1 and mehlich 3 extractants for P, K, Ca, Mg, Mn, Cu and Zn in Atlantic coastal plain soils[J]. Communications in Soil Science and Plant Analysis, 1989, 20(17/18): 1707-1726 (  0) 0) |
| [6] |
徐森, 陈相, 段瑞坤, 等. 硝酸铵乳胶在持续受热条件下的热失控特性[J]. 化工学报, 2014, 65(3): 1135-1141 DOI:10.3969/j.issn.0438-1157.2014.03.051 (  0) 0) |
| [7] |
Kumar D, Elias A J. The explosive chemistry of nitrogen[J]. Resonance, 2019, 24(11): 1253-1271 DOI:10.1007/s12045-019-0893-2 (  0) 0) |
| [8] |
澳大利亚农业, 水和环境部, 对硝酸铵的管制: 农业人士须知[OL]. 2004. https://www.agriculture.gov.au/sites/default/files/sitecollectiondocuments/languages/chinese/mandarin/Chinese_simpl_amnitrate.pdf.
(  0) 0) |
| [9] |
联合国, 关于危险货物运输的建议书-试验和标准手册[OL]. 2019. https://www.unece.org/fileadmin/DAM/trans/danger/publi/manual/Rev7/ST-SG-AC10-11-Rev7c_WEB.pdf.
(  0) 0) |
| [10] |
中华人民共和国国家质量监督检验检疫总局. 硝酸铵类物质危险特性分类方法: GB/T 29879—2013[S]. 北京: 国家标准出版社. 2013.
(  0) 0) |
| [11] |
Jiang J, Xu R K. Application of crop straw derived biochars to Cu(Ⅱ) contaminated Ultisol: Evaluating role of alkali and organic functional groups in Cu(Ⅱ) immobilization[J]. Bioresource Technology, 2013, 133: 537-545 DOI:10.1016/j.biortech.2013.01.161 (  0) 0) |
| [12] |
Palansooriya K N, Ok Y S, Awad Y M, et al. Impacts of biochar application on upland agriculture: A review[J]. Journal of Environmental Management, 2019, 234: 52-64 (  0) 0) |
| [13] |
Wang H, Dong Y, Tong X J, et al. The amelioration effects of canola straw biochar on Ultisol acidity varied with the soil in which the feedstock crop was cultivated[J]. Journal of Soils and Sediments, 2020, 20(3): 1424-1434 DOI:10.1007/s11368-019-02504-2 (  0) 0) |
| [14] |
Mehra O P, Jackson M L. Iron oxide removal from soils and clays by a dithionite-citrate system buffered with sodium bicarbonate[J]. Clays and Clay Minerals, 1958, 7(1): 317-327 DOI:10.1346/CCMN.1958.0070122 (  0) 0) |
| [15] |
Zhang P, Wu T, Ata-Ul-Karim S, et al. Influence of soil properties and aging on antimony toxicity for barley root elongation[J]. Bulletin of Environmental Contamination and Toxicology, 2020, 104(5): 714-720 DOI:10.1007/s00128-020-02826-9 (  0) 0) |
| [16] |
Jiang J, Yuan M, Xu R K, et al. Mobilization of phosphate in variable-charge soils amended with biochars derived from crop straws[J]. Soil and Tillage Research, 2015, 146: 139-147 DOI:10.1016/j.still.2014.10.009 (  0) 0) |
| [17] |
Shi R Y, Li J Y, Xu R K, et al. Ameliorating effects of individual and combined application of biomass ash, bone meal and alkaline slag on acid soils[J]. Soil and Tillage Research, 2016, 162: 41-45 DOI:10.1016/j.still.2016.04.017 (  0) 0) |
| [18] |
Bray R H, Kurtz L T. Determination of total, organic, and available forms of phosphorus in soils[J]. Soil Science, 1945, 59(1): 39-46 DOI:10.1097/00010694-194501000-00006 (  0) 0) |
| [19] |
Olsen S R, Cole C V, Watanabe F S, et al. Estimation of available P in soil by extraction with sodium bicarbonate[EB/OL]. 1953
(  0) 0) |
| [20] |
刘婷娜, 苏永中, 范桂萍, 等. 常规浸提剂与联合浸提剂测定我国北方石灰性土壤有效磷钾的比较[J]. 土壤, 2018, 50(5): 924-928 (  0) 0) |
| [21] |
丁竹红, 胡忻, 尹大强. 螯合剂在重金属污染土壤修复中应用研究进展[J]. 生态环境学报, 2009, 18(2): 777-782 DOI:10.3969/j.issn.1674-5906.2009.02.067 (  0) 0) |
| [22] |
Yu J Z, Klarup D. Extraction kinetics of copper, zinc, iron, and manganese from contaminated sediment using Disodium Ethylenediaminetetraacetate[J]. Water, Air, and Soil Pollution, 1994, 75(3/4): 205-225 (  0) 0) |
| [23] |
Sawyer J E, Mallarino A P. Differentiating and understanding the Mehlich 3, Bray, and Olsen soil phosphorus tests[C]. Agronomy Conference Proceedings and Presentations.
(  0) 0) |
| [24] |
宋春丽, 樊剑波, 何园球, 等. 我国南方地区典型红壤有效磷测定方法研究[J]. 土壤, 2012, 44(1): 133-139 DOI:10.3969/j.issn.0253-9829.2012.01.022 (  0) 0) |
| [25] |
Tran T S, Giroux M, Guilbeault J, et al. Evaluation of Mehlich-Ⅲ extractant to estimate the available P in Quebec soils[J]. Communications in Soil Science and Plant Analysis, 1990, 21(1/2): 1-28 (  0) 0) |
| [26] |
李承绪, 丁鼎治, 杨思治, 等. 河北土壤[M].
河北科学技术出版社, 石家庄, 1989
(  0) 0) |
2. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2021, Vol. 53
2021, Vol. 53


