2. 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所), 南京 210008
酞酸酯,又名邻苯二甲酸酯,作为增塑剂或添加剂广泛应用于增强聚氯乙烯等塑料制品的可塑性和柔软性[1-2]。日常化工及生活用品,如油漆、橡胶制品、黏合剂和化妆品等,以及农膜、有机肥等农业生产资料均被检测出含有一定含量的酞酸酯[3]。近年来,越来越多的研究表明,酞酸酯具有内分泌干扰性[4],会对呼吸、神经、生殖系统等产生不利影响[5]。考虑到酞酸酯的健康风险,美国环境保护局(USEPA)、欧盟(EU)和中国国家环境监测中心将邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二正丁酯(DBP)、邻苯二甲酸二正辛酯(DnOP)、邻苯二甲酸二(2-乙基)己酯(DEHP)和邻苯二甲酸丁基苄基酯(BBP) 6种常见酞酸酯列为优先控制污染物[6]。据报道,全球塑料制品年产量约为3亿t,每年酞酸酯使用量达到近800万t[7]。而塑料中添加的酞酸酯与聚合物间大多为物理结合,并非化学结合,因此很容易在工业和塑料制品的生产、使用和最终处置过程中释放到环境[8]。中国是最大的塑料消费国,频繁使用农用地膜、农药、化肥等农业投入品使酞酸酯成为我国农业土壤中普遍存在且最受关注的有机污染物之一[9],有些地区土壤中酞酸酯含量已达到mg/kg数量级[10],农膜覆盖土壤中酞酸酯含量是未覆盖土壤的2.5倍~ 3倍[11]。因此如何加速污染农田土壤中酞酸酯消减已成为目前亟需解决的重大环境科技问题。
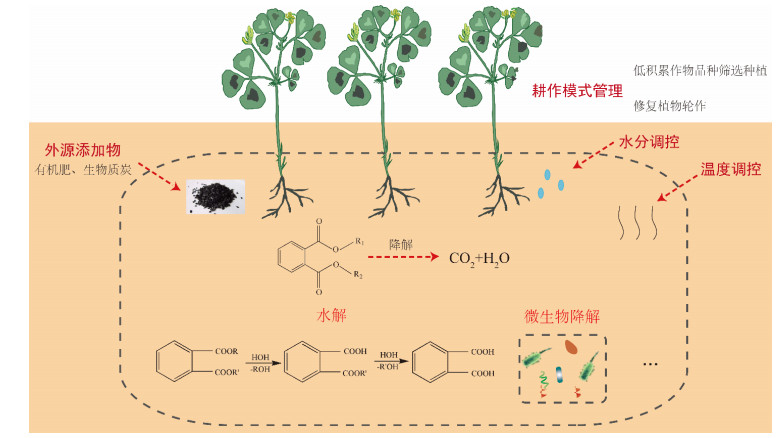
农田土壤中酞酸酯消减涉及水解、光解、化学降解和生物降解等多种过程,存在效率低、周期长等特点,在实际生产或修复过程中仍需采取一定强化措施以加速消减。农艺调控措施具有绿色环保、经济成本低、可实现原位修复且不产生二次污染等优点,可以同时实现边修复边生产,近年来逐渐成为适宜大面积污染农田土壤较为理想的修复措施之一[12]。农艺措施一方面可以通过改变土壤理化性质从而影响污染物在土壤中的迁移转化过程;另一方面也可以通过调控土著微生物丰度或功能从而强化污染物的生物降解。目前,关于农艺调控措施强化土壤中酞酸酯消减已开展了一些研究,主要包括水分调控、温度调控、添加生物质炭及有机肥等土壤改良剂以及耕作模式管理等。本文结合国内外研究,综述了不同农艺措施对土壤中酞酸酯消减行为的调控作用和影响因素(图 1),并对该领域的进一步研究提出了展望,以期为创新与发展酞酸酯污染农田土壤的农艺措施强化修复原理与技术提供参考。
|
图 1 土壤中酞酸酯消减的农艺调控示意图 Fig. 1 Schematic diagram of agronomic measures regulating dissipation of phthalic acid esters in soil |
农田水分管理是操作简单、绿色经济的有效农艺调控措施之一。土壤含水量的变化一方面很大程度上通过直接影响土壤氧化还原电位和酸碱度,以及有机质、养分总量和有效态含量等土壤理化性质,而影响土壤中酞酸酯的化学降解过程;另一方面,土壤水分是影响微生物活性的重要因素,因此含水量差异可能会直接影响土壤生态系统的净化功能。这两方面综合作用于土壤中酞酸酯的消减,影响其消减过程与速率。
1.1 水分调控改变土壤中酞酸酯的化学转化过程酞酸酯具有酯类的共性,可以在含水环境中发生酸碱催化反应而水解[13]。酸性或碱性环境下,酞酸酯水解效率明显低于中性pH条件[14]。土壤pH受土壤水分影响显著[15],一般情况下,土壤pH与土壤含水量呈正相关。除了直接作用于水解过程,土壤pH变化也可能会影响酞酸酯在土壤中的积累程度。大多研究表明,由于水分变化导致土壤pH升高时,土壤表面与污染物发生同性电荷排斥,降低了土壤对有机污染物的吸附能力,因此有机污染物在土壤中的积累量通常与土壤pH呈负相关[16]。酞酸酯的水解过程通常受到多种因素的共同影响,目前已有文章详细综述了酞酸酯水解过程的影响因素[17],这里不再赘述。水解过程虽然能够初步降解酞酸酯,但在自然条件下酞酸酯的水解效率仍然不同,且水解周期较长[13]。因此,水解通常并不是土壤中酞酸酯的主要降解过程。
此外,土壤水分含量的变化还能够改变含氧量、有机质和氮、铁等典型元素地球化学过程。过多的水分使土壤缺氧甚至达到厌氧环境,从而降低土壤有机质分解的速率[18],而有机质是影响土壤中酞酸酯吸附迁移的重要因素。相较于低有机质土壤,酞酸酯在有机质含量较高的土壤中存在更强的吸附特性[16],从而表现出更弱的生物有效性[19]。土壤水分含量也是调控土壤中氮、铁氧化还原过程及其耦合的碳转化过程的关键环境因子[20],这些重要元素的生物地球化学循环过程通常与有机污染物的降解转化存在耦合作用,因此可能会直接影响土壤中酞酸酯的消减过程。例如,红壤黏土矿物中较高的铁含量能够促进·OH自由基的产生,发生Fenton反应,从而加速降解酞酸酯[21]。但目前关于水分调控改变土壤中酞酸酯的化学转化过程的研究报道仍较为有限,亟需开展深入研究。
1.2 水分调控影响土壤中酞酸酯的微生物降解土壤微生物参与到许多关键的土壤生物化学反应过程中,是土壤生态系统的重要组成部分之一,也是土壤中有机污染物主要的转化器与净化器[22]。土壤水分变化会直接影响土壤微生物的结构和功能,含水量过高或过低的情况下都会抑制其活性。土壤微生物在干旱环境中会因缺少水分而处于休眠状态,导致活性降低[23];当土壤水分过多时,土壤中的孔隙被水填满致使氧气不能向土壤中扩散,土壤中氧气含量降低,也会抑制土壤微生物活性[24]。周际海等[25]研究了土壤水分为饱和含水量的35%、50% 和65% 时对土壤微生物活性的影响,发现65% 的水分处理显著提高了土壤微生物活性。土著微生物中如真菌、细菌均已被报道存在对酞酸酯具有降解能力的菌属,多项研究表明,土壤真菌的数量随土壤水分减少而增加,而细菌数量随水分减少而降低[26]。已有研究报道,DEHP降解率与土壤中细菌数量呈正相关关系[14]。陈英旭等[27]研究了水分对土壤中DEHP和DBP降解的影响,将土壤含水量分别调节为30% 和100%以模拟旱地环境和淹水环境,结果表明,旱地的好氧条件更利于土壤微生物降解DEHP和DBP。Zhu等[28]通过宏基因组测序进一步发现,在旱地好氧和淹水厌氧条件下,潜在降解菌属对DEHP在土壤环境的生物降解起着重要作用。
土壤水分含量的变化导致的理化性质改变与土壤微生物生长活动密切相关,也会直接影响土壤微生物群落的结构、丰度、多样性和功能,从而影响土壤中酞酸酯的微生物降解。比如,水分变化导致的pH改变可以显著影响土壤微生物群落,从而可能会改变土壤中酞酸酯的消减过程。Rousk等[29]发现真菌在酸性土壤中(pH 4.5)生长速率最大,pH升高则生长速率降低,细菌在碱性土壤中(pH > 7)生长最快,与pH正相关。目前已报道的大部分酞酸酯降解菌属都生长在中性环境中,最适生长pH为7.0 ~ 8.0[30]。Zhu等[14]研究表明,DEHP在酸性(pH < 6.0)或碱性(pH > 8.0)土壤中去除率较低(< 25%)。土壤水分变化同样影响着微生物丰度,从而影响土壤微生物对有机污染物的消减。Liu等[31]发现通过调节土壤含水量为15%,可以提高厚壁菌门(Firmicutes)和芽孢杆菌属(Bacillus sp.)的相对丰度,利于石油烃的降解。
尽管土壤水分变化既可能通过改变土壤理化性质,从而影响土壤中酞酸酯的化学转化过程,也可能通过影响土壤微生物,从而改变土壤中酞酸酯的消减,但目前关于这方面的研究仍相当有限,且已报道的研究对水分调控的影响机制阐明仍不清楚,其有待进一步深入研究。此外,已有研究表明,土壤含水量变化对微生物群落的影响与土壤类型有关[32],提示在考虑通过水分调控土壤中酞酸酯消减的影响时,要考虑土壤类型的差别,但这方面还未见报道。
2 温度调控对土壤中酞酸酯消减的影响土壤环境中的温度是影响污染物微生物转化的重要因素。在一定范围内,提高温度可刺激微生物的生长和活性,提高污染物的传质速率,促进其吸收和代谢过程,从而提高污染物的降解转化速率。
2.1 改变温度调控土壤微生物的生长活性和群落结构微生物降解是土壤环境中酞酸酯完全矿化的重要途径。土壤呼吸强度常用于评估土壤微生物整体活性。呼吸作用强度越大,表明土壤微生物活性越高,从而越利于土壤中污染物的生物降解。土壤温度与土壤呼吸显著相关,是影响农田生态系统土壤呼吸的主要因子之一。采用多种类型土壤研究土壤呼吸与温度间的关系,结果表明,在一定温度范围内,土壤呼吸速率与温度呈正相关[33]。通常情况下,降解微生物发挥对酞酸酯的最佳降解作用需要合适的温度条件。每种降解微生物都有其最适的生长温度,大部分降解微生物的最适生长温度在20 ~ 40 ℃,温度过高或过低都会抑制土壤微生物活性,但有些酞酸酯降解菌在低温条件下(10 ℃)对DBP的降解速率也能达到最高[30]。在不同温度条件土壤中DEHP降解速率的动态变化研究发现,DEHP降解率与降解速率均随着温度的升高而增加,DEHP降解率在35 ℃时达到最大[27]。
土壤温度除影响土壤微生物的生长活性之外,也能够改变土壤微生物群落结构,但目前关于温度对土壤微生物群落结构的调控效应并未呈现出一致的结果。王文立等[34]对前人发表的增温控制试验的96组数据进行Meta分析,研究了土壤微生物对增温的响应模式,结果表明,土壤真菌数量随温度升高而增加,而土壤细菌数量随温度升高而降低;赵建琪等[35]研究了增温对南亚热带季风常绿阔叶林土壤微生物群落的影响,结果表明,由于温度升高影响土壤硝态氮和有机碳含量,导致了土壤微生物群落结构及其相对丰度发生改变;温度升高显著增加了细菌相对丰度、细菌真菌之比(B/F)以及革兰氏阳性菌与革兰氏阴性菌之比(G+/G–),使真菌和丛枝菌根真菌的相对丰度降低。但杨杰等[36]发现,旱地土壤即使土壤温度相差超过25 ℃,土壤细菌群落结构、丰度和多样性均没有产生显著差异。这可能与旱地土壤水分含量过低有关,微生物群落长期处于恶劣环境,因此受温度变化影响较小。土壤微生物群落结构改变可能会直接作用于土壤中酞酸酯的微生物降解,进而影响土壤中酞酸酯的消减行为。有研究表明,低浓度DEHP虽然可以促进细菌的生长,但并未对霉菌及放线菌产生类似影响[37],说明细菌群落能够利用DEHP作为其生长的碳源,是DEHP在土壤中降解的主导者。尽管目前越来越多的研究关注到温度对土壤微生物群落结构和功能的调控效应,但尚不清楚土壤中酞酸酯的生物转化过程中微生物群落的动态变化及其对温度的响应机制。
2.2 改变温度调控污染物的生物有效性提高温度通常能够增强土壤中有机污染物的溶解度,从而提高其生物有效性[38]。从前人研究结果可知,DBP、DEHP在土壤中的吸附性能随温度升高而显著降低,从而促进两者在土壤中的微生物降解,其中DEHP对温度的变化更为敏感[39]。温度也是影响化学反应速率的重要因素,提高温度通常可以促进酞酸酯转化过程的速率。于志彬等[40]通过正交试验发现,氢氧化钠浓度、水解时间和水解温度是影响DEHP水解的主要因素。温度升高能够提高水解过程的速率[17]。土壤有机质是土壤的重要组成部分,与土壤的物理、化学、生物等许多过程都直接或间接相关[41],温度是影响土壤有机质分解的主要环境因素之一[18],会影响土壤中有机质的积累,而土壤有机质含量最终会影响酞酸酯在土壤中的浓度。Xiang等[42]研究发现,在较低温度条件下,DBP在低有机质含量土壤中表现出较高的移动性和生物有效性。这与Tang等[43]研究结果一致,他们也发现DBP的生物降解速率与土壤溶解性有机质(DOM)浓度呈正相关,但认为主要是因为DOM为微生物生长提供了营养物质以及提高了酶活性,从而促进了PAEs的生物降解。温度同样也能够影响土壤养分含量。欧阳青等[44]研究增温对草甸土壤养分的影响,结果表明增温显著增加了表层土壤的速效磷含量。土壤温度还会影响土壤氮素的积累,温度是影响土壤氮矿化的重要因素之一。王士超等[45]研究结果表明,土壤氮素累积矿化量随温度升高而增加。温度对土壤养分的影响也取决于不同的土壤类型。王帘里和孙波[46]研究发现,土壤累积净矿化氮量在高有机质含量黑土中与温度呈正相关关系,但在有机质含量较低的潮土和红壤中净矿化氮量在25 ℃以上与温度呈负相关。土壤养分含量升高可以明显促进有机污染物在农业土壤中的消减,因此温度调控对于强化污染土壤酞酸酯消减具有重要的现实意义。但目前关于温度调控的大多研究仍停留在单一微生物对酞酸酯的降解方面,而关于其对土壤中酞酸酯消减行为的影响研究还较为有限,提高温度对酞酸酯在土壤中生物有效性的增强以及微生物功能的促进贡献仍不清楚,有待进一步深入研究。
3 外源添加物对土壤中酞酸酯消减的影响 3.1 生物质炭对土壤中酞酸酯消减的影响生物质炭是利用生物质材料在缺氧或无氧条件下通过热解生成的一种固态碳化颗粒物[47]。因其特殊的微观结构而具有高度的物化稳定性。生物质炭表面疏松多孔、比表面积较大、富含大量含氧基团,因此对污染物具有强吸附能力[48]。将生物质炭作为修复污染土壤的改良剂可以改善土壤环境,前人已有生物质炭对土壤理化性质影响的相关综述[49]。施加生物质炭可以提高土壤的持水能力,促进土壤团聚体的形成,从而改善土壤结构[49];提高土壤pH,中和土壤酸度[50]。生物质炭的添加还可以提高土壤有效养分含量,田间试验表明,生物炭具有提高农田土壤有机碳、氮含量的能力[51]。基于生物质炭既能作为土壤改良剂改善土壤环境,又能以良好的吸附性能影响土壤中有机污染物的迁移,因此生物质炭常被用作有机污染土壤的修复剂。
生物质炭对酞酸酯具有很强的吸附能力[52],可以有效降低酞酸酯在土壤中的迁移风险,成为土壤中酞酸酯的聚集汇。生物质炭对酞酸酯的吸附能力与制备生物质炭的原材料有关。Jing等[53]利用花生壳和麦秆为原料制成的生物质炭对DMP和DEP进行吸附–解吸研究,结果表明,麦秆生物质炭对DMP/DEP的吸附符合二级动力学,且吸附能力高于花生壳生物质炭;热力学和等温解吸试验表明,DMP、DEP在生物质炭上的吸附是物理自发的吸热过程,且吸附稳定。生物质炭对酞酸酯的吸附不仅与生物质炭原材料有关,生物质炭添加量、热解温度及土壤有机碳含量等也是影响生物质炭对酞酸酯吸附的主要因素。在添加不同含量生物质炭的土壤中,周震峰等[54]研究发现,添加1% 生物质炭含量的土壤对DMP吸附力最强,土壤对DMP的吸附作用与生物质炭添加量呈显著正相关。Jing等[53]研究发现,相比于650 ℃热解制得的生物质炭,低温(450 ℃)制得的生物质炭因其具有更大的极性和丰富的含氧官能团,对DEP有较强的吸附力,且新鲜生物质炭的吸附性能强于老化生物质炭。这是因为生物质炭对DEP的吸附是由范德华力和氢键驱动的,而老化生物质炭的表面由于三维水簇的形成而导致堵塞,使DEP与生物质炭之间的氢键效应降低。相比于稻草炭和秸秆炭等,竹炭对DEP的吸附效果最佳[55-56]。生物质炭原材料的性质对其吸附能力有很大影响,如pH等。He等[57]研究了生物质炭对DEHP在不同类型土壤中生物有效性的影响,发现土壤有机碳含量对DEHP在生物质炭改良土壤中的生物有效性起着关键作用;高有机碳土壤中DEHP残留浓度显著低于低有机碳土壤。生物质炭对酞酸酯良好的吸附性能可以使酞酸酯进入人类食物链和淋溶到地下水的风险降到最低。
此外,生物质炭因其自身特殊结构,可以成为土壤微生物的栖息地,促进土壤微生物的生长。已有文献报道,生物质炭的添加可以增加土壤中细菌、真菌以及放线菌的数量,并且细菌和放线菌数量随生物质炭施用量增加而增加[58]。添加生物质炭还可以显著增加土壤中氨氧化古菌、氨氧化细菌和nirK基因型反硝化细菌的丰度,提高土壤的硝化潜势[59]。这表明生物质炭的添加对土壤相关功能微生物群落丰度有着重要影响。生物质炭在富集土壤中酞酸酯的同时,可以促进微生物的生长活性,调控土壤中微生物群落结构,从而改变土壤中酞酸酯的消减行为,但目前关于施用生物质炭对土壤中酞酸酯微生物降解影响的相关文献仍较为有限,尤其缺乏生物质炭对土壤中酞酸酯消减行为的影响机制研究。
3.2 有机肥对土壤中酞酸酯消减的影响长期施用化肥虽然能够提高粮食产量,但过量施肥会造成严重的农业土壤退化以及环境污染。因此,自20世纪80年代以来我国开始大力推广有机肥的使用。有机肥是替代化肥的一种土壤改良剂。施用有机肥可以降低土壤容重,增加土壤孔隙度;增强土壤保水、保肥和通透性能[60];增加土壤有机质,提高土壤养分含量[61]。相比不施有机肥对照,有机肥的添加能够显著提高细菌丰度、丰富度和多样性,提高真菌丰富度和多样性,显著改变微生物群落结构[62]。有机肥的应用不仅能够改善土壤环境质量,还能够通过影响土壤微生物群落加强酞酸酯污染的生物降解。
土壤中酞酸酯污染主要影响了土壤微生物活性,而有机肥的施用可以促进有机污染土壤细菌、真菌的生长,恢复土壤微生物的活性。于小彬等[63]分析了有机肥对酞酸酯污染土壤生物修复的影响,结果表明,DBP、DEHP浓度为50 mg/kg的污染土壤对细菌、真菌生长有抑制作用,但施用有机肥能够显著恢复和增加被抑制的土壤细菌、真菌数量。Zhao等[64]的研究结果也证实了堆肥的添加能够通过刺激微生物活性而提高DBP在土壤中的降解率。近年来,生物质炭通常作为肥料载体用于生产炭肥,其与堆肥一起对土壤中酞酸酯降解也表现出较好的促进作用。He等[65]研究了生物质炭和堆肥的相互作用对土壤中DEHP降解的影响,结果表明,生物质炭和堆肥混合改良的土壤中DEHP降解速率明显快于只有单一改良的土壤。综上所述,生物质炭和堆肥的施用能够减小酞酸酯污染对土壤微生物的抑制作用,加强土壤对酞酸酯毒害的缓冲能力,增强土壤自身的生物修复功能,促进土壤中酞酸酯的吸附与降解,但有关促进的化学和微生物学机制还有待进一步深入研究。
4 耕作模式管理对土壤中酞酸酯消减的影响我国农业土壤中酞酸酯含量较高,针对不同浓度酞酸酯污染农田土壤,在强化土壤中酞酸酯消减的同时维持土壤的生产功能是目前污染土壤修复领域比较认可的修复方法,也是大面积酞酸酯污染农田土壤修复较为可行的方式。目前针对低浓度酞酸酯污染农田土壤,筛选酞酸酯低积累作物品种,利用低积累作物的根际降解作用,加速土壤中酞酸酯的消减,阻碍土壤中酞酸酯向作物中转运累积,可实现边生产边修复;针对高浓度酞酸酯污染农田土壤,多采用修复植物轮作,通过种植修复植物强化土壤中酞酸酯的消减,最大程度地降低土壤中酞酸酯的含量。
4.1 低积累作物品种筛选及种植种类不同的植物对酞酸酯的吸收累积能力不同,即使是同种植物的不同基因型品种对酞酸酯的吸收能力也存在显著差别。目前针对酞酸酯低积累作物品种的筛选已经开展了一些研究,筛选了水稻、玉米、通菜等作物的酞酸酯低积累品种。Cai等[66]研究了20个水稻品种间DEHP积累和转运的差异,发现不同水稻品种、不同生育期和不同组织间DEHP浓度存在显著差异,天丰优316、五优308和培杂泰丰是最理想的水稻品种。在蔡全英等[67]的研究中,不同品种的通菜对于DEHP吸收累积与土壤中DEHP的残留浓度存在显著差异,这与通菜的叶片大小和DEHP污染水平相关。在低污染、中污染以及高污染的DEHP土壤中,较大叶子、中等叶子和较小叶子的通菜品种是最优的种植品种。Li等[68]研究了8个玉米品种在DEHP污染土壤中吸收累积以及促进消减DEHP的能力,结果表明,玉米品种华农1号在种植40 d之后对DEHP的去除率高达87.5%。低积累作物除吸收弱外,其根际对土壤中酞酸酯的强化消减作用也是积累低的一个主要原因。植物根际降解是促进有机污染去除最重要的途径。在植物去除酞酸酯的过程中,植物根际产生的污染物降解转化作用最为显著,主要包含根系分泌物的促进作用。根系分泌物一方面能够促进根际微生物生长从而促进酞酸酯的降解;另一方面,根系分泌物可以提高酞酸酯的生物有效性,提高植物对酞酸酯的吸收累积及微生物降解能力。Du等[69]研究了高、低PAEs积累水稻品种根系分泌物对土壤PAEs生物有效性和消减的影响,发现培杂泰丰根系分泌物中含有较高含量的有机酸,增加了土壤溶解性有机碳(DOC),提高了DBP和DEHP的解吸作用和生物利用度,促进了酞酸酯在土壤中的消减。曾巧云等[70]研究了不同基因型品种的菜心根系分泌物对水稻土中DEHP解吸作用的影响,发现油青60 d菜心根系分泌物对土壤中DEHP的解吸作用显著大于特青60 d菜心,其根系分泌物更能促进根系吸收DEHP。由此可见,不同基因型作物的根系分泌物对酞酸酯的根际降解存在显著差异,筛选并种植最优的低积累作物品种对酞酸酯的农艺调控修复具有重要意义。
4.2 修复植物轮作植物修复是有机污染土壤修复的经济有效方法之一,主要基于植物及其共存微生物体系清除环境中的污染物[71]。目前关于酞酸酯污染土壤的植物修复报道还较为有限。研究表明,某些水生植物对水体中的酞酸酯去除效果较好,同时具有环境友好性[72]。Dorney等[73]研究发现,酞酸酯在高羊茅中的富集系数较高,能够成为修复酞酸酯污染土壤的模式植物。本研究组前期研究发现,紫花苜蓿对土壤中6种酞酸酯具有较高的去除效率,历经1年修复,其总去除率在90% 以上[74]。魏丽琼等[75]研究也发现,相比于单作,甜菜/苜蓿间作修复效果最好,对酞酸酯的去除率可达66.48%。尽管针对酞酸酯污染土壤修复植物已经开展了一些研究,但可供采用的修复植物品种仍然较少,关于修复植物对土壤中酞酸酯的高效修复机理还不清楚,尚需进一步深入研究。
5 展望农艺措施操作简单,相比于其他修复措施较为经济,可实现污染农田土壤边生产边修复,更适合于大面积污染农田土壤修复,作为强化酞酸酯污染土壤修复的有力手段日益受到研究者的重视。目前关于农艺措施对土壤中酞酸酯消减的调控作用已经开展了一些研究,但对其调控机制研究仍不够深入,缺乏实际农田中可用的农艺措施综合调控技术参数,针对多种酞酸酯复合存在及其与中间代谢产物的复合影响研究还相当有限,建议今后重点加强以下工作:
1) 深入系统揭示农艺措施对土壤中酞酸酯消减的化学–微生物学调控机制。水分调控、温度调控、施用外源添加物和种植制度管理等农艺措施对土壤中酞酸酯的消减均存在两方面的调控作用:酞酸酯的生物有效性和土壤微生物。应从土壤–酞酸酯–土壤微生物三者间关系出发,深入研究农艺措施对土壤中酞酸酯生物有效性的影响,评价农艺措施介导的生物有效性变化对土壤中酞酸酯消减的贡献;采用宏基因组、宏转录组、宏蛋白组和宏代谢组等组学手段系统研究农艺措施对土壤微生物降解酞酸酯的调控机理,综合两方面研究深入系统揭示农艺措施对土壤中酞酸酯消减的化学–微生物学调控作用机制。
2) 建立土壤中酞酸酯消减的农艺措施综合调控技术。土壤中酞酸酯的微生物降解转化过程与机制是调控酞酸酯消减效率的关键,可能会同时受到土壤条件、温度、湿度、含氧量、外源添加物及种植植物等多要素多措施共同影响,多要素多措施协同处理可更有效发挥土著微生物的降解功能,应进一步深入研究多要素多措施(温度、土壤含水率和氧气间歇交换等)对酞酸酯降解效率的协同驱动作用,确定土壤中酞酸酯降解的最佳强化条件,构建基于温度、湿度、外源添加物及种植植物等多种农艺措施的生物高效降解综合调控方法。
3) 充分考虑多种酞酸酯复合污染及其与中间代谢产物复合存在时农艺措施对土壤中酞酸酯消减的调控作用。土壤中酞酸酯种类丰富多样,通常为多种酞酸酯复合共存,但目前国内外大多关注某一种酞酸酯的降解或消减行为,而较少考虑多种酞酸酯共同存在时对彼此消减的复合作用。此外,酞酸酯在土壤中通常与中间代谢产物共存,因此在考虑酞酸酯的消减行为时需更多地考虑中间代谢产物共同存在时对酞酸酯在土壤中消减的影响。
| [1] |
Wang J, Chen G C, Christie P, et al. Occurrence and risk assessment of phthalate esters (PAEs) in vegetables and soils of suburban plastic film greenhouses[J]. Science of the Total Environment, 2015, 523: 129-137 DOI:10.1016/j.scitotenv.2015.02.101 (  0) 0) |
| [2] |
He Y, Wang Q M, He W, et al. The occurrence, composition and partitioning of phthalate esters (PAEs) in the water-suspended particulate matter (SPM) system of Lake Chaohu, China[J]. Science of the Total Environment, 2019, 661: 285-293 DOI:10.1016/j.scitotenv.2019.01.161 (  0) 0) |
| [3] |
Wang X L, Lin Q X, Wang J, et al. Effect of wetland reclamation and tillage conversion on accumulation and distribution of phthalate esters residues in soils[J]. Ecological Engineering, 2013, 51: 10-15 DOI:10.1016/j.ecoleng.2012.12.079 (  0) 0) |
| [4] |
de Moura Carrara S M C, Morita D M, Boscov M E G. Biodegradation of di(2-ethylhexyl)phthalate in a typical tropical soil[J]. Journal of Hazardous Materials, 2011, 197: 40-48 DOI:10.1016/j.jhazmat.2011.09.058 (  0) 0) |
| [5] |
Ren L, Lin Z, Liu H M, et al. Bacteria-mediated phthalic acid esters degradation and related molecular mechanisms[J]. Applied Microbiology and Biotechnology, 2018, 102(3): 1085-1096 DOI:10.1007/s00253-017-8687-5 (  0) 0) |
| [6] |
Huang H, Zhang X Y, Chen T L, et al. Biodegradation of structurally diverse phthalate esters by a newly identified esterase with catalytic activity toward di(2-ethylhexyl) phthalate[J]. Journal of Agricultural and Food Chemistry, 2019, 67(31): 8548-8558 DOI:10.1021/acs.jafc.9b02655 (  0) 0) |
| [7] |
Lü H, Mo C H, Zhao H M, et al. Soil contamination and sources of phthalates and its health risk in China: A review[J]. Environmental Research, 2018, 164: 417-429 DOI:10.1016/j.envres.2018.03.013 (  0) 0) |
| [8] |
Liu S S, Peng Y F, Lin Q T, et al. Di-(2-ethylhexyl) phthalate as a chemical indicator for phthalic acid esters: An investigation into phthalic acid esters in cultivated fields and E-waste dismantling sites[J]. Environmental Toxicology and Chemistry, 2019, 38(5): 1132-1141 DOI:10.1002/etc.4402 (  0) 0) |
| [9] |
Liu X W, Shi J H, Bo T, et al. Occurrence of phthalic acid esters in source waters: A nationwide survey in China during the period of 2009-2012[J]. Environmental Pollution, 2014, 184: 262-270 DOI:10.1016/j.envpol.2013.08.035 (  0) 0) |
| [10] |
Wang Y Y, Zhan W H, Ren Q, et al. Biodegradation of di-(2-ethylhexyl) phthalate by a newly isolated Gordonia sp. and its application in the remediation of contaminated soils[J]. Science of the Total Environment, 2019, 689: 645-651 DOI:10.1016/j.scitotenv.2019.06.459 (  0) 0) |
| [11] |
He L Z, Gielen G, Bolan N S, et al. Contamination and remediation of phthalic acid esters in agricultural soils in China: A review[J]. Agronomy for Sustainable Development, 2015, 35(2): 519-534 DOI:10.1007/s13593-014-0270-1 (  0) 0) |
| [12] |
农艺措施修复重金属污染土壤的研究进展[J]. 农学学报, 2020, 10(8): 38-41 (  0) 0) |
| [13] |
邻苯二甲酸酯在环境中的降解机制[J]. 生态科学, 2015, 34(4): 180-187 (  0) 0) |
| [14] |
Zhu F X, Zhu C Y, Doyle E, et al. Fate of di (2‑ethylhexyl) phthalate in different soils and associated bacterial community changes[J]. Science of the Total Environment, 2018, 637/638: 460-469 DOI:10.1016/j.scitotenv.2018.05.055 (  0) 0) |
| [15] |
Hong S B, Gan P, Chen A P. Environmental controls on soil pH in planted forest and its response to nitrogen deposition[J]. Environmental Research, 2019, 172: 159-165 DOI:10.1016/j.envres.2019.02.020 (  0) 0) |
| [16] |
土壤酞酸酯污染及主要影响因素研究进展[J]. 环境科学与技术, 2019, 42(2): 113-120 (  0) 0) |
| [17] |
Huang J Y, Nkrumah P N, Li Y, et al. Chemical behavior of phthalates under abiotic conditions in landfills[M]// Reviews of Environmental Contamination and Toxicology Volume 224. New York: Springer New York, 2012: 39–52.
(  0) 0) |
| [18] |
温度和水分对有机质及活性炭组分的影响[J]. 中国农业信息, 2016(12): 116-119 (  0) 0) |
| [19] |
土壤中酞酸酯多界面迁移转化与效应研究进展[J]. 浙江大学学报(农业与生命科学版), 2017, 43(6): 700-712 (  0) 0) |
| [20] |
土壤微生物活性和生物量对干湿交替的响应[J]. 土壤与作物, 2020, 9(4): 348-354 (  0) 0) |
| [21] |
Chen N, Fang G D, Zhou D M, et al. Effects of clay minerals on diethyl phthalate degradation in Fenton reactions[J]. Chemosphere, 2016, 165: 52-58 DOI:10.1016/j.chemosphere.2016.09.016 (  0) 0) |
| [22] |
生物炭对烤烟根际土壤微生物群落碳代谢的影响[J]. 中国农业科技导报, 2018, 20(9): 49-56 (  0) 0) |
| [23] |
森林土壤微生物对干旱和氮沉降的响应[J]. 应用生态学报, 2020, 31(7): 2464-2472 (  0) 0) |
| [24] |
Merilä P, Ohtonen R. Soil microbial activity in the coastal Norway spruce [Picea abies (L.) Karst.] forests of the Gulf of Bothnia in relation to humus-layer quality, moisture and soil types[J]. Biology and Fertility of Soils, 1997, 25(4): 361-365 DOI:10.1007/s003740050326 (  0) 0) |
| [25] |
土壤水分含量对石油污染土壤微生物活性的影响[J]. 南昌工程学院学报, 2019, 38(6): 27-32 (  0) 0) |
| [26] |
水分条件对滨海芦苇湿地土壤微生物多样性的影响[J]. 海洋科学, 2017, 41(5): 144-152 (  0) 0) |
| [27] |
酞酸酯类有机毒物在土壤中降解规律的研究[J]. 环境科学学报, 1997, 17(3): 84-89 (  0) 0) |
| [28] |
Zhu F X, Doyle E, Zhu C Y, et al. Metagenomic analysis exploring microbial assemblages and functional genes potentially involved in di (2-ethylhexyl) phthalate degradation in soil[J]. Science of the Total Environment, 2020, 715: 137037 DOI:10.1016/j.scitotenv.2020.137037 (  0) 0) |
| [29] |
Rousk J, Brookes P C, Bååth E. Contrasting soil pH effects on fungal and bacterial growth suggest functional redundancy in carbon mineralization[J]. Applied and Environmental Microbiology, 2009, 75(6): 1589-1596 DOI:10.1128/AEM.02775-08 (  0) 0) |
| [30] |
酞酸酯污染农田土壤生物修复研究进展[J]. 微生物学杂志, 2018, 38(4): 120-128 DOI:10.3969/j.issn.1005-7021.2018.04.017 (  0) 0) |
| [31] |
Liu H, Gao H, Wu M L, et al. Distribution characteristics of bacterial communities and hydrocarbon degradation dynamics during the remediation of petroleum- contaminated soil by enhancing moisture content[J]. Microbial Ecology, 2020, 80(1): 202-211 DOI:10.1007/s00248-019-01476-7 (  0) 0) |
| [32] |
Ouyang Y, Li X Y. Effect of repeated drying-rewetting cycles on soil extracellular enzyme activities and microbial community composition in arid and semi-arid ecosystems[J]. European Journal of Soil Biology, 2020, 98: 103187 DOI:10.1016/j.ejsobi.2020.103187 (  0) 0) |
| [33] |
辽东山区3种人工林土壤呼吸对土壤温度和土壤水分的响应[J]. 辽宁林业科技, 2017(4): 1-4, 19 DOI:10.3969/j.issn.1001-1714.2017.04.001 (  0) 0) |
| [34] |
土壤微生物对增温响应的Meta分析[J]. 农业环境科学学报, 2015, 34(11): 2169-2175 DOI:10.11654/jaes.2015.11.019 (  0) 0) |
| [35] |
增温对南亚热带季风常绿阔叶林土壤微生物群落的影响[J]. 生态环境学报, 2019, 28(5): 881-889 (  0) 0) |
| [36] |
南方红壤丘陵区土壤细菌对土壤水分和温度的响应差异[J]. 热带作物学报, 2019, 40(3): 609-615 (  0) 0) |
| [37] |
邻苯二甲酸二异辛酯(DEHP)对土壤中微生物和动物的影响[J]. 农业环境科学学报, 2004, 23(6): 1156-1159 DOI:10.3321/j.issn:1672-2043.2004.06.029 (  0) 0) |
| [38] |
Amponsah N Y, Wang J Y, Zhao L. Modelling PAH degradation in contaminated soils in Canada using a modified process-based model (DNDC)[J]. Soil Science Society of America Journal, 2019, 83(3): 605-613 DOI:10.2136/sssaj2018.11.0435 (  0) 0) |
| [39] |
酞酸酯类增塑剂对土壤─作物系统的影响[J]. 土壤学报, 1999, 36(1): 118-126 DOI:10.3321/j.issn:0564-3929.1999.01.016 (  0) 0) |
| [40] |
邻苯二甲酸酯类增塑剂水解条件的研究[J]. 包装工程, 2010, 31(13): 42-44, 59 (  0) 0) |
| [41] |
土壤有机质含量与作物产量的相关性[J]. 水土保持应用技术, 2021(1): 20-22 (  0) 0) |
| [42] |
Xiang L, Wang X D, Chen X H, et al. Sorption mechanism, kinetics, and isotherms of di- n-butyl phthalate to different soil particle-size fractions[J]. Journal of Agricultural and Food Chemistry, 2019, 67(17): 4734-4745 DOI:10.1021/acs.jafc.8b06357 (  0) 0) |
| [43] |
Tang J P, Rong X, Jin D C, et al. Biodegradation of phthalate esters in four agricultural soils: Main influencing factors and mechanisms[J]. International Biodeterioration & Biodegradation, 2020, 147: 104867 (  0) 0) |
| [44] |
短期增温对亚高山草甸土壤养分和脲酶的影响[J]. 草业科学, 2018, 35(12): 2794-2800 DOI:10.11829/j.issn.1001-0629.2018-0104 (  0) 0) |
| [45] |
温度对不同年限日光温室土壤氮素矿化特性的影响[J]. 植物营养与肥料学报, 2015, 21(1): 121-127 (  0) 0) |
| [46] |
温度和土壤类型对氮素矿化的影响[J]. 植物营养与肥料学报, 2011, 17(3): 583-591 (  0) 0) |
| [47] |
生物炭制备技术研究进展[J]. 河北农业科学, 2019, 23(5): 95-98 (  0) 0) |
| [48] |
赵仪. 生物炭对邻苯二甲酸酯吸附及迁移性的影响[D]. 北京: 中国地质大学(北京), 2017.
(  0) 0) |
| [49] |
生物炭对土壤理化和微生物性质影响研究进展[J]. 生态科学, 2018, 37(1): 192-199 (  0) 0) |
| [50] |
生物炭施入对农田土壤及作物生长影响的研究进展[J]. 江苏农业科学, 2016, 44(10): 10-15 (  0) 0) |
| [51] |
施用生物炭对旱作农田土壤有机碳、氮及其组分的影响[J]. 农业环境科学学报, 2015, 34(3): 509-517 (  0) 0) |
| [52] |
Yao S, Li X N, Cheng H, et al. Resource utilization of a typical vegetable waste as biochars in removing phthalate acid esters from water: A sorption case study[J]. Bioresource Technology, 2019, 293: 122081 DOI:10.1016/j.biortech.2019.122081 (  0) 0) |
| [53] |
Jing F Q, Sohi S P, Liu Y Y, et al. Insight into mechanism of aged biochar for adsorption of PAEs: Reciprocal effects of ageing and coexisting Cd2+[J]. Environmental Pollution, 2018, 242: 1098-1107 DOI:10.1016/j.envpol.2018.07.124 (  0) 0) |
| [54] |
生物炭对邻苯二甲酸二甲酯在土壤中自然降解和吸附行为的影响[J]. 环境工程学报, 2014, 8(10): 4474-4479 (  0) 0) |
| [55] |
老化过程对生物质炭吸附-解吸附邻苯二甲酸二乙酯的影响[J]. 环境科学学报, 2015, 35(12): 4012-4020 (  0) 0) |
| [56] |
Zhang X K, He L Z, Sarmah A K, et al. Retention and release of diethyl phthalate in biochar-amended vegetable garden soils[J]. Journal of Soils and Sediments, 2014, 14(11): 1790-1799 DOI:10.1007/s11368-014-0929-x (  0) 0) |
| [57] |
He L Z, Fan S L, Müller K, et al. Biochar reduces the bioavailability of di-(2-ethylhexyl) phthalate in soil[J]. Chemosphere, 2016, 142: 24-27 DOI:10.1016/j.chemosphere.2015.05.064 (  0) 0) |
| [58] |
秸秆生物质炭对菜田土壤微生物、理化性质及青菜生长的影响[J]. 上海农业学报, 2017, 33(4): 48-54 (  0) 0) |
| [59] |
生物炭对设施退化土壤氮相关功能微生物群落丰度的影响[J]. 土壤学报, 2013, 50(3): 624-631 (  0) 0) |
| [60] |
有机肥对土壤理化性质的影响[J]. 农业与技术, 2010, 30(3): 65-66 DOI:10.3969/j.issn.1671-962X.2010.03.018 (  0) 0) |
| [61] |
有机肥替代化肥对小麦产量及土壤养分和酶活性的影响[J]. 长江大学学报(自然科学版), 2019, 16(5): 46–52, 7–8 DOI:10.3969/j.issn.1673-1409.2019.05.011 (  0) 0) |
| [62] |
施肥影响土壤性状和微生物组的研究进展[J]. 生物技术通报, 2019, 35(9): 21-28 (  0) 0) |
| [63] |
生物有机肥对酞酸酯污染农田土壤的微生物效应研究[J]. 安徽农业科学, 2011, 39(35): 21715-21716, 21830 DOI:10.3969/j.issn.0517-6611.2011.35.060 (  0) 0) |
| [64] |
Zhao H M, Du H, Feng N X, et al. Biodegradation of di-n-butylphthalate and phthalic acid by a novel Providencia sp 2D and its stimulation in a compost- amended soil[J]. Biology and Fertility of Soils, 2016, 52(1): 65-76 DOI:10.1007/s00374-015-1054-8 (  0) 0) |
| [65] |
He L Z, Fan S L, Müller K, et al. Comparative analysis biochar and compost-induced degradation of di-(2- ethylhexyl) phthalate in soils[J]. Science of the Total Environment, 2018, 625: 987-993 DOI:10.1016/j.scitotenv.2018.01.002 (  0) 0) |
| [66] |
Cai Q Y, Xiao P Y, Chen T, et al. Genotypic variation in the uptake, accumulation, and translocation of di-(2-ethylhexyl) phthalate by twenty cultivars of rice (Oryza sativa L.)[J]. Ecotoxicology and Environmental Safety, 2015, 116: 50-58 DOI:10.1016/j.ecoenv.2015.02.038 (  0) 0) |
| [67] |
邻苯二甲酸酯在不同品种通菜-土壤系统中的累积效应研究[J]. 应用生态学报, 2004, 15(8): 1455-1458 DOI:10.3321/j.issn:1001-9332.2004.08.031 (  0) 0) |
| [68] |
Li Y W, Cai Q Y, Mo C H, et al. Plant uptake and enhanced dissipation of di(2-ethylhexyl) phthalate (DEHP) in spiked soils by different plant species[J]. International Journal of Phytoremediation, 2014, 16(6): 609-620 DOI:10.1080/15226514.2013.803021 (  0) 0) |
| [69] |
Du P P, Huang Y H, Lü H, et al. Rice root exudates enhance desorption and bioavailability of phthalic acid esters (PAEs) in soil associating with cultivar variation in PAE accumulation[J]. Environmental Research, 2020, 186: 109611 DOI:10.1016/j.envres.2020.109611 (  0) 0) |
| [70] |
2种基因型菜心根系分泌物对水稻土中DEHP解吸效应的初步研究[J]. 农业环境科学学报, 2010, 29(8): 1466-1470 (  0) 0) |
| [71] |
土壤有机污染植物修复的机理与影响因素[J]. 应用生态学报, 2003, 14(10): 1799-1803 DOI:10.3321/j.issn:1001-9332.2003.10.047 (  0) 0) |
| [72] |
Cai Q Y, Mo C H, Zeng Q Y, et al. Potential of Ipomoea aquatica cultivars in phytoremediation of soils contaminated with di-n-butyl phthalate[J]. Environmental and Experimental Botany, 2008, 62(3): 205-211 DOI:10.1016/j.envexpbot.2007.08.005 (  0) 0) |
| [73] |
Dorney J R, Weber J B, Overcash M R, et al. Plant uptake and soil retention of phthalic acid applied to Norfolk sandy loam[J]. Journal of Agricultural and Food Chemistry, 1985, 33(3): 398-403 DOI:10.1021/jf00063a019 (  0) 0) |
| [74] |
Ma T T, Teng Y, Luo Y M, et al. Legume-grass intercropping phytoremediation of phthalic acid esters in soil near an electronic waste recycling site: A field study[J]. International Journal of Phytoremediation, 2013, 15(2): 154-167 DOI:10.1080/15226514.2012.687016 (  0) 0) |
| [75] |
甜菜-牧草体系对土壤中4种邻苯二甲酸酯的修复研究[J]. 农业环境科学学报, 2016, 35(6): 1097-1102 (  0) 0) |
2. Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2022, Vol. 54
2022, Vol. 54


