2. 污染场地安全修复技术国家工程实验室, 北京 100015;
3. 中国科学院南京土壤研究所, 南京 210008
由自然或人为活动引起的有机物质不完全燃烧而产生的多环芳烃(PAHs)是一类持久性有机污染物,这类化合物在环境中广泛存在,且具有生物富集性与“三致”效应[1-2]。PAHs在大气和水环境中可以进行长距离输送,以大气沉降、污水灌溉及污泥农用等方式累积在农田土壤中[2-3]。污染土壤中PAHs可通过根系被植物吸收,并在植物体内迁移累积,随着食物链进入人体,对人类健康构成极大威胁[4]。因此,降低土壤中PAHs的生物有效性,实现PAHs在土壤中的有效固定对于土壤健康和食品安全至关重要[5]。
黏土矿物因具有巨大的比表面积和丰富的可交换阳离子容量,具有良好的吸附潜力,同时其具有良好的分散性、环境友好性和经济适用性,因而被广泛应用于水体及土壤的污染修复中[6-7]。为了增加黏土矿物对疏水性有机污染物的亲和力和吸附效果[8],许多学者(如刘香玉等[9]、朱利中等[10]、Ake等[11])通过对黏土矿物进行有机改性增大了黏土矿物层间距并增强了其表面的疏水性,大大增加了对水中有机污染物的吸附能力[10, 12]。然而,目前关于有机黏土对有机污染物吸附固定的研究多数集中于废水处理领域[13],而有机黏土修复PAHs污染土壤却鲜有研究,尚不清楚有机改性黏土对土壤中PAHs的固定及其阻控效果。
根据本实验室前期研究[14],十六烷基三甲基溴化铵改性蒙脱土(CTAB-SMF)和3-巯基丙基三甲氧基硅烷改性蒙脱土(TMSP-SMF)对萘具有良好的吸附效果。基于此,本研究将选用TMSP-SMF和CTAB- SMF作为PAHs污染农田土壤的改良剂,探究有机黏土在实际污染土壤中固定及阻控PAHs的效果。试验以苋菜为供试农作物,菲和芘为PAHs的代表污染物,通过盆栽试验,研究了:①有机黏土的添加对土壤性质的影响;②苋菜体内及土壤中PAHs的含量变化;③有机黏土的添加对PAHs污染土壤种植的植物生长和氧化胁迫的影响,以进一步探讨有机黏土在PAHs污染土壤中施用的可行性,评价其作为土壤改良剂对土壤性质以及植物的影响,为PAHs污染农田修复提供科学数据和参考。
1 材料与方法 1.1 供试土壤供试土壤为采自南京市紫金山表层的干净土壤。其基本理化性质为pH 7.10,有机质含量10.2 g/kg,黏粒、粉粒和砂粒含量分别为144 g/kg、721 g/kg和135 g/kg,土壤类型为黄棕壤。
已有调查显示,我国表层土壤中的PAHs含量中位值达0.52 mg/kg[15]。因此本试验中,将供试土壤风干磨细(20目),用菲和芘的丙酮溶液污染后,充分搅拌均匀,老化90 d,期间每7 d混合搅拌,使得土壤初始菲含量为0.58 mg/kg,芘含量为0.50 mg/kg。
1.2 实验试剂与实验仪器菲、蒽、荧蒽和芘标准物质均购自阿拉丁试剂有限公司;十六烷基三甲基溴化铵(CTAB,99%)购自Biosharp;3-巯基丙基三甲氧基硅烷(TMSP,95%)购自Sigma Aldrich;蒙脱土(SMF)购自浙江丰虹粘土化工有限公司;丙酮、二氯甲烷、正己烷(色谱纯)购自德国默克股份有限公司;苋菜种子购自南京金盛达种子有限公司;植物酶试剂盒购自南京建成生物工程研究所;精制型层析硅胶(200 ~ 300目)购自青岛海洋化工有限公司;浓硫酸(分析纯)购自南京化工试剂股份有限公司。
实验所用仪器如下:岛津气相色谱–质谱联用仪(GCMS-QP 2010 Plus,岛津日本)、加速溶剂萃取仪(ASE 350,戴安中国有限公司)、旋转蒸发仪(R-100,瑞士布琦有限公司)、真空冷冻干燥器(1-2 LD plus,德国克里斯公司)、高速分散器(XHF-D,宁波新芝生物科技股份有限公司)、酶标仪(Sunrise RC TS TC,奥地利Tecan公司)、土壤渗透性测定仪(TST-55型,常州德杜精密仪器有限公司)、离心机(CT15RT,上海天美科学仪器有限公司)、pH计(MT-5000,上海三本环保科技有限公司)。
1.3 盆栽试验根据文献报道,当有机黏土添加量为1% ~ 4% 时,其对植物生长的影响可忽略不计[16]。因此,本研究选择有机黏土添加量为2.5% 进行后续盆栽试验。每盆装污染土2.0 kg,与有机黏土充分搅拌均匀后浇水,使土壤保持田间持水量的65%。污染土和有机黏土老化一个星期之后播种,等到种子出苗后长到2片真叶时,间苗,每盆留苗5株。在苋菜生长期间,每两天浇一次水,使盆栽土壤保持田间持水量的65%。盆栽试验设置4个处理,每个处理5次重复,试验设计如表 1所示。播种后45 d进行土样和植物样的采集。
|
|
表 1 苋菜盆栽试验设计 Table 1 Pot experimental design of Amaranthus tricolor L. |
土壤pH测定采用电位法(HJ962—2018)[17],土水质量比为1∶2.5;土壤的渗透系数(KT)按照变水头试验法测定,计算公式如下:
| $ {K_T} = 2.3\frac{{aL}}{{A({t_1} - {t_2})}}\lg \frac{{{H_1}}}{{{H_2}}} $ | (1) |
式中:2.3为ln和lg的变换因数;a为测压管面积,cm2;L为试样高度,cm;A为试样段面积,cm2;t1和t2分别为测读水头的起始和终止时间,s;H1和H2分别为起始和终止水头,cm。
1.4.2 土壤微生物指标测定微生物高通量测序委托派诺森基因云进行分析。利用实时荧光定量PCR,16S rDNA基因的扩增引物为F:ACTCCTACGGGAGGCAGCA,R:TCGGACTACHVGGGTWTCTAAT。借助QIIME2(2019.4)测序平台研究土壤微生物群落组成,并在门水平上分析与比较不同处理间土壤细菌群落组成的变化。
1.4.3 植物光合色素测定称取0.01 g新鲜的苋菜叶片,用5 ml 80% 丙酮提取叶绿素a、叶绿素b和类胡萝卜素,并于离心机3 000 r/min离心10 min,用分光光度计分别在663、646、470 nm处测量提取液的吸光度,通过下列公式计算各光合色素的含量[18]:
| $ [叶绿素 {\rm{a}}]=(12.21×A_{663}) – (2.59×A_{646}) $ | (2) |
| $ [叶绿素 {\rm{b}}]=(20.13×A_{646}) – (5.03×A_{663}) $ | (3) |
| $ [类胡萝卜素]=(1 000×A_{470} – 3.27×[叶绿素 {\rm{a}}] – \\ 104×[叶绿素 {\rm{b}}])/229 $ | (4) |
植物和土壤中PAHs通过加速溶剂提取,提取液经固相萃取柱净化,旋转蒸发仪浓缩后于气相色谱–质谱联用仪进行测定。具体操作如下:植物和土壤样品真空冷冻干燥过夜,准确称取0.5 g土壤样品或0.1 g植物样品,与3.0 g硅藻土和0.2 ml的5 mg/L内标(蒽、荧蒽)搅拌均匀,放入加速溶剂萃取仪(ASE)萃取池中提取植物与土壤样品中PAHs。提取条件:系统压力为10.5 MPa,萃取温度为100℃,加热时间5 min,静态时间5 min,冲洗体积为萃取池体积的60%,循环1次,吹扫60 s。提取液在36℃下旋转浓缩,用提取溶剂定容至2 ml。土壤提取溶剂为正己烷/二氯甲烷(4∶1,V/V)混合溶液,植物提取溶剂为正己烷/二氯甲烷(1∶1,V/V)混合溶液。固相萃取(SPE)柱,其从下至上填充物依次是:0.5 g无水硫酸钠、1.0 g改性磺化硅胶、1.0 g无水硫酸钠,上下均填有玻璃纤维滤膜。提取液加到固相萃取柱上后进行淋洗。首先用5 ml正己烷对SPE柱活化,再用5 ml二氯甲烷淋洗,弃去淋洗液,然后用15 ml提取溶剂进行洗脱,收集洗脱液并将其旋转蒸发浓缩,最后用提取溶剂定容至1 ml,用气相色谱–质谱联用仪进行分析。
气相色谱–质谱联用仪分析条件:SH-Rxi- 5SiL MS (30 m×0.25 mm×0.25 μm)色谱柱,250℃进口温度,不分流进样;1 min进样时间,1.00 ml/min柱流量。程序升温如下:初始温度60℃,以10℃/min升至260℃并保持1 min,再以15℃/min升至300℃并保持3 min。质谱条件离子源:电子轰击离子源,200℃离子源温度,250℃接口温度,离子扫描(SIM)模式。
在本试验该提取方法中,蒽和荧蒽作为菲和芘的内标在植物样品中的回收率为76.4% ~ 100.5% 和88.9% ~ 110.4%,在土壤样品中的回收率为88.4% ~ 104.0% 和83.3% ~ 111.1%。
1.4.5 植物酶活性测定称取新鲜苋菜根部分用于测定植物酶活性,分别通过过氧化物酶(POD)、总超氧化物歧化酶(SOD)、丙二醛(MDA)、多酚氧化酶(PPO)试剂盒提取,采用酶标仪测定。
1.4.6 植物生物量(鲜重)的测定测定苋菜的鲜重时,先将其清洗干净,然后擦干根和叶表面的水分,选取每个处理中6株苋菜用精度0.001 g的电子天平测定。
1.5 数据处理及统计分析在本研究中,所有结果均以均值±标准差表示。采用SAS 9.3软件Duncan法进行方差分析,P < 0.05为判断显著差异的标准。
2 结果与讨论 2.1 有机黏土对土壤理化性质的影响本研究各处理之间土壤样品pH没有显著变化(P > 0.05),但由于添加了有机黏土使得土壤渗透性稍有改变。其中2.5% 的TMSP-SMF添加,使土壤渗透系数从8.41×10–5 cm/s减少为6.99×10–5 cm/s,但与控制处理相比差异不显著;而2.5% 的CTAB-SMF添加显著降低了土壤的渗透性,渗透系数改变为6.46×10–5 cm/s。这与王红等[19]研究相符,外源添加有机蒙脱土可能会对土壤的物理化学性质造成影响。Al-Shayea等[20]研究表明,低黏粒含量的砂土渗透系数显著大于高黏粒含量的砂土。因此TMSP-SMF和CTAB-SMF的添加增加了土壤的黏粒含量,能够提高土壤对水分的吸持能力、土壤紧实度和粘结性[21],提高土壤保肥保水能力。
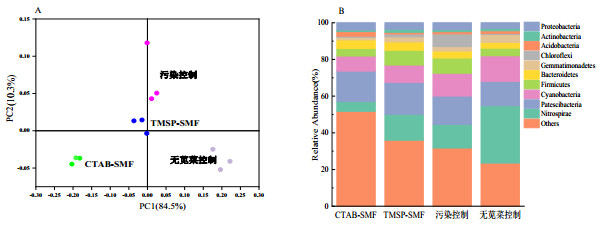
2.2 有机黏土对土壤细菌门相对丰度的影响如图 1A所示,有机黏土的添加导致盆栽土壤中微生物群落沿第一主成分(解释度84.5%)发生明显的变化。在门水平上(图 1B),所有处理中的细菌群落主要是变形菌门(Proteobacteria)、放线菌门(Actinomycetes)、酸杆菌门(Acidobacteria)、绿弯菌门(Chloroflexi)、芽单胞菌门(Gemmatimonadetes)、拟杆菌门(Bacteroides)、蓝藻菌门(Cyanobacteria)、厚壁菌门(Firmicutes)、髌骨细菌门(Patescibacteria)和硝化螺旋菌门(Nitrospirae),占微生物总数的98%。在这些菌群中最主要的是变形菌门,其次是放线菌、酸杆菌门和绿弯菌门。Geng等[22]研究表明,变形菌门、酸杆菌门和厚壁菌门是烃类污染土壤的主要细菌类群,在PAHs污染土壤中存在富集现象。并且大多数参与PAHs代谢和遗传调控的降解菌也属于这几个细菌门[23]。
|
图 1 CTAB-SMF和TMSP-SMF对土壤微生物群落结构(A)及细菌菌门相对丰度(B)的影响 Fig. 1 Effects of CTAB-SMF and TMSP-SMF on microbial community structure (A) and microbial phylum (B) |
CTAB-SMF和TMSP-SMF的使用未明显影响土壤中各细菌菌门的种类,但特定功能菌门的相对丰度发生了显著的变化。例如,CTAB-SMF增加了变形菌门的相对丰度(38.65% ± 2.72%)和酸杆菌门的相对丰度(6.50% ± 20.16%);TMSP-SMF增加了变形菌门的相对丰度(11.70% ± 5.29%)和酸杆菌门的相对丰度(11.71% ± 14.06%)。而这些优势菌群均与PAHs的降解有关,CTAB-SMF和TMSP-SMF对变形菌门和酸杆菌门相对丰度的提高可能是因为其增加了PAHs降解微生物栖息地,而且有机改性黏土还可以通过交换H+来为微生物提供最佳的酸碱条件,从而促进微生物的生长[24-25]。其中,有机黏土对有机污染物的解吸行为以及吸附在有机黏土表面和层间的PAHs如何被土壤微生物利用还需进一步研究。
2.3 有机黏土对苋菜生理特性的影响在苋菜盆栽45 d后,CTAB-SMF和TMSP-SMF处理苋菜生物量(鲜重)分别为42.54 g/株和40.80g/株,与污染控制处理(45.20 g/株)和无污染控制处理(47.59 g/株)相比并没有显著差异(P > 0.05)。
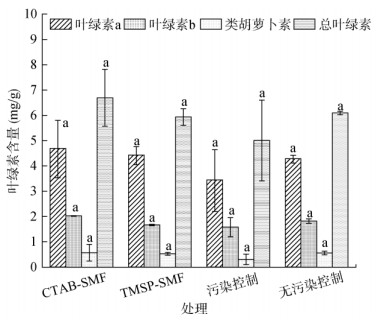
如图 2所示,各处理叶绿素含量没有显著差异(P > 0.05),但污染控制处理苋菜叶绿素a和总叶绿素相比于无污染控制处理减少了19.7% ± 2.9% 和17.8% ± 0.9%。这是由于植物在受到有机污染物胁迫时,有机污染物会破坏植物体内的叶绿素合成酶或者激活叶绿素降解酶,导致叶绿素含量下降[26]。而添加TMSP-SMF和CTAB-SMF能使叶绿素a和总叶绿素含量有所增加,这可能是因为TMSP-SMF和CTAB-SMF减少了苋菜体内PAHs的积累,从而导致苋菜体内氧化胁迫减弱。
|
(图中不同小写字母表示同一指标不同处理间差异显著(P < 0.05),下同) 图 2 不同处理下盆栽苋菜的叶绿素含量 Fig. 2 Chlorophyll contents of Amaranthus tricolor L. under different treatments |
如图 3A所示,与污染控制处理相比,TMSP-SMF和CTAB-SMF处理可有效降低苋菜根部菲和芘的累积,菲含量分别降低了16.7% ± 6.6% 和59.1% ± 4.7%,芘含量分别降低了21.2% ± 13.3% 和60.0% ± 8.1%。所有处理中苋菜根部菲和芘含量的差异,可能是由于在土壤老化过程中土壤对芘和菲吸附作用不一致导致的。另外,土壤中不同PAHs的生物可利用性取决于其疏水性,菲的lgKow=4.57,芘的lgKow= 5.18[27],因此芘和菲在苋菜体内的累积和迁移不同。本试验中,污染物主要来自根部和叶片吸收,由于苋菜体内的PAHs易从根部迁移到叶片,因此所有处理中苋菜地上部菲和芘的含量显著高于地下部(P < 0.05)。同样地,TMSP-SMF和CTAB-SMF处理中苋菜地上部菲和芘的含量比污染控制处理有显著的降低(P < 0.05)(图 3B),菲分别降低了20.1% ± 9.5% 和47.0% ± 8.7%,芘分别降低了13.9% ± 16.9% 和44.3% ± 7.0%。

|
图 3 不同处理下苋菜根部(A)及地上部分(B)PAHs的含量 Fig. 3 Concentrations of PAHs in Amaranthus tricolor L. shoots (A) and roots (B) under different treatments |
以上结果说明,TMSP-SMF和CTAB-SMF可以有效地阻控污染土壤中菲和芘进入植物体内,减弱了苋菜对土壤中菲和芘的吸收与累积,从而降低了菲和芘对苋菜的胁迫,这也解释了CTAB-SMF和TMSP- SMF处理苋菜叶绿素含量高于污染控制处理的原因。另外,相较TMSP-SMF,CTAB-SMF具有更好的阻控效果。
2.5 有机黏土对土壤中PAHs含量的影响如图 4所示,污染控制处理PAHs含量与无苋菜控制处理对比有显著降低(P < 0.05),一方面由于植物对菲和芘的吸收,另一方面大量根际微生物的存在对有机污染物有降解作用,导致土壤中菲和芘的含量降低。在TMSP-SMF和CTAB-SMF处理土壤中菲和芘含量均略高于污染控制处理(P > 0.05)。这是由于TMSP-SMF表面和CTAB-SMF层间存在的有机相有利于PAHs的吸附[28]。同时,TMSP-SMF和CTAB- SMF在环境中具有良好的稳定性,其有机改性剂再释放以及污染物脱附可忽略不计[29]。因此,TMSP- SMF和CTAB-SMF能够有效地固定土壤中的菲和芘,使得盆栽土壤中菲和芘的消散受到抑制,移动性变弱,从而降低其生物有效性。而污染控制处理土壤中PAHs更容易被植物累积,出现自然挥发及浇水淋溶等损失[30]。这与刘总堂等[16]的研究结果相似,其研究表明添加1% ~ 8% 有机改性黏土可固定土壤中50.4% ~ 78.5% 的六六六。

|
图 4 不同处理下盆栽土样菲和芘的含量 Fig. 4 Concentrations of PAHs in soils under different treatments |
图 3、图 4显示CATB-SMF在土壤中固定及阻控PAHs的效果更好,这与TMSP-SMF和CTAB-SMF在水相中对PAHs的吸附效果相符。这可能是因为:① CTAB-SMF具有更高的疏水性。本课题前期通过观察TMSP-SMF和CTAB-SMF在耗散型石英晶体微天平上的黏土膜形成时间来研究其疏水性大小,结果表明,3种黏土的疏水性大小依次为CTAB-SMF > TMSP-SMF > SMF[14];②与TMSP-SMF相比,CTAB-SMF可以提供更多的吸附位点,包括黏土颗粒表面位点以及黏土层间的CTAB基团。
2.6 有机黏土对PAHs胁迫下植物氧化应激反应的影响在PAHs污染胁迫下,植物体内的氧化代谢动态平衡被打破,植物体内会产生大量的活性氧自由基。这些自由基若不能及时被清除,则引起植物氧化应激反应,进而可能产生脂质过氧化酶失活等毒理效应[31]。植物体内的抗氧化系统中酶促系统(例如POD、SOD、MDA和PPO)能清除机体内活性氧自由基,快速将O2–· 转化为H2O2[32],维持体内活性氧自由基产生和猝灭的动态平衡,从而阻控脂质过氧化进程[33]。因此,在本研究测定POD、SOD、MDA和PPO活性来评价苋菜在不同处理中菲和芘引起氧化胁迫毒害的程度。
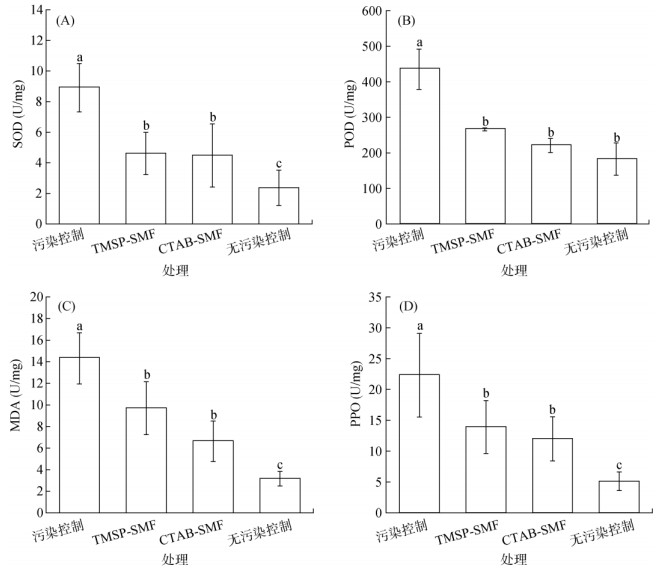
如图 5A所示,污染控制处理苋菜在PAHs的胁迫下SOD活性显著增加(P < 0.05),而TMSP-SMF和CTAB-SMF处理苋菜的SOD活性基本恢复。SOD催化产生的H2O2需要经POD进一步催化分解,因此,POD活性变化应与SOD相对应[34]。有研究表明,在低剂量PAHs暴露下植物体内的POD活性随PAHs浓度的增加而增加[35]。在本研究中(图 5B),TMSP-SMF和CTAB-SMF处理苋菜POD活性较污染控制处理下降了38.86% ± 10.78% 和49.27% ± 23.85%,这与SOD活性变化趋势相符。同时,本研究也检测了MDA指标(图 5C)。MDA是生物膜系统脂质过氧化的产物,其活性变化不仅可以反映O2–· 生成的量及氧化反应强烈程度,还可以反映细胞受损伤和对逆境的反应程度[36]。如图 5C所示,污染控制处理苋菜与无污染控制处理相比,MDA活性显著升高(P < 0.05);但TMSP-SMF和CTAB-SMF处理苋菜MDA活性较污染控制处理分别显著下降了32.31% ± 14.36%、53.60% ± 11.45%(P < 0.05)。MDA活性越大,生物膜系统受损程度越大[37]。本研究MDA活性检测结果表明,TMSP-SMF和CTAB-SMF处理苋菜的细胞膜结构损伤程度相比污染控制处理较轻,其中CTAB-SMF处理效果更明显。
|
图 5 不同处理下苋菜根部SOD(A)、POD(B)、MDA(C)、PPO(D)的活性 Fig. 5 Activities of POD (A), SOD (B), MDA (C) and PPO (D) in Amaranthus tricolor L. roots under different treatments |
植物受到PAHs胁迫时,体内PPO活性增强,促进植物体内PAHs降解[38]。与污染控制处理相比,TMSP-SMF和CTAB-SMF处理苋菜体内PPO活性分别降低了37.64% ± 19.22%、46.26% ± 16.02%(图 5D),推测可能是由于有机黏土固定了土壤中PAHs,导致植物体内PAHs含量相对较少,从而减轻了PAHs对植物的毒害。
3 结论在PAHs污染土壤中,TMSP-SMF和CTAB-SMF的添加有效地将菲和芘固定在土壤中,能在一定程度上阻控其进入植物体内,并降低其对植物氧化胁迫。两种有机黏土的施用未改变土壤的pH,但使土壤的渗透性分别降低了18.39% ± 2.28% 和24.62% ± 1.26%,从而提高了土壤保水保肥的能力。TMSP-SMF和CTAB-SMF增加了土壤中变形菌门及放线菌门的相对丰度,对微生物降解PAHs起到了正面作用。TMSP-SMF和CTAB-SMF可作为一种PAHs污染农田的修复剂,有效阻控农产品中有机污染物的积累,其中CTAB-SMF对土壤中菲和芘的固定效果更佳,更适用于PAHs污染农田的原位修复。
| [1] |
Sun Z Y, Wang X H, Liu C, et al. Persistent free radicals from low-molecular-weight organic compounds enhance cross-coupling reactions and toxicity of anthracene on amorphous silica surfaces under light[J]. Environmental Science & Technology, 2021, 55(6): 3716-3726 (  0) 0) |
| [2] |
Włóka D, Placek A, Rorat A, et al. The evaluation of polycyclic aromatic hydrocarbons (PAHs) biodegradation kinetics in soil amended with organic fertilizers and bulking agents[J]. Ecotoxicology and Environmental Safety, 2017, 145: 161-168 DOI:10.1016/j.ecoenv.2017.07.021 (  0) 0) |
| [3] |
Usman M, Hanna K, Haderlein S. Fenton oxidation to remediate PAHs in contaminated soils: A critical review of major limitations and counter-strategies[J]. Science of the Total Environment, 2016, 569/570: 179-190 DOI:10.1016/j.scitotenv.2016.06.135 (  0) 0) |
| [4] |
Ni N, Kong D Y, Wu W Z, et al. The role of biochar in reducing the bioavailability and migration of persistent organic pollutants in soil-plant systems: A review[J]. Bulletin of Environmental Contamination and Toxicology, 2020, 104(2): 157-165 DOI:10.1007/s00128-019-02779-8 (  0) 0) |
| [5] |
徐远远, 朱利中. 溴化十四烷基吡啶对黑麦草吸收土壤中菲的影响[J]. 环境科学学报, 2008, 28(4): 738-741 DOI:10.3321/j.issn:0253-2468.2008.04.020 (  0) 0) |
| [6] |
García-Romero E, Lorenzo A, García-Vicente A, et al. On the structural formula of smectites: A review and new data on the influence of exchangeable cations[J]. Journal of Applied Crystallography, 2021, 54(Pt 1): 251-262 (  0) 0) |
| [7] |
Aboudi Mana S C, Hanafiah M M, Chowdhury A J K. Environmental characteristics of clay and clay-based minerals[J]. Geology, Ecology, and Landscapes, 2017, 1(3): 155-161 DOI:10.1080/24749508.2017.1361128 (  0) 0) |
| [8] |
Sarkar B, Xi Y F, Megharaj M, et al. Bioreactive organoclay: A new technology for environmental remediation[J]. Critical Reviews in Environmental Science and Technology, 2012, 42(5): 435-488 DOI:10.1080/10643389.2010.518524 (  0) 0) |
| [9] |
刘香玉, 孙娟, 赵朝成, 等. CTAB改性膨润土制备及其对海洋溢油的吸附性能[J]. 环境工程学报, 2019, 13(1): 68-78 (  0) 0) |
| [10] |
朱利中, 任晓刚, 俞绍斌, 等. CTMAB-膨润土去除水中有机物的性能及机理[J]. 中国环境科学, 1998, 18(5): 450-454 DOI:10.3321/j.issn:1000-6923.1998.05.018 (  0) 0) |
| [11] |
Ake C L, Wiles M C, Huebner H J, et al. Porous organoclay composite for the sorption of polycyclic aromatic hydrocarbons and pentachlorophenol from groundwater[J]. Chemosphere, 2003, 51(9): 835-844 DOI:10.1016/S0045-6535(03)00040-7 (  0) 0) |
| [12] |
柴琴琴, 呼世斌, 刘建伟, 等. 有机改性凹凸棒石对养猪废水中有机物的吸附研究[J]. 环境科学学报, 2016, 36(5): 1672-1682 (  0) 0) |
| [13] |
Zhu R L, Chen Q Z, Zhou Q, et al. Adsorbents based on montmorillonite for contaminant removal from water: A review[J]. Applied Clay Science, 2016, 123: 239-258 (  0) 0) |
| [14] |
侯静雯, 施维林, 高娟. 有机改性蒙脱土对萘的吸附机制和影响因子[J]. 环境科学, 2020, 41(11): 5133-5142 (  0) 0) |
| [15] |
Wang C H, Wu S H, Zhou S L, et al. Polycyclic aromatic hydrocarbons in soils from urban to rural areas in Nanjing: Concentration, source, spatial distribution, and potential human health risk[J]. Science of the Total Environment, 2015, 527/528: 375-383 DOI:10.1016/j.scitotenv.2015.05.025 (  0) 0) |
| [16] |
刘总堂, 许敏, 林云青, 等. 有机黏土对污染土中HCH的固定及黑麦草生长的影响[J]. 中国环境科学, 2010, 30(4): 533-538 (  0) 0) |
| [17] |
生态环境部. 土壤pH值的测定电位法: HJ 962—2018[S]. 北京: 中国环境科学出版社, 2018.
(  0) 0) |
| [18] |
Zhao L J, Hu Q R, Huang Y X, et al. Response at genetic, metabolic, and physiological levels of maize (Zea mays) exposed to a Cu(OH)2 nanopesticide[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(9): 8294-8301 (  0) 0) |
| [19] |
王红, 张淑辉, 彭福田, 等. 不同土壤改良剂对土壤理化性质、微生物及桃植株生长的影响[J]. 山东农业科学, 2020, 52(12): 59-65, 70 (  0) 0) |
| [20] |
Al-Shayea N A. The combined effect of clay and moisture content on the behavior of remolded unsaturated soils[J]. Engineering Geology, 2001, 62(4): 319-342 DOI:10.1016/S0013-7952(01)00032-1 (  0) 0) |
| [21] |
张继义, 赵哈林. 退化沙质草地恢复过程土壤颗粒组成变化对土壤-植被系统稳定性的影响[J]. 生态环境学报, 2009, 18(4): 1395-1401 (  0) 0) |
| [22] |
Geng S Y, Cao W, Yuan J, et al. Microbial diversity and co-occurrence patterns in deep soils contaminated by polycyclic aromatic hydrocarbons (PAHs)[J]. Ecotoxicology and Environmental Safety, 2020, 203: 110931 (  0) 0) |
| [23] |
王荔, 张腾飞, 杨苏才, 等. 焦化厂PAHs污染土壤中微生物群落多样性特征[J]. 环境工程技术学报, 2021, 11(4): 720-726 (  0) 0) |
| [24] |
Timmer N, Gore D, Sanders D, et al. Application of seven different clay types in sorbent-modified biodegradability studies with cationic biocides[J]. Chemosphere, 2020, 245: 125643 (  0) 0) |
| [25] |
Chaerun S K, Tazaki K, Okuno M. Montmorillonite mitigates the toxic effect of heavy oil on hydrocarbon- degrading bacterial growth: Implications for marine oil spill bioremediation[J]. Clay Minerals, 2013, 48(4): 639-654 (  0) 0) |
| [26] |
Shen Y, Li J F, Gu R C, et al. Phenanthrene-triggered Chlorosis is caused by elevated Chlorophyll degradation and leaf moisture[J]. Environmental Pollution, 2017, 220: 1311-1321 (  0) 0) |
| [27] |
Wang W W, Qu X L, Lin D H, et al. Octanol-water partition coefficient (logKow) dependent movement and time lagging of polycyclic aromatic hydrocarbons (PAHs) from emission sources to lake sediments: A case study of Taihu Lake, China[J]. Environmental Pollution, 2021, 288: 117709 (  0) 0) |
| [28] |
朱利中, 陈宝梁, 陶澍. 溴化十四烷基吡啶增强固定土壤中萘及其机理[J]. 中国环境科学, 2003, 23(1): 43-47 (  0) 0) |
| [29] |
Yaron-Marcovich D, Nir S, Chen Y. Fluridone adsorption-desorption on organo-clays[J]. Applied Clay Science, 2004, 24(3/4): 167-175 (  0) 0) |
| [30] |
许敏, 靳伟, 林云青, 等. 纳米有机二氧化硅对土壤-青菜系统六六六迁移的影响[J]. 安徽农业科学, 2009, 37(5): 2167-2169 (  0) 0) |
| [31] |
Winston G W. Oxidants and antioxidants in aquatic animals[J]. Comparative Biochemistry and Physiology Part C: Comparative Pharmacology, 1991, 100(1/2): 173-176 (  0) 0) |
| [32] |
Ma C X, White J C, Dhankher O P, et al. Metal-based nanotoxicity and detoxification pathways in higher plants[J]. Environmental Science & Technology, 2015, 49(12): 7109-7122 (  0) 0) |
| [33] |
Zhang P, Guo Z L, Luo W H, et al. Graphene oxide- induced pH alteration, iron overload, and subsequent oxidative damage in rice (Oryza sativa L.): A new mechanism of nanomaterial phytotoxicity[J]. Environmental Science & Technology, 2020, 54(6): 3181-3190 (  0) 0) |
| [34] |
黄磊, 陈玉成, 赵亚琦, 等. 生物炭添加对湿地植物生长及氧化应激响应的影响[J]. 环境科学, 2018, 39(6): 2904-2910 (  0) 0) |
| [35] |
卢晓丹. 多环芳烃污染对植物酶活性的影响研究[D]. 南京: 南京农业大学, 2009.
(  0) 0) |
| [36] |
Liu C F, Xiao R B, Dai W J, et al. Cadmium accumulation and physiological response of Amaranthus tricolor L. under soil and atmospheric stresses[J]. Environmental Science and Pollution Research, 2021, 28(11): 14041-14053 (  0) 0) |
| [37] |
杜志伟, 杨肖松, 刘月仙, 等. 有机污染物芘胁迫下白菜生理特性变化规律[J]. 生态学报, 2021, 41(3): 998-1005 (  0) 0) |
| [38] |
Moradi B, Kissen R, Maivan H Z, et al. Assessment of oxidative stress response genes in Avicennia marina exposed to oil contamination - Polyphenol oxidase (PPOA) as a biomarker[J]. Biotechnology Reports, 2020, 28: e00565 (  0) 0) |
2. National Engineering Laboratory for Safe Remediation Technology of Contaminated Sites, Beijing 100015, China;
3. Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2022, Vol. 54
2022, Vol. 54


