砷是一种典型的毒性较强的环境污染物,其已成为全球尤其是东南亚地区面临的重大环境问题之一。土壤砷经稻谷积累进入食物链对人类健康构成潜在威胁[1]。我国是一个砷污染相对严重的国家,一些工矿企业附近农田砷含量更高。例如,中国莲花山钨矿附近水稻籽粒砷含量高达1.0 mg/kg,高出我国食品安全国家标准5倍(砷≤0.2 mg/kg,GB 2762—2017)[2]。Lei等[3]对湖南省34个水稻品种籽粒砷含量(0.26 ~ 0.52 mg/kg)的测定结果表明,如果以这些水稻为主食,成人每天砷的摄入量为0.10 ~ 0.21 mg,超过了世界卫生组织建议的每日砷摄入量。人体的砷摄入过量易导致各种癌症,如膀胱癌、肺癌和肝癌等,严重威胁了人类健康[4]。水稻是全球3亿人的主食,它比其他谷物农作物更容易从土壤中积累砷,水稻是人体砷暴露的主要来源,所以减少砷在稻谷中的积累对生活在砷污染地区的以稻米为主食的人们身体健康至关重要[5]。减少水稻砷积累的策略非常重要,尤其是在砷污染土壤中,主要包括:添加土壤改良剂[6]、水分管理[7]和叶面喷施[8]等方法。利用化学物质减少作物砷积累,是粮食安全生产中切实可行的方法。其中,叶面喷施硅或硒被认为是缓解作物砷积累的有效途径[8-9]。
水稻是典型的嗜硅作物,硅对水稻生长发育起着非常重要的作用。由于亚热带地区土壤的严重风化、淋溶、脱硅和团聚体化,中国南方水稻土中的植物有效硅含量不足[10]。研究表明,土壤施硅(20 g/kg)可显著降低水稻糙米砷含量[11]。由于硅施入土壤易被固定,黄崇玲等[12]发现与土壤施硅相比,叶面喷施硅溶胶降低水稻镉含量的能力更强。最近,Zhang等[8]的试验结果表明,与对照相比,叶面喷施硅溶液显著降低了20.3% 的稻米砷含量。此外,还有研究显示,叶面喷施低浓度硅(硅: 砷=100:1)可降低砷在水稻幼苗体内的浓度和转运[13]。因此,叶面喷施硅溶液可为砷污染稻田土壤治理提供新的策略。Wu等[14]进行了6种不同基因型水稻施硅试验,发现提高植物体硅含量并不能降低所有水稻品种砷含量,也就是说硅对水稻积累砷效应存在品种差异。到目前为止,尽管有许多研究表明外源硅能降低水稻砷积累,但是叶面喷施硅溶液是如何影响不同品种水稻砷积累,目前还没有相关的报道。
硒是人和动物必需的营养元素,硒对人体抗氧化、抗癌和抗衰老等多方面起着非常重要的作用[15]。然而,我国约51% 的土地缺乏硒,缺硒的省份多达22个,导致39% ~ 61% 的居民每日膳食硒摄入量低于WHO/FAO推荐的硒营养摄入量[16]。研究表明,叶面喷施硒可以显著增加水稻籽粒硒含量[17];并且叶面喷硒可降低水稻砷、镉和汞等多种重金属的积累,提高水稻抗逆性[18-19]。徐向华等[9]的研究表明,叶面喷施硒溶液能显著降低19.0%稻米砷含量。然而,徐琴等[20]研究表明,大田喷施复合硒叶面肥对水稻精米和糙米中砷含量没有显著影响。最新的一项研究表明,叶面喷施低浓度硒(1.0 mg/L)能有效降低水稻茎和叶中砷含量,但高浓度(5.0 mg/L)则没有显著作用[21]。尽管许多研究表明,外源硒能减轻水稻砷积累和砷毒性,但仍然缺少硒对降低水稻砷积累的作用机理研究。因此,对水稻进行叶面喷施硒,不仅满足了我国居民日常的硒摄入量,同时降低水稻砷积累,起到了“补硒降砷”的作用。
虽然有许多研究评估了叶面喷施硅和硒对水稻砷积累的调节作用[8-9],但叶面喷施硅和硒对砷污染土壤上种植水稻的光合作用的影响机制以及对不同水稻品种砷累积差异尚不清楚,这限制了人们在生产实践中选择和应用适合的降低水稻砷积累方法。为此,本试验以3个籽粒砷积累量不同的水稻品种为试验材料,研究3种叶面喷施处理对水稻砷积累和光合参数的影响,以期阐明叶面喷施硅、硒降低水稻砷积累的机理,为生产实践中有效降低水稻砷积累提供新的应用策略。
1 材料与方法 1.1 供试材料供试土壤为采自中国重庆北碚区水稻土(0 ~ 20 cm),自然风干1个月,过4 mm筛,充分混匀,用于盆栽试验。再取部分水稻土,放于温室内,自然风干2个月,过0.84 mm筛,充分混匀后,存放于黑暗处,用于测定试验前土壤基础理化性质。试验前土壤基本理化性质:pH,5.6;全氮,2.12 g/kg;有效氮,126.7 mg/kg;全磷,0.93 g/kg;有效磷,15.67 mg/kg;速效钾,132.5 mg/kg;有机质,23.2 mg/kg;全硒,0.23 mg/kg;有效硅,151.3 mg/kg;全砷,2.36 mg/kg。
试验所用外源砷由亚砷酸钠(NaAsO2)提供。根据GB 15618—2018《中国环境质量标准》 (砷: 30 mg/kg),本试验加入的砷浓度为35 mg/kg。试验加入的氮、磷和钾肥分别为:N 200 mg/kg,由CO(NH2)2提供;P 35 mg/kg,由CaHPO4·2H2O提供;K 70.5 mg/kg,由K2SO4提供。本试验为盆栽试验,每盆装土9 kg。将土壤与基肥和砷混合均匀后装盆,淹水4周,之后取部分塑料盆中的土,自然风干,用于砷的测定,然后将水稻幼苗移栽进每个盆中。
1.2 试验设计水稻幼苗培育的方法参照文献[22],待水稻幼苗适宜移栽时,选取长势相似的幼苗,于2019年5月1日移栽至装好土的塑料盆中,每盆移栽3株。将移栽后的水稻,置于温室(室温:16 ~ 38 ℃,相对湿度:60% ~ 70%),自然光照射,培育140 d。
选择3个籽粒砷积累能力不同的水稻进行研究:籽粒砷积累能力相对较低的水稻品种旌1优华珍和C两优华占,籽粒砷积累能力相对较高的水稻品种丰优香占,均为籼型杂交水稻。3种叶面肥溶液成分和对照处理见表 1,每个处理设置3个重复。研究表明,在拔节期或分蘖期施用叶面肥更有利于抑制砷的转运[8]。因此,我们在水稻的分蘖期(2019年6月1日)和抽穗期(2019年7月1日)喷施叶面肥。
|
|
表 1 叶面肥成分与粒径 Table 1 Compositions and particle sizes of foliage fertilizers |
采用Liu等[23]所述方法制备硒和硅溶液。叶面喷施硅硒混合溶液的制备:在制备2.5 mmol/L硅溶液的过程中,加入40 mg亚硒酸钠,最后定容至1 L。每个处理(3盆)叶面喷施量为200 ml,并于喷施前加入2 ml表面活性剂(吐温80),并且在喷施前用塑料袋将栽种水稻的塑料盆表面罩住,避免在喷施的过程中液体溅入盆中。用动态光散射法(BT-90)测量了硅、硒和硅硒混合溶液中的粒径分布,结果见表 1。
1.3 光合参数的测定在抽穗期施用叶面肥大约7 d后,选取晴朗天气(2019年7月9日),于上午9: 30—11: 30进行光合参数的测定。本次试验使用CI-340手持便携式光合作用测定仪进行光合参数的测定。测定时每盆水稻随机选取3片叶子,并在剑叶的相同位置进行测定,以自然光源提供光合有效辐射,进气CO2浓度约为200 mg/L,测定项目包括光合速率、气孔导度、胞间CO2浓度和蒸腾速率。
1.4 样品的收集和处理水稻成熟时(2019年9月18日),收获水稻,并将水稻分成根、茎、叶和籽粒。把籽粒最外层的壳去掉,得到糙米。水稻根部用柠檬酸二亚硫酸氢钠(DCB)溶液去除根表铁膜。最后用去离子水把水稻样品冲洗干净,放进65 ℃的烘箱烘72 h(DHG-9240A)。样品烘干、称重后,研磨机磨碎,装进聚乙烯自封袋中,用于砷的测定。
砷的测定采用混合酸溶液(HNO3: HClO4=4:1)消煮法[24],同时取与消煮样品相同量的混合酸按同一方法作空白试验。用AF-610A原子荧光光谱仪测定总砷,同时对空白和标准物质进行了测定。其中植物标准物质(GBWO7602(GSV-1))购于中国标准物质中心。
1.5 数据分析砷从土壤到地上部分的转运系数(TF)和生物富集系数(BCF)计算公式如下:
| $ \text{TF}_{根到茎}=C_{茎}/C_{根}×100\% $ | (1) |
| $ \text{TF}_{茎到叶}=C_{叶}/C_{茎}×100\% $ | (2) |
| $ \text{TF}_{茎到糙米}=C_{糙米}/C_{茎}×100\% $ | (3) |
| $ \text{BCF}_{糙米}=C_{糙米}/C_{土壤} $ | (4) |
式中:C根、C茎、C叶、C糙米和C土壤分别代表根、茎、叶、糙米和土壤中的砷含量(mg/kg,以干物质量计)。所有的数据用SPSS 22.0和Excel 2007进行处理,用Origin 8.0作图。所有的数据进行邓肯单因素方差分析(ANOVA)。
2 结果 2.1 叶面喷施硅、硒和硅硒混合液对水稻各组织砷积累的影响从图 1可知,3种水稻吸收积累砷能力不同,表现为:丰优香占>C两优华占>旌1优华珍,对照组的组间差异性检验结果表明,3种水稻间总砷含量有显著性差异(P < 0.05)。

|
(图中小写字母不同表示同一水稻品种不同处理间差异达显著水平(P < 0.05,n = 3)) 图 1 叶面喷施硅、硒和硅硒混合液对不同品种水稻根(A)、茎叶(B)、糙米(C)和整株水稻(D)砷积累的影响 Fig. 1 Effects of foliage spraying Si, Se and Si+Se on As accumulation in roots (A), shoots (B), brown rice (C) and whole rice plants (D) of different rice varieties |
对于旌1优华珍来说,与对照相比,叶面喷施硅溶液使其根、茎叶和糙米砷含量都显著降低,分别降低了9.9%、17.9% 和26.4%(P < 0.05);对于C两优华占来说,与对照相比,叶面喷施硅溶液使其茎叶和糙米砷含量显著降低,分别降低了16.7% 和21.1% (P < 0.05)。叶面喷施硒溶液和硅硒混合溶液对旌1优华珍和C两优华占各组织砷含量没有显著影响,但能降低它们的砷含量。对于丰优香占来说,虽然叶面喷施处理对其各部分砷含量没有显著影响,但对各部分砷含量的降低有一定积极作用。综上,叶面喷施硅溶液对于降低水稻砷含量的效果要好于喷施硒或硒硅溶液,并且叶面单独喷施硅与对照相比,显著降低了籽粒砷含量相对较低的两个水稻品种的籽粒砷含量。
2.2 叶面喷施硅、硒和硅硒混合液对水稻生物量、砷转运系数和生物富集系数的影响由表 2可知,与对照相比,叶面喷施硅溶液能显著提高C两优华占茎叶生物量,提高了5.9% (P < 0.05);其他叶面喷施处理对水稻根、茎叶和糙米生物量均无显著影响,但从总体来看,与对照相比,叶面喷施处理有提高3种水稻生物量的趋势。在对照组中,组间差异性检验结果表明,3种水稻间生物量有显著差异(P < 0.05)。
|
|
表 2 叶面喷施硅、硒和硅硒混合液对不同品种水稻组织生物量的影响 Table 2 Effects of foliage spraying Si, Se and Si+Se on tissue biomass of different rice varieties |
由表 3可知,在对照组中,与其他两种水稻相比,旌1优华珍有最高的TF根到茎以及最低的TF茎到糙米、TF叶到糙米和BCF糙米;C两优华占的砷转运和积累能力居中;丰优香占有最低的TF根到茎,以及最高的TF茎到糙米、TF茎到叶和BCF糙米。在旌1优华珍中,与对照相比,3种叶面喷施处理对TF根到茎、TF茎到糙米和BCF糙米无显著影响,然而,叶面喷施硒溶液,使其TF茎到叶显著增加了9.0%(P < 0.05)。在C两优华占中,与对照相比,3种叶面喷施处理对其TF茎到糙米和BCF糙米无显著影响,然而,叶面喷施硅溶液,使其TF根到茎显著降低了12.7%,叶面喷施硅硒混合溶液,使其TF茎到叶显著增加了9.6%(P < 0.05)。在丰优香占中,与对照相比,3种叶面喷施处理对其TF根到茎、TF茎到糙米和BCF糙米无显著影响,然而,叶面喷施硅溶液、硒溶液和硅硒混合溶液都能显著增加其TF茎到叶,分别增加了11.3%、9.6% 和8.3%(P < 0.05)。
|
|
表 3 叶面喷施硅、硒和硅硒混合液对不同品种水稻砷转运系数(TF)和生物富集系数(BCF)的影响 Table 3 Effects of foliage spraying Si, Se and Si+Se on As transfer factors (TF) and bioaccumulation factors (BCF) of different rice varieties |
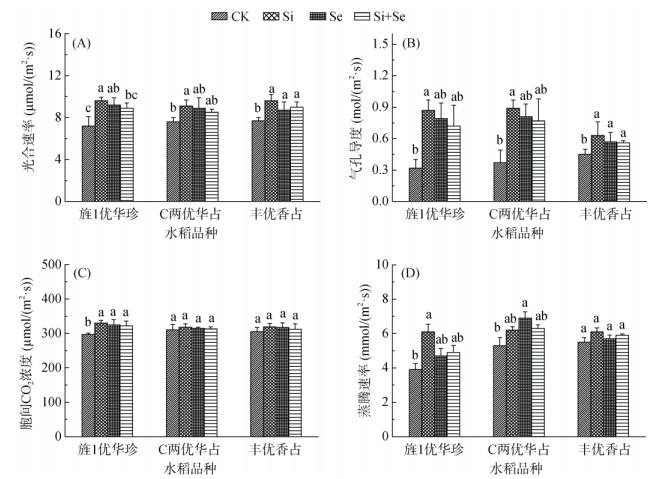
叶面喷施硅、硒和硅硒混合液使3种水稻的光合参数都呈现增加趋势(图 2)。在对照组中,组间差异性检验结果表明,3种水稻品种同一光合参数间的差异不显著。总体来看,3种叶面喷施处理增加水稻光合参数的能力大小顺序为:硅溶液>硒溶液>硅硒混合溶液。在旌1优华珍中,与对照相比,叶面喷施硅溶液使其光合速率、气孔导度、胞间CO2浓度和蒸腾速率分别显著增加了33.3%、171.8%、11.1% 和56.4%(P < 0.05);叶面喷施硒溶液使其光合速率和胞间CO2浓度分别显著增加了27.2% 和9.4%(P < 0.05);叶面喷施硅硒混合溶液使其胞间CO2浓度显著增加了8.4%(P < 0.05)。在C两优华占中,与对照相比,叶面喷施硅溶液,使其光合速率和气孔导度分别显著增加了19.7% 和140.5%(P < 0.05);叶面喷施硒溶液,使其蒸腾速率显著增加了30.1%(P < 0.05);叶面喷施硅硒混合溶液虽然使其光合参数增加,但无显著影响。在丰优香占中,与对照相比,叶面喷施硅、硒和硅硒混合液都能显著增加其光合速率和气孔导度(P < 0.05);3种叶面喷施处理虽然能增加其、胞间CO2浓度和蒸腾速率,但差异未达到显著水平。
|
图 2 叶面喷施硅、硒和硅硒混合液对不同品种水稻光合速率(A)、气孔导度(B)、胞间CO2浓度(C)和蒸腾速率(D)的影响。 Fig. 2 Effects of foliage spraying Si, Se and Si+Se on photosynthetic rates (A), stomatal conductance (B), intercellular CO2 concentrations (C) and transpiration rates (D) of different rice varieties. |
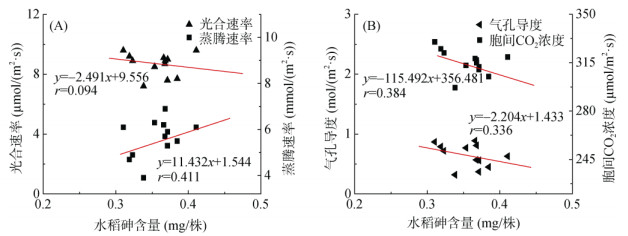
整株水稻砷含量与光合参数两者间相关性如图 3所示,结果表明,水稻砷含量与光合参数无显著相关;光合速率、气孔导度和胞间CO2浓度与水稻砷含量呈负相关,这说明,水稻砷含量与光合参数关系密切。
|
图 3 水稻砷含量与光合参数的线性关系 Fig. 3 Relationship between photosynthetic parameters and As concentration in rice |
3种水稻吸收积累砷能力不同,表现为:丰优香占>C两优华占>旌1优华珍,从对照组组间差异性检验结果来看,3种水稻间总砷含量有显著性差异(P < 0.05),这说明水稻基因型对水稻砷含量有显著影响。其原因可能有以下两点:一方面,不同品种水稻生长发育程度不同,对照组的组间差异性检验结果表明,不同品种水稻间生长发育有显著差异,对照组中3种水稻生物量不同,其大小顺序为:旌1优华珍>C两优华占>丰优香占(表 2),生物稀释作用可能是导致不同品种水稻总砷含量差异的原因;另一方面,不同品种水稻其砷的转运能力不同,在对照组中,旌1优华珍有最高的TF根到茎以及最低的TF茎到糙米,丰优香占有最低的TF根到茎以及最高的TF茎到糙米(表 3),说明对于旌1优华珍来说,与其他两个水稻品种相比,砷在转运的过程中,较多地固定在其茎中,因此其籽粒砷含量是供试水稻品种中最低的(图 1)。Li等[25]的研究也表明,不同基因型水稻,其根系、木质部和韧皮部发育程度以及转运砷的能力不同。总之,以上结果说明了籽粒砷含量相对较低的水稻品种更多比例的砷固定在茎中,从而导致其稻米砷积累能力较弱。这与Bhattacharya等[26]的研究结果一致,籽粒砷含量相对较低的水稻品种砷从根到茎的转运能力也相对较强,这个现象是否具有普遍性还需进一步探索。
叶面喷施硅处理对于降低水稻籽粒砷含量的效果要好于喷施硒或硒硅溶液,叶面喷施硅可显著降低旌1优华珍和C两优华占水稻籽粒砷含量,但没有显著降低丰优香占籽粒砷含量(图 1),这说明叶面喷施硅降低水稻籽粒砷含量存在基因型差异。叶面喷施硅溶液使旌1优华珍和C两优华占糙米砷含量分别从0.341 2 mg/kg下降到0.251 2 mg/kg,以及从0.432 1 mg/kg下降到0.341 1 mg/kg,虽然没有达到国家食品安全标准(砷 < 0.2 mg/kg),但叶面喷施硅溶液显著降低两品种水稻籽粒砷含量。Zhang等人[8]的研究也表明,叶面喷施1 mmol/L的硅溶液能显著降低稻米砷含量。叶面喷施的硅被水稻吸收后,会形成硅双层,以及促进水稻内外胚层凯氏带的形成[27]。硅双层和凯氏带可能抑制了水稻对砷的吸收和转运。同时,叶面喷施硅溶液还可能增加了水稻细胞壁的果胶含量,提高了其负电位,增加了砷与水稻茎和叶细胞壁结合的比例,降低了砷向籽粒的转运,进而降低籽粒砷的含量[28]。另一方面,叶面施硅还可能显著降低水稻根部(Lsi1和Lsi2)和叶鞘(Lsi6)砷吸收转运相关基因表达[8],从而降低水稻籽粒砷的积累。
适量的硒对植物生长是有益的。试验结果表明,与对照相比,叶面喷施硒溶液使旌1优华珍、C两优华占和丰优香占糙米砷含量分别下降20.5%、9.2% 和12.9%。与以前的研究结果相似[9]。从总体来看,叶面喷施硒溶液降低水稻砷含量的效果低于叶面喷施硅溶液,但高于叶面喷施硅硒混合溶液(图 1)。这可能是由于外源硒可以诱导和促进细胞壁栓质的形成,这有助于抑制重金属向木质部及地上部分转运[29]。砷可与谷胱甘肽(GSH)或植物螯合素(PCs)螯合,固定在根细胞的液泡中,硒能增加谷胱甘肽过氧化酶(GSH-Px)和谷胱甘肽(GSH)的活性,从而降低了砷向地上部的转运[30]。
叶面单喷施硅或硒对水稻籽粒砷含量降低效果强于叶面喷施硅硒混合溶液(图 1)。究其原因,可能是不同喷施溶液的粒径不同造成的,喷施溶液粒径越小,水稻叶面越容易吸收,混合溶液的平均粒径要显著高于单喷硅或硒溶液(表 1)。Cui等[31]研究表明较小粒径的SiO2颗粒对水稻吸收Cd2+有较强的抑制作用。本研究中不同粒径的硅和硒溶液对水稻砷吸收的影响,可能存在类似机理,这需要进一步验证。然而,也有研究指出,与单独喷施硅和单独喷施硒相比,叶面喷施1% 硒掺杂的硅硒混合溶液(粒径35.4 nm)降低糙米砷含量的效果最好[9],造成上述研究结果不同的原因可能是叶面喷施溶液粒子的粒径不同。因此,在以后的生产实践中,应尽量选择粒径较小的溶质粒子进行叶面喷施,以便取得较好的降砷效果。
3.2 叶面喷施硅和硒对不同品种水稻光合作用的影响在对照组中,组间差异性检验结果表明,3种水稻品种同一光合参数间的差异不显著,说明其差别主要由喷施不同溶液引起的。我们的研究和以往的研究均证明,砷处理降低了水稻的生长和光合作用[32]。叶面喷施硅、硒和硅硒混合液均可减轻砷对植物光合作用的影响。从总体来看,3种叶面喷施处理提高水稻光合参数的能力大小顺序为:硅溶液 > 硒溶液 > 硅硒混合溶液,并且本文也得出,光合参数(如光合速率、气孔导度、胞间CO2浓度)与水稻籽粒砷浓度呈负相关关系(图 3)。那么,叶面喷施硅或硒对水稻叶片光合参数的影响差异可能是造成籽粒砷含量差异的重要原因。以往的研究也证明,外源硅或硒均能减轻砷对植物光合作用的影响[18],本研究结果与此一致。Sanglard等[33]报道,外源硅可通过调节某些基因(如OsABCC1基因)的表达来缓解砷胁迫对植物的光合损伤,提高植物光合速率。外源硒和硅还能通过修复受损的叶绿体,提高叶绿素含量,抑制活性氧的过量产生,从而提高光合效率[34-35]。最近的一项研究表明,硒还能提高砷胁迫下与光合作用相关的醛缩酶、RuBisCo小亚基和叶绿素A-b结合蛋白等蛋白质的表达和增加光合色素[36],从而提高水稻光合参数。总之,叶面喷施硅或硒对水稻光合参数的影响可能与某些基因(OsABCC1基因)的表达、光合作用相关酶和光合色素量有关。
从水稻不同品种来看,叶面喷施硅或硒对籽粒砷含量相对较低的两个水稻品种的光合参数的提高程度要高于籽粒砷含量相对较低的水稻品种,也就是说,不同水稻品种叶片光合参数对外源硅或硒的敏感度或响应度不同。Ding等[21]人也发现了这一有趣的现象,这意味着不同植物也许对硅或硒有不同的耐受性或敏感性,综上,叶面喷施适量的硅或硒有助于降低水稻籽粒砷含量,但在生产实践中,要注意植物品种间的差异,研究结果可为砷污染地区的水稻生产提供参考。
4 结论3种叶面喷施处理相比较而言,以叶面喷施硅对降低水稻籽粒砷含量效果最好,优于叶面喷施硒和硅硒混合液处理。叶面喷施硅处理与对照相比,显著降低了籽粒砷含量相对较低的两个水稻品种的籽粒砷含量,但对籽粒砷含量相对较高的水稻品种则没有显著影响。
3种叶面喷施处理与对照相比均提高了水稻光合参数(如光合速率、气孔导度、胞间CO2浓度),光合参数与水稻砷含量呈负相关,叶面喷施硅或硒对水稻叶片光合参数的影响差异可能是造成籽粒砷含量差异的重要原因,但不同水稻品种叶片光合参数对外源硅或硒的敏感度或响应度不同。总之,叶面喷施硅溶液是减少水稻籽粒砷含量一项经济有效的措施,在生产实践中,要注意植物品种间的差异。
| [1] |
Zhao F J, McGrath S P, Meharg A A. Arsenic as a food chain contaminant: Mechanisms of plant uptake and metabolism and mitigation strategies[J]. Annual Review of Plant Biology, 2010, 61: 535-559 DOI:10.1146/annurev-arplant-042809-112152 (  0) 0) |
| [2] |
Yu H Y, Ding X D, Li F B, et al. The availabilities of arsenic and cadmium in rice paddy fields from a mining area: The role of soil extractable and plant silicon[J]. Environmental Pollution, 2016, 215: 258-265 DOI:10.1016/j.envpol.2016.04.008 (  0) 0) |
| [3] |
Lei M, Tie B Q, Zeng M, et al. An arsenic-contaminated field trial to assess the uptake and translocation of arsenic by genotypes of rice[J]. Environmental Geochemistry and Health, 2013, 35(3): 379-390 DOI:10.1007/s10653-012-9501-z (  0) 0) |
| [4] |
Farnese F S, Oliveira J A, Farnese M S, et al. Uptake arsenic by plants: Effects on mineral nutrition, growth and antioxidant capacity[J]. Idesia (Arica), 2014, 32(1): 99-106 DOI:10.4067/S0718-34292014000100012 (  0) 0) |
| [5] |
Su Y H, McGrath S P, Zhao F J. Rice is more efficient in arsenite uptake and translocation than wheat and barley[J]. Plant and Soil, 2010, 328(1/2): 27-34 (  0) 0) |
| [6] |
Yu H Y, Li F B, Liu C S, et al. Iron redox cycling coupled to transformation and immobilization of heavy metals: Implications for paddy rice safety in the red soil of South China[J]. Advances in Agronomy, 2016, 137: 279-317 (  0) 0) |
| [7] |
Wan Y N, Camara A Y, Huang Q Q, et al. Arsenic uptake and accumulation in rice (Oryza sativa L.) with selenite fertilization and water management[J]. Ecotoxicology and Environmental Safety, 2018, 156: 67-74 DOI:10.1016/j.ecoenv.2018.02.074 (  0) 0) |
| [8] |
Zhang S J, Geng L P, Fan L M, et al. Spraying silicon to decrease inorganic arsenic accumulation in rice grain from arsenic-contaminated paddy soil[J]. Science of the Total Environment, 2020, 704: 135239 DOI:10.1016/j.scitotenv.2019.135239 (  0) 0) |
| [9] |
叶面喷施硒硅复合溶胶抑制水稻砷积累效应研究[J]. 生态环境学报, 2014, 23(6): 1064-1069 DOI:10.3969/j.issn.1674-5906.2014.06.025 (  0) 0) |
| [10] |
Klotzbücher T, Marxen A, Vetterlein D, et al. Plant-available silicon in paddy soils as a key factor for sustainable rice production in Southeast Asia[J]. Basic and Applied Ecology, 2015, 16(8): 665-673 DOI:10.1016/j.baae.2014.08.002 (  0) 0) |
| [11] |
Li G, Zheng M Z, Tang J F, et al. Effect of silicon on arsenic concentration and speciation in different rice tissues[J]. Pedosphere, 2018, 28(3): 511-520 DOI:10.1016/S1002-0160(17)60409-0 (  0) 0) |
| [12] |
土施和喷施硅肥对镉污染农田水稻不同部位镉含量及富集的影响[J]. 西南农业学报, 2013, 26(4): 1532-1535 DOI:10.3969/j.issn.1001-4829.2013.04.048 (  0) 0) |
| [13] |
Liu W J, Sun Y, Zhao Q L. Effects of foliar application of silicon on uptake and translocation of arsenite and DMA in rice (Oryza sativa)[M]//Environmental Arsenic in a Changing World. Leiden, Netherlands: : CRC Press, 2019: 297–298.
(  0) 0) |
| [14] |
Wu C, Zou Q, Xue S G, et al. Effects of silicon (Si) on arsenic (As) accumulation and speciation in rice (Oryza sativa L.) genotypes with different radial oxygen loss (ROL)[J]. Chemosphere, 2015, 138: 447-453 DOI:10.1016/j.chemosphere.2015.06.081 (  0) 0) |
| [15] |
Zhang H, Feng X B, Zhu J M, et al. Selenium in soil inhibits mercury uptake and translocation in rice (Oryza sativa L.)[J]. Environmental Science & Technology, 2012, 46(18): 10040-10046 (  0) 0) |
| [16] |
Dinh Q T, Cui Z W, Huang J, et al. Selenium distribution in the Chinese environment and its relationship with human health: A review[J]. Environment International, 2018, 112: 294-309 DOI:10.1016/j.envint.2017.12.035 (  0) 0) |
| [17] |
不同施硒方式对水稻硒利用效率的影响[J]. 土壤学报, 2019, 56(1): 186-194 (  0) 0) |
| [18] |
Liao G J, Xu Y, Chen C, et al. Root application of selenite can simultaneously reduce arsenic and cadmium accumulation and maintain grain yields, but show negative effects on the grain quality of paddy rice[J]. Journal of Environmental Management, 2016, 183: 733-741 DOI:10.1016/j.jenvman.2016.09.031 (  0) 0) |
| [19] |
Camara A Y, Wan Y N, Yu Y, et al. Effect of endogenous selenium on arsenic uptake and antioxidative enzymes in as-exposed rice seedlings[J]. International Journal of Environmental Research and Public Health, 2019, 16(18): E3350 DOI:10.3390/ijerph16183350 (  0) 0) |
| [20] |
施硒对水稻外观品质及籽粒硒、镉和砷含量的影响[J]. 中国农业科技导报, 2019, 21(5): 135-140 (  0) 0) |
| [21] |
Ding Y Z, Di X R, Norton G J, et al. Selenite foliar application alleviates arsenic uptake, accumulation, migration and increases photosynthesis of different upland rice varieties[J]. International Journal of Environmental Research and Public Health, 2020, 17(10): 3621 DOI:10.3390/ijerph17103621 (  0) 0) |
| [22] |
Zhou X B. The role of selenium in soil: Effect on the uptake and translocation of arsenic in rice (Oryza sativa)[J]. International Journal of Agriculture and Biology, 2017, 19(5): 1227-1234 DOI:10.17957/IJAB/15.0430 (  0) 0) |
| [23] |
Liu C P, Li F B, Luo C L, et al. Foliar application of two silica sols reduced cadmium accumulation in rice grains[J]. Journal of Hazardous Materials, 2009, 161(2/3): 1466-1472 (  0) 0) |
| [24] |
土壤和植物中总砷、无机砷及有机砷的测定方法[J]. 农村生态环境, 1990, 6(2): 57-60 (  0) 0) |
| [25] |
Li R Y, Zhou Z G, Xu X H, et al. Effects of silicon application on uptake of arsenic and phosphorus and formation of iron plaque in rice seedlings grown in an arsenic-contaminated soil[J]. Bulletin of Environmental Contamination and Toxicology, 2019, 103(1): 133-139 DOI:10.1007/s00128-019-02552-x (  0) 0) |
| [26] |
Bhattacharya P, Samal A C, Majumdar J, et al. Accumulation of arsenic and its distribution in rice plant (Oryza sativa L.) in Gangetic West Bengal, India[J]. Paddy and Water Environment, 2010, 8(1): 63-70 DOI:10.1007/s10333-009-0180-z (  0) 0) |
| [27] |
Mitani N, Ma J F, Iwashita T. Identification of the silicon form in xylem Sap of rice (Oryza sativa L.)[J]. Plant and Cell Physiology, 2005, 46(2): 279-283 DOI:10.1093/pcp/pci018 (  0) 0) |
| [28] |
Cui J H, Li Y D, Jin Q, et al. Silica nanoparticles inhibit arsenic uptake into rice suspension cells via improving pectin synthesis and the mechanical force of the cell wall[J]. Environmental Science: Nano, 2020, 7(1): 162-171 DOI:10.1039/C9EN01035A (  0) 0) |
| [29] |
Wang X, Tam N F Y, Fu S, et al. Selenium addition alters mercury uptake, bioavailability in the rhizosphere and root anatomy of rice (Oryza sativa)[J]. Annals of Botany, 2014, 114(2): 271-278 DOI:10.1093/aob/mcu117 (  0) 0) |
| [30] |
Yin H Q, Qi Z Y, Li M Q, et al. Selenium forms and methods of application differentially modulate plant growth, photosynthesis, stress tolerance, selenium content and speciation in Oryza sativa L[J]. Ecotoxicology and Environmental Safety, 2019, 169: 911-917 DOI:10.1016/j.ecoenv.2018.11.080 (  0) 0) |
| [31] |
Cui J H, Liu T X, Li F B, et al. Silica nanoparticles alleviate cadmium toxicity in rice cells: Mechanisms and size effects[J]. Environmental Pollution, 2017, 228: 363-369 DOI:10.1016/j.envpol.2017.05.014 (  0) 0) |
| [32] |
无机砷对不同水稻品种种子萌发和幼苗光合生理的影响[J]. 农业环境科学学报, 2014, 33(6): 1067-1074 (  0) 0) |
| [33] |
Sanglard L M V P, Detmann K C, Martins S C V, et al. The role of silicon in metabolic acclimation of rice plants challenged with arsenic[J]. Environmental and Experimental Botany, 2016, 123: 22-36 DOI:10.1016/j.envexpbot.2015.11.004 (  0) 0) |
| [34] |
Zhong Y, Chen T F, Zheng W J, et al. Selenium enhances antioxidant activity and photosynthesis in Ulva fasciata[J]. Journal of Applied Phycology, 2015, 27(1): 555-562 DOI:10.1007/s10811-014-0350-2 (  0) 0) |
| [35] |
Vaculík M, Pavlovič A, Lux A. Silicon alleviates cadmium toxicity by enhanced photosynthetic rate and modified bundle sheath's cell chloroplasts ultrastructure in maize[J]. Ecotoxicology and Environmental Safety, 2015, 120: 66-73 DOI:10.1016/j.ecoenv.2015.05.026 (  0) 0) |
| [36] |
Chauhan R, Awasthi S, Indoliya Y, et al. Transcriptome and proteome analyses reveal selenium mediated amelioration of arsenic toxicity in rice (Oryza sativa L.)[J]. Journal of Hazardous Materials, 2020, 390: 122122 DOI:10.1016/j.jhazmat.2020.122122 (  0) 0) |
 2022, Vol. 54
2022, Vol. 54


