2. 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所), 南京 210008;
3. 浙江省杭州市富阳区农业技术推广中心, 浙江富阳 311400
镉(Cd)是生物毒性极强的环境污染元素之一,我国农田Cd污染面积大、程度严重。2014年《全国土壤污染状况调查公报》显示,耕地土壤污染物点位超标率高达19.4%,其中以Cd污染最为突出,点位超标率达7.0%[1]。目前,针对农田土壤Cd污染采取的措施主要包括物理修复、化学修复、生物修复及农艺调控等。而化学修复中的原位钝化修复技术,是通过向污染土壤中添加钝化剂,改变重金属在土壤中的存在形态,降低其作物有效性,以实现安全生产,现已被诸多学者广泛研究。研究表明,随着土壤pH的降低,土壤对重金属的吸附性减弱,其生物有效性提高;反之,随着土壤pH升高,重金属在土壤上的吸附能力增强,同时重金属可形成沉淀,生物有效性降低[2]。不同类型调理剂可能具有不同的土壤Cd稳定作用和作物吸收调控机理,已有文献对调理剂筛选及其降低稻米Cd吸收性的报道较多,但对不同类型调理剂降低农田土壤重金属有效性的比较研究相对较少[3]。浙江杭州郊区因长期受乡镇企业污水排放影响,农田土壤重金属污染问题突出,稻米Cd超标情况也较为严重[4]。因此,本研究拟选择文献报道及其他课题组试验筛选的对Cd稳定效果较好的土壤调理剂,包括含钙、含硅、或者复配有机质和大量元素(如钾)的调理剂,以浙江杭州郊区富春江沿岸某污染水稻土为研究对象,通过室内培养试验和温室盆栽试验,比较研究不同调理剂对污染土壤pH变化和Cd有效性以及对水稻生长和Cd吸收的影响,以期为高效优质调理剂的选用及我国Cd超标农田土壤的安全利用提供理论依据和技术支撑。
1 材料与方法 1.1 供试土壤供试土壤采自浙江杭州富阳郊区富春江沿岸,为河流冲积物母质发育的水稻土。取0 ~ 20 cm耕层土壤,自然风干,去除杂物,研磨后过10目尼龙筛,备用。土壤pH(H2O)为5.57,有机质含量为40.3 g/kg,土壤全量Cd为0.69 mg/kg。
1.2 供试调理剂土壤重金属调理剂也称钝化剂,本试验选择中国科学院亚热带农业生态研究所推荐的产品,均为在湖南进行了多季且对稻米降Cd效果较好的产品,一类主要成分为钙、镁、硅,加入少量钾、有机质,另一类是单纯以氧化硅为主要成分。另外,选择分析纯氧化钙作为调理剂的对比材料。4种商品化调理剂的代号及主要成分等信息见表 1。
|
|
表 1 供试调理剂性质 Table 1 Properties of tested passivators |
试验一:不同调理剂对土壤pH及提取态镉的影响。准确称取100.00 g供试土壤于黑色小塑料盆中,加入表 1列出的4种供试调理剂,每种调理剂设置推荐用量、3倍推荐用量和推荐用量+生石灰3个处理。生石灰用量根据前期预备试验结果得到,即将土壤pH调高1个单位,生石灰(CaO)的平均用量为1.40 g/kg。试验同时设置不加调理剂对照和单加生石灰两个处理。每个处理3次重复,共计42盆。调理剂与土壤混匀后向小塑料盆中加入70 ml去离子水,放置在自然通风处培养14 d,每2 d用竹棒搅拌一次并加水保持水层在土面上约2 cm,以模拟土壤淹水条件。培养室温度在10 ~ 25 ℃。培养结束时,先将土壤搅拌均匀,放置0.5 h,以倾倒方式提取土壤悬液,并用0.45 μm滤膜过滤,滤液用于测定pH。称取约10 g新鲜土样,记录实际重量,用于测定土壤含水量;同时,称取新鲜土样,用于二乙三胺五乙酸–三乙醇胺(DTPA-TEA,简称DTPA法)和硝酸铵(pH 7.0、1 mol/L NH4NO3)提取态Cd的测定,土壤干重利用所测土壤含水量结果予以换算,以计算鲜土提取态Cd含量。
在称取上述土样后,将CK、3倍YM和3倍TX1处理土样自然风干7 d后采集样品以测定土壤NH4NO3和DTPA提取态Cd,以比较淹水与落干条件下土壤pH和Cd有效性的差异。
试验二:不同调理剂对水稻生长和镉吸收的影响。该试验在中国科学院南京土壤研究所玻璃温室进行,共设10个处理,分别为:①对照,不施用石灰或调理剂;② ~ ⑤按照推荐用量施用选取的4种供试调理剂,分别是YM、ZTF、TX1、YQ;⑥施用1.40 g/kg生石灰(CaO);⑦ ~ ⑩在② ~ ⑤的基础上再分别施用1.40 g/kg生石灰。试验每处理3次重复,共计30盆,每盆装土0.80 kg。供试水稻品种为甬优15,2020年4月3日播种、4月23日移栽,每盆2株。在盆栽装土时每盆施入0.50 g尿素、0.50 g磷酸二氢钾作为基肥(均为分析纯化学试剂)。由于盆栽试验用土量较少,因此后续每月下旬施少量追肥,5月21日第一次追肥(每盆施入0.30 g磷酸氢二铵、0.20 g氯化钾),6月8日第二次追肥(每盆施入0.50 g尿素、0.50 g磷酸二氢钾),7月22日第三次追肥(每盆施入0.50 g尿素、0.30 g磷酸二氢钾),8月23日第四次追肥(每盆施入0.20 g尿素、0.20 g磷酸二氢钾),9月22日第五次追肥(每盆施入0.20 g尿素、0.20 g磷酸二氢钾)。试验每天浇去离子水,保持土面水层约2 cm。6月3日分蘖期结束后统一采集1株水稻地上部;10月26日收获所有的成熟期水稻样品,并将其分为秸秆和糙米两部分。水稻收获后,将每盆土壤风干至适当含水量,倒至一大塑料盆,破摔、混匀,每盆取约300 g,风干,用于土壤含水量和提取态重金属测定。
1.4 测定项目与方法土壤pH的测定:采用玻璃电极法(土液质量比为1∶2.5)。
土壤全量Cd的测定:准确称量0.200 0 g左右过0.149 mm尼龙筛的土样并转移至消解罐中,同时加入5 ml HNO3和5 ml HCl在105 ℃下密封消解6 h,后置于电热板上蒸干至约1 ml,定容,测定消解液中Cd浓度。土壤有效态Cd的测定:利用DTPA和NH4NO3两种提取剂提取,详细步骤见文献[5]。消解液及提取液中Cd浓度用电感耦合等离子体质谱仪(ICP-MS, Nexion 2000 PE, Shelton, CA, USA)测定。为保证分析质量,每个消解批次均使用从中国国家标准研究中心购买的土壤标准物质GSS-5做参比,测定的该标准物质Cd浓度与其参考Cd浓度的误差在100% ± 10% 之内。每个批次消煮的样品中还包括空白对照,用以检验消解过程中可能存在的污染,同时样品上机测定过程中每2 h插入分析空白,用以观察空白的变异。所有测定数值经土壤含水量校正,换算成烘干基。
植物样品中全量Cd的测定:将收获的水稻籽粒和秸秆用自来水洗净,再用去离子水冲洗2 ~ 3次,吸水纸吸干表面水分后称取鲜重,随后放入烘箱105 ℃杀青30 min,75 ℃烘干至恒重,称重,将烘干的植物样品用不锈钢粉碎机粉碎。植物样品采用8 ml 1∶3(V/V)的H2O2-HNO3混合液进行消解,等离子体质谱仪测定。
1.5 数据处理所有数据均使用Microsoft Excel 2016和SPSS 16.0进行处理和分析,采用单因素方差分析法(ANOVA)和最小显著性差异法(LSD)对处理间的差异进行检验(P < 0.05)。
2 结果与分析 2.1 不同调理剂对土壤pH和提取态镉的影响在推荐用量下,施加调理剂的各处理土壤pH均为中性,且较CK处理均显著升高(图 1)。其中,调理剂YM和TX1处理下,土壤pH升高幅度最大,较CK处理分别提高了0.52和0.49个单位,与等量生石灰(CaO)处理效果相似。YQ调理剂对土壤pH调控效果略差,但土壤pH也提高了0.23个单位,显著高于CK处理。施用调理剂处理与CK处理土壤pH均高于供试原始土壤(5.57),这可能是由于淹水条件下土壤pH趋于中性的原因。
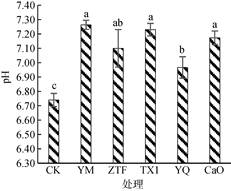
|
(图中不同小写字母表示处理间差异显著(P < 0.05),下同) 图 1 淹水培养条件下推荐用量调理剂对土壤pH的影响 Fig. 1 Effects of recommended dosage of passivators on soil pH under flooded condition |
如表 2所示,在推荐用量下,施用调理剂可显著降低土壤NH4NO3提取态Cd(NH4NO3-Cd)含量,YM和TX1处理较CK处理降低幅度较大,达82.3%和85.3%。这是由于NH4NO3-Cd主要为水溶态和部分可交换态Cd,调理剂通过提高土壤pH(图 1),降低可交换态Cd含量。施调理剂的各处理土壤DTPA提取态Cd (DTPA-Cd)含量均较CK处理有所升高,其中CaO和ZTF处理上升显著(表 2)。DTPA对土壤中吸附Cd的浸提能力较强,可置换出土壤中大部分可解吸的Cd[6],而随着调理剂中Ca2+以及有机质组分进入土壤,与Cd2+竞争土壤表面的吸附位点,部分可氧化态Cd进入土壤溶液,导致土壤有效态Cd含量增加[7]。
|
|
表 2 调理剂不同用量对土壤DTPA-Cd和NH4NO3-Cd含量的影响(μg/kg) Table 2 Effects of different dosages of passivators on DTPA-Cd and NH4NO3-Cd concentrations in soil |
施加调理剂3倍推荐量处理和推荐用量+生石灰处理相较于推荐用量处理,其DTPA-Cd含量均略有升高(表 2)这说明调理剂产生的石灰效应导致土壤DTPA-Cd含量呈上升趋势。调理剂推荐用量+石灰处理DTPA-Cd含量略低于调理剂3倍用量处理,但差异并不显著。
对于NH4NO3-Cd,施加3倍推荐用量的调理剂处理相较于推荐用量处理呈现降低趋势,3倍推荐用量的YQ调理剂处理下NH4NO3-Cd含量降低幅度最大(表 2)。说明该提取态Cd受土壤pH影响较大,因调理剂施用而使土壤pH升高、Cd有效性降低。而与3倍推荐用量处理相比,推荐用量+生石灰处理NH4NO3-Cd含量的变化规律不明显,其中ZTF调理剂处理显著降低,YQ调理剂处理则显著上升。总体上,土壤NH4NO3-Cd含量较DTPA-Cd含量低得多,约为后者的2% ~ 7%。
落干水分后土壤pH明显低于淹水条件(图 2)。落干条件下调理剂推荐用量处理土壤pH较不施调理剂的CK处理显著上升,且其增幅大于淹水条件,说明在调理剂作用下土壤pH升高,且在旱作情形下更为显著。

|
(图中不同小写、大写字母分别表示淹水、落干条件下处理间差异显著(P < 0.05)) 图 2 淹水与落干条件下不同调理剂3倍推荐用量对土壤pH的影响 Fig. 2 Effects of triple-recommended dosage of passivators on soil pH under flooded and aerobic conditions |
由图 3可见,淹水后土壤NH4NO3-Cd和DTPA-Cd含量均远低于落干条件,这与淹水后土壤pH趋于中性化即酸性土壤pH升高有关;其次,淹水使土壤氧化还原电位(Eh)下降,硫(S)被还原,生成CdS沉淀,这可能也是Cd有效性下降的又一原因[8-9]。
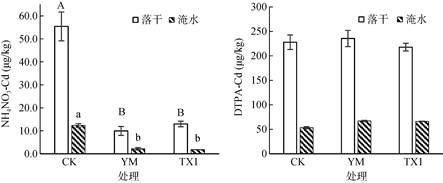
|
(图中无标记字母,表示各处理间差异不显著(P > 0.05)) 图 3 淹水与落干条件下不同调理剂3倍推荐用量对NH4NO3-Cd和DTPA-Cd含量的影响 Fig. 3 Effects of triple-recommended dosage of passivators on NH4NO3-Cd and DTPA-Cd concentrations in soil under flooded and aerobic conditions |
从表 3可见,施用调理剂的各处理相较于未施调理剂CK处理,其糙米生物量均有所上升,但仅CaO+YQ处理的糙米生物量显著上升,较CK提高了41.7%;ZTF处理上升幅度最小,较CK仅提高了5.99%,这可能与ZTF调理剂的性质有关,其硅酸盐含量较高,对于土壤养分状况的改善效果不如其他调理剂。各处理的秸秆生物量没有显著性变化。
|
|
表 3 不同调理剂对水稻生物量及镉含量的影响 Table 3 Effects of different passivators on biomass and Cd concentration of rice |
除YM、ZTF处理外,其余施用调理剂的处理均显著降低了水稻糙米Cd含量(表 3),所有施调理剂的水稻糙米Cd含量都低于GB 2762—2017《食品安全国家标准食品中污染物限量》[10]中0.2 mg/kg限值,且调理剂与生石灰复合施用能更有效降低糙米Cd吸收,钝化效果更显著;而对比处理间水稻秸秆中Cd含量变化也能得到类似的结论。相对而言,分蘖期水稻秸秆中Cd含量总体高于成熟期(表 3);复合施用处理相对于单施处理,成熟期水稻秸秆Cd含量下降幅度可达25.0% ~ 63.5%;在4个单施调理剂处理中,ZTF处理水稻秸秆Cd含量显著高于其他3种调理剂处理,这是由于ZTF调理剂中氧化硅成分占比较高,对土壤Cd的钝化效果较其他调理剂略低。
2.3 不同调理剂对水稻收获后土壤pH和提取态镉的影响水稻收获后,调理剂与生石灰复合施用处理相较于单施调理剂间以及生石灰处理更能显著提高土壤pH,而复合施用各处理以及单施调理剂处理间的差异并不显著(表 4)。施用调理剂的处理相较于未施调理剂的处理,其NH4NO3-Cd含量都有显著性下降;4种不同类型的调理剂处理间,ZTF处理的NH4NO3-Cd含量较其他3种调理剂处理高且差异相对显著,而各处理间的DTPA-Cd含量并没有显著差异。结合表 2可以看出,NH4NO3-Cd含量相较于DTPA-Cd含量能更好地表征土壤Cd的有效性。
|
|
表 4 盆栽水稻收获后土壤pH及NH4NO3-Cd和DTPA-Cd含量 Table 4 Soil pH and NH4NO3-Cd and DTPA-Cd concentrations in soil after rice harvest |
综合比较本试验所选择的4种商品调理剂以及生石灰,其施用后土壤pH均显著升高,而土壤NH4NO3-Cd含量则显著下降,因此,水稻秸秆和糙米中Cd含量也呈降低趋势,且以含石灰、有机质和养分的调理剂类型对水稻Cd吸收的降低作用更为显著,含硅为主的调理剂则降Cd效果略低。
3 讨论 3.1 调理剂类型对土壤pH及提取态镉影响的机理由于土壤性质的差异,土壤重金属与其他元素直接存在复杂的相互作用和界面过程。因此,针对不同类型土壤中的重金属选择调理剂进行修复时其钝化效果不尽相同[11]。施入土壤中的调理剂主要通过吸附、沉淀、络合、离子交换和氧化还原等方式,使重金属转化为有效性较低的形态[12],降低土壤重金属的植物有效性。
石灰施入土壤中能有效提高土壤pH,而土壤pH与Cd有效性有着密切的联系。詹绍军[13]研究表明,添加石灰后土壤有效Cd含量随时间的增加而降低,培养60 d后有效态Cd从0.112 mg/kg降至0.061 mg/kg。土壤pH升高将使土壤颗粒表面负电荷增加,促使土壤中Cd、Cu、Hg、Zn等元素通过表面吸附、形成氢氧化物或碳酸盐结合态盐类沉淀[14]。生石灰施用于土壤中还会使土壤中Ca2+浓度增加,从而影响土壤溶液中Cd的吸附–解吸动态平衡,阳离子浓度升高,与Cd产生拮抗作用降低溶液Cd浓度[15]。本研究结果显示,施用调理剂使土壤pH上升,NH4NO3-Cd含量降低,说明调理剂能通过调节土壤pH影响土壤Cd的吸附–解吸,降低Cd有效性。
硅酸盐调理剂也广泛应用于生产实践[16],与石灰性调理剂相比具有来源广泛、不破坏土壤结构、改良酸性土壤和不引入二次污染物等优点。硅酸盐调理剂主要通过大量有效硅溶解后产生的硅酸根离子与弱酸溶态Cd结合形成难溶性的硅酸镉和偏硅酸镉,从而降低土壤Cd的有效性[17-18]。另外,该类调理剂也提高了土壤pH,增加了土壤胶体和矿物表面的负电荷量,促使重金属向氢氧化物沉淀和碳酸盐结合态沉淀转化[19]。
3.2 调理剂中有机质与养分的作用机理有机质可以通过改变土壤pH、Eh、阳离子交换量等土壤理化性质,提高土壤对Cd2+的吸附能力,使Cd2+被吸附到土壤胶体表面,增强土壤对Cd2+的固持能力[20]。在调理剂中添加有机质不仅可以提高土壤肥力水平,改善土壤性质,还可以通过络合反应与土壤中的Cd2+形成稳定的络合物,降低Cd的有效性,从而达到安全生产的目的[21]。但有机质和石灰等碱性物质的复合施用也会导致土壤溶液中可溶性有机碳含量升高,可溶性的重金属有机质络合增加,从而使土壤中Cd的有效性升高[22]。
本试验中,YM和TX1调理剂含有养分物质,如氧化钾。钾是植物必需的大量营养元素之一,参与植物的多种生命活动与酶的代谢等过程,施用足量的钾肥可促进植物根系生长,提高作物的生物量[23]。钾也是土壤主要的盐基饱和离子之一,通过与Cd2+竞争土壤的吸附点位影响土壤对Cd2+的吸附。施入适量的钾肥可以增加土壤中水溶性钾的含量,随着土壤溶液中钾含量增加,Cd的解吸量也会随之升高[24]。因此,有机质和养分物质的加入,可能在增大作物养分吸收性、增强作物抗逆性的同时,解吸作用可能会增大土壤Cd的有效性。从本试验结果看,可能在促进水稻生长方面的作用更为明显。
3.3 淹水对土壤镉有效性的影响土壤淹水作为一种调控措施,可以调控土壤pH和Eh,进一步降低土壤重金属有效性。淹水会使土壤处于还原状态,土壤Eh下降,淹水初期变化尤为显著[25]。而淹水条件下,酸性土壤pH升高主要是因为土壤铁氧化物的还原溶解作用,碱性土壤pH降低则主要由于土壤中大量碳酸盐的溶解作用以及土壤中CO2的累积所导致[26-27]。土壤pH能够影响土壤对Cd的吸附,一方面铁锰氧化物溶解生成新的铁锰氧化物会改变土壤对Cd的吸附能力,影响土壤有效态Cd浓度[28];另一方面,土壤pH升高将增加土壤表面胶体所带负电荷量,从而增加重金属离子的静电吸附,同时导致金属阳离子羟基态的形成,产生更多的土壤吸附点位[29]。此外,土壤pH升高还会使重金属以氢氧化物的形式沉淀,降低重金属有效态浓度[30]。从本试验结果可以看出,落干后土壤Cd有效性较淹水条件下显著上升,且pH也有显著下降。因此,本试验对土壤pH的调控是淹水和施调理剂双重作用的结果。
4 结论本研究培养试验所选调理剂,在推荐用量下对土壤pH和Cd有效性均有较好的调控效果。施用调理剂后土壤pH显著上升,土壤NH4NO3-Cd含量下降,其中YM、TX1等含石灰、有机质及养分的复合调理剂对NH4NO3-Cd含量的降低效果较好;但DTPA-Cd含量上升。调理剂用量增加,进一步降低NH4NO3-Cd含量,但提高土壤DTPA-Cd含量,进一步混施生石灰效果介于两个用量效果之间。落干水分后土壤pH相较于淹水条件下显著下降,DTPA-Cd含量显著上升。
盆栽试验结果显示,调理剂和生石灰混施相比于调理剂单施更能显著提升水稻籽粒产量,并降低水稻糙米Cd含量,与调理剂和生石灰配施后土壤Cd有效性降低相一致,是生石灰提高土壤pH及调理剂降低土壤Cd有效性共同作用的结果。此外,含钙、能调节土壤pH并辅以有机质和养分的复合调理剂因兼具养分作用,对水稻增产和糙米Cd含量的降低更为有效。
| [1] |
环境保护部和国土资源部发布全国土壤污染状况调查公报[J]. 资源与人居环境, 2014(4): 26-27 (  0) 0) |
| [2] |
重金属污染土壤修复技术及其修复实践[J]. 农业环境科学学报, 2013, 32(3): 409-417 (  0) 0) |
| [3] |
钝化材料复配对土壤Cd生物有效性的影响[J]. 环境工程学报, 2018, 12(10): 2884-2891 DOI:10.12030/j.cjee.201804040 (  0) 0) |
| [4] |
土壤调理剂应用现状及施用风险研究[J]. 农业环境科学学报, 2021, 40(6): 1141-1149 (  0) 0) |
| [5] |
鲁如坤. 土壤农业化学分析方法[M].
中国农业科技出版社, 北京, 2000
(  0) 0) |
| [6] |
不同提取剂提取土壤中重金属能力的对比研究[J]. 华南师范大学学报(自然科学版), 2020, 52(1): 55-62 (  0) 0) |
| [7] |
DTPA浸提条件下土壤性质对镉浸提效果的影响[J]. 水电与新能源, 2018, 32(12): 68-72, 75 (  0) 0) |
| [8] |
Kitagishi K, Yamane I. Heavy metal pollution in soils of Japan[M]. Heavy metal pollution in soils of Japan. Japan Scientific Societies Press, 1981, 426.
(  0) 0) |
| [9] |
Gambrell R P, Wiesepape J B, Patrick W H, et al. The effects of pH, redox, and salinity on metal release from a contaminated sediment[J]. Water, Air, and Soil Pollution, 1991, 57/58(1): 359-367 DOI:10.1007/BF00282899 (  0) 0) |
| [10] |
中华人民共和国国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品安全国家标准食品中污染物限量GB 2762—2017[S]. 北京: 中国标准出版社, 2017.
(  0) 0) |
| [11] |
不同钝化剂对重金属复合污染土壤的修复效应研究[J]. 农业环境科学学报, 2015, 34(3): 438-448 (  0) 0) |
| [12] |
海泡石对镉–铅复合污染钝化修复效应及其土壤环境质量影响研究[J]. 环境科学, 2014, 35(12): 4720-4726 (  0) 0) |
| [13] |
詹绍军. 有机物料与石灰性物质对土壤镉有效性及小麦吸收镉的影响[D]. 雅安: 四川农业大学, 2011.
(  0) 0) |
| [14] |
Lombi E, Hamon R E, McGrath S P, et al. Lability of Cd, Cu, and Zn in polluted soils treated with lime, beringite, and red mud and identification of a non-labile colloidal fraction of metals using istopic techniques[J]. Environmental Science & Technology, 2003, 37(5): 979-984 (  0) 0) |
| [15] |
岩溶区棕色石灰土胶体对镉铅的等温吸附特性研究[J]. 农业环境科学学报, 2020, 39(3): 554-562 (  0) 0) |
| [16] |
西南喀斯特山地的土壤硅酸盐矿物物质平衡与土壤流失[J]. 地球与环境, 2009, 37(2): 97-102 (  0) 0) |
| [17] |
新型硅酸盐钝化剂对镉污染土壤的钝化修复效应研究[J]. 农业环境科学学报, 2017, 36(10): 2007-2013 DOI:10.11654/jaes.2017-0471 (  0) 0) |
| [18] |
硅酸盐钝化剂在土壤重金属污染修复中的研究与应用[J]. 土壤, 2017, 49(3): 446-452 (  0) 0) |
| [19] |
不同钝化剂对铜污染土壤原位钝化修复[J]. 土壤, 2016, 48(4): 742-747 (  0) 0) |
| [20] |
土壤有机质对镉污染土壤修复的影响[J]. 土壤通报, 2015, 46(4): 1018-1024 (  0) 0) |
| [21] |
土壤质地、pH、有机质含量对镉存在形态的影响及其机理研究[J]. 上海交通大学学报(农业科学版), 2019, 37(3): 29-33 DOI:10.3969/J.ISSN.1671-9964.2019.03.005 (  0) 0) |
| [22] |
长期施用有机肥对土壤和糙米铜、锌、铁、锰和镉积累的影响[J]. 植物营养与肥料学报, 2010, 16(1): 129-135 (  0) 0) |
| [23] |
不同配方富钾土壤调理剂施用对土壤钾素及烟叶品质的影响[J]. 西南农业学报, 2021, 34(1): 94-99 (  0) 0) |
| [24] |
钾对土壤镉有效性的影响及其机理[J]. 中国矿业大学学报, 2010, 39(3): 453-458 (  0) 0) |
| [25] |
Sun L N, Chen S, Chao L, et al. Effects of flooding on changes in Eh, pH and speciation of cadmium and lead in contaminated soil[J]. Bulletin of Environmental Contamination and Toxicology, 2007, 79(5): 514-518 DOI:10.1007/s00128-007-9274-8 (  0) 0) |
| [26] |
淹水还原作用对红壤镉生物有效性的影响[J]. 农业环境科学学报, 2009, 28(11): 2333-2337 DOI:10.3321/j.issn:1672-2043.2009.11.022 (  0) 0) |
| [27] |
不同类型土壤淹水对pH、Eh、Fe及有效态Cd含量的影响[J]. 农业环境科学学报, 2017, 36(8): 1508-1517 (  0) 0) |
| [28] |
淹水稻田中土壤性质的变化及其对土壤镉活性影响的研究进展[J]. 农业环境科学学报, 2016, 35(12): 2260-2268 DOI:10.11654/jaes.2016-0892 (  0) 0) |
| [29] |
Naidu R, Bolan N S, Kookana R S, et al. Ionic-strength and pH effects on the sorption of cadmium and the surface charge of soils[J]. European Journal of Soil Science, 1994, 45(4): 419-429 DOI:10.1111/j.1365-2389.1994.tb00527.x (  0) 0) |
| [30] |
不同钝化剂对Cu、Cr和Ni复合污染土壤的修复研究[J]. 土壤, 2016, 48(1): 123-130 (  0) 0) |
2. Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China;
3. Center for Agricultural Technology Extension in Fuyang District of Hangzhou City Zhejiang Province, Fuyang, Zhejiang 311400, China
 2022, Vol. 54
2022, Vol. 54


