2. 国家环境保护土壤环境管理与污染控制重点实验室, 南京 210042;
3. 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所), 南京 210008
小麦是全球第三大粮食作物,也是我国第二大粮食作物,在我国粮食作物的生产和消费中占主导地位。我国的小麦种植区域主要集中在长江中下游及其以北地区,包括河北、河南、湖北、四川、山东、安徽和江苏等地。相比于水稻,我国小麦镉(Cd)污染的研究较少。作为食物链的起点,小麦也会吸收土壤中的有毒元素,并通过食物链传递危害人体健康。调查发现江苏省稻麦轮作体系下,在全Cd含量为0.481(0.278 ~ 1.10)mg/kg的农田土壤中,小麦籽粒Cd含量为0.130(0.043 ~ 0.621)mg/kg[1]。在长三角工农业过渡区采集的126个小麦样品中,小麦籽粒Cd含量为0.065(0.018 ~ 0.245)mg/kg[2]。而对华北某污灌区的调查结果则表明,污灌后土壤Cd含量达到1.56(1.23 ~ 1.97)mg/kg,小麦籽粒Cd含量达0.110(0.070 ~ 0.140)mg/kg,与GB 2762—2017《食品安全国家标准食品中污染物限量》[3]规定的小麦Cd含量限值比较,小麦籽粒Cd超标率为76.7%[4]。因此,小麦对Cd的富集能力较高,其种植过程中的Cd污染风险不容忽视。
目前,重金属Cd在土壤–小麦系统的积累和传递已有较多研究[5-8],小麦籽粒对重金属的积累主要受小麦品种[5]和土壤性质[6]的影响。Liu等[7]研究发现,在对30个品种小麦进行Cd胁迫研究时,不同品种间小麦Cd含量存在巨大差异。也有研究表明,小麦籽粒Cd含量与土壤全量Cd、有机碳和黏粒含量显著正相关,与土壤pH和阳离子交换量(CEC)显著负相关,说明土壤性质可显著影响Cd的生物有效性,进而影响小麦籽粒的Cd吸收性[1, 2, 9, 10]。诸多研究也基于土壤基本性质,建立了小麦籽粒Cd含量预测模型。但因土壤类型、小麦品种等多重因素的影响,不同预测模型得到的结果并不一致,如Zhou等[1]发现土壤全Cd是影响小麦Cd吸收的唯一变量,而Adams等[6]、Liu等[11]、Ran等[12]和Brus等[13]发现土壤全量Cd、pH和有机质是影响小麦Cd吸收的主要变量。此外,当前的农田土壤重金属污染治理与修复技术也多通过改变pH、有机质等土壤基本性质,来降低土壤重金属的生物有效性,进而减少作物根系的吸收量。因此,探明土壤–小麦体系中Cd的积累特征及其影响因素,也可指导Cd污染农田土壤的治理修复与安全利用实践。
本研究拟以我国主要农作区的33个典型农田土壤为供试材料,分别种植两个常规小麦品种,探明两个小麦品种在不同土壤类型上的Cd吸收性,以比较不同类型土壤上两个品种小麦籽粒Cd的积累特征,探明土壤性质对小麦籽粒Cd吸收的影响,并探究影响小麦籽粒Cd吸收的土壤主控因子,建立基于土壤性质的不同品种小麦籽粒Cd浓度的预测模型,并评价模型的不确定性。本研究可为小麦实际生产过程中存在的Cd污染问题提供新的认识,相关研究成果也可指导小麦的安全生产。
1 材料与方法 1.1 盆栽试验设计2015年在我国水稻优势产区共采集33个耕层水稻土(0 ~ 20 cm)。采样点位分别位于黑龙江、吉林、辽宁、山东、河南、陕西、宁夏、安徽、江苏、浙江、湖北、湖南、江西、云南、广西、福建和贵州。供试土壤的pH、有机碳(SOC)、CEC、黏粒、全Cd含量平均值分别为6.31、21.1 g/kg、12.4 cmol/kg、221 g/kg、0.26 mg/kg。土壤基本理化性质变异较大,pH变化在强酸性到弱碱性。与GB 15618—2018《土壤环境质量农用地土壤污染风险管控标准》(试行)[14]中的土壤污染风险筛选值相比,33个土壤样品中有5个(15.1%)存在Cd超标风险。
供试土壤风干过2 mm尼龙网筛、装盆,每盆土重2 kg。小麦品种选择蓉麦4号(RM4)和山农22号(SN22)。小麦种植前每盆施0.6 g CO(NH2)2和0.6 g K2H2PO4作为基肥。小麦种子浸泡在5% NaClO中消毒20 min,然后将种子催芽3 d后,每盆播种15粒,待长出幼苗后进行间苗,每盆定苗8株。小麦拔节期后、灌浆期前每盆施用0.4 g Na2H2PO4、0.4 g KCl和0.6 g CO(NH2)2作为追肥。小麦生长过程中,不同的盆栽随机排列,并定期重新排列位置。小麦于2017年11月15日播种,2018年5月18日收获。小麦成熟后收获麦穗,晒干后脱壳,得到小麦籽粒(全麦)。小麦籽粒带回实验室,用自来水清洗3次,再用蒸馏水清洗3次后,转移至烘箱以70 ℃烘至恒重,用粉碎机打成细粉末,待测。
1.2 样品分析和测定土壤pH以土水比1:2.5(m/V)浸提,玻璃电极法测定;有机碳(SOC)用重铬酸钾–外加热法测定;CEC用醋酸铵(1.0 mol/L,pH 7.0)交换,然后用HCl滴定法测定;黏粒含量用吸管法测定。上述土壤性质测定方法参考《土壤农化分析》[15]。土壤中重金属的消解过程如下:准确称取过0.15 mm筛的土壤样品0.2 g,置于50 ml聚四氟乙烯高压消解罐中,加入10 ml的HCl-HNO3混合酸(体积比1:1),旋紧消解罐盖后放入105 ℃烘箱,消解6 h。消解结束后,将消解罐移至130 ℃电热板上赶走多余的酸,直至约剩1 ml。待样品充分冷却后,将消解液转移至15 ml的离心管中,并用超纯水进行定容。定容后的溶液过0.45 µm的滤膜,待测。植物中重金属的消解过程如下:准确称取0.5 g粉碎后的小麦籽粒样品于50 ml的聚四氟乙烯高压消解罐中,加入2 ml 30% H2O2和6 ml 65% HNO3后,旋紧消解罐盖后放入105 ℃烘箱,消解6 h。其他过程均与土壤样品消解过程一致。消解所用的HCl、H2O2和HNO3均为优级纯。消解液中Cd浓度用电感耦合等离子体质谱仪(ICP-MS, Agilent 7700x, Santa Clara, CA)测定。为保证分析质量和准确性,在土壤和植物消解过程中,加入国家标准物质土壤(GSS-5)和大米(GBW(E)100348)进行校正。标准物质实际测定的Cd浓度与参考浓度吻合度较高(100% ± 10%),保证了样品分析和测定过程中的精确度和准确性。每批次消解样中,均插入空白样以检验系统误差。同时在样品上机测定过程中,每2 h插入空白来检验仪器的稳定性。
1.3 小麦籽粒镉含量预测模型的建立和验证本研究利用多元逐步回归分析方法,建立基于土壤pH、全Cd、CEC、SOC和黏粒含量的小麦籽粒Cd含量预测模型。GBM(generalized boosted models)分析是一种根据数据变量的类型,利用自适应算法自动估算大量混杂变量与处理变量之间非线性关系的一种分析方法,特别是当变量之间线性、非线性或交互关系等函数形式无法确定时,此方法具有明显优势。本研究通过GBM分析,量化土壤性质对小麦籽粒Cd积累的贡献,获得所选土壤性质对小麦籽粒Cd含量的相对重要性和偏相关分析图。该分析利用gbm软件包在R 3.2.2统计环境中进行。同时本研究还采用迭代方法,将预测误差较大的变量通过序列迭代组合成预测性能较好的强化模型,并通过比较盆栽试验中测定的小麦籽粒Cd含量与模型预测的Cd含量,确定模型预测的精度。
1.4 数据处理与分析小麦和土壤中Cd的单项污染指数计算:
| $ \mathrm{PI}=\left[\mathrm{Cd}_{\text {测 }}\right] /\left[\mathrm{Cd}_{\text {标 }}\right] $ | (1) |
式中:[Cd测]代表样品中Cd含量实测值;[Cd标]代表土壤和小麦籽粒中Cd含量标准值,其中,土壤参考GB 15618—2018[14]中污染风险筛选值,小麦参考GB 2762—2017[15]中规定的小麦Cd含量限量值。
小麦籽粒Cd的生物富集系数(BCF):小麦籽粒Cd含量和对应土壤Cd含量的比值。
文中数据利用Microsoft Excel 2016和SPSS 21.0进行整理和统计分析, 采用单因素方差分析法(One- way ANOVA)对土壤和小麦籽粒样品中Cd含量以及BCF的差异性进行检验(P < 0.05)。若方差分析的残差不符合正态分布(P < 0.05)或Levene’s检验方差存在异质性,将数据进行自然对数转换后再进行统计分析,数据均值、标准差(SD)或标准误(SEm)仍以未转换的数据形式列出。
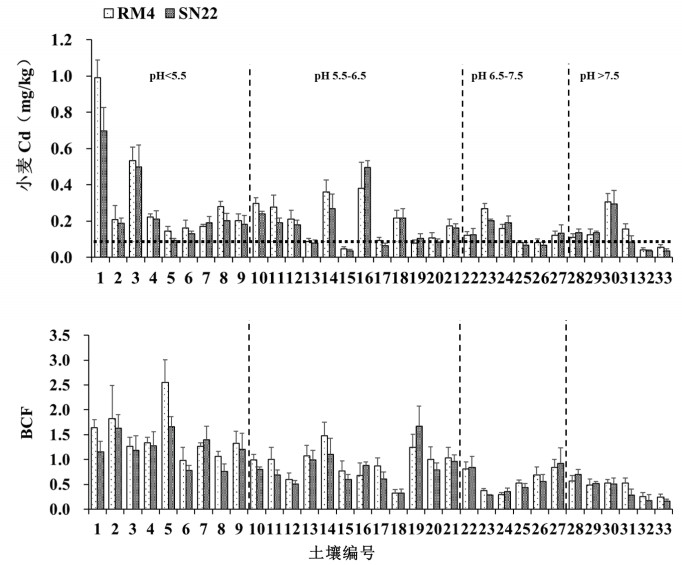
2 结果与讨论 2.1 土壤–小麦系统中镉的富集特征如图 1所示,RM4和SN22两个品种的小麦籽粒Cd含量分别为0.21(0.040 ~ 0.99)mg/kg和0.18(0.037 ~ 0.70)mg/kg。供试33个土壤中,RM4和SN22这两个品种中分别有25个和23个小麦籽粒Cd含量超过GB 2762—2017[3]规定的食品污染物限值,超标率分别达75.6% 和69.7%。上述研究结果表明,小麦的Cd超标风险较高,本研究中小麦籽粒Cd含量超标率也高于江苏宜兴市(53.8%) [1]和长三角某工农业过渡区(14.3%)[2]的田间调查结果。与GB 15618—2018[14]的风险筛选值比较,5个Cd含量超标土壤上的小麦籽粒Cd含量均超标,但在未污染土壤上RM4和SN22仍分别有20个和18个小麦籽粒Cd含量超标。Zhang等[16]对美国地区种植的小麦调查后发现,即使生长在非污染土壤上,小麦籽粒中Cd含量在0.002 ~ 0.207 mg/kg,存在一些超过世界卫生组织(WHO)规定的小麦安全食用上限(0.1 mg/kg)的情形。上述结果进一步表明,小麦种植具有较高的Cd超标风险。
|
(平行于横坐标的虚线代表GB 2762—2017中规定的小麦籽粒Cd含量限值(0.1 mg/kg)) 图 1 不同类型土壤下小麦籽粒镉含量和富集系数变化 Fig. 1 Cd concentrations and bioconcentratiuon factor (BCF) values of wheat grains in different soil types |
此外,两个品种小麦的Cd生物富集系数(BCF)分别是0.92(0.24 ~ 2.55)和0.81(0.16 ~ 1.67)。RM4和SN22小麦籽粒对Cd的BCF最大值分别为是2.55和1.67,其对应的土壤分别采自广东江门(pH 5.50)和云南德宏(pH 6.22)的酸性土壤;BCF最小值分别是0.24和0.16,其对应的土壤均为采自江苏连云港的碱性土壤(pH 8.94)。通过分析两个品种小麦籽粒Cd的BCF可发现,RM4和SN22的BCF > 1的样品数分别是14个和9个,说明小麦是一种对Cd富集能力较强的作物。主要原因是小麦籽粒Cd的积累主要是通过根部富集后运输到旗叶韧皮部再进入籽粒,即小麦植株内较强的Cd转运能力导致其籽粒Cd大量积累[17]。进一步分析还发现,在强酸性(pH < 5.5)土壤中小麦籽粒Cd含量和BCF值均较大,且BCF值也随土壤pH升高均呈下降趋势,说明土壤pH也是影响小麦籽粒Cd的BCF的重要土壤性质。
2.2 小麦籽粒镉预测模型建立及预测精度验证本研究基于土壤pH、CEC、SOC、黏粒含量以及全量Cd等基本性质,采用逐步回归分析方法建立了小麦籽粒Cd含量预测模型(表 1)。土壤全Cd和pH是影响小麦籽粒Cd含量的主要变量。与仅考虑土壤全量Cd的预测模型相比,引入其他土壤性质可显著提高模型的预测精度。如表 1所示,RM4和SN22两个小麦品种仅引入土壤全Cd预测方程的回归系数R2值分别是0.41和0.42,继续引入变量土壤pH后两个品种小麦籽粒Cd含量预测方程的回归系数R2分别提高到0.77和0.82。本研究中,SOC、CEC和黏粒含量并未进入方程,说明上述变量在本试验条件下对小麦籽粒Cd吸收的影响不显著。其中,小麦籽粒Cd含量与土壤pH显著负相关,与土壤全Cd含量显著正相关,说明随土壤pH下降和全Cd含量的增加,小麦籽粒的Cd积累能力增加。目前,已有较多研究建立了小麦籽粒Cd含量的预测模型(表 2)。在Adams等[6]、Liu等[11]和Ran等[12]的研究中全量Cd和pH是小麦籽粒Cd含量预测模型的主要变量,与本研究结果一致。但Zhou等[1]通过对田间采集的26对土壤–小麦样品建立的预测模型发现,土壤全Cd含量是影响小麦籽粒Cd含量的唯一变量,可能原因是其采样范围较小,土壤基本理化性质变异较小。而Brus等[13]建立的小麦籽粒Cd含量预测模型的土壤变量是全量Cd、pH和有机质含量。
|
|
表 1 基于土壤基本性质和全量镉的小麦籽粒镉含量多元逐步回归预测方程(n=33) Table 1 Multiple regression models for Cd concentration in wheat grains based on soil basic properties and total Cd |
|
|
表 2 文献报道的关于小麦籽粒镉含量预测模型 Table 2 Models found in literatures to predict Cd concentration in wheat grains |
通过绘制盆栽小麦籽粒Cd含量的预测值和相应的实测值组成的散点图(图 2)可检验模型预测的精确度。如图 2所示,所有数据点均匀分布在1:1线两侧,绝大部分数据点在方程的95% 置信区间内,表明该预测模型准确度较高。两个品种的小麦籽粒Cd含量的实测值均分别与模型预测值显著相关(P < 0.01),进一步说明模型的预测精度较高,可通过土壤性质准确预测小麦籽粒Cd含量。

|
(实线表示1:1线,虚线表示回归方程的95% 置信区间) 图 2 小麦籽粒镉含量实测值和预测值比较 Fig. 2 Relationship between measured and predicted Cd concentrations in wheat grains |
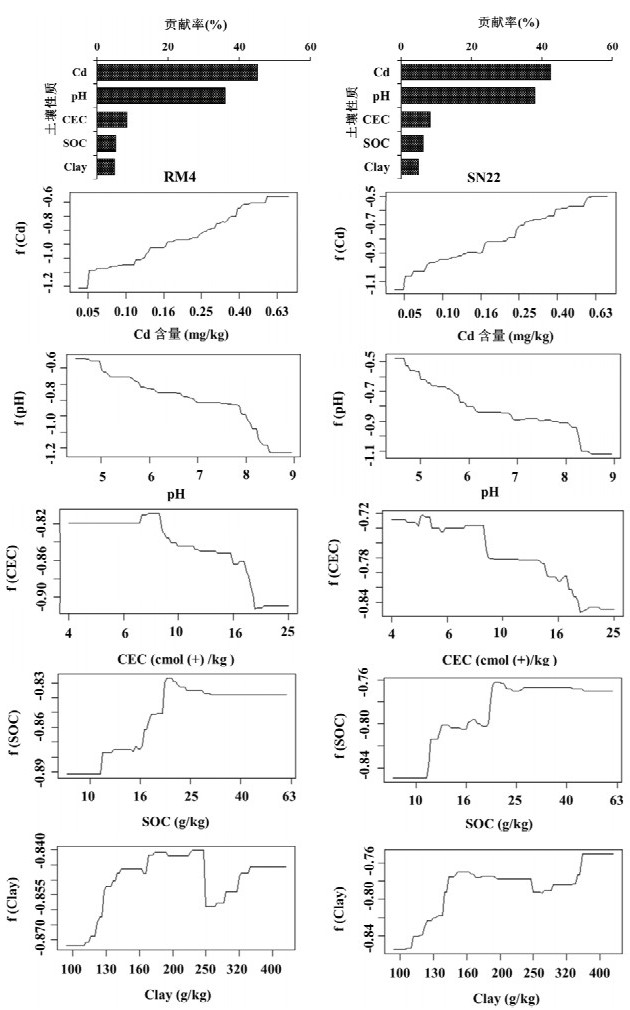
本研究利用GBM分析土壤全Cd、pH、SOC、CEC和黏粒含量对两个品种小麦籽粒Cd积累的相对重要性和贡献率。首先,对上述土壤变量(除pH外)进行对数转换,以保证方差的齐性。如图 3所示,土壤全量Cd和pH对两个品种小麦籽粒Cd含量相对贡献率较高,而土壤CEC、黏粒含量和SOC含量的相对影响较弱。土壤性质对RM4籽粒Cd含量的贡献率排序为:全Cd(45.2%) > pH(36.1%) > CEC(8.40%) > SOC(5.30%) > 黏粒(5.00%);对SN22籽粒Cd含量的贡献率排序为:全Cd(42.5%) > pH(38.0%) > CEC (8.30%) > SOC(6.20%) > 黏粒(5.00%)。单一变量的偏相关图(图 3)表明,全量Cd和pH对两个品种小麦籽粒Cd含量的影响表现出相同的趋势,土壤全量Cd在供试测定范围内促进小麦籽粒Cd吸收,土壤pH从4.5上升至8.5将降低小麦籽粒Cd吸收。土壤CEC由9.0 cmol/kg上升至20.0 cmol/kg,RM4品种小麦籽粒Cd吸收明显下降;但对SN22,CEC影响范围是4.0 ~ 20.5 cmol/kg。在11.0 ~ 20.5 g/kg范围内,两个品种小麦籽粒Cd吸收随SOC含量的增大而升高。黏粒含量在110 ~ 140 g/kg和320 ~ 360 g/kg范围内两个品种小麦籽粒Cd吸收随黏粒含量上升而升高(图 3)。
|
图 3 土壤性质对小麦籽粒镉含量的贡献率及偏相关分析 Fig. 3 Relative contribution and partial dependency plots for soil properties influencing Cd concentrations in wheat grains |
小麦籽粒Cd的转运和积累受土壤性质(pH、Eh和CEC)、小麦品种(基因型差异)和农艺措施(水分和施肥管理)等的共同影响[18-20]。土壤pH和全Cd是影响Cd生物有效性和小麦籽粒Cd积累的重要因子[10, 21-24]。土壤pH升高,土壤表面负电荷的增加导致其吸附更多的Cd离子,减少了土壤溶液中Cd离子的移动性和有效性;相反,土壤pH较低时,吸附在土壤颗粒表面的Cd离子释放,增加了其移动性和生物有效性[25-27]。通常情况下,由于不同品种小麦Cd吸收和积累能力的差异,小麦籽粒Cd吸收变异较大[18, 20]。Yang等[28]对采自江苏省的30对土壤–小麦样品分析发现,土壤pH、全量Cd和EC可以解释小麦籽粒Cd含量的60.5%。本研究中,土壤pH和全量Cd对RM4和SN22小麦籽粒Cd含量贡献率分别是81.3% 和80.5%,SOC对两个品种小麦籽粒Cd含量无显著影响。但Wenzel等[29]研究发现,土壤pH对小麦Cd吸收无影响,但是SOC含量的升高会使小麦籽粒Cd吸收下降。土壤pH、黏粒及SOC含量可通过影响Cd有效性而影响其在土壤–作物系统的转运[30-32]。有研究发现,小麦籽粒Cd含量与SOC含量显著负相关,可能原因是SOC可通过吸附作用形成稳定的化合物,从而降低土壤中Cd的有效性[7, 33];土壤有机质在影响土壤pH的同时也向土壤中释放有机酸,提高Cd的生物有效性[34-35]。因此,土壤SOC含量与小麦籽粒Cd含量正相关可能是由于土壤–小麦系统SOC对Cd的活化作用掩盖了其对Cd的固定作用[7],但本研究中土壤SOC对小麦籽粒Cd吸收无显著影响。
3 结论本试验中小麦籽粒Cd含量超标情况不容忽视,应重视小麦籽粒Cd含量的超标风险。土壤性质是影响小麦Cd吸收的重要因素,其中土壤全量Cd和pH是影响小麦籽粒Cd含量的重要变量,分别解释33个土壤中变量的81.3% 和80.5%。本研究结果为小麦实际生产中存在的Cd污染问题提供了指导,通过预测影响小麦Cd吸收的土壤主控因子,可为小麦的安全生产提供技术指导。
| [1] |
Zhou Y J, Jia Z Y, Wang J X, et al. Heavy metal distribution, relationship and prediction in a wheat-rice rotation system[J]. Geoderma, 2019, 354: 113886 DOI:10.1016/j.geoderma.2019.113886 (  0) 0) |
| [2] |
Wang C, Ji J F, Yang Z F, et al. Effects of soil properties on the transfer of cadmium from soil to wheat in the Yangtze River Delta region, China—a typical industry-agriculture transition area[J]. Biological Trace Element Research, 2012, 148(2): 264-274 DOI:10.1007/s12011-012-9367-z (  0) 0) |
| [3] |
中华人民共和国国家卫生和计划生有委员会, 国家食品药品监督管理总. 《食品安全国家标准食品中污染物限量》: GB 2762—2017[S]. 北京: 中国标准出版社, 2017.
(  0) 0) |
| [4] |
基于田块尺度的农田土壤和小麦籽粒镉砷铅污染特征及健康风险评价[J]. 环境科学, 2020, 41(6): 2869-2877 (  0) 0) |
| [5] |
Shi G L, Zhu S, Bai S N, et al. The transportation and accumulation of arsenic, cadmium, and phosphorus in 12 wheat cultivars and their relationships with each other[J]. Journal of Hazardous Materials, 2015, 299: 94-102 DOI:10.1016/j.jhazmat.2015.06.009 (  0) 0) |
| [6] |
Adams M L, Zhao F J, McGrath S P, et al. Predicting cadmium concentrations in wheat and barley grain using soil properties[J]. Journal of Environmental Quality, 2004, 33(2): 532-541 DOI:10.2134/jeq2004.5320 (  0) 0) |
| [7] |
Liu K, Lv J, He W, et al. Major factors influencing cadmium uptake from the soil into wheat plants[J]. Ecotoxicology and Environmental Safety, 2015, 113: 207-213 DOI:10.1016/j.ecoenv.2014.12.005 (  0) 0) |
| [8] |
Wu J, Norvell W A, Hopkins D G, et al. Spatial variability of grain cadmium and soil characteristics in a durum wheat field[J]. Soil Science Society of America Journal, 2002, 66(1): 268-275 DOI:10.2136/sssaj2002.2680 (  0) 0) |
| [9] |
Zhang S Z, Wang S X, Shan X Q, et al. Influences of lignin from paper mill sludge on soil properties and metal accumulation in wheat[J]. Biology and Fertility of Soils, 2004, 40(4): 237-242 (  0) 0) |
| [10] |
Zhao K L, Liu X M, Xu J M, et al. Heavy metal contaminations in a soil-rice system: Identification of spatial dependence in relation to soil properties of paddy fields[J]. Journal of Hazardous Materials, 2010, 181(1/2/3): 778-787 (  0) 0) |
| [11] |
Liu Y Z, Xiao T F, Baveye P C, et al. Potential health risk in areas with high naturally-occurring cadmium background in southwestern China[J]. Ecotoxicology and Environmental Safety, 2015, 112: 122-131 DOI:10.1016/j.ecoenv.2014.10.022 (  0) 0) |
| [12] |
Ran J, Wang D J, Wang C, et al. Heavy metal contents, distribution, and prediction in a regional soil-wheat system[J]. Science of the Total Environment, 2016, 544: 422-431 DOI:10.1016/j.scitotenv.2015.11.105 (  0) 0) |
| [13] |
Brus D J, de Gruijter J J, Römkens P F A M. Probabilistic quality standards for heavy metals in soil derived from quality standards in crops[J]. Geoderma, 2005, 128(3/4): 301-311 (  0) 0) |
| [14] |
生态环境部, 国家市场监督管理总局土壤环境质量农用地土壤污染风险管控标准(试行): GB 15618—2018[S]. 北京: 中国标准出版社, 2018.
(  0) 0) |
| [15] |
土壤农化分析(3版)[M].
中国农业出版社, 北京, 2000
(  0) 0) |
| [16] |
Zhang M K, Liu Z Y, Wang H. Use of single extraction methods to predict bioavailability of heavy metals in polluted soils to rice[J]. Communications in Soil Science and Plant Analysis, 2010, 41(7): 820-831 DOI:10.1080/00103621003592341 (  0) 0) |
| [17] |
大、小麦对镉的吸收、运输及在籽粒中的积累[J]. 麦类作物学报, 2002, 22(3): 82-86 DOI:10.3969/j.issn.1009-1041.2002.03.020 (  0) 0) |
| [18] |
Gray C W, Yi Z C, Munir K, et al. Cadmium concentrations in new Zealand wheat: Effect of cultivar type, soil properties, and crop management[J]. Journal of Environmental Quality, 2019, 48(3): 701-708 DOI:10.2134/jeq2018.12.0430 (  0) 0) |
| [19] |
Fairbrother A, Wenstel R, Sappington K, et al. Framework for metals risk assessment[J]. Ecotoxicology and Environmental Safety, 2007, 68(2): 145-227 DOI:10.1016/j.ecoenv.2007.03.015 (  0) 0) |
| [20] |
Wångstrand H, Eriksson J, Öborn I. Cadmium concentration in winter wheat as affected by nitrogen fertilization[J]. European Journal of Agronomy, 2007, 26(3): 209-214 DOI:10.1016/j.eja.2006.09.010 (  0) 0) |
| [21] |
Yu H Y, Liu C P, Zhu J S, et al. Cadmium availability in rice paddy fields from a mining area: The effects of soil properties highlighting iron fractions and pH value[J]. Environmental Pollution, 2016, 209: 38-45 DOI:10.1016/j.envpol.2015.11.021 (  0) 0) |
| [22] |
Guo F Y, Ding C F, Zhou Z G, et al. Effects of combined amendments on crop yield and cadmium uptake in two cadmium contaminated soils under rice-wheat rotation[J]. Ecotoxicology and Environmental Safety, 2018, 148: 303-310 DOI:10.1016/j.ecoenv.2017.10.043 (  0) 0) |
| [23] |
Li D Q, Li W Y, Lu Q, et al. Cadmium bioavailability well assessed by DGT and factors influencing cadmium accumulation in rice grains from paddy soils of three parent materials[J]. Journal of Soils and Sediments, 2018, 18(7): 2552-2561 DOI:10.1007/s11368-018-1950-2 (  0) 0) |
| [24] |
Hamid Y, Tang L, Yaseen M, et al. Comparative efficacy of organic and inorganic amendments for cadmium and lead immobilization in contaminated soil under rice-wheat cropping system[J]. Chemosphere, 2019, 214: 259-268 DOI:10.1016/j.chemosphere.2018.09.113 (  0) 0) |
| [25] |
Wang A S, Angle J S, Chaney R L, et al. Soil pH effects on uptake of Cd and Zn by Thlaspi caerulescens[J]. Plant and Soil, 2006, 281(1/2): 325-337 (  0) 0) |
| [26] |
Chen H Y, Yuan X Y, Li T Y, et al. Characteristics of heavy metal transfer and their influencing factors in different soil-crop systems of the industrialization region, China[J]. Ecotoxicology and Environmental Safety, 2016, 126: 193-201 DOI:10.1016/j.ecoenv.2015.12.042 (  0) 0) |
| [27] |
He Y B, Huang D Y, Zhu Q H, et al. A three-season field study on the in situ remediation of Cd-contaminated paddy soil using lime, two industrial by-products, and a low-Cd-accumulation rice cultivar[J]. Ecotoxicology and Environmental Safety, 2017, 136: 135-141 DOI:10.1016/j.ecoenv.2016.11.005 (  0) 0) |
| [28] |
Yang J L, Cang L, Wang X, et al. Field survey study on the difference in Cd accumulation capacity of rice and wheat in rice-wheat rotation area[J]. Journal of Soils and Sediments, 2020, 20(4): 2082-2092 DOI:10.1007/s11368-020-02587-2 (  0) 0) |
| [29] |
Wenzel W W, Blum W E H, Brandstetter A, et al. Effects of soil properties and cultivar on cadmium accumulation in wheat grain[J]. Zeitschrift Für Pflanzenernä hrung Und Bodenkunde, 1996, 159(6): 609-614 DOI:10.1002/jpln.1996.3581590613 (  0) 0) |
| [30] |
Bolan N S, Adriano D C, Duraisamy P, et al. Immobilization and phytoavailability of cadmium in variable charge soils. III. Effect of biosolid compost addition[J]. Plant and Soil, 2003, 256(1): 231-241 DOI:10.1023/A:1026288021059 (  0) 0) |
| [31] |
Welch R M, Norvell W A. Mechanisms of Cadmium Uptake, Translocation and Deposition in PlantsCadmium in Soils and Plants, 1999: 125–150.
(  0) 0) |
| [32] |
François M, Grant C, Lambert R, et al. Prediction of cadmium and zinc concentration in wheat grain from soils affected by the application of phosphate fertilizers varying in Cd concentration[J]. Nutrient Cycling in Agroecosystems, 2009, 83(2): 125-133 DOI:10.1007/s10705-008-9204-0 (  0) 0) |
| [33] |
Liu L N, Chen H S, Cai P, et al. Immobilization and phytotoxicity of Cd in contaminated soil amended with chicken manure compost[J]. Journal of Hazardous Materials, 2009, 163(2/3): 563-567 (  0) 0) |
| [34] |
Laing G D, Rinklebe J, Vandecasteele B, et al. Trace metal behaviour in estuarine and riverine floodplain soils and sediments: A review[J]. Science of the Total Environment, 2009, 407(13): 3972-3985 DOI:10.1016/j.scitotenv.2008.07.025 (  0) 0) |
| [35] |
Impellitteri C A, Lu Y F, Saxe J K, et al. Correlation of the partitioning of dissolved organic matter fractions with the desorption of Cd, Cu, Ni, Pb and Zn from 18 Dutch soils[J]. Environment International, 2002, 28(5): 401-410 DOI:10.1016/S0160-4120(02)00065-X (  0) 0) |
2. State Environmental Protection Key Laboratory of Soil Environmental Management and Pollution Control, Nanjing 210042, China;
3. Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2022, Vol. 54
2022, Vol. 54


