2. 中国科学院大学, 北京 100049
农药是农业生产中必不可少的生产资料,在作物病虫害防治以及增产增收方面起积极作用[1]。但是大量使用的农药通过雨水冲刷和地表径流等方式进入水体,给水生生态系统和人类健康造成严重威胁,已成为农业面源污染的重要来源之一[2]。阿特拉津(Atrazine, ATR)作为世界各地农业生产中使用最广的三嗪类除草剂,具有生物毒性,易溶于水,是地表水和地下水检出率最高的除草剂之一[3]。多菌灵(Carbendazim, CAR)是一种常见的苯并咪唑类杀菌剂,主要用于水稻、蔬菜和水果等病害防治,对鱼类等水生生物具有潜在风险[4]。啶虫脒(Acetamiprid, ACE)是一类被广泛使用的新烟碱类杀虫剂,具有神经毒性,可抑制乙酰胆碱酯酶的活性[5]。在水生态环境中,农药往往以复合污染物的形式存在。由于ATR、CAR和ACE等农药的大量使用,其残留污染物在水环境中检出频率高[6],且经常共存于农业水体中。我国流域地表水体中ATR、CAR和ACE等复合农药残留浓度范围分别在0.67 ~ 3.9、0.075 ~ 4.172、0.153 ~ 8.895 µg/L[7-9]。研究人员对俄亥俄州农田流域ATR污染的动态监测显示,单次降雨径流中ATR最高浓度达3.452 mg/L[3],均高于国内外水质污染控制标准,水体农药污染较为严重。因此,亟需寻求适用于农业水体复合农药污染物的控制技术。
生物质炭是生物有机材料在缺氧及低氧环境中经热裂解后的固体产物,具有廉价、多孔、富含氧官能团等特性,已广泛应用于土壤修复、温室气体减排和水环境治理,其对环境中氮磷、重金属、抗生素和农药等污染物均表现出良好的吸附性能[10-12]。目前关于生物质炭对农药吸附降解研究主要关注单一农药或同一类型农药。研究表明,杉木生物质炭对水中新烟碱类杀虫剂ACE具有良好的吸附效果,且吸附过程符合准二级吸附动力学方程[13];多次裂解再生后的FeCl3改性污泥生物质炭对水中吡虫啉的去除效率可达93%[14]。然而,生物质炭对水体多种类型农药复合污染物的吸附特性及机制研究报道较少。
此外,生物质炭的吸附性能与植物原材料和结构组成密切相关。生物质炭原料来源广泛,常见的主要是经济价值低、资源化利用水平差的秸秆、市政污泥、动物粪便和木材等[15]。木屑是典型农林废弃物,同时也是重要的生物质资源,木屑废弃物大多被焚烧或掩埋,造成了资源浪费和环境污染。利用木屑制备生物质炭是木屑废弃物再利用的出路之一。有关研究通过模拟计算,发现主要成分为木质素的生物质炭对农药分子乙草胺和ATR的吸附能力远远高于以纤维素和半纤维素为主的生物质炭[16]。因此,高木质素含量的木屑生物质炭可能具有高效去除水体农药污染的潜力。本研究选取木屑为原材料,在不同热解温度下制备木屑生物质炭,研究不同热解温度下制备的木屑生物质炭对水体ATR、CAR和ACE复合农药污染的吸附特性与机制,并探讨了pH与生物质炭投加量对其吸附农药的影响,以期为复合农药污染水体净化提供理论依据与技术支撑。
1 材料与方法 1.1 主要试剂与仪器试验所使用化学标准品阿特拉津(ATR,99%)、多菌灵(ACR,99%)、啶虫脒(ACE,99%),购买于Sigma-Aldrich公司;甲醇(色谱纯)购买于上海安谱实验科技股份有限公司。试验时,首先配置浓度为1 g/L的农药储备液,根据试验需要稀释后使用。ATR、CAR、ACE农药单体储备液配制:分别称取ACR、CAR、ACE标准品0.1 g,置100 ml容量瓶中,加5 ml的甲醇溶解并用去离子水定容至刻度,摇匀,得1 g/L的储备液。复合农药溶液配制:分别取1 ml ATR、CAR、ACE 1g/L的储备液于100 ml的容量瓶,用去离子水定容至刻度,摇匀,得10 mg/L的农药溶液,再稀释100倍,最终得到复合农药ATR(100 µg/L)、CAR(100 µg/L)和ACE(100 µg/L)溶液。农药基本性质见表 1。试验所用主要仪器包括:红外光谱仪(Nicolet iS10,尼高利仪器公司,美国)、超快速高分离液相色谱仪(Prominence UFLC XR,岛津仪器公司,日本)、高速离心机(Centrifuge 5430R,Eppendorf,德国)、恒温振荡器(ZQZY-75BN,上海怡赛科学仪器有限公司,中国)等。
|
|
表 1 ATR、CAR、ACE的基本性质 Table 1 Basic properties of ATR, CAR and ACE |
本试验所使用的生物质炭为木屑生物质炭,由江苏省农业科学院农业资源与环境研究所冯彦房副研究员提供。其中木屑生物质炭分别于500、700℃下高温热解制备得到,所制备的生物质炭分别记为MX500、MX700。制备方法如下:将原材料木屑放入马弗炉中,然后设置升温速率为5℃/min,并分别在500、700℃下保持8 h,最后同样以5℃/min的速率降至室温后研磨过筛(100目),将所得样品放在干燥器中,留存备用。
1.3 吸附试验 1.3.1 吸附动力学在50 ml锥形瓶中,分别加入0.05 g生物质炭和25 ml浓度为100 µg/L混合农药溶液,于室温25(±1)℃条件下,在恒温振荡器上以180 r/min的速率匀速振荡,再分别于0.25、0.5、2、4、6、10、16、24 h后,将吸附液上层倒入10 ml离心管中,加盖后在离心机中以8 000 r/min的转速离心20 min,然后取上清液过0.45 μm滤膜(聚醚砜PES微孔滤膜,下同)以去除残留的生物质炭,测定滤液中残留农药的浓度。最后,分别用准一级动力学方程(式(1))、准二级动力学方程(式(2))及颗粒内扩散方程(式(3))拟合两种木屑生物质炭对ATR、CAR、ACE的吸附过程。
| $ \ln \left[ {{q_{{\text{ee}}}} - {q_t}} \right] = \ln {q_{\text{e}}} - {K_1}t $ | (1) |
| $ {t \mathord{\left/ {\vphantom {t {{q_t}}}} \right. } {{q_t}}} = {1 \mathord{\left/ {\vphantom {1 {{K_2}q_t^2}}} \right. } {{K_2}q_t^2}} + {t \mathord{\left/ {\vphantom {t {{q_{\text{e}}}}}} \right. } {{q_{\text{e}}}}} $ | (2) |
| $ {q_t} = {K_{\text{a}}}{t^{0.5}} + C $ | (3) |
式中:qee:实际平衡吸附量,µg/g;qe:平衡吸附量拟合值,µg/g;qt:t时刻的吸附量,µg/g;K1:准一级动力学吸附速率常数,h–1;K2:准二级动力学吸附速率常数,g/(µg·h);Kd:颗粒内扩散速率常数,g/(µg·h0.5);t:吸附时间,h;C:截距,与边界层厚度有关。
1.3.2 吸附等温线将浓度分别为25、50、75、100、125、150、175 µg/L的ATR、CAR、ACE混合农药溶液25 ml倒入50 ml锥形瓶中,称取0.05 g木屑生物质炭依次加入到上述溶液中,溶液pH调节为5.0 ± 0.1,然后在室温下以160 r/min转速振荡24 h后,将吸附液上层倒入10 ml离心管中,加盖后在离心机中以8 000 r/min的转速离心20 min,然后过0.45 μm滤膜滤掉残留的生物质炭,测定滤液中残留农药的浓度。最后分别采用典型的Langmuir方程(式(4))和Freundlich方程(式(5))对等温吸附数据进行拟合。
| $ {q_{{\text{e1}}}} = {q_{\text{m}}}{K_{\text{L}}}{C_{\text{e}}}/\left( {1 + {K_{\text{L}}}{C_{\text{e}}}} \right) $ | (4) |
| $ {q_{{\text{e2}}}} = {K_{\text{F}}}{C_{\text{e}}}^{{1 \mathord{\left/ {\vphantom {1 n}} \right. } n}} $ | (5) |
式中:
① 取100 µg/L混合农药ATR、CAR、ACE溶液25 ml,倒入50 ml锥形瓶中,用0.1 mol/L NaOH或HCl将其pH调节为3、5、7、9和11;分别取0.05 g生物质炭置于50 ml的锥形三角瓶中,密封后在恒温振荡器(25℃,60 r/min) 内振荡24 h;之后,取上层10 ml溶液于15 ml离心管中,于离心机中以8 000 r/min离心10 min,再取上清液过0.45 μm滤膜以去除残留的生物质炭,测定滤液中残留农药的浓度。②分别称取0.025、0.05、0.075、0.10、0.15 g生物质炭,置于装有25 ml 100 µg/L混合农药的50 mL锥形三角瓶中,用0.1 mol/L NaOH或HCl将溶液的pH调至5.0 ± 0.1,密封后在恒温振荡器(25℃,60 r/min) 内振荡24 h,之后取上层10 ml溶液于15 ml离心管中,于离心机中以8 000 r/min离心10 min,再取上清液过0.45 μm滤膜以去除残留的生物质炭,测定滤液中残留农药的浓度。
1.4 分析方法采用全自动快速比表面和孔隙度分析仪(BET) (ASAP2020 HD88,Micromeritics,美国)测定生物质炭的比表面积、孔体积和平均孔径;采用土壤碳氮全自动分析仪(ZX_2019,Thermo Fisher Scientific (Bremen), 德国)测定生物质炭中C、H、O、N含量;采用pH漂移法[17]测定生物质炭的零点电荷(pHzpc);采用傅里叶变换红外光谱(FTIR)分别对MX500、MX700吸附ATR、CAR、ACE前后的特征官能团变化进行测量,扫描范围为4 000 ~ 400 cm–1,分辨率为0.4 cm–1,用纯KBr作为背景。
吸附前后农药浓度采用超快速高分离液相色谱仪测定,测定条件为:BEH-C18色谱柱(2.1 mm×100 mm,1.7 µm),流动相A为甲醇、B为水溶液。梯度洗脱条件:初始10% A;0 ~ 1 min,10% ~ 50% A;1 ~ 2 min,50% ~ 60% A;2 ~ 4 min,60% ~ 80% A;4 ~ 8 min,80% ~ 95% A;8 ~ 9 min,95% A;9 ~ 12 min,95% ~ 10% A;流速0.8 ml/min;柱温:35℃;进样量20 µl;吸收波长为245 nm。
2 结果与讨论 2.1 木屑生物质炭的结构特征MX700和MX500两种生物质炭的结构特征参数如表 2所示。从BET分析结果看,MX700的比表面积为5.45 m2/g,孔体积为0.102 cm3/g,分别是MX500的2.71倍和3.92倍,可能是随着热解温度升高,木屑中纤维素、木质素等成分被热解为生物油和合成气使孔隙结构更发达,这有利于提高MX700对农药的吸附容量。MX700与MX500的零点电荷分别为7.04和6.82。MX700相比MX500的H、O、N元素含量分别增加了73.7%、68.6% 和8.6%,而元素C含量基本不变,因此,H/C、O/C、(O+N)/C比增大,表明随着热解温度升高,木屑生物质炭表面的芳香度、亲水性和极性均增强[18]。
|
|
表 2 木屑生物质炭的理化特征 Table 2 Physicochemical properties of sawdust biochars |
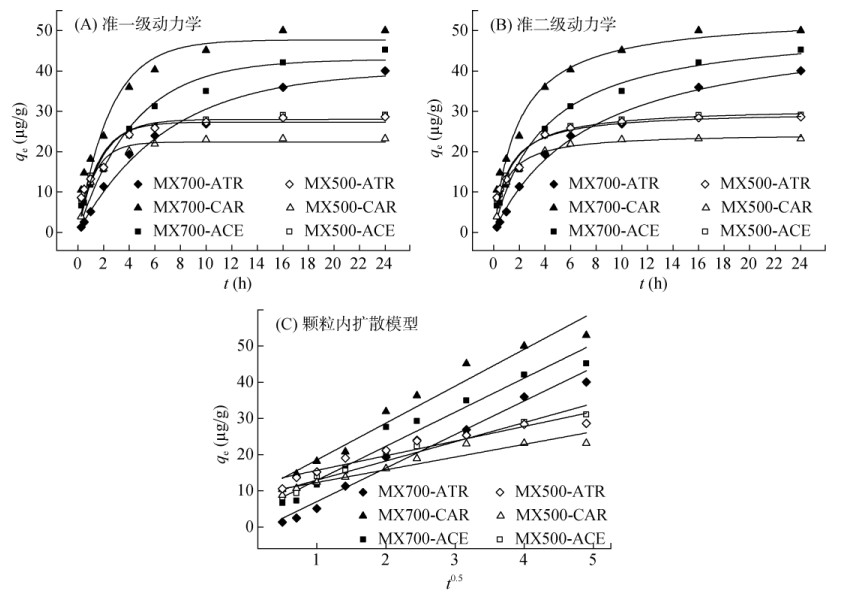
木屑生物质炭对农药的吸附量随时间的变化如图 1所示。采用准一级动力学方程、准二级动力学方程、颗粒内扩散方程对吸附结果进行拟合。从图 1可得,木屑生物质炭对农药的吸附过程可以分成3个阶段:快速吸附、缓慢吸附、吸附平衡。前4 h左右为快速吸附阶段,并且该阶段农药的去除率达整个过程的90% 左右;缓慢吸附阶段约持续到10 h,随后基本达到平衡。表面结合位点和传质驱动力是导致快速吸附过程的主要原因[19]。3种农药的吸附动力学过程基本相同,拟合参数如表 3所示。吸附平衡时,MX700对ATR、CAR、ACE的吸附量qe大于MX500,而MX700对3种复合农药ATR、CAR、ACE的吸附速率K1和K2均小于MX500,这可能是因为MX700具有更高的孔体积,农药在孔隙中需要更长的时间达到吸附平衡,总吸附容量也较大,而MX500的孔体积较小,农药能够较快地达到吸附平衡,导致吸附容量相对有限[13]。此外,MX700对ATR、CAR、ACE吸附的准二级动力学方程拟合参数(R2 = 0.998、0.970、0.987),高于准一级动力学方程拟合参数(R2 = 0.996、0.935、0.973)。类似地,MX500对ATR、CAR、ACE吸附的准二级动力学方程拟合参数(R2 = 0.963、0.975、0.950)也高于准一级动力学方程拟合参数(R2 = 0.811、0.943、0.911)。而且,准二级动力学方程计算出的理论值qe更加接近于试验测得的数据。因此,准二级动力学方程可以更准确地描述木屑生物质炭对水中复合农药ATR、CAR、ACE的吸附过程。准二级动力学方程假定了化学吸附是吸附过程的速率控制步骤[20],因此该吸附过程以化学吸附为主。这与生物质炭对单一农药的吸附特征类似,不同来源生物质炭对单一ATR、CAR和ACE的吸附均更符合准二级吸附动力学方程[20-22],因此,生物质炭对复合农药的动力学吸附规律可能与农药单体存在相似性和外推性。然而,本研究仅在3种农药单一浓度(100 µg/L)下开展研究,木屑生物质炭对其他浓度复合农药的吸附规律是否与农药单体一致,是否会存在竞争吸附还有待进一步研究。
|
图 1 木屑生物质炭对ATR、CAR、ACE的吸附动力学和颗粒内扩散模型 Fig. 1 Adsorption kinetics and intraparticle diffusion models for ATR, CAR and ACE adsorption onto sawdust biochar |
|
|
表 3 木屑生物质炭对ATR、CAR、ACE的吸附动力学和颗粒内扩散模型特征参数 Table 3 Adsorption kinetics and intraparticle diffusion parameters for ATR, CAR and ACE adsorption onto sawdust biochar |
为了进一步分析ATR、CAR、ACE在木屑生物质炭中的扩散过程,采用颗粒内扩散方程进行模拟,结果如图 1C所示。颗粒内扩散方程也能较好地模拟不同温度制备木屑生物质炭对ATR、CAR、ACE的吸附,MX700和MX500的拟合参数分别为R2 =(0.954、0.975、0.963和0.914、0.935、0.954。而且,木屑生物质炭对混合农药ATR、CAR、ACE的吸附曲线为一条不通过原点的直线,说明颗粒内扩散不是控制吸附过程的唯一因素,而是由外部液膜扩散和颗粒内扩散联合控制[23]。
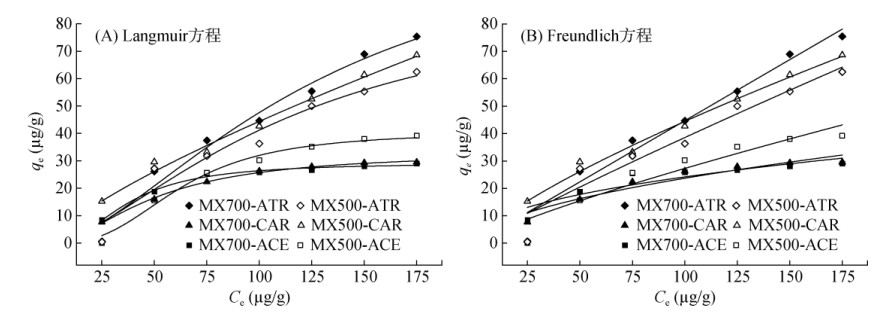
2.2.2 吸附等温线不同温度热解木屑生物质炭对3种农药的吸附等温线如图 2所示,Langmuir和Freundlich方程计算所得参数如表 4所示。可以看出,木屑生物质炭的平衡吸附量qe随着农药浓度增加而增大,MX700对ATR、CAR和ACE的平衡吸附量分别为58.5、73.4和63.6 µg/g,是MX500的1.92倍、1.87倍和2.30倍,与动力学试验一致。MX700对ATR、CAR、ACE的吸附等温线Langmuir方程拟合参数(R2 = 0.947、0.973、0.989)比Freundlich方程拟合参数(R2 = 0.933、0.961、0.987)略高。MX500对于ATR、CAR、ACE的吸附等温线Langmuir方程拟合参数(R2 = 0.997、0.997、0.990)也比Freundlich方程拟合参数(R2 = 0.922、0.897、0.851)高。可见,Langmuir方程比Freundlich方程对吸附过程的拟合程度更好,更适合用于描述木屑生物质炭对混合农药ATR、CAR、ACE的吸附过程。这也说明木屑生物质炭对ATR、CAR、ACE的吸附主要是单分子层吸附,以化学吸附为主[13],这与吸附动力学方程结果一致。以往玉米、小麦秸秆生物质炭及改性花生壳生物质炭和杉木生物质炭等对ATR、CAR和ACE农药单体的吸附等温线结果同样显示,Langmuir方程所得R2比Freundlich方程所得R2更大,表明Langmuir方程对3种单体农药吸附过程模拟的吻合程度更高[22-24],这说明生物质炭对复合农药的等温吸附拟合规律可能与农药单体相似。此外,在Langmuir模型中,MX700对农药吸附的KL值大于MX500,表明MX700对ATR、CAR和ACE的亲和力比MX500高。在Freundlich模型中,MX700和MX500的n值均大1,说明MX700和MX500对复合农药的吸附属于良性吸附[24]。
|
图 2 木屑生物质炭对ATR、CAR和ACE的吸附等温线 Fig. 2 Adsorption isotherms of ATR, CAR and ACE adsorption onto sawdust biochar |
|
|
表 4 木屑生物质炭对ATR、CAR和ACE的等温吸附方程参数 Table 4 Parameters of isothermal for adsorption of ATR, CAR and ACE onto sawdust biochar |
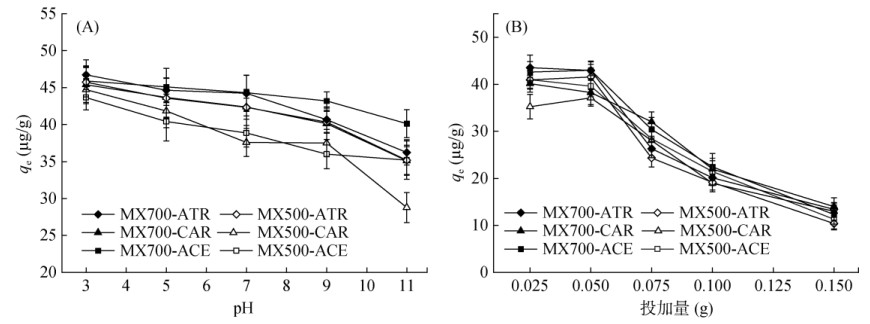
不同初始pH条件下木屑生物质炭对农药的吸附效果如图 3A所示,溶液pH对木屑生物质炭吸附3种复合农药的影响较大。在pH 3下,两种木屑生物质炭对ATR、CAR、ACE的吸附量均达43 µg/g以上。但在pH 11时,两种木屑生物质炭对ATR、CAR、ACE的吸附量低至约28 µg/g。可见,酸性环境木屑生物质炭对3种农药的吸附大于碱性条件,木屑生物质炭对ATR、CAR、ACE吸附对pH有依赖性,这与玉米秸秆生物质炭在酸性条件下对水中农药戊唑醇和稻瘟酰胺的吸附率最高、碱性条件最弱一致[18]。pH会影响溶液中农药的解离常数和生物质炭的表面电荷。本研究3种农药pKa值较小,分别为ATR 1.64、CAR 4.48、ACE –0.44。当溶液pH大于农药pKa值,农药主要以阴离子形式存在而携带负电,而MX700与MX500的零点电荷分别为7.04和6.82,因此当pH 3 ~ 7时,木屑生物质炭表面带正电荷,主要通过静电引力吸附ATR、CAR和ACE;由于3种农药分子中含有电负性较强的N和O原子,在酸性或中性条件下,MX700和MX500表面的含氧官能团会通过氢键作用力与这些原子基团结合使其吸附能力增强[14]。随着pH升高,木屑生物质炭表面所带有的正电荷数量减少导致吸附量逐渐降低。当pH 7 ~ 11时,木屑生物质炭表面均带负电,与ATR–、CAR–和ACE–的静电斥力会随pH的增加而增大,且体系OH–的浓度逐渐升高也会与带负电荷的农药分子产生竞争,导致生物质炭对复合农药的吸附效果减弱。
|
图 3 不同pH和生物质炭投加量对木屑生物质炭吸附ATR、CAR和ACE效果的影响 Fig. 3 Effects of initial pH and different dosage on adsorption of ATR, CAR and ACE onto sawdust biochar |
木屑生物质炭投加量对ATR、CAR、ACE的吸附效果如图 3B所示。随着生物质炭投加量增加,不同温度木屑生物质炭对3种农药吸附能力下降。添加0.05 g(2.0 g/L)时,MX700、MX500对于3种农药的吸附量均接近最大值,其中MX500对ATR、CAR、ACE吸附量分别为41.6、37.1、39.6 µg/g,MX700对ATR、CAR、ACE吸附量分别为43.0、38.3、42.9 µg/g。提高生物质炭投加量能增加生物质炭和水溶液中农药相互作用的吸附位点,从而增加生物质炭的吸附量。然而超过2.0 g/L投加量后,生物质炭吸附能力下降,可能是因为生物质炭过量容易导致吸附位点产生聚集,覆盖了表面部分吸附位点[19]。
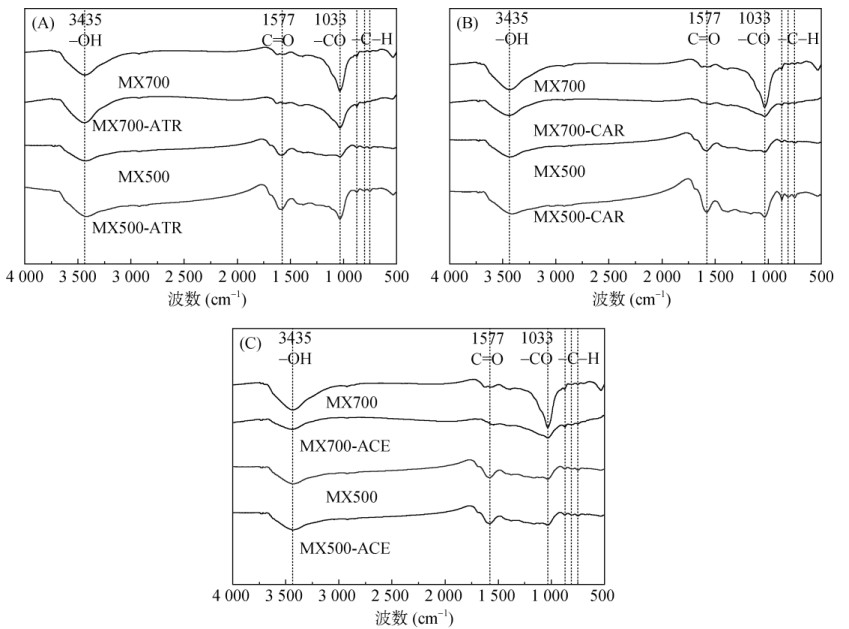
2.4 生物质炭吸附水溶液中ATR、CAR、ACE前后的FTIRMX700和MX500吸附3种农药前后的FTIR如图 4所示。把MX700和MX500吸附同一种农药的FTIR谱图叠放在一起比较可以看出,它们的谱图非常相似,其生物质炭含氧官能团的特征吸收峰的位置基本相同,表明其表面基团种类大致相同,但是特征吸收峰的数量存在差异,说明不同温度裂解的生物质炭含有的官能团的丰富程度不同。木屑生物质炭在波数为3 435 cm–1处的吸收峰主要是分子间氢键缔合的醇、酚的–OH伸缩振动产生的[22]。双键伸缩振动区1 600 ~ 1 750 cm–1之间的吸收峰为C=O和芳香环C=C的骨架伸缩振动产生[22]。波数约为1 000 ~ 1 600 cm–1处的振动带表明木屑生物质炭中含有C=O、C=C、C–O、C–H键[22]。波数约为1 000 ~ 650 cm–1处的振动带表明存在芳香族C–H键[25]。可见,MX700和MX500上主要的含氧官能团均为–OH、C=O、–COOH,且相比MX500,MX700主要在3 435 cm−1的–OH和1 033 cm−1的羧基中C–O所在峰的峰强有显著增加,表明高温使得木屑生物质炭表面的含氧官能团酚羟基和羧基数量增多。
|
图 4 木屑生物质炭吸附农药前后的FTIR图谱 Fig. 4 FTIR of sawdust biochar before and after adsorption of pesticides |
木屑生物质炭吸附3种农药前后–OH、C–O等含氧官能团处的峰强均减弱,说明以上含氧官能团参与了吸附过程,可能与3种农药分子ATR、CAR和ACE中的–NH基团(表 1)发生了氢键作用,而MX700表面的含氧官能团多于MX500,氢键作用增强,能解释为什么MX700农药吸附效果好于MX500,且氢键作用与上述pH影响试验分析的结果相对应。同时,MX700相比MX500,H/C增加,芳香性提高(表 2),这为木屑生物质炭与农药分子间发生π–π键相互作用提供了基础,且生物质炭吸附农药后在1 000 ~ 650 cm–1系列处芳香族C–H峰强也有减弱,表明3种农药分子的芳香环结构(表 1)与木屑生物质炭的芳香环结构之间易形成π–π键共轭结构[25],特别是MX700对ATR、CAR和ACE的吸附依赖于这种π–π键相互作用。其他研究也表明,松木木屑生物质炭的含氧官能团–OH、C–O等均参与了对水溶液中ATR的吸附作用[26]。FeCl3改性污泥生物质炭的含氧官能团–OH、C–O等均通过氢键作用力及π–π键相互作用力参与了对水溶液中吡虫啉的吸附作用[14]。
在农业生产中为了达到更好的病虫害防治效果,常常会将几种农药复配后使用或者同一时期先后施用,因此,农药污染物往往以除草剂、杀菌剂和杀虫剂混合物的形式共存在农业水体中[6-9]。目前较多研究集中在生物质炭对单一农药或同一类型农药的去除效果上[27-29],可能会限制生物质炭的应用范围。本研究探索了木屑生物质炭对典型除草剂ATR、杀菌剂CAR和杀虫剂ACE的联合去除效果,发现MX700对3种农药的去除率为85% ~ 96%,达到或超过以往生物质炭对单一农药的去除效果[27-29]。可见,相比其他来源生物质炭,木屑生物质炭可能具有更优越的农药复合污染物去除潜力,这可能与其表面大量的–OH、C–O等含氧官能团位点以及特定的木质素含量和孔径大小有关[16]。鉴于木屑生物质炭对氮磷等也有优异的吸附效果[30],木屑生物质炭有望成为减少农业面源污染物的一种有效修复剂。
3 结论本文通过研究木屑生物质炭对水溶液中ATR、CAR、ACE三种农药的吸附特性、影响因素及机制,证实了木屑生物质炭去除水体农业面源污染物ATR、CAR、ACE复合农药的可行性。研究发现,在温度700℃、pH 3.0、生物质炭投加量为2.0 g/L时,木屑生物质炭对3种混合农药的吸附量最大。MX700和MX500两种生物质炭对3种农药的吸附过程更符合准二级动力学方程(R2 > 0.950),主要以化学吸附为主;吸附等温数据更符合Langmuir方程(R2 > 0.947),主要以单层吸附为主。木屑生物质炭主要通过酚羟基和羧基等含氧官能团以及芳香环结构去除水中ATR、CAR和ACE。木屑生物质炭对农药的吸附机理包括静电作用力、氢键作用力及π–π键相互作用力。在农药浓度为100 µg/L下,木屑生物质炭对ATR、CAR和ACE三种复合农药的吸附效果与机理与该三种农药单体类似。
致谢: 感谢江苏省农业科学院农业资源与环境研究所冯彦房副研究员提供的木屑生物质炭,以及在本文写作过程中给予的意见和建议。
| [1] |
李正名. 我国农药化学进展[J]. 化学通报, 1992, 55(8): 31-35 (  0) 0) |
| [2] |
杨林章, 冯彦房, 施卫明, 等. 我国农业面源污染治理技术研究进展[J]. 中国生态农业学报, 2013, 21(1): 96-101 (  0) 0) |
| [3] |
Shipitalo M J, Owens L B. Atrazine, deethylatrazine, and deisopropylatrazine in surface runoff from conservation tilled watersheds[J]. Environmental Science & Technology, 2003, 37(5): 944-950 (  0) 0) |
| [4] |
徐铭阳, 卢家森, 孟献雨, 等. 多菌灵降解菌djl-6和啶虫脒降解菌D-2固体菌剂的研发[J]. 土壤, 2021, 53(2): 329-335 (  0) 0) |
| [5] |
周育, 庾琴, 侯慧锋, 等. 新型烟碱类杀虫剂啶虫脒研究进展[J]. 植物保护, 2006, 32(3): 16-20 DOI:10.3969/j.issn.0529-1542.2006.03.005 (  0) 0) |
| [6] |
沈俭龙, 纪明山, 田宏哲. 农药的水环境化学行为研究进展[J]. 农药, 2015, 54(4): 248-250 (  0) 0) |
| [7] |
徐雄, 李春梅, 孙静, 等. 我国重点流域地表水中29种农药污染及其生态风险评价[J]. 生态毒理学报, 2016, 11(2): 347-354 (  0) 0) |
| [8] |
周怡彤, 李清雪, 王斌, 等. 太湖流域西北部地表水中农药的污染特征及生态风险评价[J]. 生态毒理学报, 2020, 15(3): 171-183 (  0) 0) |
| [9] |
臧路. 我国主要流域新烟碱类农药时空分布、来源及生态风险[D]. 杭州: 浙江工业大学, 2019.
(  0) 0) |
| [10] |
Sun H J, Shi W M, Zhou M Y, et al. Effect of biochar on nitrogen use efficiency, grain yield and amino acid content of wheat cultivated on saline soil[J]. Plant, Soil and Environment, 2019, 65(No.2): 83-89 DOI:10.17221/525/2018-PSE (  0) 0) |
| [11] |
Wang Y Y, Liu Y D, Zhan W H, et al. Stabilization of heavy metal-contaminated soils by biochar: Challenges and recommendations[J]. The Science of the Total Environment, 2020, 729: 139060 DOI:10.1016/j.scitotenv.2020.139060 (  0) 0) |
| [12] |
Ngigi A N, Ok Y S, Thiele-Bruhn S. Biochar-mediated sorption of antibiotics in pig manure[J]. Journal of Hazardous Materials, 2019, 364: 663-670 DOI:10.1016/j.jhazmat.2018.10.045 (  0) 0) |
| [13] |
白金龙, 郭丽, 石冬瑾, 等. 杉木生物炭对水中啶虫脒和噻虫胺的吸附特性[J]. 环境工程学报, 2020, 14(12): 3339-3351 DOI:10.12030/j.cjee.202001002 (  0) 0) |
| [14] |
邹意义, 袁怡, 沈涛, 等. FeCl3改性污泥生物炭对水中吡虫啉的吸附性能研究[J]. 环境科学学报, 2021, 41(9): 3478-3486 (  0) 0) |
| [15] |
杨琼杰, 王聪慧, 任娜, 等. 生物质炭的制备和应用研究[J]. 应用化工, 2020, 49(7): 1835–1838, 1844 (  0) 0) |
| [16] |
汤家喜, 朱永乐, 刘悦, 等. 生物炭对农业面源污染物中农药分子的吸附性能研究[J]. 环境工程技术学报, 2020, 10(6): 1057-1062 (  0) 0) |
| [17] |
Shimabuku K K, Kearns J P, Martinez J E, et al. Biochar sorbents for sulfamethoxazole removal from surface water, stormwater, and wastewater effluent[J]. Water Research, 2016, 96: 236-245 DOI:10.1016/j.watres.2016.03.049 (  0) 0) |
| [18] |
孙彤, 李梦瑶, 吕学红, 等. 玉米秸秆生物炭对水中戊唑醇和稻瘟酰胺的吸附特性研究[J]. 山东农业科学, 2019, 51(6): 117-124 (  0) 0) |
| [19] |
马锋锋, 赵保卫, 刁静茹. 小麦秸秆生物炭对水中Cd2+的吸附特性研究[J]. 中国环境科学, 2017, 37(2): 551-559 (  0) 0) |
| [20] |
Peng Y, Fang W D, Krauss M, et al. Screening hundreds of emerging organic pollutants (EOPs) in surface water from the Yangtze River Delta (YRD): Occurrence, distribution, ecological risk[J]. Environmental Pollution, 2018, 241: 484-493 DOI:10.1016/j.envpol.2018.05.061 (  0) 0) |
| [21] |
Wang Y R, Miao J B, Saleem M, et al. Enhanced adsorptive removal of carbendazim from water by FeCl3-modified corn straw biochar as compared with pristine, HCl and NaOH modification[J]. Journal of Environmental Chemical Engineering, 2022, 10(1): 107024 DOI:10.1016/j.jece.2021.107024 (  0) 0) |
| [22] |
Lee Y G, Shin J, Kwak J, et al. Enhanced adsorption capacities of fungicides using peanut shell biochar via successive chemical modification with KMnO4 and KOH[J]. Separations, 2021, 8(4): 52 DOI:10.3390/separations8040052 (  0) 0) |
| [23] |
Afzal M Z, Sun X F, Liu J, et al. Enhancement of ciprofloxacin sorption on chitosan/biochar hydrogel beads[J]. Science of the Total Environment, 2018, 639: 560-569 DOI:10.1016/j.scitotenv.2018.05.129 (  0) 0) |
| [24] |
Zhao L L, Yang F, Jiang Q, et al. Characterization of modified biochars prepared at low pyrolysis temperature as an efficient adsorbent for atrazine removal[J]. Environmental Science and Pollution Research International, 2018, 25(2): 1405-1417 DOI:10.1007/s11356-017-0492-2 (  0) 0) |
| [25] |
季雪琴, 吕黎, 陈芬, 等. 秸秆生物炭对有机染料的吸附作用及机制[J]. 环境科学学报, 2016, 36(5): 1648-1654 (  0) 0) |
| [26] |
ALBERTO BENTO CHARRUA, 王航, 吕春欣, 等. 不同温度下松木生物质炭对阿特拉津的吸附性能研究[J]. 生态环境学报, 2015, 24(3): 505-510 (  0) 0) |
| [27] |
Voorhees J P, Phillips B M, Anderson B S, et al. Comparison of the relative efficacies of granulated activated carbon and biochar to reduce chlorpyrifos and imidacloprid loading and toxicity using laboratory bench scale experiments[J]. Bulletin of Environmental Contamination and Toxicology, 2020, 104(3): 327-332 DOI:10.1007/s00128-020-02790-4 (  0) 0) |
| [28] |
Ćwieląg-Piasecka I, Medyńska-Juraszek A, Jerzykiewicz M, et al. Humic acid and biochar as specific sorbents of pesticides[J]. Journal of Soils and Sediments, 2018, 18(8): 2692-2702 DOI:10.1007/s11368-018-1976-5 (  0) 0) |
| [29] |
Suo F Y, You X W, Ma Y Q, et al. Rapid removal of triazine pesticides by P doped biochar and the adsorption mechanism[J]. Chemosphere, 2019, 235: 918-925 DOI:10.1016/j.chemosphere.2019.06.158 (  0) 0) |
| [30] |
孟依柯, 王媛, 汪传跃. 木屑生物炭在雨水径流中的氮磷淋出和吸附特性[J]. 环境科学, 2021, 42(9): 4332-4340 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China
 2022, Vol. 54
2022, Vol. 54