2. 西北农林科技大学西北农业部植物营养与农业环境重点实验室, 陕西杨凌 712100;
3. 西北农林科技大学黄土高原土壤侵蚀与旱地农业国家重点实验室, 陕西杨凌 712100;
4. 中国科学院水利部水土保持研究所, 陕西杨凌 712100
土壤碳库是陆地生态系统中最大的碳库,可分为有机碳库和无机碳库,二者之间的转化是全球碳循环的重要环节[1-2]。无机碳库能有效缓解大气CO2浓度的升高,对全球碳储存的贡献日益显著[3]。在占据全球陆地面积40% 以上的干旱地区[4],无机碳存量比有机碳高1倍~ 9倍[5-6]。有学者发现在半干旱地区土壤剖面2 m处无机碳含量是有机碳含量的17倍[7]。与有机碳研究相比,对无机碳的特性及固碳能力研究仍然比较缺乏[8-9]。
碳酸钙是土壤无机碳库的主要存在形式。土壤碳酸钙根据来源可以分为3类:①地质来源,即继承自成土母质;②生物来源,即动植物残体含有的碳酸钙;③形成于成土过程,即上述碳酸钙溶解后重新沉淀析出形成的碳酸钙[10]。碳酸钙在不同地区的存在形态不同,如在半淋溶地区多以假菌丝形态存在于土壤结构体表面;在干旱半干旱地区,碳酸钙在土壤中呈现晶状、斑块状及结核状。碳酸钙结核即为CaCO3在CO2作用下生成Ca(HCO3)2,后者随水分在黄土母质中聚集,水分蒸发后,CO2析出,CaCO3重新沉积而形成[11]。碳酸钙含量高的地区土壤均偏碱性[12]。在石灰性土壤中,因其具有较高的碳酸钙含量,能比酸性土壤更好地形成团粒结构。碳酸钙对土壤酸碱性有一定的缓冲作用,可使其pH维持在7.5 ~ 8.5。除此之外,碳酸钙对于控制磷的活性(固化)、协调土壤CO2平衡、控制土壤孔隙度及大小、防治病虫害等方面有着重要的影响[13-14]。
碳酸钙是黄土母质发育土壤中的重要胶结物质。郭玉文等[15]发现在黄土高原土壤团粒表面及内部都分布碳酸钙。团粒平均重量直径越大,碳酸钙含量越高;其中少数碳酸钙大颗粒镶嵌在矿物之间起骨架作用,多数碳酸钙小颗粒附着在矿物表面。碳酸钙通过有机-无机碳的转化影响团聚体的形成,其在产生次生碳酸盐过程中溶出的Ca2+可与土壤中的黏粒形成团聚体[16-17]。Virto等[18]通过激光衍射粒度仪分析两种碳酸盐土壤去除碳酸钙的研究发现,碳酸钙去除后,土壤中粒径为30 μm和37 μm左右的团聚体消失,而粒径为4 μm和10 μm的团聚体增多,表明碳酸钙对大团聚体的形成起到重要的胶结作用。然而,目前有关碳酸钙产生胶结作用的微观机理还有待深入研究。
研究发现方解石具有胶体特性,其在pH 5 ~ 11范围内表面带负电荷[19]。电荷数量受到溶液pH、电解质类型和浓度及CO2分压的影响,此外还发现Mg2+和CO32−含量都对方解石的表面性质有影响[20]。然而土壤环境中的碳酸钙表面性质及胶体特性如何尚不得知,这阻碍了人们对碳酸钙胶结作用的深入认识。本文以碳酸盐褐土中采集的碳酸钙结核为研究对象,对其粒径大小、表面特性及胶体稳定性进行研究。研究结果将有助于深入理解碳酸钙通过胶结作用促进土壤团聚体形成的微观机理。
1 材料与方法 1.1 样品采集碳酸盐褐土采自陕西省咸阳市淳化县。褐土是关中平原最主要的地带性土壤,其亚类主要包括塿土、淋溶褐土、典型褐土和碳酸盐褐土。碳酸盐含量是区分褐土亚类的重要参数[21]。碳酸盐褐土剖面通体均分布有灰白色碳酸钙沉淀。本文所采集的碳酸盐褐土剖面中,其0 ~ 20 cm为淋溶层,pH为8.38,碳酸钙含量为181.94 g/kg。碳酸钙结核采自40 ~ 100 cm的钙积层,将碳酸钙结核带回实验室,于通风处自然风干研磨后过100目筛。碳酸钙结核中碳酸钙与黏土矿物紧密结合,成分较为复杂。为了系统了解碳酸钙的表面特性,本文选用工业纳米碳酸钙与褐土碳酸钙结核进行对比研究。工业纳米碳酸钙购自山西芮城华纳纳米材料有限公司。
1.2 碳酸钙胶体的分散性研究目前常用的细颗粒分离方法分为物理分散法和化学分散法[22]。物理分散法,或高速离心法,是目前分离土壤纳米颗粒的常用方法[23-24]。物理分散手段除了高速离心外,还包括球磨等手段。第二种为化学分散法,即添加化学分散剂[22]。由于所购买的工业纳米碳酸钙直接分散在水中时,仅悬浮在表层水面,因此通过加入质量分数为10% 的六偏磷酸钠进行预处理。六偏磷酸钠解离带电后吸附在胶体颗粒表面提高颗粒表面电位,使颗粒之间的静电斥力增大,从而增大颗粒稳定性[25]。所制备的工业纳米碳酸钙悬液整体呈淡乳白色,表明颗粒均匀分散在水溶液中。
采用高速离心法提取褐土碳酸钙结核纳米颗粒。试验称取50 g碳酸钙结核于500 ml蒸馏水中,用细胞破碎仪在450 W功率下超声1 h。超声结束后将悬液倒入5 L烧杯并加蒸馏水至5 L,用自动搅拌机搅拌1 h。充分搅拌后的悬液过300目筛后离心。根据Stokes定律求得离心机设置参数。
| $ t = \frac{{{\mathtt{η}}\log \left( {{R_2}/{R_1}} \right)}}{{3.81{C^2}{r^2}\Delta {\text{d}}}} $ | (1) |
式中:R1为液面至轴心的距离(cm);R2为颗粒沉降处至轴心的距离(cm);C为离心机每秒转速(r/s);r为土壤颗粒半径(cm);d为土壤颗粒密度与水介质密度之差(1.71 g/cm3);η为25 ℃时水的粘滞系数,0.008 39 g/(cm∙s)。在转速为9 500 r/min条件下离心9 min 6 s可获得包含直径小于100 nm碳酸钙结核的悬液,将其保存在4 ℃条件下备用,并将部分悬液经冷冻干燥后进行性质表征。
同时采用化学分散法对碳酸钙结核进行处理,使得其与工业纳米碳酸钙颗粒的表面改性处理相同。首先使用行星球磨仪(MITR-YXQM-4L, 长沙)对碳酸钙结核进行球磨使其颗粒变细,条件为球磨5 min,休息5 min,时长为4 h[26]。然后将球磨后的碳酸钙配制成悬液,并加入质量分数为10% 的六偏磷酸钠。使用磁力搅拌器搅拌30 min,再用细胞破碎仪在450 W功率下超声20 min,可获得经化学分散剂处理的褐土碳酸钙结核胶体悬液。
为排除胶体和纳米颗粒悬液中含有的可溶性离子对试验的干扰,采用火焰原子吸收分光光度法(美国, PinAAciie, 900F)测定3种碳酸钙胶体悬浮液中K+、Na+、Ca2+、Mg2+浓度。
1.3 碳酸钙胶体的基本性质表征和表面电化学性质计算采用X射线衍射仪(ZX 2012, UItima IV, 日本)测定上述两种褐土碳酸钙结核细颗粒样品和工业纳米碳酸钙的矿物组成。将干燥的样品粉末不经其他前处理,直接上机测定。测试条件:Cu靶Kα射线,入射波长为λ = 0.154 nm,扫描速度1°/min,扫描范围2° ~ 60°。采用动态光散射仪(NanoBrook Omni, Brookhaven公司, 美国)在入射波长为635 nm和散射角90°条件下,测定其初始粒径。采用BET-N2∙SA仪器(ASAP. 2460, Micromeritics仪器, 上海)测定比表面积。采用zeta电位分析仪(ZetaPALS, Brookhaven公司, 美国)测定表面电位。基于Gouy-Chapmann理论[27],3种碳酸钙样品的表面电荷密度可通过公式(2)计算获得:
| $ \sigma = \sqrt {8{\mathtt{ε}}{{\mathtt{ε}}_0}{c_0}{\rm{RT}}} \sinh \left( {\frac{{Z{\rm{F}}\zeta }}{{2{\rm{RT}}}}} \right) $ | (2) |
式中:σ为表面电荷密度(C/m2);ε为相对介电常数,水的相对介电常数为78.54;ε0为真空下介电常数,8.85 × 10−12 C2/(J·m);с0为电解质浓度(mol/m3);R为气体常数,8.314 J/(mol·K);T为绝对温度,298 K;Z为原子价;F为法拉第常数,96 485 C/mol;ζ为zeta电位(V)。
3种碳酸钙样品的表面电荷数量可通过公式(3)获得:
| $ Q{\text{ = 1}}{{\text{0}}^5}\frac{{S\sigma }}{{\text{F}}} $ | (3) |
式中:Q为表面电荷数量(cmol/kg);S为比表面积(m2/g)。
1.4 碳酸钙胶体的稳定性研究在入射波长为635 nm,散射角为90°的条件下利用动态光散射仪测定3种碳酸钙样品在NaCl和CaCl2溶液中的凝聚动力学曲线。测试颗粒浓度为50 mg/L,悬液pH为8.0 ± 0.1(此时悬液中CO2溶解量可忽略不计)。仪器每隔2 min自动记录一次有效粒径,监测30 min后获得一条凝聚动力学曲线,设计不同浓度电解质后即可获取一系列胶体颗粒凝聚动力学曲线。每个样品重复3次。通过公式(4)求出粘结系数α,α表示颗粒碰撞的结合几率。将α与电解质浓度采用“对数-对数”作图所得转折点即临界聚沉浓度。
| $ \alpha {\text{ = }}\frac{1}{W} = \frac{{{k_{11}}}}{{{{\left( {{k_{11}}} \right)}_{{\text{fast}}}}}} = \frac{{\frac{1}{{{N_0}}}{{\left( {\frac{{{\text{d}}{D_{\text{h}}}\left( t \right)}}{{{\text{d}}t}}} \right)}_{t \to 0}}}}{{\frac{1}{{{{\left( {{N_0}} \right)}_{{\text{fast}}}}}}{{\left( {\frac{{{\text{d}}{D_{\text{h}}}\left( t \right)}}{{{{\text{d}}_t}}}} \right)}_{t \to 0, {\text{fast}}}}}} $ | (4) |
式中:Dh为颗粒的有效直径(nm);t为时间(min);N0为颗粒密度(单位m3的颗粒数量);k11为慢速凝聚阶段凝聚速率(m3/s);(k11)fast为快速凝聚阶段凝聚速率(m3/s);α为粘结系数;W为稳定率。
通过上述凝聚动力学曲线计算所形成凝聚体的分形维数。分形维数表示凝聚体的结构特征,它是描述质量随长度变化的物理量[28]。对于给定的电解质,颗粒在快速凝聚阶段的粒径增长曲线可用公式(5)拟合,而后用df=1/a求得凝聚体的分形维数。
| $ D_{\mathrm{h}}(t)=\mathrm{b} \times t^{\mathrm{a}}+D_0 $ | (5) |
式中:D0为初始有效直径(nm);系数a和b为随凝聚曲线变化的常数。
2 结果与分析 2.1 碳酸钙胶体的基本性质本文通过两种方法对褐土碳酸钙结核和工业纳米碳酸钙进行提取,获得了3种碳酸钙胶体,其颗粒直径范围见表 1。通过添加六偏磷酸钠获得工业纳米碳酸钙颗粒,其平均直径为98.50 nm;粒度分布曲线表明中值粒径为94.36 nm,D10和D90值分别为55.60 nm和160.14 nm。通过高速离心法获得褐土碳酸钙结核纳米颗粒,其平均直径为88.01 nm,与工业纳米碳酸钙的直径大小接近。采用六偏磷酸钠处理褐土碳酸钙结核发现,化学分散法只能获得褐土碳酸钙结核胶体,其平均直径为224.24 nm,中值粒径为133.26 nm,表明褐土碳酸钙结核胶体的粒径分布曲线为偏态分布,且大颗粒占比较少。但由于颗粒所反射的光强与其颗粒直径大小成六次方关系,所以大颗粒的存在显著影响平均直径大小,因此褐土碳酸钙结核胶体的平均直径大于中值粒径。表 1说明3种样品均属于胶体范畴,而样品2和3同属于纳米材料范围。从多分散度可以看出,3种胶体颗粒均属于多分散体系,工业纳米碳酸钙的多分散度小于其他两者,表明工业纳米碳酸钙粒径分布相对更均匀。褐土碳酸钙结核胶体和工业纳米碳酸钙的比表面积相接近,而褐土碳酸钙结核纳米颗粒的比表面积是其他两种胶体的两倍多,这与其更小的颗粒直径有关。
|
|
表 1 三种碳酸钙胶体的粒径分布特征和比表面积 Table 1 Particle size distributions and specific surface areas of three calcium carbonate colloids |
褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒与工业纳米碳酸钙的矿物组成如表 2所示。褐土碳酸钙结核胶体主要矿物类型为方解石和石英,其含量(质量分数)分别为70.3% 和16.0%;其次为长石和伊利石,含量分别为8.1% 和4.5%。褐土碳酸钙结核纳米颗粒主要矿物类型为方解石和伊利石,含量各占48% 和45%。伊利石为次生矿物,石英和长石为原生矿物。与褐土碳酸钙结核胶体相比,褐土碳酸钙结核纳米颗粒的伊利石含量较多,平均直径也更小(表 1)。与褐土碳酸钙结核胶体和褐土碳酸钙结核纳米颗粒相比,工业纳米碳酸钙矿物组成单一,为纯方解石。3种碳酸钙胶体中的可溶性盐离子浓度均较低,而褐土碳酸钙结核纳米颗粒悬液中各离子的浓度相对较高,这可能是由于其粒径略小(表 1)而溶解性略高。
|
|
表 2 三种碳酸钙胶体的矿物组成(质量分数,%)及阳离子含量(mmol/L) Table 2 Mineral compositions (mass percentage, %) and cation contents (mmol/L) of three calcium carbonate colloids |
3种碳酸钙胶体颗粒在不同pH条件下的zeta电位变化如图 1所示。碳酸钙属于难溶性矿物,溶液pH影响溶液中的离子形态。在pH 6 ~ 9范围内,溶液中的阴离子主要以HCO3−形式存在,当溶液pH过低时,会释放出CO2;当溶液pH更高时,主要以CO32−形式存在[29]。本文主要选取pH 6 ~ 9范围内进行研究。总体来说,在不同pH条件下,褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒及工业纳米碳酸钙的zeta电位均为负值,且其绝对值随pH增大而增大,表明3种胶体表面的负电荷随溶液pH升高而增多[30]。3种碳酸钙胶体都表现为可变电荷表面。

|
图 1 三种碳酸钙胶体zeta电位随溶液pH的变化 Fig. 1 Zeta potentials of three calcium carbonate colloids changing with solution pH |
研究表明,碳酸钙表面同时存在羟基化的阳离子型位点 > CaOH0和质子化的阴离子型位点 > CO3H0[31]。> CaOH0与H+结合形成 > CaOH2+,使得碳酸钙表面带正电荷;> CaOH0与OH−结合形成 > CaO−,使其表面带负电荷。> CO3H0可与OH−结合形成 > CO3−,导致负电荷表面。因此,当溶液pH增大时,工业纳米碳酸钙表面逐渐与溶液中的OH−结合,而使得其表面负电荷逐渐增大。对褐土碳酸钙结核胶体和褐土碳酸钙结核纳米颗粒而言,其除了含有方解石,还含有一定数量的石英和伊利石(表 2)。石英是一种表面携带负电荷的原生土壤矿物[32],其表面电荷数量较小;而伊利石是恒电荷表面,其电荷数量不受pH的影响[33]。所以碳酸钙胶体主要是其成分碳酸钙的表面电荷伴随pH发生变化。在褐土碳酸钙结核纳米颗粒中,伊利石的含量最高,其电荷可变性最弱。
从图 2可得,3种碳酸钙胶体的表面电荷密度在不同pH下的变化量遵循:工业纳米碳酸钙 > 褐土碳酸钙结核胶体 > 褐土碳酸钙结核纳米颗粒。石英的电荷密度和电荷可变性均小于方解石。由于褐土碳酸钙结核纳米颗粒具有较大的比表面积(表 1),使得其表面电荷数量大于其他两者。Vdović[34]通过研究不同来源的天然碳酸钙发现,在pH 6 ~ 11范围内,碳酸钙表面始终带负电荷,如科奇亚克碳酸钙(湖底沉积物)的电位变化为从−14.2 mV降为−31.0 mV;亚德兰碳酸盐(海底沉积物)从−20.7 mV降为−28.7 mV;帕拉维亚碳酸盐(石灰岩)从−16.2 mV降为−29.9 mV;米尔纳碳酸盐(石灰岩)从−4.2 mV降为−17.2 mV。这表明,不同类型天然碳酸钙的zeta电位高低不同,这与其本身结合的黏土矿物种类等有关,同时表明电位变化程度受pH影响的程度也不同,但都随pH的增大而碳酸钙表面负电荷增多。本文所研究的褐土碳酸钙结核表面性质变化趋势也与之相似。

|
图 2 三种碳酸钙胶体电荷密度(A)和电荷数量(B)随溶液pH的变化 Fig. 2 Charge density (A) and charge number (B) of three calcium carbonate colloids changing with solution pH |
图 3是3种碳酸钙胶体在不同浓度NaCl和CaCl2溶液中的电位变化曲线。从图中可以看出,随着溶液Na+或Ca2+浓度增大,3种碳酸钙胶体的zeta电位绝对值逐渐减小[35]。在NaCl溶液中,褐土碳酸钙结核胶体电位绝对值最大,工业纳米碳酸钙与褐土碳酸钙结核纳米颗粒的电位相差较小。在CaCl2溶液中,三者电位绝对值大小遵循:工业纳米碳酸钙 > 褐土碳酸钙结核纳米颗粒 > 褐土碳酸钙结核胶体。在褐土碳酸钙结核胶体悬液中,Na+从200 mmol/L增至1 000 mmol/L,其zeta电位从−20.79 mV变为−6.41 mV;Ca2+从0.5 mmol/L增至3 mmol/L,其zeta电位从−12.45 mV变为−6.96 mV;褐土碳酸钙结核纳米颗粒悬液中Na+从20 mmol/L增至250 mmol/L,其zeta电位从−25.32 mV变为−7.50 mV;Ca2+从0.5 mmol/L增至1.6 mmol/L,其zeta电位从−18.29 mV变为−13.25 mV。这表明Ca2+压缩双电层的能力远大于Na+,较小浓度的Ca2+即可使颗粒zeta电位绝对值显著下降。

|
图 3 三种碳酸钙胶体在NaCl(A)和CaCl2溶液(B)中的zeta电位 Fig. 3 Zeta potential values of three calcium carbonate colloids in NaCl (A) and CaCl2 (B) solutions |
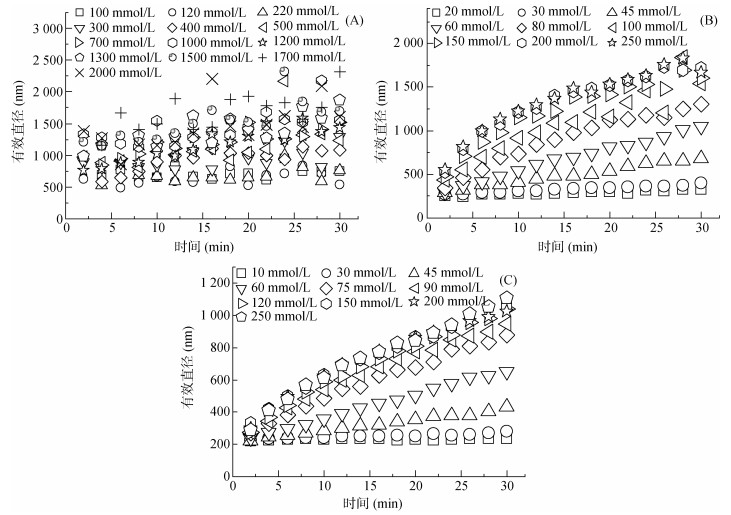
图 4为褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒及工业纳米碳酸钙在NaCl溶液中的凝聚过程。从图中可看出,3种碳酸钙胶体的凝聚过程分为反应控制扩散阶段(慢速凝聚阶段)和扩散控制凝聚阶段(快速凝聚阶段)。在反应控制扩散阶段,颗粒之间存在排斥力,并不是每一次碰撞后都能产生粘结。褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙分别在100 ~ 500、20 ~ 80和10 ~ 75 mmol/L的NaCl溶液中,其粒径随时间大致呈线性增长,颗粒凝聚速率受电解质浓度的影响。随电解质浓度增加,颗粒进入扩散控制凝聚阶段,颗粒间排斥力消失,每一次碰撞都能使颗粒粘结,此时凝聚速率不再受电解质浓度的影响[36]。褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙在700 ~ 2 000、100 ~ 250和90 ~ 250 mmol/L NaCl溶液中属于扩散控制凝聚阶段。
|
(A. 褐土碳酸钙结核胶体;B. 褐土碳酸钙结核纳米颗粒;C. 工业纳米碳酸钙) 图 4 三种碳酸钙胶体在NaCl溶液凝聚动力学曲线 Fig. 4 Aggregation curves of three calcium carbonate colloids in NaCl solution |
3种碳酸钙胶体在CaCl2溶液中的凝聚动力学曲线如图 5所示。碳酸钙胶体在Ca2+溶液中的凝聚趋势与在Na+溶液中相似,同样可以分为反应控制扩散阶段和扩散控制凝聚阶段。褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙分别在0.5 ~ 2.0、0.4 ~ 1.1和0.4 ~ 1.5 mmol/L CaCl2溶液中属于反应控制扩散阶段,在3.0 ~ 15.0、1.2 ~ 2.0和1.6 ~ 2.6 mmol/L CaCl2溶液中属于扩散控制凝聚阶段。

|
(A. 褐土碳酸钙结核胶体;B. 褐土碳酸钙结核纳米颗粒;C. 工业纳米碳酸钙) 图 5 三种碳酸钙胶体在CaCl2溶液凝聚动力学曲线 Fig. 5 Aggregation curves of three calcium carbonate colloids in CaCl2 solution |
褐土碳酸钙结核胶体在Na+体系中形成凝聚体的最大直径在2 200 nm左右,在Ca2+体系中最大凝聚体粒径在1 800 nm左右。褐土碳酸钙结核纳米颗粒在Na+和Ca2+体系中的最大凝聚体粒径均为1 800 nm左右,而工业纳米碳酸钙为1 200 nm左右。褐土碳酸钙结核胶体所形成的凝聚体粒径最大,可能是因为其初始粒径最大(表 1),在加入电解质溶液后,形成了较大的凝聚体。同时,从图 4和图 5中还可以看到,褐土碳酸钙结核胶体的粒径增长曲线波动性最强,而工业纳米碳酸钙的曲线波动性最弱,这与体系的多分散度有关(表 1)。工业纳米碳酸钙的颗粒直径较小,且分布比较均匀,因此其粒径增长曲线波动性小。
根据公式(5)可以得到在样品添加NaCl电解质后,褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙在快速凝聚阶段的分形维数分别为2.38、2.07和1.34,在Ca2+体系中的分形维数分别为2.32、1.84和1.20。扩散控制凝聚阶段的典型分形维数df为1.8左右[36]。碳酸钙胶体在CaCl2溶液中所形成的凝聚体结构更为疏松。褐土碳酸钙结核胶体的凝聚体结构最致密,工业纳米碳酸钙形成的凝聚体结构更疏松。这可能是由于褐土碳酸钙结核胶体和褐土碳酸钙结核纳米颗粒的直径分布范围较宽(表 1),小颗粒可以填充在大颗粒形成凝聚体的骨架中,从而导致与工业纳米碳酸钙相比,土壤碳酸钙所形成的凝聚体更为致密。
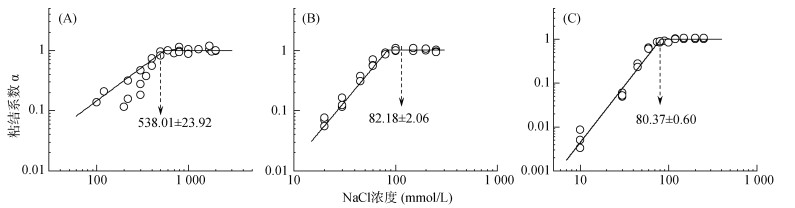
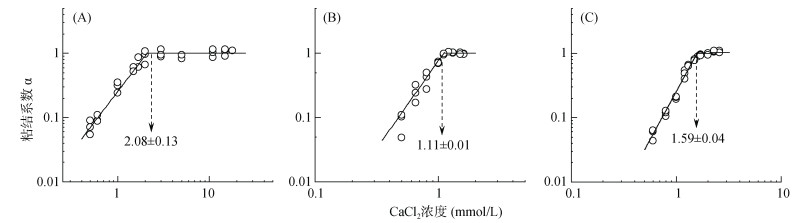
2.4 碳酸钙胶体的稳定性图 6为褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙在NaCl溶液中的临界聚沉浓度值,三者在NaCl溶液中临界聚沉浓度值分别为538.01、82.18和80.37 mmol/L。根据表 2可知3种碳酸钙胶体本身释放的可溶性离子含量是有限的,对测定的临界聚沉浓度值影响相当小。通过对比可以发现褐土碳酸钙结核胶体的临界聚沉浓度值几乎是其他两者的6倍,在Na+体系中的稳定性最强;褐土碳酸钙结核纳米颗粒的稳定性略大于工业纳米碳酸钙,与上述zeta电位测定的结果一致。图 7为褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙在CaCl2溶液中测定的临界聚沉浓度值,分别为2.08、1.11和1.59 mmol/L。褐土碳酸钙结核胶体、褐土碳酸钙结核纳米颗粒和工业纳米碳酸钙的临界聚沉浓度值在两种体系中比值分别为2−8.01、2−6.21和2−5.66,与舒尔策-哈迪规则的预测结果接近[37]。
|
(A. 褐土碳酸钙结核胶体;B. 褐土碳酸钙结核纳米颗粒;C. 工业纳米碳酸钙) 图 6 三种碳酸钙胶体在NaCl溶液中的临界聚沉浓度值 Fig. 6 Critical coagulation concentrations of three calcium carbonate colloids in NaCl solution |
|
(A. 褐土碳酸钙结核胶体;B. 褐土碳酸钙结核纳米颗粒;C. 工业纳米碳酸钙) 图 7 三种碳酸钙胶体在CaCl2溶液中的临界聚沉浓度值 Fig. 7 Critical coagulation concentrations of three calcium carbonate colloids in CaCl2 solution |
通过对比同种胶体颗粒在Na+和Ca2+体系的临界聚沉浓度值可以发现,其在Na+溶液中的临界聚沉浓度值远大于在Ca2+溶液中,这是因为Ca2+压缩双电层的能力更强,Ca2+可以更有效地屏蔽颗粒表面电荷。本文褐土碳酸钙结核胶体的临界聚沉浓度值远大于有关研究中土壤胶体凝聚的临界聚沉浓度数值[23]。这可能是由于其添加了六偏磷酸钠,有效增强了颗粒间的分散性,使悬液稳定性增强。在Na+体系中,褐土碳酸钙结核纳米颗粒稳定性略大于工业纳米碳酸钙,而在Ca2+体系中,可能是工业纳米碳酸钙悬液中添加的六偏磷酸钠与外源Ca2+发生络合,消耗了一部分Ca2+,使得工业纳米碳酸钙的临界聚沉浓度值大于褐土碳酸钙结核纳米颗粒。
3种碳酸钙胶体的矿物组成存在差异,这是造成其胶体稳定性有差别的内在原因。褐土碳酸钙结核胶体的稳定性明显高于褐土碳酸钙结核纳米颗粒,这是化学分散剂的表面修饰作用和黏土矿物组成差异共同引起的。其次,褐土碳酸钙结核胶体的分散方法与工业纳米碳酸钙相同,而初始粒径存在显著差异,二者之间的稳定性差异较大。褐土碳酸钙结核纳米颗粒的初始粒径与工业纳米碳酸钙近似,分散方法不同,而稳定性差异较小。这表明,胶体颗粒的初始粒径大小是胶体凝聚特性差异的又一重要因素。胶体凝聚行为的差异及其凝聚体结构参数的变化会影响其后续形成土壤团聚体的结构差异。本文研究结果表明,碳酸钙同黏土矿物和有机质等胶结物质一样具有显著的胶体特性,其对干旱和半干旱区石灰性土壤团聚体形成和结构稳定性的影响值得进一步深入探讨。
3 结论本文从褐土碳酸钙结核中提取得到褐土碳酸钙结核纳米颗粒和褐土碳酸钙结核胶体,并对其胶体特性进行了研究。物理分散法获得的褐土碳酸钙结核纳米颗粒大小与工业纳米碳酸钙接近,两者直径均小于100 nm,而通过化学分散法获得的褐土碳酸钙结核胶体直径更大。工业纳米碳酸钙为纯方解石,褐土碳酸钙结核胶体和褐土碳酸钙结核纳米颗粒除含方解石外,还含有石英、伊利石等矿物。在不同pH条件下,三者表面均携带负电荷,且表面负电荷随pH的增大而增多。褐土碳酸钙结核胶体和褐土碳酸钙结核纳米颗粒因含有石英和伊利石,两者表面电荷密度受pH影响较小。当悬液中加入Na+和Ca2+时,胶体表面电荷被屏蔽,电位绝对值逐渐减小,悬液稳定性减弱,颗粒产生凝聚。碳酸钙胶体的矿物组成、颗粒直径和溶液化学条件是引起其凝聚行为和结构体特征差异的重要因素。
| [1] |
Grover S P, Butterly C R, Wang X, et al. The short-term effects of liming on organic carbon mineralisation in two acidic soils as affected by different rates and application depths of lime[J]. Biology and Fertility of Soils, 2017, 53(4): 431-443 DOI:10.1007/s00374-017-1196-y (  0) 0) |
| [2] |
李忠徽, 魏彬萌, 刘丹, 等. 黄绵土中碳酸钙含量和有机肥施用对土壤有机碳组分及CO2排放的影响[J]. 环境科学学报, 2018, 38(6): 2498-2505 (  0) 0) |
| [3] |
Wang J P, Wang X J, Zhang J, et al. Soil organic and inorganic carbon and stable carbon isotopes in the Yanqi Basin of northwestern China[J]. European Journal of Soil Science, 2015, 66(1): 95-103 DOI:10.1111/ejss.12188 (  0) 0) |
| [4] |
Eamus D, Zolfaghar S, Villalobos-Vega R, et al. Groundwater-dependent ecosystems: Recent insights from satellite and field-based studies[J]. Hydrology and Earth System Sciences, 2015, 19(10): 4229-4256 DOI:10.5194/hess-19-4229-2015 (  0) 0) |
| [5] |
Wang X J, Wang J P, Zhang J. Comparisons of three methods for organic and inorganic carbon in calcareous soils of northwestern China[J]. PLoS One, 2012, 7(8): e44334 DOI:10.1371/journal.pone.0044334 (  0) 0) |
| [6] |
Zhang F, Wang X J, Guo T W, et al. Soil organic and inorganic carbon in the loess profiles of Lanzhou area: Implications of deep soils[J]. CATENA, 2015, 126: 68-74 DOI:10.1016/j.catena.2014.10.031 (  0) 0) |
| [7] |
Dı́az-Hernández J L, Fernández E B, González J L. Organic and inorganic carbon in soils of semiarid regions: A case study from the Guadix-Baza basin (Southeast Spain)[J]. Geoderma, 2003, 114(1/2): 65-80 (  0) 0) |
| [8] |
Wang X J, Wang J P, Xu M G, et al. Carbon accumulation in arid croplands of northwest China: Pedogenic carbonate exceeding organic carbon[J]. Scientific Reports, 2015, 5: 11439 DOI:10.1038/srep11439 (  0) 0) |
| [9] |
Zhao W, Zhang R, Huang C Q, et al. Effect of different vegetation cover on the vertical distribution of soil organic and inorganic carbon in the Zhifanggou Watershed on the loess plateau[J]. CATENA, 2016, 139: 191-198 DOI:10.1016/j.catena.2016.01.003 (  0) 0) |
| [10] |
Zamanian K, Pustovoytov K, Kuzyakov Y. Pedogenic carbonates: Forms and formation processes[J]. Earth-Science Reviews, 2016, 157: 1-17 DOI:10.1016/j.earscirev.2016.03.003 (  0) 0) |
| [11] |
吴道祥, 曹亚娟, 钟轩民, 等. 安徽淮北平原钙质结核土分布及成因年代研究[J]. 岩土力学, 2009, 30(S2): 434-439 DOI:10.16285/j.rsm.2009.s2.006 (  0) 0) |
| [12] |
Jennings D H. Mineral nutrition in higher plants (book)[J]. Plant, Cell and Environment, 1988, 11(2): 147 (  0) 0) |
| [13] |
Lang E, Beese F. Reaction of the microbial soil population of beech forest to miming treatments[J]. Allgemeine Forest Zeitschrift, 1985, 43: 1166-1169 (  0) 0) |
| [14] |
Al-Ani A N, Dudas M J. Influence of calcium carbonate on mean weight diameter of soil[J]. Soil and Tillage Research, 1988, 11(1): 19-26 DOI:10.1016/0167-1987(88)90028-1 (  0) 0) |
| [15] |
郭玉文, 加藤诚, 宋菲, 等. 黄土高原黄土团粒组成及其与碳酸钙关系的研究[J]. 土壤学报, 2004, 41(3): 362–368, 493 DOI:10.3321/j.issn:0564-3929.2004.03.006 (  0) 0) |
| [16] |
张耀方, 赵世伟, 王子龙, 等. 黄土高原土壤团聚体胶结物质的分布及作用综述[J]. 中国水土保持科学, 2015, 13(5): 145-150 DOI:10.3969/j.issn.1672-3007.2015.05.022 (  0) 0) |
| [17] |
陶漉, 马东豪, 张丛志, 等. 石灰性土壤团聚体中钙形态特征及其与有机碳含量的关系[J]. 土壤, 2021, 53(4): 715-722 DOI:10.13758/j.cnki.tr.2021.04.007 (  0) 0) |
| [18] |
Virto I, Gartzia-Bengoetxea N, Fernández-Ugalde O. Role of organic matter and carbonates in soil aggregation estimated using laser diffractometry[J]. Pedosphere, 2011, 21(5): 566-572 DOI:10.1016/S1002-0160(11)60158-6 (  0) 0) |
| [19] |
Chen L F, Zhang G C, Wang L, et al. Zeta potential of limestone in a large range of salinity[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2014, 450: 1-8 (  0) 0) |
| [20] |
Al Mahrouqi D, Vinogradov J, Jackson M D. Zeta potential of artificial and natural calcite in aqueous solution[J]. Advances in Colloid and Interface Science, 2017, 240: 60-76 DOI:10.1016/j.cis.2016.12.006 (  0) 0) |
| [21] |
陕西省土壤普查办公室. 陕西土壤[M].
科学出版社, 北京, 1992
(  0) 0) |
| [22] |
熊毅. 土壤胶体-第二册-土壤胶体研究法[M].
科学出版社, 北京, 1985
(  0) 0) |
| [23] |
Li W, He Y, Wu J, et al. Extraction and characterization of natural soil nanoparticles from Chinese soils[J]. European Journal of Soil Science, 2012, 63(5): 754-761 DOI:10.1111/j.1365-2389.2012.01480.x (  0) 0) |
| [24] |
Xu C Y, Zhou T T, Wang C L, et al. Aggregation of polydisperse soil colloidal particles: Dependence of Hamaker constant on particle size[J]. Geoderma, 2020, 359: 113999 DOI:10.1016/j.geoderma.2019.113999 (  0) 0) |
| [25] |
梁文玉. 纳米CaCO3在水中的分散及其机理研究[D]. 无锡: 江南大学, 2008.
(  0) 0) |
| [26] |
李琪瑞, 许晨阳, 耿增超, 等. 纳米生物炭的制备方法比较及其特性研究[J]. 中国环境科学, 2020, 40(7): 3124-3134 DOI:10.3969/j.issn.1000-6923.2020.07.039 (  0) 0) |
| [27] |
Li S Z, Xu R K. Electrical double layers' interaction between oppositely charged particles as related to surface charge density and ionic strength[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2008, 326(3): 157-161 DOI:10.1016/j.colsurfa.2008.05.023 (  0) 0) |
| [28] |
López-López J M, Schmitt A, Moncho-Jordá A, et al. Stability of binary colloids: Kinetic and structural aspects of heteroaggregation processes[J]. Soft Matter, 2006, 2(12): 1025-1042 DOI:10.1039/b608349h (  0) 0) |
| [29] |
Alroudhan A, Vinogradov J, Jackson M D. Zeta potential of intact natural limestone: Impact of potential-determining ions Ca, Mg and SO4[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2016, 493: 83-98 (  0) 0) |
| [30] |
陆海龙, 徐仁扣. 玉米和大豆根尖和非根尖部位对Mn(II)的吸附研究[J]. 土壤, 2020, 52(5): 1038-1042 (  0) 0) |
| [31] |
Romanuka J, Hofman J, Ligthelm D J, et al. Low salinity EOR in carbonate proceedings of the SPE improved oil recovery symposium[C]. Oklahoma, USA: Tulsa; April 2012 SPE-153869-MS2012, 14-18.
(  0) 0) |
| [32] |
李忠意, 刘芳铭, 吴金雯, 等. 测量模拟土体zeta电位的简易流动电位装置及其使用方法[J/OL]. 土壤学报, https://kns.cnki.net/kcms/detail/32.1119.p.20210719.1731.002.html.
(  0) 0) |
| [33] |
温晓翠, 李九玉, 宋洁, 等. 电位滴定法研究可变电荷土壤表面酸碱性质的进展[J/OL]. 土壤学报, https://kns.cnki.net/kcms/detail/32.1119.P.20210331.1103.004.html.
(  0) 0) |
| [34] |
Vdović N. Electrokinetic behaviour of calcite—the relationship with other calcite properties[J]. Chemical Geology, 2001, 177(3/4): 241-248 (  0) 0) |
| [35] |
姜军, 徐仁扣. 离子强度对三种可变电荷土壤表面电荷和Zeta电位的影响[J]. 土壤, 2015, 47(2): 422-426 (  0) 0) |
| [36] |
Xu C Y, Xu R K, Li J Y, et al. Phosphate-induced aggregation kinetics of hematite and goethite nanoparticles[J]. Journal of Soils and Sediments, 2017, 17(2): 352-363 DOI:10.1007/s11368-016-1550-y (  0) 0) |
| [37] |
Lin D, Story S D, Walker S L, et al. Influence of extracellular polymeric substances on the aggregation kinetics of TiO2 nanoparticles[J]. Water Research, 2016, 104: 381-388 (  0) 0) |
2. Key Laboratory of Plant Nutrition and the Agri-environment in Northwest China, Ministry of Agriculture, Northwest A & F University, Yangling, Shaanxi 712100, China;
3. State Key Laboratory of Soil Erosion and Dryland Farming on Loess Plateau, Northwest A & F University, Yangling, Shaanxi 712100, China;
4. Institute of Soil and Water Conservation, Chinese Academy of Sciences & Ministry of Water Resources, Yangling, Shaanxi 712100, China
 2022, Vol. 54
2022, Vol. 54


