2. 中国科学院南京地理与湖泊研究所流域地理学重点实验室, 南京 210008;
3. 河海大学水文水资源与水利工程科学国家重点实验室, 南京 210098;
4. 中国科学院大学, 北京 100049
土壤氮循环是全球氮循环的重要环节之一,对土壤质量与肥力、碳及其他元素的养分循环、陆地生态系统生产力与多样性、全球环境变化等产生重要影响[1-2]。氮循环中不同生物化学过程具有不同程度的同位素分馏效应,即参与反应的底物与产物氮同位素组成有明显差异的现象[3]。因此,氮同位素自然丰度(δ15N)成为量化土壤氮循环强弱程度的有力指标,研究土壤δ15N空间变异格局及其影响机制能够加深对于陆地生态系统氮循环的认识和理解。
一般情况下,氮输入过程(氮沉降、固定)导致土壤15N贫化,氮输出(液态淋溶、气态损失)导致土壤15N富集,二者的平衡分馏系数与相对通量大小决定土壤δ15N值[3-4]。以往研究指出,气象、土壤等环境因子通过控制氮输入、输出过程,从而对土壤δ15N的空间变异格局产生影响。例如,Amundson等[5]在全球尺度的研究中发现,土壤δ15N值随年平均降雨量减小、年平均气温增加而升高;Wang等[4]在中国北部某样带的研究发现,土壤δ15N值与干旱指数(降雨量与蒸散量之比)呈凸向上关系;Yang等[6]在青藏高原的研究发现,土壤δ15N值随土壤黏粒含量的增加而略有增加,但随土壤碳氮比的增加而减少。也有研究考虑了不同环境因子的协同作用,如Cheng等[7]在长白山自然保护区的研究发现,气象、土壤因子与植物种类等协同影响土壤δ15N值。但土壤含水量、气象因子的时间变化特征对土壤δ15N空间变异的影响尚未引起足够关注。气象、土壤性质和植被等环境因子综合影响土壤含水量的空间变异特征[8],且土壤含水量是影响氮循环的关键变量,对土壤氮排放有显著影响。因而,气象、土壤等环境因子可通过改变土壤含水量,进而引起土壤δ15N值的空间变异。此外,气象的时间变化特征能进一步解释土壤氮循环的剧烈程度。例如,柳菲等[9]在太湖流域典型茶园的研究发现,季节性干旱导致土壤硝态氮淋失滞后,对后续季节影响显著,季节性湿润则导致硝态氮淋失提前且对后续季节影响较小;Urakawa等[10]在日本北部的研究发现,冬季气候变化引起的加速冻融循环通过改变微生物群落与功能,显著影响随后生长季的氮转化速率。因此,反映气候时间变化特征的因子对土壤δ15N空间变异的解释能力同样值得关注。
基于以上认识,本研究搜集全球尺度上的土壤δ15N值及土壤含水量、气象和土壤性质因子的数据集,构建全球尺度上不同环境因子与土壤δ15N值的关系,以揭示不同环境因子对土壤δ15N空间变异的影响机制和直接间接效应,以及土壤含水量和气象时间变化特征因子在解释土壤δ15N空间变异中的关键作用。
1 材料与方法 1.1 土壤δ15N数据集及研究区域本文土壤δ15N数据集来源于Craine等[11]整理的全球910个样点,及Wang等[4]在中国北部沿3 200 km样带测定的50个样点。去除一个重复值并删除含环境因子空值或异常值的点,剩余812个有效样点。这些土壤样点位于非农田、建筑用地的自然生态系统中,从而排除人类活动对土壤氮循环的干扰,其在全球分布如图 1所示,在全球及六大洲、不同气候带、不同海拔范围的统计特征如表 1所示。可以看出,样点在不同空间区域内的分布数量相当,说明样点空间分布较为合理,数据能反映全球特征。

|
(矢量底图源于国家地理信息公共服务平台天地图,WMTS服务器:http://t0.tianditu.gov.cn/vec_c/esri/wmts) 图 1 土壤δ15N样点在全球的空间分布 Fig. 1 Spatial distribution of soil δ15N samples on global scale |
|
|
表 1 全球和六大洲及不同气候带和海拔范围内的土壤δ15N样点数和统计特征 Table 1 Number of samples and statistical descriptions of soil δ15N on global scale, in six continents, and in different climate zones, and in different elevation ranges |
环境因子数据集包括土壤含水量、土壤性质和气象因子三大类。其中,土壤含水量数据来源于欧洲航天局“气候变化倡议”与土壤湿度产品[12](ESA CCI SM Product V06.1,zz http://www.esa-soilmoisture-cci.org/),选取1978—2016年间月尺度融合产品的均值,空间分辨率为0.25°。土壤性质因子包括砂粒含量、粉粒含量、黏粒含量、容重、土壤全氮含量和有机碳含量,来源于世界土壤信息数据中心SoilGrids250m 2.0土壤数据集[13](https://data.isric.org/),空间分辨率为250 m。气象因子来源于WorldClim 2.1数据集[14] (https://www.worldclim.org/),包括1970—2000年的年平均气温、平均气温日较差、年平均降雨量、降雨季节变率和太阳辐射,空间分辨率为30 s。其中,平均气温日较差和降雨季节变率的计算如下:
| $ {\text{MDR = }}\frac{{\sum\limits_{i = 1}^{{\text{12}}} {\left( {{T_{{{\max }_i}}} - {T_{{{\min }_i}}}} \right)} }}{{12}} $ | (1) |
式中:MDR为平均气温日较差;
| $ {\text{PS}} = \frac{{{\text{SD}}\left( {{\text{PP}}{{\text{T}}_{\text{1}}},\; \cdot\cdot\cdot ,\;{{{\mathrm{PPT}} }_{12}}} \right)}}{{1 + \left( {\frac{{{\text{MAP}}}}{{{\text{12}}}}} \right)}} \times 100 $ | (2) |
式中:PS为降雨季节变率;PPT1, …, PPT12分别表示1—12月的总降雨量(mm),MAP表示年平均降雨量(mm)。
利用ArcMap 10.7提取样点对应环境因子值,并删除含有空值和异常值的点,剩余共812组数据,其12类环境因子的统计特征如表 2所示。
|
|
表 2 812个样点的气象和土壤因子数据统计特征 Table 2 Statistical characteristics of meteorological factors and soil properties at 812 sampling sites |
利用R软件分别绘制土壤δ15N值、土壤含水量与11个环境因子的散点图,并进行线性拟合,计算皮尔逊相关系数r与显著概率P值,以揭示土壤δ15N、土壤含水量和各环境因子之间的线性关系。
1.3.2 结构方程模型的构建结构方程模型(structural equation model, SEM)是一种建立、估计和检验先验理论模型的多变量统计技术,能反映不同变量之间的关系,探讨不同因子对同一过程直接或间接的影响,判别不同因子的相对重要性[15]。本研究利用Amos 22.0构建SEM,进一步分析土壤δ15N与土壤含水量、土壤性质和气象因子之间的关系。首先,根据前面建立的土壤δ15N、土壤含水量与不同环境因子的相关关系,筛选出对土壤δ15N和土壤含水量有显著作用的气象和土壤性质因子,用于构建SEM;然后,输入812组数据集运行模型,得到初始理论模型各参数的标准化估计值,并采用卡方自由度比值(
基于全球812个有效样点的计算结果,土壤δ15N平均值为4.51‰,变化范围为–3.40‰ ~ 16.20‰,标准差为2.33‰。较低的土壤δ15N值(平均值< 4‰)多分布于欧洲、北美洲、大洋洲,较高的土壤δ15N值(平均值> 4.6‰)多分布于非洲和南美洲(表 1)。从气候带来看,赤道和干旱气候带土壤δ15N值(平均值> 5.3‰)明显高于暖温、冷温和极地气候带(平均值< 4‰)(表 1)。从海拔高度分类来看,低海拔(< 500 m)、高海拔(> 3 500 m)地区的土壤δ15N值相对较低(平均值< 4.4‰)且变化范围较小(标准差 < 2.2‰),中低(500 ~ 1 000 m)、中(1 000 ~ 2 000 m)、中高海拔(2 000 ~ 3 500 m)地区的土壤δ15N值相对较高(平均值> 4.7‰),且中低、中海拔的土壤δ15N值变化范围较大(标准差 > 2.6‰)(表 1)。
土壤δ15N值主要表现为区域内的变化,区域间的差异较小(表 1)。尽管如此,全球尺度下土壤δ15N变异格局的研究仍是有必要的。其一,区域尺度内土壤δ15N的空间变化特征无法完全涵盖全球尺度的变化特征(表 1);其二,虽然不同区域间δ15N的空间变化特征相似,但关键影响机制(气候和土壤等)可能存在不同。
2.2 土壤δ15N值、土壤含水量与环境因子的关系土壤δ15N值与土壤含水量及各环境因子的散点图及线性拟合结果如图 2所示。土壤含水量与土壤δ15N值呈显著负相关关系(r=–0.28,P < 0.01)(图 2A)。气象因子中年平均气温、平均气温日较差、降雨季节变率以及太阳辐射均与土壤δ15N值呈显著正相关关系(P < 0.01),其中平均气温日较差和太阳辐射与其相关性较强(r > 0.4)(图 2C、2F);年平均降雨量与土壤δ15N值呈显著负相关关系(P < 0.01),但相关性较弱(r=–0.14)(图 2D)。土壤性质因子中砂粒含量、容重与土壤δ15N值呈显著正相关关系(P < 0.01),容重与其相关程度较高(r=0.41)(图 2J);粉粒含量、全氮和有机碳含量与土壤δ15N值呈显著负相关关系(P < 0.01),其中全氮含量对数值和有机碳含量对数值与其相关性较强(|r| > 0.4)(图 2K、2L);黏粒含量与土壤δ15N值无显著线性关系(P > 0.05)(图 2I)。

|
(土壤全氮与有机碳含量取原数据的对数值,以呈现与土壤δ15N值较好的线性关系;下同) 图 2 土壤δ15N值与环境因子散点图 Fig. 2 Scatter plots of soil δ15N value and environmental factors |
土壤含水量与各环境因子的散点图及线性拟合结果如图 3所示。气象因子中平均气温日较差、降雨季节变率和太阳辐射与土壤含水量呈显著负相关关系(P < 0.01),其中平均气温日较差和降雨季节变率与土壤含水量相关性较强(前者r= –0.69,后者r= –0.59)(图 3B、3D);年平均降雨量与土壤含水量呈显著正相关关系(r=0.68)(图 3C);年平均气温与土壤含水量无显著线性关系(P > 0.05)(图 3A)。土壤性质因子中粉粒含量、黏粒含量、全氮含量和有机碳含量与土壤含水量呈显著正相关关系(P < 0.01),其中全氮含量对数值和有机碳含量对数值与其相关程度较高(前者r=0.61,后者r=0.66)(图 3J、3K);砂粒含量和容重与土壤含水量呈显著负相关关系(P < 0.01),其中容重与其相关性较强(r= –0.61)(图 3I)。综合来看,土壤含水量与环境因子的相关性均较强,表明其受到气象和土壤性质因子强烈的交互影响。

|
图 3 土壤含水量与环境因子散点图 Fig. 3 Scatter plots of soil moisture and environmental factors |
根据2.2的结果,本文选择平均气温日较差、降雨季节变率和太阳辐射这3个与土壤δ15N值和土壤含水量均具有显著关系且能较全面反映气象特征的因子作为气象因子的指标,选择土壤粉粒含量、容重和全氮含量这3个与土壤δ15N值和土壤含水量均具有显著关系且能较全面反映土壤特征的因子作为土壤性质因子的指标。根据筛选的测量指标构建SEM,经修正后模型与数据适配(图 4)。
|
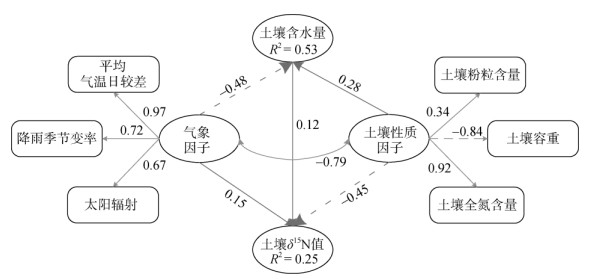
(潜在变量以椭圆形符号表示,测量指标以方形符号表示;模型的适配统计量χ2/df = 1.197 (P > 0.05),RMSEA = 0.016,AGFI = 0.987,NFI = 0.999,均表明模型与数据呈良好适配度) 图 4 SEM模型及计算结果 Fig. 4 SEM model and calculation results |
由SEM计算结果可见,土壤性质因子、气象因子和土壤含水量解释了全球尺度上土壤δ15N值25% 的空间变异性,土壤性质因子和气象因子解释了土壤含水量53% 的空间变异性(图 4)。土壤性质因子对土壤δ15N空间变异的总效应最高,为–0.41,直接效应为–0.45,间接效应为0.04;气象因子与土壤含水量对土壤δ15N空间变异的总效应相当,分别为0.09和0.12,其中气象因子的直接效应为0.15,间接效应为–0.06。土壤含水量空间变异受到气象因子的影响大于土壤性质因子,总效应分别为–0.48和0.28。从各指标对潜变量的负荷看,在气象因子测量模型中,3个指标都呈现较高的正向负荷量,其中平均气温日较差负荷量最高,为0.97;在土壤性质因子测量模型中,容重与全氮呈现较高的负荷量,前者为–0.84,后者为0.92,土壤粉粒含量的负荷量仅为0.34。气象因子与土壤性质因子之间呈显著的相关关系(r= –0.79,P < 0.01)。
3 讨论 3.1 土壤含水量与土壤δ15N值相关关系的内在机制全球尺度上,土壤δ15N值随着土壤含水量的增加整体呈下降的趋势(图 2A),这说明较高的土壤δ15N值往往分布在土壤含水量较低的地区,例如一些沙漠地带(图 2A,表 1)。前人研究也指出,在高温干旱的地区土壤δ15N含量往往较高[5, 11, 16]。原因可能是干旱地区通常平均气温日较差、降雨季节变率以及太阳辐射较大(图 3B、3D、3E),意味着气候冷热交替,温差大,常年降雨稀少但出现脉冲式降雨[17];同时干旱地区土壤中砂粒含量较高、粉粒和黏粒含量较低、土壤容重大(图 3F、3G、3H、3I),说明土壤孔隙结构差;而干旱地区土壤全氮和有机碳含量较低(图 3J、3K),则表明其土壤肥力低,植被稀少,生物和微生物活性低。这些环境条件导致干旱地区生物固氮量及土壤内部氮周转率较低,而非生物的氮排放例如氨挥发往往较高,且土壤微生物易受到偶发降雨事件的刺激,从而引发大量气态氮排放[5, 16]。这种模式使得土壤氮素的固定少而排放多,从而导致土壤15N的富集。相反,在土壤含水量较高的地区,湿润的土壤环境有利于15N贫化的生物固氮过程,一定程度上抵消了土壤氮排放引起的15N富集,从而具有较低的土壤δ15N值[16]。
3.2 气象因子和土壤性质因子与土壤δ15N值相关关系的内在机制气象因子中,土壤δ15N值随年平均气温的增加而增加(图 2B)。这是因为温度升高可促进土壤反硝化作用[18]与氨挥发过程[19],从而导致土壤氮的排放量增大,引起15N的富集;此外,有研究认为全球模式下年平均温度与土壤δ15N值的正相关关系是间接的,温暖生态系统一般富含黏土,易滞留更高比例的有机质15N[19]。土壤δ15N值随年平均降雨量的增加而减小(图 2D),这与以往许多全球或区域尺度的研究结论一致[5, 16, 20]。相比湿润地区,干旱与半干旱生态系统的氮循环“开度”更大,即氮内部周转率低,而输出排放量大[21],故土壤δ15N值较高。土壤δ15N值随着太阳辐射的增加而增加(图 2F),可能的解释是,太阳辐射是土壤表面温度的直接驱动因素,较高的地表温度刺激氮的气态损失这一强分馏过程[22],从而导致土壤15N的富集。
此外,土壤δ15N值与平均气温日较差和降雨季节变率存在显著的正相关关系(图 2C、2E),表明气温、降雨的大幅波动会造成土壤系统的15N富集现象。其原因可能是气温变化和降雨波动引发的频繁干湿交替,可能刺激土壤微生物活性,引发大量土壤氮排放,使得土壤系统的δ15N值升高。前人关于气象的时间变化特征对土壤水文过程、土壤碳氮的影响均有不少研究,如Aranibar等[16]在南非卡拉哈里沙漠的研究发现,干旱地区的15N富集现象可能源于降雨的高变异性和不可预测性,而不是其较低的年平均降雨量;Schuerings等[23]认为未来温带地区冬季的气温变异性增加,将通过改变土壤温度的时间动态,对土壤生物活性和氮循环产生显著影响。本研究表明,相对于均值,气象的时间变化特征更能用于解释土壤δ15N的空间变异(图 2),因此在构建SEM时选择平均气温日较差和降雨季节变率作为气象因子的构成因素。
土壤性质因子中,土壤δ15N值随着土壤砂粒含量和容重的增加而增加(图 2G、2J),而随粉粒、全氮和有机碳含量的增加而减少(图 2H、2K、2L)。由图 3可知,砂粒含量、容重较大而粉粒、全氮和有机碳含量较低的土壤主要出现在干旱地区。一者,这种干旱环境下成土速率慢,而土壤侵蚀严重,导致土壤理化性质与基岩相似,具有相对于成熟土壤更高的15N含量[24]。许多研究指出,土壤δ15N值随土层深度增加而增加[25],同样可说明土壤发育早期δ15N值更高。二者,由3.1的讨论可知,这种孔隙结构粗糙、质地差的土壤持水和保肥能力差,生物固氮能力低,而氮素排放量又相对较大,从而导致15N的富集。
3.3 土壤含水量、土壤性质因子和气象因子对土壤δ15N值空间变异的相对效应SEM结果表明,相对于气象因子和土壤含水量,土壤性质因子对土壤δ15N空间变异的影响更大(图 4),说明土壤孔隙结构(粉粒含量和容重)和养分状况(全氮含量)是影响土壤氮循环速率更为关键的因子。这一结果与以前的研究结论一致,如Craine等[11]发现全球模式下土壤δ15N值与气候之间的关系是间接的,并通过气候对土壤有机碳和黏粒的影响来调节;Yang等[6]在青藏高原的研究发现,土壤δ15N值与年平均气温或降雨量关系并不显著,而与土壤变量有较大关系。土壤性质因子对土壤δ15N空间变异的总效应和直接效应均为负(图 4)。这是因为土壤性质因子表现出与土壤粉粒和全氮含量的正相关,而与土壤容重负相关(图 4);土壤δ15N值随土壤粉粒、全氮含量增加而减小,而随土壤容重增加而增加(图 2)。此外,土壤性质因子可通过影响土壤含水量间接作用于土壤δ15N空间分布,从而表现出微弱的正间接效应(0.04)。这可解释为较高的土壤粉粒含量与较低的土壤容重,即良好的土壤孔隙结构,以及较强的滞水能力,从而导致厌氧反硝化氮排放,引起土壤δ15N升高。
气象因子和土壤含水量对土壤δ15N空间变异的直接效应相当(图 4)。原因可能是土壤含水量主要受气象因子调控(图 3和图 4),从而表现出对土壤δ15N空间变异相似的影响幅度。此外,气象因子可通过影响土壤含水量间接作用于土壤δ15N的空间变异,其间接效应为–0.06。这种负的间接效应是因为土壤含水量对土壤δ15N的效应为正(0.12),而气象因子对土壤含水量的效应为负(–0.48)(图 4)造成的。土壤含水量的正效应说明当排除气象因子和土壤性质因子的影响后,土壤δ15N值随土壤含水量增加而增加。一方面,土壤含水量上升,微生物与酶的活性增强,促进异养呼吸及氮的矿化,土壤环境从富含有机物转向无机氮较丰富,反硝化作用增强(底物浓度上升和厌氧环境增强),从而产生大量的气态氮排放;另一方面,较高的土壤含水量引发水分运动,携带土壤硝化产物NO3−流失[26]。氮的气体排放和淋溶损失是导致土壤15N富集的两大途径[4]。
4 结论土壤δ15N空间变异受土壤含水量、气象因子和土壤性质因子的显著影响(P < 0.01),其中随土壤含水量增加而呈减小趋势;平均气温日较差和降雨季节变率对土壤δ15N值和土壤含水量空间变异的解释能力比常用的年平均气温和年平均降雨量更强。SEM结果表明,土壤性质因子较气象因子和土壤含水量对土壤δ15N空间变异的解释度更高,表明土壤性质因子是影响土壤氮循环的更关键因子;当排除气象因子和土壤性质因子的影响后,土壤含水量对土壤δ15N值的效应为正。
| [1] |
Vitousek P M, Aber J D, Howarth R W, et al. Human alteration of the global nitrogen cycle: Sources and consequences[J]. Ecological Applications, 1997, 7(3): 737-750 (  0) 0) |
| [2] |
Watanabe M D B, Ortega E. Ecosystem services and biogeochemical cycles on a global scale: Valuation of water, carbon and nitrogen processes[J]. Environmental Science & Policy, 2011, 14(6): 594-604 (  0) 0) |
| [3] |
Denk T R A, Mohn J, Decock C, et al. The nitrogen cycle: A review of isotope effects and isotope modeling approaches[J]. Soil Biology and Biochemistry, 2017, 105: 121-137 DOI:10.1016/j.soilbio.2016.11.015 (  0) 0) |
| [4] |
Wang C, Wang X B, Liu D W, et al. Aridity threshold in controlling ecosystem nitrogen cycling in arid and semi-arid grasslands[J]. Nature Communications, 2014, 5: 4799 DOI:10.1038/ncomms5799 (  0) 0) |
| [5] |
Amundson R, Austin A T, Schuur E A G, et al. Global patterns of the isotopic composition of soil and plant nitrogen[J]. Global Biogeochemical Cycles, 2003, 17(1): 1031 (  0) 0) |
| [6] |
Yang Y H, Ji C J, Robinson D, et al. Vegetation and soil 15N natural abundance in alpine grasslands on the Tibetan Plateau: Patterns and implications[J]. Ecosystems, 2013, 16(6): 1013-1024 DOI:10.1007/s10021-013-9664-1 (  0) 0) |
| [7] |
Cheng S L, Fang H J, Yu G R, et al. Foliar and soil 15N natural abundances provide field evidence on nitrogen dynamics in temperate and boreal forest ecosystems[J]. Plant and Soil, 2010, 337(1/2): 285-297 (  0) 0) |
| [8] |
Wu D D, Wang T J, Di C L, et al. Investigation of controls on the regional soil moisture spatiotemporal patterns across different climate zones[J]. Science of the Total Environment, 2020, 726: 138214 DOI:10.1016/j.scitotenv.2020.138214 (  0) 0) |
| [9] |
柳菲, 赖晓明, 朱青, 等. 季节性干湿气候对茶园坡面土壤硝态氮淋失的影响[J]. 农业现代化研究, 2021, 42(2): 223-231 (  0) 0) |
| [10] |
Urakawa R, Shibata H, Kuroiwa M, et al. Effects of freeze-thaw cycles resulting from winter climate change on soil nitrogen cycling in ten temperate forest ecosystems throughout the Japanese archipelago[J]. Soil Biology and Biochemistry, 2014, 74: 82-94 DOI:10.1016/j.soilbio.2014.02.022 (  0) 0) |
| [11] |
Craine J M, Elmore A J, Wang L X, et al. Convergence of soil nitrogen isotopes across global climate gradients[J]. Scientific Reports, 2015, 5: 8280 DOI:10.1038/srep08280 (  0) 0) |
| [12] |
Gruber A, Scanlon T, van der Schalie R, et al. Evolution of the ESA CCI Soil Moisture climate data records and their underlying merging methodology[J]. Earth System Science Data, 2019, 11(2): 717-739 DOI:10.5194/essd-11-717-2019 (  0) 0) |
| [13] |
Poggio L, de Sousa L M, Batjes N H, et al. SoilGrids 2.0: Producing soil information for the globe with quantified spatial uncertainty[J]. SOIL, 2021, 7(1): 217-240 DOI:10.5194/soil-7-217-2021 (  0) 0) |
| [14] |
Fick S E, Hijmans R J. WorldClim 2: New 1-km spatial resolution climate surfaces for global land areas[J]. International Journal of Climatology, 2017, 37(12): 4302-4315 DOI:10.1002/joc.5086 (  0) 0) |
| [15] |
Eisenhauer N, Bowker M A, Grace J B, et al. From patterns to causal understanding: Structural equation modeling (SEM) in soil ecology[J]. Pedobiologia, 2015, 58(2/3): 65-72 (  0) 0) |
| [16] |
Aranibar J N, Otter L, Macko S A, et al. Nitrogen cycling in the soil-plant system along a precipitation gradient in the Kalahari sands[J]. Global Change Biology, 2004, 10(3): 359-373 DOI:10.1111/j.1365-2486.2003.00698.x (  0) 0) |
| [17] |
Collins S L, Sinsabaugh R L, Crenshaw C, et al. Pulse dynamics and microbial processes in aridland ecosystems[J]. Journal of Ecology, 2008, 96(3): 413-420 DOI:10.1111/j.1365-2745.2008.01362.x (  0) 0) |
| [18] |
马秀艳, 蒋磊, 宋艳宇, 等. 温度和水分变化对冻土区泥炭地土壤氮循环功能基因丰度的影响[J]. 生态学报, 2021, 41(17): 6707-6717 (  0) 0) |
| [19] |
Craine J M, Brookshire E N J, Cramer M D, et al. Ecological interpretations of nitrogen isotope ratios of terrestrial plants and soils[J]. Plant and Soil, 2015, 396(1/2): 1-26 (  0) 0) |
| [20] |
Shan Y, Huang M B, Suo L Z, et al. Composition and variation of soil δ15N stable isotope in natural ecosystems[J]. CATENA, 2019, 183: 104236 DOI:10.1016/j.catena.2019.104236 (  0) 0) |
| [21] |
Martinelli L A, Piccolo M C, Townsend A R, et al. Nitrogen stable isotopic composition of leaves and soil: Tropical versus temperate forests[J]. Biogeochemistry, 1999, 46(1/2/3): 45-65 (  0) 0) |
| [22] |
McCalley C K, Sparks J P. Abiotic gas formation drives nitrogen loss from a desert ecosystem[J]. Science, 2009, 326(5954): 837-840 DOI:10.1126/science.1178984 (  0) 0) |
| [23] |
Schuerings J, Jentsch A, Hammerl V, et al. Increased winter soil temperature variability enhances nitrogen cycling and soil biotic activity in temperate heathland and grassland mesocosms[J]. Biogeosciences, 2014, 11(23): 7051-7060 DOI:10.5194/bg-11-7051-2014 (  0) 0) |
| [24] |
Morford S L, Houlton B Z, Dahlgren R A. Increased forest ecosystem carbon and nitrogen storage from nitrogen rich bedrock[J]. Nature, 2011, 477(7362): 78-81 DOI:10.1038/nature10415 (  0) 0) |
| [25] |
Hobbie E A, Ouimette A P. Controls of nitrogen isotope patterns in soil profiles[J]. Biogeochemistry, 2009, 95(2/3): 355-371 (  0) 0) |
| [26] |
Zhu Q, Castellano M J, Yang G S. Coupling soil water processes and the nitrogen cycle across spatial scales: Potentials, bottlenecks and solutions[J]. Earth-Science Reviews, 2018, 187: 248-258 (  0) 0) |
2. Key Laboratory of Watershed Geographic Sciences, Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, Nanjing 210008, China;
3. State Key Laboratory of Hydrology-water Resources and Hydraulic Engineering, Hohai University, Nanjing 210098, China;
4. University of Chinese Academy of Sciences, Beijing 100049, China
 2022, Vol. 54
2022, Vol. 54


