2. 中国科学院大学, 北京 100049;
3. 常熟农田生态系统国家野外科学观测研究站, 南京 210008
氮素是水稻产量形成的重要限制因素之一,通过施用氮肥提升水稻产量对解决粮食安全问题发挥了巨大作用。然而,水稻的氮素利用效率随施氮水平的增加趋于平缓,甚至表现出负面效应,并随之引发一系列环境问题。品种改良和氮高效品种的选育,对高量氮投入下的水稻氮素利用率的提升作用明显。另外,从植物营养生理的角度出发,对有关氮高效基因和碳氮平衡调控的研究对改善水稻氮素利用现状也发挥了重要用。本文从当前水稻氮素利用效率的研究现状出发,对水稻氮素利用的基因型差异,基于不同氮素形态吸收和同化利用方式的分子调控手段,以及通过碳氮协同调控水稻氮素利用的研究进行综述,以期对当前氮素生产条件下的水稻氮素营养改良提供支撑。
1 国内外氮肥利用研究现状水稻(Oryza sativa L.)作为全世界最重要的粮食作物之一,为超过半数的人口提供了口粮[1-2]。我国水稻种植面积占耕地总面积的33.0%,水稻生产氮肥消耗量占总量的15.4%。然而,高氮肥消耗不仅造成养分流失,也不利于环境和粮食安全[3]。Dobermann[4]曾认为粮食作物氮肥农学效率为10~30 kg/kg,氮肥利用率为30.0% ~ 50.0%。我国单季稻作区稻田平均氮肥用量为200 kg/hm2,相比世界平均水平高出70%以上,国内主要稻作省份氮肥用量的变幅在50 ~ 400 kg/hm2 [5-6]。张福锁等[7]研究指出,我国水稻的氮肥农学效率为10.4 kg/kg,氮肥利用率为28.3%,和国际水平相比存在较大差距。造成肥料利用率低的主要原因包括高产农田过量施肥,土壤和肥料养分生产潜力未得到充分发挥[8];当然,对土壤和环境养分的利用,以及养分损失未能得到有效阻控等也是氮肥利用率不高的主要原因[3]。另有报道指出,当前中国79% 的水稻产区的产量增势已经趋于停滞[9-10]。可见,水稻生产实践中,在大量施氮以追求持续高产的背景下,氮素营养潜力的发挥并不理想。
2 水稻氮素吸收和利用的基因型差异不同水稻品种氮素利用效率基因型潜力存在较大差异。张亚丽等[11]根据产量表现将177份粳稻材料划分为双高效型、高氮高效型、双低效型、低氮高效型4个基因型,这种划分对氮肥利用率基因型差异的研究提供了新思路。诸多研究也从水稻植株氮素积累和分配、植株农艺性状、生理生化特性、物质积累及产量形成等层面对水稻氮效率基因型差异产生的原因进行了探讨。
2.1 水稻基因型差异在其生育期内氮素营养特征的体现水稻氮效率基因型差异与氮素营养特征密切相关[12-15]。氮素利用效率(NUE)作为评价氮肥生产效益的重要指标,包括吸收和利用两个方面。在不设置不施氮肥的小区试验中,表征方式包括氮素籽粒生产效率(NUEg)、氮素干物质生产效率(NUEb)、氮肥偏生产力(PFPN)和氮素收获指数(NHI)等。而在设置不施氮肥的小区试验中,用氮肥吸收效率(REN)、氮素生理效率(PEN)和氮肥农学效率(AEN)等指标来衡量[16]。据报道,在田间常规氮素管理下,607份不同类型国内外水稻种质AEN、NUEb和NHI存在显著基因型差异;频数分布结果表明,籼型杂交稻的AEN、NUEb和NHI差异小,但分布较集中,常规粳稻最分散,常规籼稻居中[12]。可见,粳稻和籼稻对氮素吸收和利用的差异较大,这种差异或许主要受不同水稻品种本身生理特征差异的影响。有学者以3个NHI有显著差异的基因型水稻品种4434(低NHI)、滇瑞302(中NHI)和余赤231(高NHI)为材料进行研究,发现NHI高的品种花后植株氮素转运量和成熟期水稻茎叶及籽粒全氮含量、蛋白氮和非蛋白氮含量更有优势,不同基因型水稻品种间全氮含量和蛋白氮含量存在显著差异,余赤231灌浆期叶片和籽粒谷氨酰胺合成酶(GS)和谷氨酸合成酶(GOGAT)活性显著高于4434和滇瑞302 [13]。且通过氮效率存在显著差异的水稻研究发现,其NUEb和NHI随施氮水平增加而下降,AEN随生育期推进而上升,水稻NUEb表现为拔节期 > 抽穗期 > 成熟期 > 孕穗期,基因型和氮水平对水稻AEN、NUEb和NHI的影响达极显著水平[14]。另外,也有研究通过长江中下游地区5种生育期类型中相对高产和低产的20个粳稻品种为材料开展田间试验,发现氮素生育期累积量和氮素利用率随着生育期的延长逐渐增加,高产类型明显高于低产类型,两类水稻品种氮素阶段性累积量不尽相同[15]。可见,水稻品种间氮素生理特征在同一或不同生育期均存在明显差异,而这种生理特征的不同导致了氮素利用效率的不同。
深入研究水稻氮效率基因型差异的机理,有利于水稻生产和良种选育。研究人员利用国内外不同年代育成的常规籼稻代表品种进行群体试验,发现NUEg高的品种抽穗期及成熟期茎、鞘、叶中氮素比例小、穗中氮素比例大,结实期茎鞘和叶片氮素运转量大、转运率高[17]。另外,通过群体聚类法研究特青/Lemont F2无性系群体140个株系的氮素吸收利用性状发现,库容量对抽穗期氮素在不同器官的分配比例无明显影响,但随库容量的增大,成熟期氮素在根、茎、叶中的分配比例明显降低,在穗部的分配比例明显增加[18]。随库容的增加,NUEg、NUEb及NHI随库容量的增大均显著提高[18]。氮高效类型水稻相比氮低效类型,在株型构建和物质生产与积累方面存在比较明显的优势。另有研究发现,水稻氮素的阶段性积累量,除有效分蘖临界叶龄期至拔节阶段外,其余各阶段氮高效类型水稻的氮积累量均极显著高于氮低效类型。就水稻氮素的阶段性积累率而言,移栽至拔节阶段氮低效类型水稻显著大于氮高效类型,而在拔节至成熟阶段则表现出相反的趋势。抽穗前的氮素转移量和转移率,氮高效类型水稻显著或极显著大于氮低效类型,而抽穗前氮对籽粒的贡献率,氮高效类型极显著低于氮低效类型[19]。另外,与高产氮中效品种相比,高产氮高效品种总氮累积量低于其1.7%,但在齐穗期至成熟期的氮积累量高出其6.5%,可以认为最终总氮积累量的高低并不是判定是否氮高效品种的绝对条件[20];而常规籼稻和粳稻相比,籼粳杂交稻有更强的氮素积累和茎鞘氮素转移能力[21-22]。有研究通过15N标记试验发现,氮高效水稻在齐穗期以后比氮低效水稻具有更强的氮素吸收和转运能力,其中一个重要原因是各氮效率基因型水稻生育后期衰老特性差异较大[23]。可以看出,氮素利用效率在不同品种间的差异较大,主要受不同品种生理生化特征和不同生育期植株氮素积累和转运效率不同的影响,而这种差异也与研究人员选择的材料和衡量指标关系密切。
2.2 水稻氮效率基因型差异与产量形成和光合特征水稻产量特征与光合作用的基因型差异也是解释水稻氮效率生理机制不同的重要策略。有研究通过选用生育期相近(142 d左右)的中熟中籼和中熟中粳开展田间试验,发现粳稻平均产量随施氮量呈增加趋势,而籼稻平均产量在中氮水平达最高,高氮水平有所降低,而系列氮水平下籼稻产量高于粳稻,且籼稻有较高的穗粒数和千粒重[24]。另外,以225 kg/hm2为施氮量,通过长江中下游地区5种生育期类型中相对高产和低产的20个粳稻品种为材料开展田间试验,发现高产水稻类型的平均产量分别比低产类型高出21% 以上[15];通过4个粳稻品种进行研究,发现在施氮量低于200 kg/hm2时,淮稻5号和连粳7号籽粒产量和氮素吸收均高于宁粳1号和扬粳4038;在高施氮量时,4个品种的籽粒产量无差异[25]。可见,籼稻和粳稻的产量形成对施氮水平存在响应差异;同在粳稻品种间,同一氮水平或不同氮水平下的产量表现也存在明显不同。
水稻叶片含氮量的变化与其净光合速率关系密切,进而影响植株物质生产。研究发现,Rubisco酶在不同氮效率基因型间含量差异不大,两种氮效率基因型间的净光合速率(Pn)在幼穗分化期差异不明显,而在齐穗期氮低效基因型的Pn低于高效基因型;氮低效基因型在幼穗分化和齐穗两个时期的单位叶绿素光合速率(Pn/Chl)比氮高效基因型分别低18.51% 和29.67% 左右,孕穗期氮高效品种谷氨酰胺合成酶活性高于低效品种,而可溶性蛋白含量较低;在成熟期氮高效基因型干物质积累能力强,籽粒产量高,说明氮效率不同的基因型对氮肥的生理反应差异大[26]。超级杂交稻相对普通杂交稻的产量优势是由于源库能力的提高所产生的[27-28]。不同氮效率水稻开花期叶片Pn值差异并不显著,但氮高效基因型水稻碳氮代谢关键酶活性和蛋白质含量明显高于氮低效品种[29]。齐穗后,氮高效基因型水稻的叶绿素、叶片含氮量、净光合速率、光合功能期、叶绿素荧光动力学参数中的最大光化学效率(Fv/Fm)和PSII的潜在活性(Fv/Fo)等均显著高于氮低效基因型,这些参数与其氮素利用率和结实率有极显著相关性[30]。水稻氮素利用效率与剑叶光合速率显著相关,与氮低效基因型水稻相比,氮高效水稻花后剑叶抗氧化酶活性较高,可有效阻止叶片衰老,延长其光合功能期的同时提高氮肥利用率[31]。与宁粳1号和扬粳4038相比,淮稻5号和连粳7号灌浆过程中作物生长速率、光合效率和非结构性碳水化合物的迁移率均较高[25]。另外,也有研究认为,灌浆期较高的Pn和更有效的碳水化合物转运有助于超级杂交稻保持较高的灌浆效率[28]。光合效率的差异导致了水稻干物质生产和籽粒灌浆效率的不同。上述研究结果也表明,水稻品种间光合效率的差异与植株氮素生理特征和源库关系的协调有密切关系。
由此可见,基因型差异对水稻氮素吸收利用的影响体现在多个方面,包括氮素在生育期或阶段生育期的积累、植株干物质和籽粒生产效率、光合作用特征和氮素代谢的生理特征。氮高效基因型和氮低效基因型水稻的氮素干物质生产效率往往随植株氮素含量的升高而上升;同样氮素水平下,氮低效基因型水稻茎鞘、叶片和根系干物质占比要高于氮高效基因型水稻,而后者干物质积累向穗部转运的能力更强,更易表现出产量优势。氮高效品种在生育后期具有更为理想的库容量和更强的氮素吸收和转移能力。氮素利用效率的基因型差异或许很大程度上是由各生育期“源库关系”的不同或者强弱所造成,由这种差异所导致的产量形成潜力和生理特征的不同为氮高效水稻品种的培育提供了现实条件。
2.3 水稻氮效率基因型差异与其根系生物学特性水稻根系是植株获取生长介质中矿质养分的主要器官,与植株地上部物质交流密切。水稻根系发育直接影响地上部性状,而水稻的根系数量、体积、表面积和活力等形态建成和生理变化过程都有自身的规律[32]。同一根系中不同类型的直根系或不定根须在生长介质中的空间造型和分布决定了根系构型。水稻高产栽培要求培育有利于塑造理想根型的水稻品种。目前有关水稻根系形态与氮素利用效率关系的研究颇为活跃[33]。根系构型主要反映在各类根的根长、根重和吸收面积等指标上。根系表型上的适应性是根系对养分局部供应的反应,也是对土壤其他环境条件局部变化的反应[34]。有研究发现,拔节期氮吸收高效的水稻基因型总根长、根密度、根表面积均极显著高于氮低效、氮中效基因型,且氮高效基因型水稻根系活跃吸收面积大,氧化还原能力和氮代谢相关酶活性强[35]。与低产类型品种相比,高产类型品种在根干重、根体积、根系总吸收表面积、根系活跃吸收表面积、根系α-NA氧化量及根系伤流强度等方面在各个生育时期优势明显,说明生产力的提高伴随着根系形态特征的改善和生理活性的加强。然而,较之高产氮中效类型,高产氮高效型水稻的群体根干重、群体根体积、群体根系伤流强度和根系总吸收表面积均有所降低,而单茎根干重、单茎根体积、单茎根系伤流强度、活跃吸收表面积比及根系氧化力却有显著提高[36]。有效分蘖临界叶龄期、拔节期、抽穗期和成熟期,水稻根干重、根体积、根系α-NA氧化量、总吸收表面积、活跃吸收表面积和活跃吸收表面积比与氮素利用效率呈显著正相关[37]。有效分蘖临界叶龄期和拔节期,植株的根冠比与氮素利用效率呈显著正相关,而抽穗和成熟期则呈极显著负相关,氮高效型水稻在其整个生育期中具有良好的根系形态,并且能保持较强的根系活力,为植株大量吸收和高效利用氮素奠定了基础[37]。此外,有研究以氮高效品种南光和氮低效品种Elio作为试验材料,通过低氮和高氮供应水平研究,认为根系形态及根系活力的差异是造成水稻氮效率差异的重要原因[38]。也有研究以籼稻天优华占、两优培九和粳稻陵香优18、宁粳1号为材料进行试验,发现根系活跃吸收表面积、根系伤流量和根系活力高的水稻品种更有利于在降低施氮量的同时提高产量和氮肥利用率[39]。超级杂交稻之所以具有生产优势,更高的根系生物量和根系活力是其原因之一[27]。相比于宁粳1号和扬粳4038,淮稻5号和连粳7号灌浆过程中根系和地上部生物量、根系分布深度、根长、根系氧化活性均较高[25]。有报道指出,水稻抽穗期根系形态与产量关系极为密切,合理的水氮管理措施能够优化根系形态的同时提高籽粒产量。氮高效品种抽穗期粗分枝根长度和氮低效品种细分枝根表面积对优化的施肥措施有积极反应,通过这些措施籽粒产量均得以提升[40]。
铵态氮(NH4+-N)和硝态氮(NO3–-N)是土壤中主要存在且能被植物直接吸收利用的氮素形态[41]。通过米氏动力学方程对水稻NH4+吸收速率的研究发现,吸氮能力不同的水稻品种的vmax相差较小,而Km值差异达极显著水平[42-43],这种差异回应了氮效率基因型差异水稻对土壤氮素水平响应的不同。除此之外,水稻品种会对固氮微生物的群落结构产生显著影响,水稻品种差异是水稻根部内生固氮菌的群落结构不同的重要成因[44]。有研究通过4个水稻品种和3个氮肥施用水平对水稻根部内生固氮菌的影响进行研究,发现β变形菌是优势固氮微生物类群,氮肥对水稻根部内生固氮微生物群落结构的影响取决于水稻品种[45]。另据报道,水稻根系能通过硝酸盐转运蛋白OsNRT1.1B调控具有氮转化能力的微生物,对不同水稻品种的田间氮肥利用效率发挥作用[46]。水稻根系也可与土壤中真菌互作并形成丛枝菌根,促进水稻根系对氮素的吸收,而过低的土壤氮素水平反而抑制菌根的形成[47]。因此,作为对地上部提供矿质营养的主要器官,水稻根系表面积、根密度、根系生物量和根系活力与氮素吸收关系密切,不同氮效率基因型差异的水稻品种,根系生物学特征存在明显差异,良好的根型有利于水稻氮素利用效率的提升。当然,根型差异也与土壤氮素营养环境存在密切的交互关系,培育拥有理想根系构型和特征的水稻品种也是提升水稻氮素利用效率的重要手段。
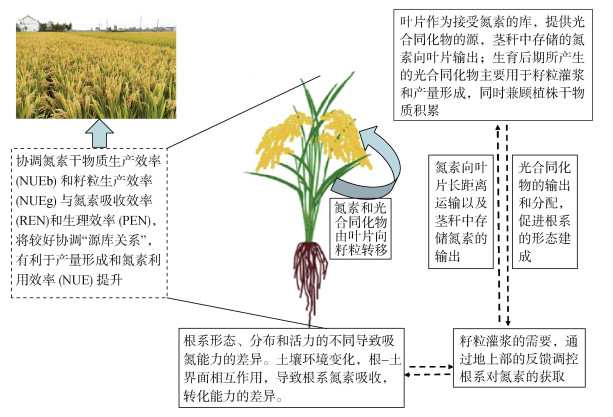
有关水稻氮素利用效率基因型差异研究的持续深入,是实际生产中氮素养分管理和氮高效品种培育的重要指引。在主要稻作区,高氮投入导致氮素利用效率不高的主要原因在于植株体内的冗余氮素不能被及时同化利用,影响植株根系生理特征对土壤氮素状况的响应,这种差异性的变化扰乱了水稻植株干物质生产与氮素生理利用过程的平衡。叶片是氮素接受和同化的主要库器官,也是光合同化物输出的源器官,根系从土壤中获取的氮素和茎秆中所存储的氮素均会向叶片输送,通过光合作用生成光合同化物,用于根系生长发育和形态建成;而在高氮投入情况下,功能叶片首先受到植株氮素环境变化的影响,不同氮效率水稻品种在这方面的体现更为明显;而功能叶高效的光合同化能力则更有利于稻株应对高氮投入时的氮素利用,尤其在灌浆阶段,协调植株的氮素干物质生产效率、籽粒生产效率与氮素吸收效率和生理效率之间的关系,将更好地协调灌浆阶段各要素间的“源库关系”,从而促进产量形成和氮素利用效率的提升(图 1)。
|
图 1 生育后期水稻氮素利用的源库关系 Fig. 1 Source-sink relationship of nitrogen utilization in late growth stage of rice |
通过分子育种或基因工程等途径培育高氮素利用效率的水稻品种将成为提高氮素利用效率至关重要的手段。水稻氮素利用效率差异在分子生理层面的体现,主要在于一系列对应氮素形态的吸收、转化和利用过程,利用分子层面的调控手段研究发现,有关遗传操作对水稻氮素利用效率均存在比较明显的作用。铵态氮是水稻吸收的主要氮素形态,就水稻铵转运蛋白(OsAMT)而言,研究的内容主要体现在OsAMT1基因家族[48];硝态氮作为可供水稻吸收的另外一种无机氮源,在水稻中也存在一套精密且高效的吸收转运系统。目前报道较多的主要是OsNRT1/PTR家族和OsNRT2家族成员[49]。另外,尿素是水稻生产中广泛使用的速效氮源,植物可以从环境中直接吸收尿素[50]。有关氨基酸吸收利用机理的研究也有较多报道,OsAAPs是其中一类研究比较深入的氨基酸转运蛋白[51]。硝态氮被根吸收后,被胞质硝酸还原酶(OsNR)还原为亚硝态氮;亚硝酸还原酶(OsNIR)将进入质体的亚硝态氮还原生成铵[52]。硝态氮进入植株体后需要在一系列转换过程下形成铵态氮才能被同化利用。正常生长条件下,GS/GOGAT循环是水稻铵态氮代谢的主要途径。在水稻中有3个GS1同工酶成员,所对应的OsGS1;1和OsGS1;2在所有器官均有表达,OsGS1;3在小穗和成熟种子专一表达,对氮素向籽粒的转移起作用[53]。除GS/GOGAT外,谷氨酸脱氢酶(GDH)也是氮素转化利用过程中的重要酶,线粒体NADH-GDH可催化谷氨酸逆转化为2-OG和铵态氮[54],而3个OsNADH-GDH基因在不同器官的差异表达取决于氮素可利用特性[55]。除此之外,天冬酰胺(Asn)在氮的动态循环中发挥关键作用,OsASN1的过表达有利于苗期氮素吸收,籽粒蛋白质含量和产量有所增加[56]。另外,天冬氨酸转氨酶(AAT)在氮代谢过程中发挥重要作用,AAT参与碳氮代谢,并催化天冬氨酸(Asp)转化为2-OG,OsAAT1和OsAAT2过表达可以改变籽粒氮代谢,有利于增加籽粒氨基酸含量[57]。相对于生产而言,特定功能基因的突变、表达水平的降低或过表达都可以理解为对水稻氮素利用效率的一种调控策略。当前更多研究的关注还是在于特定基因的过表达,而大量有关铵转运蛋白、硝酸盐转运蛋白、同化和代谢酶类、部分氨基酸转运蛋白的过表达已经被尝试探究,其中多数都对氮素的吸收利用发挥了促进作用,在一定程度上对水稻氮素利用效率有所提升(表 1)。
|
|
表 1 一些关键基因过表达后对水稻氮素利用的影响 Table 1 Effects of overexpression of some key genes on nitrogen utilization in rice |
碳源供应不足严重影响植物对氮素的吸收利用,进而将影响植株的生长发育和籽粒生产。植物所处环境CO2浓度的变化与其光合效率密切相关。自工业革命以来,大气CO2浓度由最初的280 μmol/mol上升至400 μmol/mol,预计到21世纪末达到700 μmol/mol[72]。CO2升高对水稻种植系统氮素利用效率的影响及对未来气候变化条件下的氮素管理具有重要意义。在较高的CO2条件下,植物氮素积累与生物量和籽粒产量密切关联[73]。升高的CO2强烈影响水稻的生长和产量形成,从而导致植株对氮的吸收和利用发生变化。这主要由于CO2的增加可以刺激光合作用,促进水稻营养生长的同时提高产量[74]。
大气CO2浓度升高(free-air carbon-dioxide enrichment,FACE)技术处理下,水稻氮素利用效率对升高的CO2有积极的响应,各组织和整个植株的氮含量均显著下降,其中叶和茎的氮含量下降幅度较大,总氮积累量保持不变,但大量的氮被分配到了穗部[72]。遗传改良后水稻的碳响应对氮素利用也能发挥作用,过表达OSA1可以提高质膜H+-ATPase的活性,促进NH4+吸收和同化,增强叶片在饱和光强下的气孔导度、光合速率和NH4+代谢,进而提升水稻籽粒产量。质膜H+-ATP酶被发现可以调节水稻NH4+吸收,基于OSA1的遗传操作可使水稻根系适应更大土壤NH4+含量范围,谷氨酰胺合成酶(GS1;2和GS2)和谷氨酸合成酶相关基因在OSA1过表达株系中有所上调[75]。OSA1之所以能够关联并促进NH4+的吸收和同化,主要因为该基因通过调节气孔开放参与碳的固定。OSA1过表达株系气孔开度的增加伴随气孔导度和光合速率增强,为NH4++的代谢过程提供了更多的碳骨架和能量,这也与光合作用相关基因表达上调结果一致。水稻植株的氮吸收和光合活性通过整体碳氮状况存在内在联系[76],而通过OSA1过表达可以实现水稻植株碳氮协同的目的。
由此可见,在一定生境下,稻株在生育进程中所处CO2浓度的升高对其氮素的分配和利用有积极影响,此时整个植株茎叶成为氮素向籽粒转移的源,而光合作用在这一过程中发挥主要驱动作用。叶片作为光合同化物向籽粒输出的源,碳的同化利用将增强干物质的输出,为后续的同化利用提供了更为有利的条件,这种作用在促进物质生产和合理分配的同时,提升了水稻氮素利用效率。另外,通过遗传改良手段强化光合碳同化过程,能促进植株更好利用氮素,这种手段主要体现在对气孔运动的调控过程中。气孔作为植株与外界进行气体交换的门户,通过调控保卫细胞膨压对气孔运动过程的干预,将为植株碳源的收支提供调控策略。
5 总结和展望氮素是目前稻田生态系统中研究最为广泛的营养元素。一方面,通过选用以产量和氮素收获指数等指标为前提标定的具有代表性的氮效率基因型差异水稻品种,从植株整个生育期或某一阶段生育期对氮素的积累状态、干物质和籽粒生产效率、氮素的转运状态、植株光合生理特征等各方面来阐述水稻氮素利用效率差异的生理机制,这种差异所导致的产量形成潜力和生理特征的不同,为氮高效水稻品种的选育提供了现实条件,并在高氮肥投入的生产背景下得到广泛应用。另一方面,进一步认识氮素利用效率在分子水平上各因子间的调控关系,成为解决当前水稻生产中氮素利用效率不高这一问题的关键步骤。有关水稻氮素吸收和利用的多个基因位点单独在水稻植株中过表达以调控其氮素利用的尝试已经有了诸多进展,而具体的结果仍然比较有限。
另外,水稻所处环境CO2浓度的变化与其光合效率密切相关。CO2是植物进行光合作用的底物,氮素的同化需要消耗能量和碳骨架作为支撑。在当前多个稻作区施氮过量的背景下,多数研究认为氮素利用率不高,主要是因为高施氮量打破了植株体内的碳氮平衡,碳源供应不足,导致水稻内环境中大量氮素不能被及时利用,原始氮素形态在体内累积过量,导致毒害和严重的内耗,进而影响水稻产量潜力的发挥。因此,基于气孔调控增碳的分子策略,开展高施氮背景下增加碳源供应来促进氮素吸收利用的研究,也将为水稻氮素利用效率的持续改善提供更多途径。
| [1] |
Zhang Q F. Strategies for developing green super rice[J]. Proceedings of the National Academy of Sciences of the United States of America, 2007, 104(42): 16402-16409 DOI:10.1073/pnas.0708013104 (  0) 0) |
| [2] |
Hu Q, Jiang W Q, Qiu S, et al. Effect of wide-narrow row arrangement in mechanical pot-seedling transplanting and plant density on yield formation and grain quality of Japonica rice[J]. Journal of Integrative Agriculture, 2020, 19(5): 1197-1214 DOI:10.1016/S2095-3119(19)62800-5 (  0) 0) |
| [3] |
Cui Z L, Wang G L, Yue S C, et al. Closing the N-use efficiency gap to achieve food and environmental security[J]. Environmental Science & Technology, 2014, 48(10): 5780-5787 (  0) 0) |
| [4] |
Dobermann A R. Nitrogen use efficiency-state of the art[J]. Agronomy-Faculty Publications, 2005, 316 (  0) 0) |
| [5] |
Fan M S, Lu S H, Jiang R F, et al. Nitrogen input, 15N balance and mineral N dynamics in a rice–wheat rotation in southwest China[J]. Nutrient Cycling in Agroecosystems, 2007, 79(3): 255-265 DOI:10.1007/s10705-007-9112-8 (  0) 0) |
| [6] |
Peng S B, Buresh R J, Huang J L, et al. Improving nitrogen fertilization in rice by sitespecific N management. A review[J]. Agronomy for sustainable development, 2010, 30(3): 649-656 DOI:10.1051/agro/2010002 (  0) 0) |
| [7] |
张福锁, 王激清, 张卫峰, 等. 中国主要粮食作物肥料利用率现状与提高途径[J]. 土壤学报, 2008, 45(5): 915-924 DOI:10.3321/j.issn:0564-3929.2008.05.018 (  0) 0) |
| [8] |
Ju X T, Xing G X, Chen X P, et al. Reducing environmental risk by improving N management in intensive Chinese agricultural systems[J]. PNAS, 2009, 106(9): 3041-3046 DOI:10.1073/pnas.0813417106 (  0) 0) |
| [9] |
Peng S B, Tang Q Y, Zou Y B. Current status and challenges of rice production in China[J]. Plant Production Science, 2009, 12(1): 3-8 DOI:10.1626/pps.12.3 (  0) 0) |
| [10] |
Ray D K, Ramankutty N, Mueller N D, et al. Recent patterns of crop yield growth and stagnation[J]. Nature Communications, 2012, 3: 1293 DOI:10.1038/ncomms2296 (  0) 0) |
| [11] |
张亚丽, 樊剑波, 段英华, 等. 不同基因型水稻氮利用效率的差异及评价[J]. 土壤学报, 2008, 45(2): 267-273 DOI:10.3321/j.issn:0564-3929.2008.02.011 (  0) 0) |
| [12] |
程建峰, 戴廷波, 曹卫星, 等. 不同类型水稻种质氮素营养效率的变异分析[J]. 植物营养与肥料学报, 2007, 13(2): 175-183 DOI:10.3321/j.issn:1008-505X.2007.02.001 (  0) 0) |
| [13] |
程建峰, 戴廷波, 曹卫星, 等. 不同氮收获指数水稻基因型的氮代谢特征[J]. 作物学报, 2007, 33(3): 497-502 (  0) 0) |
| [14] |
程建峰, 蒋海燕, 刘宜柏, 等. 氮高效水稻基因型鉴定与筛选方法的研究[J]. 中国水稻科学, 2010, 24(2): 175-182 DOI:10.3969/j.issn.1001-7216.2010.02.12 (  0) 0) |
| [15] |
殷春渊, 张庆, 魏海燕, 等. 不同产量类型水稻基因型氮素吸收、利用效率的差异[J]. 中国农业科学, 2010, 43(1): 39-50 DOI:10.3864/j.issn.0578-1752.2010.01.005 (  0) 0) |
| [16] |
彭少兵, 黄见良, 钟旭华, 等. 提高中国稻田氮肥利用率的研究策略[J]. 中国农业科学, 2002, 35(9): 1095-1103 DOI:10.3321/j.issn:0578-1752.2002.09.012 (  0) 0) |
| [17] |
董桂春, 王余龙, 周娟, 等. 不同氮素籽粒生产效率类型籼稻品种氮素分配与运转的差异[J]. 作物学报, 2009, 35(1): 149-155 (  0) 0) |
| [18] |
单玉华, 王海候, 龙银成, 等. 不同库容量类型水稻在氮素吸收利用上的差异[J]. 扬州大学学报, 2004, 25(1): 41-45 DOI:10.3969/j.issn.1007-8606.2004.01.012 (  0) 0) |
| [19] |
魏海燕, 张洪程, 杭杰, 等. 不同氮素利用效率基因型水稻氮素积累与转移的特性[J]. 作物学报, 2008, 34(1): 119-125 (  0) 0) |
| [20] |
Li M, Zhang H C, Yang X, et al. Accumulation and utilization of nitrogen, phosphorus and potassium of irrigated rice cultivars with high productivities and high N use efficiencies[J]. Field Crops Research, 2014, 161: 55-63 DOI:10.1016/j.fcr.2014.02.007 (  0) 0) |
| [21] |
Huang L Y, Sun F, Yuan S, et al. Different mechanisms underlying the yield advantage of ordinary hybrid and super hybrid rice over inbred rice under low and moderate N input conditions[J]. Field Crops Research, 2018, 216: 150-157 DOI:10.1016/j.fcr.2017.11.019 (  0) 0) |
| [22] |
Xu D, Zhu Y, Chen Z F, et al. Yield characteristics of Japonica/indica hybrids rice in the middle and lower reaches of the Yangtze River in China[J]. Journal of Integrative Agriculture, 2020, 19(10): 2394-2406 DOI:10.1016/S2095-3119(19)62872-8 (  0) 0) |
| [23] |
叶利庭, 宋文静, 吕华军, 等. 不同氮效率水稻生育后期氮素积累转运特征[J]. 土壤学报, 2010, 47(2): 303-310 (  0) 0) |
| [24] |
殷春渊, 魏海燕, 张庆, 等. 不同氮肥水平下中熟籼稻和粳稻产量、氮素吸收利用差异及相互关系[J]. 作物学报, 2009, 35(2): 348-355 (  0) 0) |
| [25] |
Ju C X, Buresh R J, Wang Z Q, et al. Root and shoot traits for rice varieties with higher grain yield and higher nitrogen use efficiency at lower nitrogen rates application[J]. Field Crops Research, 2015, 175: 47-55 DOI:10.1016/j.fcr.2015.02.007 (  0) 0) |
| [26] |
曾建敏, 崔克辉, 黄见良, 等. 水稻生理生化特性对氮肥的反应及与氮利用效率的关系[J]. 作物学报, 2007, 33(7): 1168-1176 DOI:10.3321/j.issn:0496-3490.2007.07.019 (  0) 0) |
| [27] |
Zhang Y B, Tang Q Y, Zou Y B, et al. Yield potential and radiation use efficiency of "super" hybrid rice grown under subtropical conditions[J]. Field Crops Research, 2009, 114(1): 91-98 DOI:10.1016/j.fcr.2009.07.008 (  0) 0) |
| [28] |
Bai P, Bai R Q, Jin Y X. Characteristics and coordination of source-sink relationships in super hybrid rice[J]. Open Life Sciences, 2016, 11(1): 470-475 DOI:10.1515/biol-2016-0061 (  0) 0) |
| [29] |
阮新民, 施伏芝, 罗志祥. 氮高效水稻品种开花期一些生理生化特性与氮肥利用率的关系[J]. 生态环境学报, 2012, 21(11): 1830-1835 DOI:10.3969/j.issn.1674-5906.2012.11.010 (  0) 0) |
| [30] |
魏海燕, 张洪程, 马群, 等. 不同氮肥利用效率水稻基因型剑叶光合特性[J]. 作物学报, 2009, 35(12): 2243-2251 (  0) 0) |
| [31] |
魏海燕, 张洪程, 马群, 等. 不同氮肥吸收利用效率水稻基因型叶片衰老特性[J]. 作物学报, 2010, 36(4): 645-654 (  0) 0) |
| [32] |
Liu K, Li T T, Chen Y, et al. Effects of root morphology and physiology on the formation and regulation of large panicles in rice[J]. Field Crops Research, 2020, 258: 107946 (  0) 0) |
| [33] |
Liang Y, Zhao X Y, Jones A M, et al. G proteins sculp root architecture in response to nitrogen in rice and Arabidopsis[J]. Plant Science, 2018, 274: 129-136 (  0) 0) |
| [34] |
Marschner H, Kirkby E A, Cakmak I. Effect of mineral nutritional status on shoot-root partitioning of photoassimilates and cycling of mineral nutrients[J]. Journal of Experimental Botany, 1996, 47(Special_Issue): 1255-1263 (  0) 0) |
| [35] |
程建峰, 戴廷波, 荆奇, 等. 不同水稻基因型的根系形态生理特性与高效氮素吸收[J]. 土壤学报, 2007, 44(2): 266-272 (  0) 0) |
| [36] |
李敏, 张洪程, 杨雄, 等. 水稻高产氮高效型品种的根系形态生理特征[J]. 作物学报, 2012, 38(4): 648-656 (  0) 0) |
| [37] |
魏海燕, 张洪程, 张胜飞, 等. 不同氮利用效率水稻基因型的根系形态与生理指标的研究[J]. 作物学报, 2008, 34(3): 429-436 (  0) 0) |
| [38] |
樊剑波, 沈其荣, 谭炯壮, 等. 不同氮效率水稻品种根系生理生态指标的差异[J]. 生态学报, 2009, 29(6): 3052-3058 (  0) 0) |
| [39] |
刘立军, 王康君, 卞金龙, 等. 水稻产量对氮肥响应的品种间差异及其与根系形态生理的关系[J]. 作物学报, 2014, 40(11): 1999-2007 (  0) 0) |
| [40] |
李娜, 杨志远, 代邹, 等. 不同氮效率水稻根系形态和氮素吸收利用与产量的关系[J]. 中国农业科学, 2017, 50(14): 2683-2695 (  0) 0) |
| [41] |
Xu G H, Fan X R, Miller A J. Plant nitrogen assimilation and use efficiency[J]. Annual Review of Plant Biology, 2012, 63: 153-182 (  0) 0) |
| [42] |
黄秀, 叶昌, 燕金香, 等. 不同氮吸收效率水稻品种的苗期铵吸收特性及生长差异分析[J]. 中国农业科学, 2021, 54(7): 1455-1468 (  0) 0) |
| [43] |
Chen M, Chen G, Di D W, et al. Higher nitrogen use efficiency (NUE) in hybrid "super rice" links to improved morphological and physiological traits in seedling roots[J]. Journal of Plant Physiology, 2020, 251: 153191 (  0) 0) |
| [44] |
Knauth S, Hurek T, Brar D, et al. Influence of different Oryza cultivars on expression of nifH gene pools in roots of rice[J]. Environmental Microbiology, 2005, 7(11): 1725-1733 (  0) 0) |
| [45] |
Wu L Q, Ma K, Lu Y H. Prevalence of betaproteobacterial sequences in nifH gene pools associated with roots of modern rice cultivars[J]. Microbial Ecology, 2009, 57(1): 58-68 (  0) 0) |
| [46] |
Zhang J Y, Liu Y X, Zhang N, et al. NRT1.1B is associated with root microbiota composition and nitrogen use in field-grown rice[J]. Nature Biotechnology, 2019, 37(6): 676-684 (  0) 0) |
| [47] |
Wang S S, Chen A Q, Xie K, et al. Functional analysis of the OsNPF4.5 nitrate transporter reveals a conserved mycorrhizal pathway of nitrogen acquisition in plants[J]. Proceedings of the National Academy of Sciences of the United States of America, 2020, 117(28): 16649-16659 (  0) 0) |
| [48] |
Konishi N, Ma J F. Three polarly localized ammonium transporter 1 members are cooperatively responsible for ammonium uptake in rice under low ammonium condition[J]. The New Phytologist, 2021, 232(4): 1778-1792 (  0) 0) |
| [49] |
Fan X R, Naz M, Fan X R, et al. Plant nitrate transporters: From gene function to application[J]. Journal of Experimental Botany, 2017, 68(10): 2463-2475 (  0) 0) |
| [50] |
Beier M P, Fujita T, Sasaki K, et al. The urea transporter DUR3 contributes to rice production under nitrogen-deficient and field conditions[J]. Physiologia Plantarum, 2019, 167(1): 75-89 (  0) 0) |
| [51] |
Taylor M R, Reinders A, Ward J M. Transport function of rice amino acid permeases (AAPs)[J]. Plant and Cell Physiology, 2015, 56(7): 1355-1363 (  0) 0) |
| [52] |
Chandna R, Hakeem K R. From agronomy to molecular genetics and proteomics in an effort to improve nitrogen use efficiency in crops[M]//Crop improvement. Boston, MA: Springer, 2013: 345–362.
(  0) 0) |
| [53] |
Tabuchi M, Abiko T, Yamaya T. Assimilation of ammonium ions and reutilization of nitrogen in rice (Oryza sativa L.)[J]. Journal of Experimental Botany, 2007, 58(9): 2319-2327 (  0) 0) |
| [54] |
Fontaine J X, Tercé-Laforgue T, Armengaud P, et al. Characterization of a NADH-dependent glutamate dehydrogenase mutant of Arabidopsis demonstrates the key role of this enzyme in root carbon and nitrogen metabolism[J]. The Plant Cell, 2012, 24(10): 4044-4065 (  0) 0) |
| [55] |
Qiu X H, Xie W B, Lian X M, et al. Molecular analyses of the rice glutamate dehydrogenase gene family and their response to nitrogen and phosphorous deprivation[J]. Plant Cell Reports, 2009, 28(7): 1115-1126 (  0) 0) |
| [56] |
Lee S, Park J, Lee J, et al. OsASN1 overexpression in rice increases grain protein content and yield under nitrogen-limiting conditions[J]. Plant and Cell Physiology, 2020, 61(7): 1309-1320 (  0) 0) |
| [57] |
Zhou Y, Cai H M, Xiao J H, et al. Over-expression of aspartate aminotransferase genes in rice resulted in altered nitrogen metabolism and increased amino acid content in seeds[J]. Theoretical and Applied Genetics, 2009, 118(7): 1381-1390 (  0) 0) |
| [58] |
Ranathunge K, El-Kereamy A, Gidda S, et al. AMT1;1 transgenic rice plants with enhanced NH4+ permeability show superior growth and higher yield under optimal and suboptimal NH4+ conditions[J]. Journal of Experimental Botany, 2014, 65(4): 965-979 (  0) 0) |
| [59] |
Bao A L, Liang Z J, Zhao Z Q, et al. Overexpressing of OsAMT1-3, a high affinity ammonium transporter gene, modifies rice growth and carbon-nitrogen metabolic status[J]. International Journal of Molecular Sciences, 2015, 16(5): 9037-9063 (  0) 0) |
| [60] |
Fan X R, Feng H M, Tan Y W, et al. A putative 6-transmembrane nitrate transporter OsNRT1.1b plays a key role in rice under low nitrogen[J]. Journal of Integrative Plant Biology, 2016, 58(6): 590-599 (  0) 0) |
| [61] |
Fang Z M, Bai G X, Huang W T, et al. The rice peptide transporter OsNPF7.3 is induced by organic nitrogen, and contributes to nitrogen allocation and grain yield[J]. Frontiers in Plant Science, 2017, 8: 1338 (  0) 0) |
| [62] |
Fang Z M, Xia K F, Yang X, et al. Altered expression of the PTR/NRT1 homologue OsPTR9 affects nitrogen utilization efficiency, growth and grain yield in rice[J]. Plant Biotechnology Journal, 2013, 11(4): 446-458 (  0) 0) |
| [63] |
Xia X D, Fan X R, Wei J, et al. Rice nitrate transporter OsNPF2.4 functions in low-affinity acquisition and long-distance transport[J]. Journal of Experimental Botany, 2014, 66(1): 317-331 (  0) 0) |
| [64] |
Hu B, Wang W, Ou S J, et al. Variation in NRT1.1B contributes to nitrate-use divergence between rice subspecies[J]. Nature Genetics, 2015, 47(7): 834-838 (  0) 0) |
| [65] |
Huang W T, Bai G X, Wang J, et al. Two splicing variants of OsNPF7.7 regulate shoot branching and nitrogen utilization efficiency in rice[J]. Frontiers in Plant Science, 2018, 9: 300 (  0) 0) |
| [66] |
Wang W, Hu B, Yuan D Y, et al. Expression of the nitrate transporter gene OsNRT1.1A/OsNPF6.3 confers high yield and early maturation in rice[J]. The Plant Cell, 2018, 30(3): 638-651 (  0) 0) |
| [67] |
Fan X R, Tang Z, Tan Y W, et al. Overexpression of a pH-sensitive nitrate transporter in rice increases crop yields[J]. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(26): 7118-7123 (  0) 0) |
| [68] |
Chen J G, Zhang Y, Tan Y W, et al. Agronomic nitrogen-use efficiency of rice can be increased by driving OsNRT2.1 expression with the OsNAR2.1 promoter[J]. Plant Biotechnology Journal, 2016, 14(8): 1705-1715 (  0) 0) |
| [69] |
Ji Y Y, Huang W T, Wu B W, et al. The amino acid transporter AAP1 mediates growth and grain yield by regulating neutral amino acid uptake and reallocation in Oryza sativa[J]. Journal of Experimental Botany, 2020, 71(16): 4763-4777 (  0) 0) |
| [70] |
Fang Z M, Wu B W, Ji Y Y. The amino acid transporter OsAAP4 contributes to rice tillering and grain yield by regulating neutral amino acid allocation through two splicing variants[J]. Rice (New York, N Y), 2021, 14(1): 2 (  0) 0) |
| [71] |
Cai H M, Zhou Y, Xiao J H, et al. Overexpressed glutamine synthetase gene modifies nitrogen metabolism and abiotic stress responses in rice[J]. Plant Cell Reports, 2009, 28(3): 527-537 (  0) 0) |
| [72] |
Jiang Q, Zhang J S, Xu X, et al. Effects of free-air CO2 enrichment (FACE) and nitrogen (N) supply on N uptake and utilization of indica and Japonica cultivars (Oryza sativa L.)[J]. Ecological Processes, 2020, 9: 35 (  0) 0) |
| [73] |
Wang J Q, Li L Q, Lam S K, et al. Changes in nutrient uptake and utilization by rice under simulated climate change conditions: A 2-year experiment in a paddy field[J]. Agricultural and Forest Meteorology, 2018, 250/251: 202-208 (  0) 0) |
| [74] |
Cai C, Li G, Yang H L, et al. Do all leaf photosynthesis parameters of rice acclimate to elevated CO2, elevated temperature, and their combination, in FACE environments?[J]. Global Change Biology, 2018, 24(4): 1685-1707 (  0) 0) |
| [75] |
Zhang M X, Wang Y, Chen X, et al. Plasma membrane H+-ATPase overexpression increases rice yield via simultaneous enhancement of nutrient uptake and photosynthesis[J]. Nature Communications, 2021, 12: 735 (  0) 0) |
| [76] |
Ariz I, Asensio A C, Zamarreño A M, et al. Changes in the C/N balance caused by increasing external ammonium concentrations are driven by carbon and energy availabilities during ammonium nutrition in pea plants: The key roles of asparagine synthetase and anaplerotic enzymes[J]. Physiologia Plantarum, 2013, 148(4): 522-537 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Changshu National Agro-Ecosystem Observation and Research Station, Nanjing 210008, China
 2022, Vol. 54
2022, Vol. 54


