2. 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所), 南京 210008
原位化学氧化(In situ chemical oxidation,ISCO)技术已经广泛应用于各种土壤与地下水污染的修复,它的基本原理是通过向土壤或地下水中注入氧化剂后,氧化剂在活化剂的作用下分解产生高活性如硫酸根自由基(SO4·–)、羟基自由基(·OH)等活性物质来达到降解污染物的目的[1]。常用的氧化剂有过氧化氢(H2O2)、臭氧(O3)、高锰酸盐(MnO4–)和过硫酸盐(persulfate,PS),在这些氧化剂中,PS由于稳定性、溶解性及传质性好,pH适用范围广等优点而备受关注[2-3]。PS主要包括单过硫酸盐(peroxymonosulfate,PMS)和过二硫酸盐(peroxydisulfate,PDS)两类。PS作为一种硫酸根自由基前体,既可通过光、热、微波、超声等物理手段活化,也可通过与过渡金属离子、金属氧化物、活性炭等发生反应进行活化[4-5],活化产自由基的本质都是PS分子结构中过氧键(-O-O-)断裂形成高活性硫酸根自由基。SO4·–含有一个孤对电子,与传统·OH的氧化还原电位相当(ESO4·–0=2.5 ~ 3.1 V,E·OH0 =1.8 ~ 2.7 V)[2],但具有更长的半衰期[6],容易在土壤或地下水中传质,从而更好地与污染物接触,降解有机污染物。与·OH降解有机污染物的反应机理类似,SO4·–降解有机污染物物反应也主要有3种,分别是:①与烷烃、醇类及酯类等饱和化合物的氢提取反应[7];②与芳香族化合物的电子转移途径[8];③与含不饱和双键的烯烃类化合物的加成反应[9]。综上,基于SO4·–化学氧化技术的优点,其近些年被广泛应用于有机污染物的降解和土壤或地下水污染修复。
当PS通过原位注射等方式投加于土壤或地下水的过程中,其在土壤中的转化分解将是影响其注射、迁移与污染物接触的关键控制因素,最终将影响污染物的修复效果和成本。研究表明,反应pH、矿物、腐殖酸等都会影响活化PS降解有机污染物的效果,但目前大多的工作都是基于纯体系的研究。而土壤是一个复杂的体系,其中土壤pH、土壤矿物和土壤有机质等在不同类型土壤中差异较大,都会影响PS的修复效果[10]。研究发现钒氧化物类矿物能与H2O2发生单电子转移反应产生降解邻苯二甲酸二乙酯(DEP)[11];铁、锰矿物等作为PS常见的活化剂,其在土壤中势必影响PS的分解过程[12]。土壤有机质组成非常复杂且不均匀,其中的活性有机质会直接参与土壤生物化学过程,也会对氧化剂分解产生影响。腐殖质本身是一种富含脂肪族和芳香族结构的物质,它的分子中含有大量活性基团如醌基、羧基和含氮基团等,研究表明醌类基团产生的半醌自由基可以活化PS产生SO4·–降解PCBs[13],但是部分腐殖质也会消耗自由基,从而降低目标污染物的修复效率[14]。Fang等[15]选取了江苏省内10种性质各异的土壤,探究了PS在这10种土壤中的分解、活化和自由基转化机理,结果表明土壤有机质和铁/锰矿物对PS在土壤中的分解起到促进作用,并通过对体系内自由基的测定进一步推测出不同有机质含量土壤中PS分解的途径,但其研究更多侧重于关注土壤中PS分解的主要控制因素及这些因素对PS分解过程中自由基生成与转化的影响,未能全面地考察土壤的其他性质与PS分解之间的相关关系。
基于此,为了系统探究土壤性质对PS在土壤中分解和自由基形成过程的影响,阐明PS与土壤组分的相互作用机制,本研究选择我国16种不同类型的典型土壤,利用电子顺磁共振技术、分子探针等表征手段,深入揭示土壤性质影响PS分解和自由基形成的机制,以期为PS化学氧化技术在土壤修复中的应用提供理论支撑。
1 材料与方法 1.1 供试土壤供试土壤样品在使用前于室内自然风干,去除杂质后磨碎过60目孔径尼龙筛待用。土壤类型根据《中国土壤系统》(1992)[16]的土类进行划分,其基本理化性质如表 1所示。
|
|
表 1 不同类型土壤的理化性质 Table 1 Physiochemical characteristics of different tested soil types |
过硫酸钠(Na2S2O8,> 99%)、碘化钾(KI)、碳酸氢钠(NaHCO3,)、阿特拉津(ATZ,97%)均为分析纯,购自国药集团化学试剂有限公司;5, 5-二甲基-1-吡咯啉-N-氧化物(DMPO,97%)购自百灵威科技有限公司。试验所用超纯水(18.2 MΩ/cm,25 ℃)由Millipore SynergyⓇ纯水机(默克,德国)制备,所有溶液均由超纯水配制。
1.3 试验设计PS分解试验在100 ml玻璃瓶中进行,瓶盖为聚四氟乙烯(PTFE)内衬。反应瓶中含有14 g土壤样品和70 ml 2.0 g/L PS溶液(土壤溶液中2.0 g/L PS相当于在土壤中10 g/kg,是土壤修复应用中氧化剂的常用剂量),并在150 r/min的30 ℃恒温振荡箱中避光培养。在不同时间间隔进行取样,每次取样0.8 ml,离心并过0.22 µm水系滤膜后进行Na2S2O8浓度分析。
1.4 测定与分析Na2S2O8浓度采用改进的碘量法测定[17]。具体操作如下:配制浓度为5 g/L的NaHCO3溶液100 ml,然后将10 g KI固体溶于100 ml的NaHCO3溶液中,配制成100 g/L的KI-NaHCO3溶液。将0.1 ml PS溶液样品和0.9 ml KI-NaHCO3溶液混合均匀,反应15 min显色,用紫外分光光度计在400 nm波长下,测定反应液的吸光度。
自由基种类鉴别采用电子顺磁共振波谱仪(EPR)进行测定,由中国科学院南京土壤研究所分析测试中心完成。用超纯水配制2 mol/L DMPO作为自由基的捕获剂,并设置最终反应浓度为0.1 mol/L。在测定时,将样品注入套有石英试管的毛细管内,将毛细管置于EPR的样品腔中。在X-波段下测试样品,调制功率100 kHz,调制幅度1.0 G,微波功率9.77 GHz,微波功率20.02 mW。
土壤基本理化性质按照《土壤理化分析与剖面描述[18]、《土壤农业化学分析方法》[19]和《土壤理化分析》[20]测定。其中土壤有机质采用重铬酸钾氧化-外加热法测定;土壤无定形铁、锰含量采用草酸-草酸铵浸提-邻菲罗林比色法测定;土壤游离铁、锰含量采用连二亚硫酸钠-柠檬酸钠-重碳酸钠浸提(DCB法)-邻菲罗啉比色法测定;土壤全量铁、锰含量采用HCl-HNO3-HF-H2O2消化-ICP-AES测定;土壤机械组成采用吸管法测定。
1.3 数据统计分析通过伪一级动力学方程(式1)描述反应过程中PS的分解,并根据式2计算出PS的半衰期(t1/2)。
| $ C_\text{t}=C_{0}\text{e}^{–K_{\text{obs}·t}}$ | (1) |
| $ t_{1/2}=\ln 2/K_\text{obs} $ | (2) |
式中:Ct和C0分别表示t时刻和0时刻PS的浓度(mmol/L),Kobs是伪一级动力学常数(d–1),代表PS的分解速率。所有数据均采用Origin 2017进行统计分析。
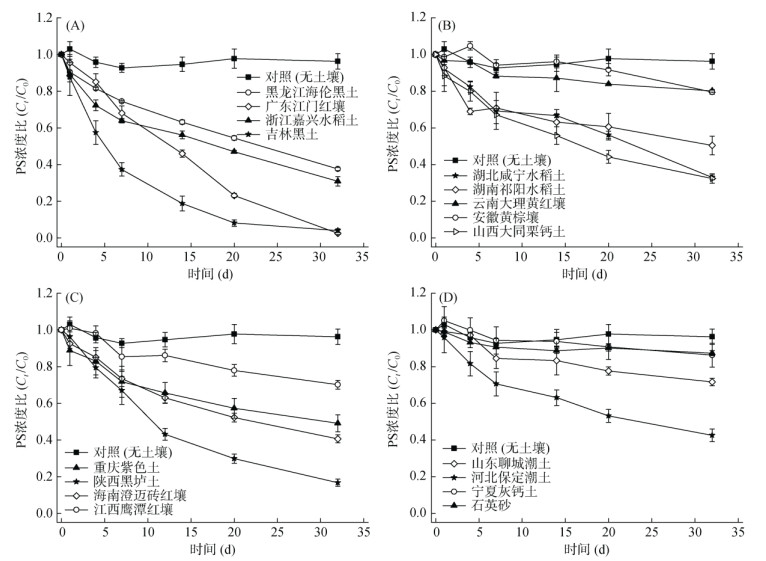
2 结果与分析 2.1 不同类型土壤对过硫酸盐分解的影响PS在不同类型土壤中的分解动力学如图 1所示,按照土壤有机质的含量将其分为 > 30、20 ~ 30、10 ~ 20和 < 10 g/kg 4组。在不同有机质含量的土壤中,PS的分解效率存在显著差异。由图 1可见,在有机质含量较高的吉林黑土处理组中,32 d后PS的分解率为96%;而在有机质含量较低的宁夏灰钙土处理组中,PS在反应结束后仅分解了13.8 %。PS的分解过程可以由准一级动力学方程描述,并根据其反应速率Kobs计算出了半衰期,结果如表 2所示。分解速率最快和最慢的分别是吉林黑土和宁夏灰钙土,Kobs值分别为0.109 2和0.004 8 d–1,对应的PS半衰期分别为6.35和145.93 d。由此可见,不同类型土壤理化性质的差异对PS的分解有显著的影响。
|
(A~D分别表示有机质含量为 > 30、20~30、10~20和 < 10 g/kg土壤类型组) 图 1 不同类型土壤中过硫酸盐的分解动力学 Fig. 1 Kinetics of persulfate decomposition in different soil types |
|
|
表 2 不同类型土壤中过硫酸盐的分解速率和半衰期 Table 2 Reaction rate constant and half-life of persulfate decomposition in different soil types |
一般来说,PS在分解过程中会产生H+降低体系的pH[21],故对反应过程中土壤/PS体系中的pH进行了测定,结果如图 2所示。不同土壤处理组中pH均有降低,在10种偏酸性土壤中,pH平均降低了1.34。其中,变化最大的为重庆紫色土组,pH从6.58降低至4.07;而降低最小的云南大理黄红壤组中pH从6.03降低至5.42。在偏碱性土壤中,除宁夏灰钙土处理组中pH降低1.55外,其余5种土壤处理组平均仅降低了0.41。土壤由于有机质含量、黏土矿物类型和黏粒含量等的不同而具有不同的缓冲性能,导致了PS分解过程中pH变化值的差异。由此可见,在进行污染场地修复时,需要考虑PS对场地土壤pH的影响。

|
图 2 不同类型土壤/过硫酸盐体系中pH的变化 Fig. 2 Changes of pH in different soil/persulfate systems |
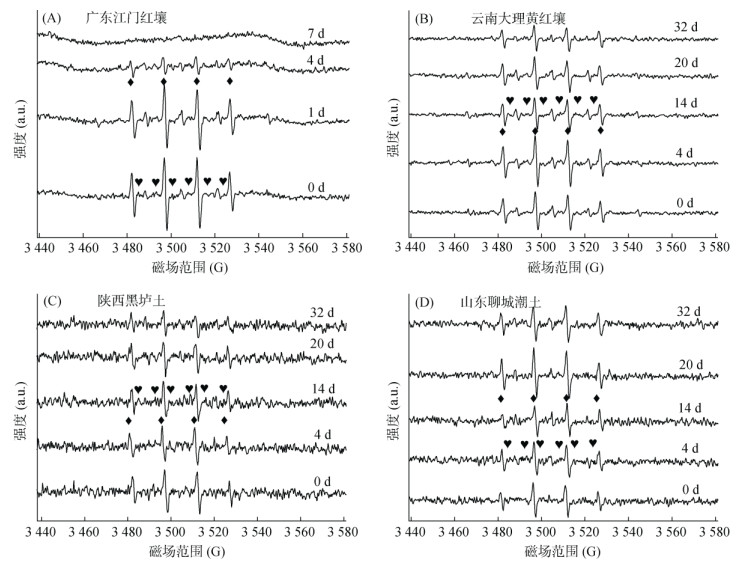
PS的分解往往伴随着自由基的生成和转化[22],这一过程也是原位化学氧化过程降解污染物至关重要的一环。为了鉴别反应过程中产生的自由基种类及变化,利用DMPO作为捕获剂,采用电子顺磁共振波谱仪(EPR)进行了自由基的测定,结果如图 3所示。根据DMPO加成物的超精细结构常数(DMPO-OH:aN=14.4 G,aH=15.6 G,g=2.005 5;DMPO-SO4:aN=13.2 G,aHβ=9.6 G,aHγ1=1.48G,aHγ2=0.78G)[23]可以看出,体系中的自由基主要为羟基自由基(·OH)和硫酸根自由基(SO4·–)。通常·OH是SO4·–与体系中HO–或H2O反应的产物,但由于自由基捕获剂DMPO更容易与·OH反应,且SO4·–在反应过程中会持续生成·OH,故所测得的·OH的信号强度要高于SO4·–的信号强度。
|
(A~D分别表示有机质含量为 > 30、20~30、10~20、< 10 g/kg土壤类型组) 图 3 不同类型土壤/过硫酸盐悬浮液的EPR图谱 Fig. 3 EPR spectroscopy in different soil/persulfate suspensions |
在有机质含量较高的广东江门红壤体系中,反应初期在体系中测到了较高的自由基信号,说明了反应初期PS的分解产生了较高浓度的自由基。但随着反应的进行,自由基信号强度有明显降低,在反应第7天检测到了一个由金属锰离子溶出而引起的宽峰。锰离子作为一种PS的活化剂,可以在反应中加速PS的分解[15]。在云南大理黄红壤和陕西黑垆土体系中,同样也可在反应32 d观察到·OH信号的减弱。而在有机质含量较低的山东聊城潮土体系中,反应32 d自由基信号没有明显降低,说明PS在低有机质含量的土壤中分解较少,自由基产生量也较少。以上结果说明了PS的分解有诱导自由基的产生,且有机质含量较高的土壤中,由于PS分解较快而在反应初期就能形成较高浓度的自由基,但随着PS浓度的降低自由基的浓度也随着降低;在低有机质的土壤中,尽管PS分解速率较慢导致自由基的浓度低,但自由基会在整个反应过程持续更长的时间。
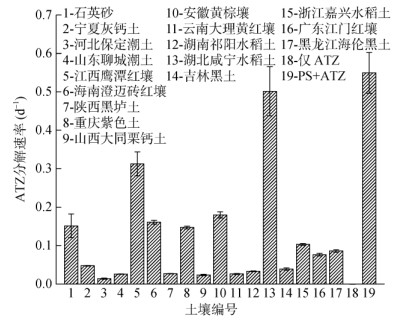
·OH和SO4·–都是高活性自由基,在两者同时存在的体系中,单独的·OH或SO4·–分子探针很难进行选择,如苯甲酸(BA)作为Fenton体系中常用的·OH探针也能与SO4·–反应[24],且·OH与BA的产物对羟基苯甲酸(p-HBA)能进一步与SO4·– 反应[25],这就使得定量产生较大误差。为了能更准确地定量自由基,选取阿特拉津(ATZ)为分子探针,对PS/土壤体系中·OH和SO4·– 的总量间接进行表征。ATZ能快速与·OH和SO4·–发生反应,并且与两者具有相似的反应速率(KATZ+·OH=(2.5 ~ 3.0)×109 L/(mol·s),KATZ+ SO4·– =(2.6 ~ 3.5)×109 L/(mol·s))[26-28],这就避免了因反应速率差异过大而导致的捕获不充分。在只有ATZ存在的对照组中,ATZ基本没有分解,故土壤体系中ATZ的分解主要归因于·OH和SO4·–的产生。根据32 d的ATZ的分解动力学,计算出了ATZ的分解速率,如图 4所示。对比PS的分解速率(表 2)发现,PS分解速率较快的几组土壤如吉林黑土、广东江门红壤和安徽黄棕壤中,ATZ分解速率却较低。这说明土壤中的有机质等活性组分会与ATZ竞争自由基,从而降低ATZ的分解速率。在没有土壤的对照组中,ATZ的分解速率达到0.549,分析可能是由于环境温度对PS产生了一定的活化效果,产生的自由基全部作用于ATZ的分解而没有其他消耗。这也从侧面表明土壤会对PS活化产生的自由基有一定的消耗。
|
图 4 不同类型土壤/过硫酸盐体系中ATZ分解的速率 Fig. 4 ATZ decomposition rates in different soil/persulfate systems |
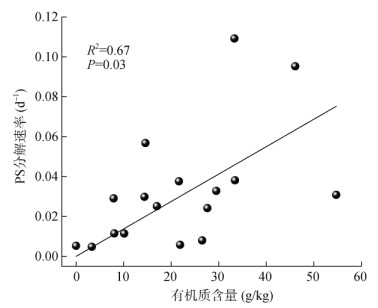
矿物和有机质是土壤固相的主要组成部分,也是很有潜力的PS活化剂[29],且土壤成分也显著影响着土壤的理化性质。为了探究土壤体系中复杂成分与PS分解之间的相关性,分别将土壤有机质含量,不同形态铁、锰浓度和颗粒含量与PS分解速率进行相关性分析。在Fang等[15]的研究中,通过将10种土壤的有机质含量与PS的分解速率进行相关性分析,表明有机质是PS分解的主要控制因素(R2=0.727,P < 0.05),本试验也获得了类似的结果,如图 5所示。PS在32 d内的分解速率与16种土壤的有机质含量呈正相关,R2为0.67(P < 0.05)。
|
图 5 过硫酸盐分解速率与土壤有机质含量之间的相关性 Fig. 5 Correlation between soil organic matter content and persulfate decomposition rate |
为进一步研究矿物与PS分解之间的关系,测定了土壤中全铁、游离铁、无定形铁含量和全锰、游离锰、无定形锰含量,并与PS的分解速率(Kobs)进行相关性分析。由图 6可见,不同类型的Fe含量与Kobs之间的相关性不显著,而无定形锰的含量与Kobs之间呈显著的正相关(R2=0.78,P < 0.05)。有研究表明,土壤中锰氧化物的含量虽然比铁氧化物的含量低一、二个数量级,但活性却比铁氧化物高得多[30],故而土壤中锰的含量更能影响到PS的分解过程。且在复杂的土壤体系中,矿物往往会相互团聚或与有机质形成复合体,这就进一步限制了土壤中铁氧化物的反应活性。在Fang等[15]的研究中发现,在去除土壤中有机质后,Fe、Mn含量与PS分解速率之间的相关性大大提高。这说明在土壤体系中,有机质往往优先于矿物与PS反应[31],故当多种活性因子同时存在时,要综合考虑各部分对氧化剂的作用效果。

|
图 6 过硫酸盐分解速率与不同形态Fe、Mn含量之间的相关性 Fig. 6 Correlation between different species of Fe, Mn contents and persulfate decomposition rate |
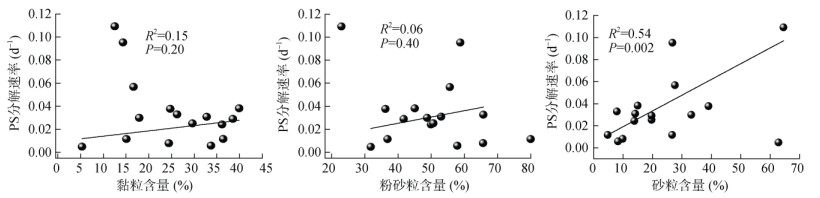
土壤颗粒是构成土壤固相的物质,其组成和含量会直接影响土壤的性质,而土壤性质的不同影响着氧化剂的分解[32]。根据土壤颗粒的大小,将其分为黏粒(< 0.002 mm)、粉砂粒(0.05~0.002 mm)和砂粒(2~0.05 mm)3部分,不同部分的含量与PS分解Kobs之间的相关性如图 7所示。由图 7可知,只有砂粒含量与Kobs之间具有一定的相关性(R2=0.54,P < 0.05),黏粒和粉砂粒含量与Kobs之间的相关性不显著。已有研究报道,土壤颗粒中黏粒含量与有机质含量呈正相关关系,但是这部分有机质与土壤黏粒往往结合紧密难以分解[33]。而砂粒易与土壤中较细颗粒结合形成更大的稳定性较差的土壤团聚体[34],且有研究表明与粗砂粒相结合的有机质分解要快于与细黏粒相结合的有机质[35-36]。故在本试验中,振荡反应使得与砂粒-有机质团聚体分散开来,释放出来的有机质与PS快速反应,引起PS的分解。
|
图 7 过硫酸盐分解速率与土壤颗粒含量之间的相关性 Fig. 7 Correlation between soil particle composition and persulfate decomposition rate |
1) 不同类型土壤中PS分解速率存在显著差异,其中有机质含量较高的土壤对PS的分解要明显快于有机质含量低的土壤,在土壤中PS半衰期会缩短一半以上。土壤有机质和无定形锰的含量是PS分解的主要影响因素。但是由于土壤组成和成分的复杂性,PS的分解与不同类型的Fe含量之间的相关性不显著,与砂粒含量之间的相关性相对显著。
2) PS活化主要产生硫酸根自由基(SO4·–)和羟基自由基(·OH),不同类型土壤中PS产生的自由基含量不同。高有机质土壤中SO4·–和·OH信号强度较高,但消耗得也较快;低有机质土壤中SO4·–和·OH信号强度较低,存在时间也较长。说明有机质既能活化PS产生SO4·–,也会加速自由基的消耗,造成PS的额外损失。
3) 以上结果说明在修复过程中,场地土壤会对PS造成不同程度的损耗,土壤性质如pH也会发生一定改变,故在原位化学氧化中要根据不同土壤的性质来适当调整施用的PS的用量,以达到预期的理想修复效果。
| [1] |
Tsitonaki A, Petri B, Crimi M, et al. In situ chemical oxidation of contaminated soil and groundwater using persulfate: A review[J]. Critical Reviews in Environmental Science and Technology, 2010, 40(1): 55-91 DOI:10.1080/10643380802039303 (  0) 0) |
| [2] |
Oh W D, Dong Z L, Lim T T. Generation of sulfate radical through heterogeneous catalysis for organic contaminants removal: Current development, challenges and prospects[J]. Applied Catalysis B: Environmental, 2016, 194: 169-201 DOI:10.1016/j.apcatb.2016.04.003 (  0) 0) |
| [3] |
Watts R J, Teel A L. Treatment of contaminated soils and groundwater using ISCO[J]. Practice Periodical of Hazardous, Toxic, and Radioactive Waste Management, 2006, 10(1): 2-9 DOI:10.1061/(ASCE)1090-025X(2006)10:1(2) (  0) 0) |
| [4] |
姚晨辉, 朱金远, 张永清, 等. 活性炭活化过硫酸盐选择降解含氯有机物的研究[J]. 广东化工, 2021, 48(20): 153-154, 164 DOI:10.3969/j.issn.1007-1865.2021.20.058 (  0) 0) |
| [5] |
Wang J L, Wang S Z. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants[J]. Chemical Engineering Journal, 2018, 334: 1502-1517 DOI:10.1016/j.cej.2017.11.059 (  0) 0) |
| [6] |
Wu S M, Wang P, Qin J W, et al. GSH-depleted nanozymes with dual-radicals enzyme activities for tumor synergic therapy[J]. Advanced Functional Materials, 2021, 31(31): 2102160 DOI:10.1002/adfm.202102160 (  0) 0) |
| [7] |
Khursan S L, Semes'ko D G, Safiullin R L. Quantum-chemical modeling of the detachment of hydrogen atoms by the sulfate radical anion[J]. Russian Journal of Physical Chemistry, 2006, 80(3): 366-371 DOI:10.1134/S0036024406030113 (  0) 0) |
| [8] |
储高升, 张淑娟, 都志文, 等. SO4-自由基氧化苯丙氨酸反应机理的图谱表征[J]. 中国科学(B辑化学), 2002, 32(3): 248-254 (  0) 0) |
| [9] |
Padmaja S, Alfassi Z B, Neta P, et al. Rate constants for reactions of SO4·- radicals in acetonitrile[J]. International Journal of Chemical Kinetics, 1993, 25(3): 193-198 DOI:10.1002/kin.550250307 (  0) 0) |
| [10] |
王肖磊, 吴根华, 方国东, 等. 过渡金属活化过硫酸盐在环境修复领域的研究进展[J]. 生态与农村环境学报, 2021, 37(2): 145-154 (  0) 0) |
| [11] |
Fang G D, Deng Y M, Huang M, et al. A mechanistic understanding of hydrogen peroxide decomposition by vanadium minerals for diethyl phthalate degradation[J]. Environmental Science & Technology, 2018, 52(4): 2178-2185 (  0) 0) |
| [12] |
Liu H Z, Bruton T A, Li W, et al. Oxidation of benzene by persulfate in the presence of Fe(Ⅲ)- and Mn(Ⅳ)-containing oxides: Stoichiometric efficiency and transformation products[J]. Environmental Science & Technology, 2016, 50(2): 890-898 (  0) 0) |
| [13] |
Fang G D, Gao J, Dionysiou D D, et al. Activation of persulfate by quinones: Free radical reactions and implication for the degradation of PCBs[J]. Environmental Science & Technology, 2013, 47(9): 4605-4611 (  0) 0) |
| [14] |
Rajabi H, Sharifipour M. Geotechnical properties of hydrocarbon-contaminated soils: A comprehensive review[J]. Bulletin of Engineering Geology and the Environment, 2019, 78(5): 3685-3717 DOI:10.1007/s10064-018-1343-1 (  0) 0) |
| [15] |
Fang G D, Chen X R, Wu W H, et al. Mechanisms of interaction between persulfate and soil constituents: Activation, free radical formation, conversion, and identification[J]. Environmental Science & Technology, 2018, 52(24): 14352-14361 (  0) 0) |
| [16] |
全国土壤普查办公室. 中国土壤分类系统[M].
中国农业出版社, 北京, 1993
(  0) 0) |
| [17] |
Liang C J, Huang C F, Mohanty N, et al. A rapid spectrophotometric determination of persulfate anion in ISCO[J]. Chemosphere, 2008, 73(9): 1540-1543 DOI:10.1016/j.chemosphere.2008.08.043 (  0) 0) |
| [18] |
刘光崧. 土壤理化分析与剖面描述[M].
中国标准出版社, 北京, 1996
(  0) 0) |
| [19] |
鲁如坤. 土壤农业化学分析方法[M].
中国农业科技出版社, 北京, 2000
(  0) 0) |
| [20] |
中国科学院南京土壤研究所. 土壤理化分析[M].
上海科学技术出版社, 上海, 1978
(  0) 0) |
| [21] |
Furman O S, Teel A L, Watts R J. Mechanism of base activation of persulfate[J]. Environmental Science & Technology, 2010, 44(16): 6423-6428 (  0) 0) |
| [22] |
Wang L, Peng L B, Xie L L, et al. Compatibility of surfactants and thermally activated persulfate for enhanced subsurface remediation[J]. Environmental Science & Technology, 2017, 51(12): 7055-7064 (  0) 0) |
| [23] |
Ye M M, Chen Z L, Liu X W, et al. Ozone enhanced activity of aqueous titanium dioxide suspensions for photodegradation of 4-chloronitrobenzene[J]. Journal of Hazardous Materials, 2009, 167(1/2/3): 1021-1027 (  0) 0) |
| [24] |
闫奇. NTA-Fe(Ⅲ)/PMS体系对水中难降解有机物效能及机理研究[D]. 南昌: 南昌航空大学, 2019.
(  0) 0) |
| [25] |
Oh W D, Dong Z L, Ronn G, et al. Surface-active bismuth ferrite as superior peroxymonosulfate activator for aqueous sulfamethoxazole removal: Performance, mechanism and quantification of sulfate radical[J]. Journal of Hazardous Materials, 2017, 325: 71-81 DOI:10.1016/j.jhazmat.2016.11.056 (  0) 0) |
| [26] |
Acero J L, Stemmler K, von Gunten U. Degradation kinetics of atrazine and its degradation products with ozone and OH radicals: A predictive tool for drinking water treatment[J]. Environmental Science & Technology, 2000, 34(4): 591-597 (  0) 0) |
| [27] |
Mandal S. Reaction rate constants of hydroxyl radicals with micropollutants and their significance in advanced oxidation processes[J]. Journal of Advanced Oxidation Technologies, 2018, 21(1): 178-195 DOI:10.26802/jaots.2017.0075 (  0) 0) |
| [28] |
Manoj P, Prasanthkumar K P, Manoj V M, et al. Oxidation of substituted triazines by sulfate radical anion (SO) in aqueous medium: A laser flash photolysis and steady state radiolysis study[J]. Journal of Physical Organic Chemistry, 2007, 20(2): 122-129 DOI:10.1002/poc.1134 (  0) 0) |
| [29] |
Liu H Z, Bruton T A, Doyle F M, et al. In situ chemical oxidation of contaminated groundwater by persulfate: Decomposition by Fe(Ⅲ)- and Mn(Ⅳ)-containing oxides and aquifer materials[J]. Environmental Science & Technology, 2014, 48(17): 10330-10336 (  0) 0) |
| [30] |
汤艳杰. 铁锰氧化物界面反应研究及其环境矿物学意义[D]. 中国科学院研究生院(广州地球化学研究所), 2003.
(  0) 0) |
| [31] |
Mueller K M. Soil organic matter: Biological and ecological effects[J]. 1988, 20(2): 149–150.
(  0) 0) |
| [32] |
Molamahmood H V, Qin J L, Zhu Y T, et al. The role of soil organic matters and minerals on hydrogen peroxide decomposition in the soil[J]. Chemosphere, 2020, 249: 126146 DOI:10.1016/j.chemosphere.2020.126146 (  0) 0) |
| [33] |
乔照华. 土壤有机质含量与土壤物理性能参数的相关性分析[J]. 中国农村水利水电, 2008(2): 3-4 (  0) 0) |
| [34] |
罗明云, 姚林林. 嘉陵江流域紫色土团聚体与粒径相关性分析[J]. 土壤科学, 2020, 8(2): 43-52 (  0) 0) |
| [35] |
Tiessen H, Stewart J W B. Particle-size fractions and their use in studies of soil organic matter: Ⅱ. cultivation effects on organic matter composition in size fractions[J]. Soil Science Society of America Journal, 1983, 47(3): 509-514 DOI:10.2136/sssaj1983.03615995004700030023x (  0) 0) |
| [36] |
Dalal R C, Mayer R J. Long term trends in fertility of soils under continuous cultivation and cereal cropping in southern Queensland. V. Rate of loss of total nitrogen from the soil profile and changes in carbon: Nitrogen ratios[J]. Soil Research, 1986, 24(4): 493 DOI:10.1071/SR9860493 (  0) 0) |
2. CAS Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
 2022, Vol. 54
2022, Vol. 54


