2. 中国科学院大学, 北京 100049
当前,我国部分地区农田土壤遭受了严重的重金属污染,且多为重金属复合污染。如贵州省铜仁市由于长期从事的汞矿开采及冶炼活动,造成周边农田土壤汞(Hg)镉(Cd)复合污染较为严重,Hg和Cd的平均含量达到14.15和0.87 mg/kg[1],均超过GB 15618— 2018《土壤环境质量农用地土壤污染风险管控标准(试行)》[2]的风险筛选值。农田土壤重金属污染不仅会降低农产品的产量,还会通过农产品可食部位累积重金属,使其进入食物链,进而对人体健康造成严重危害。研究表明,Hg、Cd复合污染土壤种植的水稻籽粒中Hg、Cd的含量最高可达0.027、1.48 mg/kg[3],均超出了GB 2762—2017《食品安全国家标准食品中污染物限量》[4]规定的Hg、Cd含量限值。因此,探究经济可行的重金属复合污染农田的修复方法,保障农产品安全生产尤为重要。
生物质炭具有比表面积大、孔隙多、性质稳定等特点,常被用于改善土壤质量或降低土壤重金属的生物有效性。研究表明,添加生物质炭改善了土壤性质和微生物代谢活性[5],使玉米粒中Cd含量下降47.3%[6];添加水稻秸秆炭可以明显降低水稻籽粒中的甲基汞含量[7-8]。但是这些都是基于3% ~ 5% 生物质炭添加量的研究结果,其对应的田间修复成本远大于5 000元/亩(1亩=667m2),很难实际应用于农田重金属污染修复。因此,研究人员开展了一系列改性生物炭的研究。如经硫脲改性的生物质炭增强了对Cd的吸附能力,最大吸附量增加了近3倍[9];硒改性生物质炭可以抑制土壤甲基汞的产生和减少水稻籽粒富集甲基汞,且生物质炭组成及用量对汞甲基化影响的差异较大[10];锰改性生物质炭对Hg[11]和Cd[12]表现出较高的吸附容量。然而,目前大多数研究还是基于单一重金属污染土壤的修复,对于Hg、Cd复合污染土壤的修复研究较少。
猪粪生物质炭是畜禽粪污处置利用的新途径。猪粪炭比其他原料制成的生物质炭含有更多易降解有机质、养分元素和微量元素,能显著提高土壤中微生物的活性,是一种应用前景广泛的生物质炭有机肥。而对猪粪炭进行锰改性处理,可以通过锰氧化物将重金属离子还原[13]或与重金属形成稳定的络合物[14],提高其对重金属的吸附能力。为了考察锰改性猪粪炭对复合重金属污染土壤的修复潜力,本文通过盆栽试验,研究KMnO4改性猪粪炭对Hg、Cd复合污染农田水稻安全生产的实际应用效果,并初步探究锰改性猪粪炭对水稻籽粒吸收累积重金属的阻控机制,为评估锰改性猪粪炭在Hg、Cd复合污染农田水稻安全生产上应用的可行性提供科学依据。
1 材料与方法 1.1 锰改性猪粪炭的制备原始猪粪生物质炭(ZC)在N2气氛条件下550℃热解6 h制得。将500 g原始猪粪炭在1 000 ml 0.1 mol/L的KMnO4溶液中超声浸泡2 h后抽滤,将固体部分用去离子水冲洗数次,置于烘箱内80℃干燥24 h,再置于管式炉内通入N2,550℃复烧0.5 h制成锰改性猪粪炭(MZC)。
两种猪粪炭的理化性质如表 1所示,经过KMnO4改性之后,MZC的比表面积是ZC的10倍。同样,MZC的总孔容约是ZC的5倍,平均孔径从9.03 nm减小到3.84 nm。MZC的C、N含量降低,O含量增加,由36.2% 增加到38.9%,pH由改性前的7.97降为7.55。猪粪炭中总汞(THg)、总镉(TCd)含量都远低于NY884—2012《生物有机肥》[15]要求的THg≤ 2 mg/kg和TCd≤3 mg/kg的限值。
|
|
表 1 原始和锰改性猪粪炭的组成和性质 Table 1 Compositions and properties of pristine and Mn-modified pig manure biochars |
试验所用土壤取自贵州省铜仁市,土壤的Hg和Cd总量分别为8.30 mg/kg和1.23 mg/kg,其有效态含量分别为0.084 mg/kg和0.63 mg/kg,pH为6.92,有机质含量为21.48 g/kg,全氮含量为1.46 g/kg,全磷含量为0.58 g/kg,全钾含量为18.27 g/kg,碱解氮含量为142.11 mg/kg,有效磷含量为8.18 mg/kg,速效钾含量为257.41 mg/kg,阳离子交换量(CEC)为8.51 cmol/kg。试验前,采集到的农田表层土(0 ~ 20 cm)自然风干后挑除石块、根系等杂物,过10目筛混匀备用。
1.3 盆栽试验于南京土壤研究所温室中进行盆栽试验。MZC设置3个添加量处理,分别为土壤质量的0.125%、0.25% 和0.5%(对应田间用量为2 812.5、5 625和11 250 kg/hm2,分别记作0.125%MZC、0.25%MZC和0.5%MZC),同时设置ZC添加量为土壤质量的0.5% 处理(记作0.5%ZC),以及空白对照处理(记作CK),共5个处理,每个处理3个重复。所有盆栽在温室中随机摆放,以减少试验误差。试验使用自制的PVC材质塑料盆,底部铺一块尼龙网,将4.0 kg污染土壤与生物质炭混匀后装入盆中,并添加0.14 g/kg CO(NH2)2和0.44 g/kg K2HPO4作为氮磷钾基肥。
采用铜仁本地水稻品种“晶两优·华占”作为试验用水稻品种。水稻种子用30.0% H2O2消毒15 min后,采用营养液育苗25 d至水稻幼苗高度约10 ~ 15 cm后移栽入盆,每盆3株。在水稻幼苗期(移栽后15 d内)保持淹水状态,其余生长期保持间歇淹水状态,淹水时盆栽水面高于土壤约1 cm。
在水稻收获期,将整个植株从盆中取出,抖掉根系周围松散的土壤后,收集附着于植物根表面的土壤,作为根际土。土壤样品采集后冷冻干燥,再经研磨后过100目筛保存备用。植物样品采集水稻的根部、茎叶、籽粒3部分,将采集的植物样品先用自来水冲洗去除表面灰尘,再用去离子水冲洗3遍后,冷冻干燥、研磨、过60目筛,放在4℃条件下保存备用。
1.4 测定项目与方法土壤THg测定:参照HJ 923—2017《土壤和沉积物总汞的测定催化热解–冷原子吸收分光光度法》[16]。土壤TCd和TMn(总锰)测定:参照HJ 803—2016《土壤和沉积物12种金属元素的测定王水提取–电感耦合等离子体质谱法》[17]。土壤有效态Hg测定:参照《土壤中有效态汞的测定方法》[18]。土壤有效态Cd、Mn测定:参照HJ 804—2016《土壤8种有效态元素的测定二乙烯三胺五乙酸浸提–电感耦合等离子体发射光谱法》[19]。植物样品THg测定参照:GB 5009.17—2021《食品安全国家标准食品中总汞及有机汞的测定》[20]。植物样品TCd测定:参照GB 5009.15—2014《食品安全国家标准食品中镉的测定》[21]。甲基汞(MeHg)的测定:参照《贵州典型汞污染区土壤–稻米汞分布特征及农艺调控效果》[22],即称取籽粒样品0.2 g于50 ml离心管中,加入250 g/L KOH-CH3OH溶液,80℃条件下水浴消解3 h,消解液再用CH2Cl2萃取、浓缩后采用乙基化试剂处理,用Tenax管氮吹富集后经气相色谱–冷原子荧光检测仪联用测定含量。
土壤理化性质的测定:参照鲁如坤编《土壤农业化学分析方法》[23],采用电位法测定土壤pH;采用水合热重铬酸钾氧化–比色法测定土壤有机质;采用开氏消煮法测定土壤全氮;采用碳酸钠熔融法测定土壤全磷;采用氢氧化钠熔融法测定土壤全钾;采用碱解扩散法法测定土壤碱解氮;采用碳酸氢钠法测定土壤有效磷;采用乙酸铵提取法测定土壤速效钾。
1.5 数据分析文中数据采用SPSS 28进行统计分析,Pearson相关系数法进行相关性分析,LSD法进行多重比较差异显著性检验;采用OriginPro 2019进行绘图。
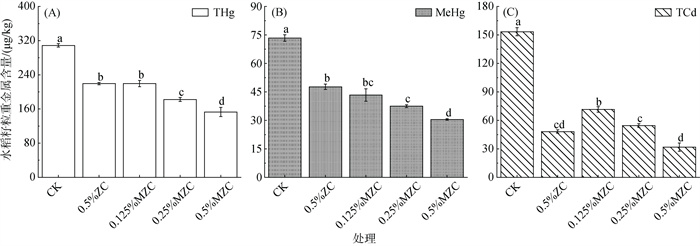
2 结果与讨论 2.1 添加猪粪炭对水稻各部位Hg、Cd含量的影响如图 1所示,添加猪粪炭的处理,水稻籽粒中总汞(THg)、甲基汞(MeHg)和总镉(TCd)的含量均低于CK处理,且MZC处理效果明显优于ZC处理。同时,随着MZC添加量从0.125% 增加到0.5%,籽粒中THg、MeHg、TCd的含量分别降低了28.9% ~ 50.4%、40.9% ~ 58.4% 及53.4% ~ 79.3%。徐振涛等[24]施用5% 的污泥生物质炭也使水稻籽粒中的无机Hg和MeHg含量分别下降了81.9% 和73.4%;而张丽等[25]却发现,水稻糙米中的Cd含量随生物质炭用量的增加呈先降低后升高的趋势。本研究发现,MZC对稻米中THg、MeHg和TCd的含量降低效果显著,且随用量增加其降低效果稳定。
|
(柱图上方不同小写字母表示处理间差异显著(P < 0.05),下同) 图 1 不同处理下水稻籽粒重金属含量 Fig. 1 Concentrations of heavy metals in rice grains under different treatments |
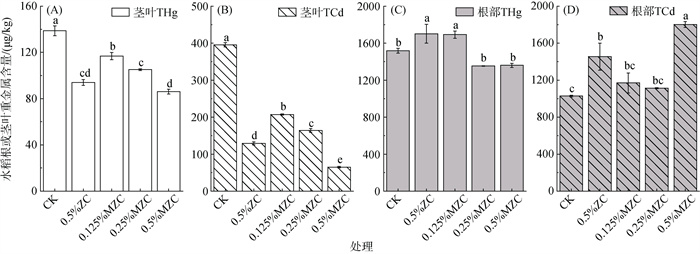
水稻茎叶中的THg、TCd分布情况(图 2)与籽粒中的结果相似。与CK处理相比,添加猪粪炭处理都显著降低了茎叶中THg、TCd含量;但0.5%MZC与0.5%ZC处理的茎叶中THg含量无显著差异,而TCd含量存在显著差异。同时随着MZC添加量的增加,水稻茎叶中THg含量降低了15.1% ~ 35.7%,TCd含量降低了47.6% ~ 83.6%。与CK处理相比,0.5% ZC和0.125%MZC处理水稻根中THg含量有所增加,但随着MZC添加量的增加,水稻根中THg含量明显降低;而0.5%ZC处理和3个用量的MZC处理都增加了水稻根中TCd含量。这与刘冲[26]在油麦菜生长过程中施加钙镁磷肥和桉树炭发现其根部重金属Cd含量升高的研究结果一致。综上可知,添加0.5%的MZC能有效降低水稻地上部对Hg、Cd的富集能力,降低水稻籽粒中Hg、Cd含量。
|
图 2 不同处理下水稻根和茎叶中重金属含量 Fig. 2 Concentrations of heavy metals in rice stems and leaves under different treatments |
相比CK处理,ZC和MZC处理都降低了土壤Hg、Cd的总量和有效态含量,且随着MZC添加量的增加,降低效果更明显(图 3)。其中,MZC处理的土壤中THg含量显著下降,而TCd含量略微下降;0.5% MZC处理对土壤有效态Hg、Cd含量的降低效果明显强于0.5%ZC处理。但是,0.125%MZC处理土壤有效Hg含量略微增加,徐振涛[27]也观察到低量的生物质炭提高了土壤中Hg的有效性。MZC处理对有效态Cd的降低率为31.1% ~ 39.9%,相比于文献报道的湿润和淹水条件下生物质炭施用降低了20.0%[28]和37.5%[29]的土壤有效态Cd,本试验所用的MZC对土壤Cd有效性的降低效果更好。

|
图 3 不同处理下土壤重金属含量及有效性 Fig. 3 Concentrations of total and available heavy metals in soils under different treatments |
同时,与CK及ZC处理相比,MZC处理显著增加了根际土壤TMn、有效态Mn含量,其中0.5%MZC处理较CK处理TMn含量提高了70.3%;而随着土壤中TMn的增加,有效Mn的比例也显著升高;。
生物质炭能改变土壤的pH、CEC、有机质等理化性质,进而改变重金属在土壤中的有效性。不同处理下土壤的理化性质如表 2所示。与CK处理相比,MZC和ZC处理增加了土壤pH、CEC、有效磷和速效钾含量,且随着MZC添加量增加而呈现明显上升趋势;0.5%ZC和0.125%MZC处理对土壤有机质含量的影响不显著,而0.25%MZC、0.5%MZC处理明显增加土壤有机质含量。
|
|
表 2 不同处理下土壤的理化性质变化 Table 2 Changes of soil properties under different treatments |
已有的研究表明,生物炭在施入土壤后,通过改善土壤理化性质及本身具有的多孔径结构和巨大的比表面积,使其具有强大的吸附能力,丰富的官能团与重金属离子发生络合反应和共沉淀反应,降低土壤中Hg、Cd的生物有效性,影响水稻对Hg、Cd的吸收,进而降低水稻各部位中Hg、Cd的含量[30-31]。重金属在水稻各部位的分布与生物质炭的性质密切相关,还受到生物炭的原材料、土壤理化性质及水稻生长环境等多种因素影响,其影响的关键因素还需进一步探讨。
2.3 影响水稻各部位Hg、Cd分布的关键因素 2.3.1 水稻各部位Hg、Cd含量的相关性水稻各部位Hg、Cd含量的相关性分析结果如表 3所示。水稻籽粒THg、MeHg和TCd含量与水稻茎叶THg和TCd含量有显著的正相关性,说明水稻茎叶中的Hg、Cd转移到籽粒中的较多。不同的是,水稻茎叶和籽粒中的THg、TCd含量与其在水稻根部的含量有微弱的负相关性,可能是水稻根部作为一种天然的屏障阻止了Hg、Cd的向上迁移。有研究表明,根表铁膜有阻碍根部重金属向上部转移的作用[32]。
|
|
表 3 水稻各部位Hg、Cd含量的相关性(n=15) Table 3 Correlations between Hg and Cd contents in various parts of rice |
为了探究Hg、Cd共存对其在水稻各部位分布的影响,本文进行了交叉相关性分析,发现水稻茎叶中Hg、Cd分布与籽粒中Cd、Hg分布存在极显著的正相关性,二者在累积过程中存在协同作用。
2.3.2 水稻各部位Hg、Cd含量与土壤重金属含量的相关性如表 4所示,水稻籽粒、茎叶中THg、MeHg含量与土壤中THg含量存在极显著正相关性,说明水稻主要吸收累积土壤中的Hg;水稻籽粒和茎叶中的TCd含量与土壤中有效态Cd含量存在极显著的正相关性,说明水稻中Cd的累积受土壤中Cd有效性的强烈影响。从相关性分析还可以看出,土壤中THg含量与水稻籽粒、茎叶TCd含量,土壤有效态Cd含量与水稻籽粒、茎叶THg含量之间存在显著的相关性,但这种相关性需要进一步研究。
|
|
表 4 水稻各部位Hg、Cd含量与土壤重金属含量的相关性(n=15) Table 4 Correlation between Hg and Cd contents in various parts of rice and heavy metals in soil |
对土壤中Mn分析发现,水稻籽粒和茎叶THg、MeHg、TCd含量与TMn、有效态Mn含量呈明显的负相关性,说明土壤中的Mn抑制了水稻各部位对Hg、Cd的累积,这可能是由于MZC中的锰氧化物对Hg、Cd的吸附作用降低了水稻对Hg、Cd的生物可利用性。已有的研究也表明,增加土壤中Mn含量,能够抑制水稻对Hg、Cd的吸收累积[33-34]。
2.3.3 水稻各部位Hg、Cd含量与土壤理化性质的相关性如表 5所示,水稻籽粒、茎叶中THg、MeHg、TCd分布与土壤pH呈极显著负相关关系。相关研究表明,土壤中有效Hg含量只有在pH 4.82 ~ 7.11范围内随着pH的升高而增加[35];水稻组织中Cd含量随pH的变化呈抛物线型,pH为6.5时,Cd吸收能力最强[36]。本试验中,土壤样品pH > 6.5,水稻中Cd累积随着土壤pH增加而减少。表 5结果还显示,水稻籽粒各部位THg、MeHg、TCd含量与土壤CEC的相关性与pH的结果相一致。
|
|
表 5 土壤性质与水稻各部位Hg、Cd含量的相关性(n=15) Table 5 Correlation between soil properties and Hg and Cd contents in various parts of rice |
在对碱解氮、有效磷、速效钾含量和水稻各部位Hg、Cd含量进行相关性分析后发现,水稻籽粒和茎叶中THg、MeHg、TCd含量与有效磷、速效钾含量存在显著负相关性,而仅有籽粒TCd含量与碱解氮含量存在显著正相关性,这与已有报道的土壤溶液中Cd浓度随着施氮量增加而显著增加的结果一致[37]。
2.4 影响土壤Hg、Cd有效性的关键因素如表 6所示,土壤有效Hg含量与土壤CEC呈显著负相关,而土壤有效Cd含量与土壤pH、CEC、TMn含量和有效态Mn含量呈显著负相关,表明MZC施用提高了土壤pH、CEC、有效磷、速效钾、TMn和有效Mn含量,进而降低了土壤中有效态Hg、Cd含量,从而抑制了水稻籽粒对土壤Hg、Cd的吸收累积。基于以上对土壤、水稻籽粒和茎叶Hg、Cd分布影响因素的相关性分析,MZC阻控对水稻籽粒Hg、Cd累积的可能机制包括:①施加ZC,尤其是MZC增加了土壤pH、CEC和有效磷、速效钾的含量,进而降低了土壤中有效态Hg、Cd的含量,从而减少水稻籽粒对Hg、Cd的吸收;②MZC的施用,增加了土壤中有效Mn含量,由于Mn和Cd在水稻中的转运蛋白相同[34],因此Mn与Cd的竞争作用促使水稻减少了对Cd的吸收。
|
|
表 6 土壤Hg、Cd有效性与土壤性质的相关性(n=15) Table 6 Correlation between availability of soil Hg and Cd and soil properties |
1) 添加锰改性猪粪炭,能显著提高土壤pH、CEC、有效磷和速效钾含量,进而降低了土壤中有效态Hg和Cd的含量,从而减少了水稻地上部对Hg、Cd的吸收累积。
2) 锰改性猪粪炭的施用还能增加土壤中TMn和有效Mn含量,并通过Mn与Cd在水稻吸收转运中的竞争作用,进一步提高了锰改性猪粪炭对水稻吸收累积土壤中Cd的阻控效果。本研究结果表明,锰改性猪粪炭是一种潜在的能保障Hg、Cd污染农田水稻安全生产的土壤修复剂。
| [1] |
胡国成, 张丽娟, 齐剑英, 等. 贵州万山汞矿周边土壤重金属污染特征及风险评价[J]. 生态环境学报, 2015, 24(5): 879-885 DOI:10.16258/j.cnki.1674-5906.2015.05.024 (  0) 0) |
| [2] |
生态环境部, 国家市场监督管理局. 土壤环境质量农用地土壤污染风险管控标准(试行): GB15618—2018[S]. 北京: 中国标准出版社, 2018.
(  0) 0) |
| [3] |
张庭艳, 何腾兵, 田茂苑, 等. 贵州喀斯特山区水稻土与稻米重金属含量的关联性探究[J]. 山地农业生物学报, 2021, 40(2): 60-66 DOI:10.15958/j.cnki.sdnyswxb.2021.02.010 (  0) 0) |
| [4] |
国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品安全国家标准食品中污染物限量: GB 2762—2017[S]. 北京: 中国标准出版社, 2017.
(  0) 0) |
| [5] |
Qi X, Gou J L, Chen X M, et al. Application of mixed bacteria-loaded biochar to enhance uranium and cadmium immobilization in a co-contaminated soil[J]. Journal of Hazardous Materials, 2021, 401: 123823 DOI:10.1016/j.jhazmat.2020.123823 (  0) 0) |
| [6] |
Xu P, Sun C X, Ye X Z, et al. The effect of biochar and crop straws on heavy metal bioavailability and plant accumulation in a Cd and Pb polluted soil[J]. Ecotoxicology and Environmental Safety, 2016, 132: 94-100 DOI:10.1016/j.ecoenv.2016.05.031 (  0) 0) |
| [7] |
赵伟, 丁弈君, 孙泰朋, 等. 生物质炭对汞污染土壤吸附钝化的影响[J]. 江苏农业科学, 2017, 45(11): 192-196 DOI:10.15889/j.issn.1002-1302.2017.11.052 (  0) 0) |
| [8] |
Shu R, Wang Y J, Zhong H. Biochar amendment reduced methylmercury accumulation in rice plants[J]. Journal of Hazardous Materials, 2016, 313: 1-8 DOI:10.1016/j.jhazmat.2016.03.080 (  0) 0) |
| [9] |
宋佳颖, 刘君, 宗海英, 等. 硫脲改性猪粪生物质炭对模拟农田径流中镉和草甘膦吸附特征[J]. 环境科学研究, 2021, 34(2): 356-364 DOI:10.13198/j.issn.1001-6929.2020.07.01 (  0) 0) |
| [10] |
王明星. 不同改性生物炭的反应活性特性及其对水稻汞积累的影响[D]. 重庆: 西南大学, 2021.
(  0) 0) |
| [11] |
Shi Y J, Ma W B, Wang D Y. Study on mercury adsorption and desorption on different modified biochars[J]. Bulletin of Environmental Contamination and Toxicology, 2022, 108(4): 629-634 DOI:10.1007/s00128-021-03381-7 (  0) 0) |
| [12] |
Liang J, Li X M, Yu Z G, et al. Amorphous MnO2 modified biochar derived from aerobically composted swine manure for adsorption of Pb(II) and Cd(II)[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(6): 5049-5058 (  0) 0) |
| [13] |
Lin L N, Qiu W W, Wang D, et al. Arsenic removal in aqueous solution by a novel Fe-Mn modified biochar composite: Characterization and mechanism[J]. Ecotoxicology and Environmental Safety, 2017, 144: 514-521 DOI:10.1016/j.ecoenv.2017.06.063 (  0) 0) |
| [14] |
Wu Y, Li W, Sparks D L. The effects of iron(II) on the kinetics of arsenic oxidation and sorption on manganese oxides[J]. Journal of Colloid and Interface Science, 2015, 457: 319-328 DOI:10.1016/j.jcis.2015.07.022 (  0) 0) |
| [15] |
中华人民共和国农业部. 生物有机肥: NY884—2012[S]. 北京: 中国农业出版社, 2012.
(  0) 0) |
| [16] |
中华人民共和国环境保护部. 土壤和沉积物总汞的测定催化热解-冷原子吸收分光光度法: HJ 923—2017[S]. 北京: 中国环境科学出版社, 2017.
(  0) 0) |
| [17] |
中华人民共和国环境保护部. 土壤和沉积物12种金属元素的测定王水提取-电感耦合等离子体质谱法: HJ 803—2016[S]. 北京: 中国环境科学出版社, 2016.
(  0) 0) |
| [18] |
王宏康, 王征, 李萍. 土壤中有效态汞的测定方法[J]. 环境科学, 1983, 4(4): 61-62, 76 DOI:10.13227/j.hjkx.1983.04.019 (  0) 0) |
| [19] |
中华人民共和国环境保护部. 土壤8种有效态元素的测定二乙烯三胺五乙酸浸提-电感耦合等离子体发射光谱法: HJ 804—2016[S]. 北京: 中国环境科学出版社, 2016.
(  0) 0) |
| [20] |
中华人民共和国国家卫生健康委员会, 国家市场监督管理总局. 食品安全国家标准食品中总汞及有机汞的测定: GB 5009.17—2021[S]. 北京: 中国标准出版社, 2021.
(  0) 0) |
| [21] |
国家卫生和计划生育委员会. 食品安全国家标准食品中镉的测定: GB 5009.15—2014[S]. 北京: 中国标准出版社, 2015.
(  0) 0) |
| [22] |
杜静静. 贵州典型汞污染区土壤—稻米汞分布特征及农艺调控效果[D]. 贵阳: 贵州大学, 2021.
(  0) 0) |
| [23] |
鲁如坤
. 土壤农业化学分析方法[M].
中国农业科技出版社, 北京, 1999
(  0) 0) |
| [24] |
徐振涛, 梁鹏, 吴胜春, 等. 不同生物质炭对土壤中有效态汞的影响及其吸附特征分析[J]. 环境化学, 2019, 38(4): 832-841 (  0) 0) |
| [25] |
张丽, 侯萌瑶, 安毅, 等. 生物炭对水稻根际微域土壤Cd生物有效性及水稻Cd含量的影响[J]. 农业环境科学学报, 2017, 36(4): 665-671 (  0) 0) |
| [26] |
刘冲. 生物炭基肥对水稻土中Cd、Cu、Pb和Zn的钝化效应研究[D]. 兰州: 兰州大学, 2016.
(  0) 0) |
| [27] |
徐振涛. 生物质炭对水稻富集汞的效应研究[D]. 杭州: 浙江农林大学, 2019.
(  0) 0) |
| [28] |
Wang T, Sun H W, Mao H J, et al. The immobilization of heavy metals in soil by bioaugmentation of a UV-mutant Bacillus subtilis 38 assisted by NovoGro biostimulation and changes of soil microbial community[J]. Journal of Hazardous Materials, 2014, 278: 483-490 DOI:10.1016/j.jhazmat.2014.06.028 (  0) 0) |
| [29] |
Wang Q, Chen L, He L Y, et al. Increased biomass and reduced heavy metal accumulation of edible tissues of vegetable crops in the presence of plant growth-promoting Neorhizobium huautlense T1-17 and biochar[J]. Agriculture, Ecosystems & Environment, 2016, 228: 9-18 (  0) 0) |
| [30] |
Uchimiya M, Bannon D I, Wartelle L H. Retention of heavy metals by carboxyl functional groups of biochars in small arms range soil[J]. Journal of Agricultural and Food Chemistry, 2012, 60(7): 1798-1809 DOI:10.1021/jf2047898 (  0) 0) |
| [31] |
刘晶晶, 杨兴, 陆扣萍, 等. 生物质炭对土壤重金属形态转化及其有效性的影响[J]. 环境科学学报, 2015, 35(11): 3679-3687 DOI:10.13671/j.hjkxxb.2014.1044 (  0) 0) |
| [32] |
Higueras P, Oyarzun R, Biester H, et al. A first insight into mercury distribution and speciation in soils from the Almadén mining district, Spain[J]. Journal of Geochemical Exploration, 2003, 80(1): 95-104 DOI:10.1016/S0375-6742(03)00185-7 (  0) 0) |
| [33] |
Huang Y, Wang M X, Li Z J, et al. In situ remediation of mercury-contaminated soil using thiol-functionalized graphene oxide/Fe-Mn composite[J]. Journal of Hazardous Materials, 2019, 373: 783-790 DOI:10.1016/j.jhazmat.2019.03.132 (  0) 0) |
| [34] |
Sasaki A, Yamaji N, Yokosho K, et al. Nramp5 is a major transporter responsible for manganese and cadmium uptake in rice[J]. The Plant Cell, 2012, 24(5): 2155-2167 DOI:10.1105/tpc.112.096925 (  0) 0) |
| [35] |
Yang Y K, Zhang C, Shi X J, et al. Effect of organic matter and pH on mercury release from soils[J]. Journal of Environmental Sciences, 2007, 19(11): 1349-1354 DOI:10.1016/S1001-0742(07)60220-4 (  0) 0) |
| [36] |
Zhang Q, Chen H F, Xu C, et al. Heavy metal uptake in rice is regulated by pH-dependent iron plaque formation and the expression of the metal transporter genes[J]. Environmental and Experimental Botany, 2019, 162: 392-398 DOI:10.1016/j.envexpbot.2019.03.004 (  0) 0) |
| [37] |
Mitchell L G, Grant C A, Racz G J. Effect of nitrogen application on concentration of cadmium and nutrient ions in soil solution and in durum wheat[J]. Canadian Journal of Soil Science, 2000, 80(1): 107-115 DOI:10.4141/S98-085 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China
 2022, Vol. 54
2022, Vol. 54


