2. 南京信息工程大学应用气象学院, 南京 210044;
3. 中国科学院大学, 北京 100049
全球农业有机物料资源丰富,每年产生约35亿吨作物秸秆以及70亿吨畜禽粪便[1],是有机肥生产的重要原料。施用有机肥能够为作物生长供应各种养分元素,并促进土壤有机质(SOM)形成,实现土壤肥力的持续提升[2]。有机肥碳在微生物作用下转化形成土壤有机质,并通过物理保护和化学结合等机制稳定存在[3]。最新全球尺度meta分析表明,与化肥相比,施用有机肥可提高农田土壤有机质储量C 7.41 Mg/hm2[4]。因此,有机肥施用是实现农田土壤固碳培肥和维持生产力的重要手段[5]。然而,研究发现有机肥的施用可能会诱导N2O大量排放,从而抵消固碳缓解气候变化的效应[6]。
作为一种重要的温室气体,N2O的百年尺度增温潜势是CO2的265倍,同时也是平流层臭氧的主要消耗物质[7]。据估算,农田对工业革命以来全球陆地生态系统N2O排放量增长的贡献率高达82%[8]。在土壤中,N2O主要通过微生物驱动的硝化和反硝化过程产生,这些过程受NH4+-N、NO3−-N和活性碳底物供应的控制,并受土壤通气状况、pH、质地等性质影响[6]。施用有机肥显著改变土壤有效碳氮含量,进而直接影响土壤N2O的产生过程[7];并通过影响土壤通气性,特别是改变有机物分解微域的氧气有效性间接调节N2O产生[9]。然而现有研究结果表明,相比化肥促进N2O排放,施用有机肥对N2O排放的影响尚不明确,可能促进、抑制或是没有显著影响[6, 10]。造成上述矛盾结果的重要原因是不同种类有机肥的性质存在较大差异,而有机肥的可分解性是影响土壤N2O排放的关键控制因素[11]。有机肥的可分解性受控于其碳氮含量以及有机碳组成[12]。据报道,土壤N2O排放量与施入有机肥的碳氮比(C/N)呈负相关关系,因为较高的C/N会导致有机肥的微生物分解出现氮限制,从而促进对土壤无机氮的同化作用[13];但也有研究发现N2O排放量与C/N并无显著关系,而是受控于有机肥中无机氮和活性碳含量[14]。有研究进一步表明,碳组分特征和内在物质构成是决定土壤N2O排放对不同有机物响应的根本因素[15]。然而,目前相关研究主要集中在基于田间观测试验探讨有机肥种类和元素计量性质对N2O排放的影响,在有机肥可分解性调控N2O产生机制尤其是对于有机碳化学组成作用的认知仍存在空缺。
位于我国东北地区的黑土素以土壤有机质和肥力高著称,生产的粮食总量占全国的1/4,是我国粮食安全的“压舱石”。但是在近几十年来,黑土地出现肥力退化的问题,主要原因是有机物质输入不足导致土壤有机质衰减[16]。因此,施用有机物料对于黑土地耕地质量提升尤为重要,是落实国家黑土地保护战略的关键举措。Chen等[9]利用原位试验研究发现,施用猪粪有机肥显著提高黑土N2O排放,但是鸡粪有机肥没有显著影响。有机肥结构性质的差异是造成这种现象的主要原因,然而其驱动机制以及关键组分与N2O排放的耦联效应并不清楚。本研究选取6种化学组分不同的有机肥,进行为期一年的培养试验,以期量化典型黑土N2O排放对不同种类有机肥响应的方向与程度;同时设置加氮和不加氮处理,探究不同有机肥施用情况下化肥对黑土N2O排放的影响,揭示调控有机肥影响N2O排放的关键组分,为气候变化情境下黑土农田有机肥施用提供科学依据。
1 材料与方法 1.1 试验地概况和试验设计采样地点位于黑龙江省的中国科学院海伦农业生态实验站(47°26′ N,126°38′ E),该地区海拔240 m,属于中温带湿润季风气候,年平均气温为1.5 ℃,降水量为550 mm。种植作物为玉米,试验地划分为10个20 m × 100 m的区域,随机采集耕层(0 ~ 20 cm)土壤样品,混匀后运至实验室,挑除根系过2 mm筛,置于4 ℃保存备用。土壤类型为典型黑土(Mollisols),质地为壤土,母质为第四纪黄土,含有8% 砂粒、72% 粉粒和20% 黏粒,pH为5.96,有机碳27.7 g/kg,全氮1.88 g/kg,NH4+-N 1.6 mg/kg,NO3−-N 13.2 mg/kg。
培养试验设7个处理,分别为不添加有机肥(CK)和添加猪粪有机肥(PGM)、鸡粪有机肥(CKM)、牛粪与稻壳有机肥(CMH)、芦蒿秸秆与中药渣有机肥(HRS)、菇渣有机肥(SMC)、糠醛渣及米渣有机肥(CFR)。采取等碳量原则,添加量为C 6120 kg/hm2,即C 3.0 g/kg[17]。同时设置两个氮水平(0、100 mg/kg,NO、N100),模拟田间不施肥背景和实际氮肥用量水平(N 204 kg/hm2)[18],氮素以尿素溶液形式添加。所有14个处理设置3次重复。试验开始时称取40 g(以干重计)土样于培养瓶中,在20 ℃下预培养1 d。预培养结束后添加有机肥,使其与土壤混合均匀,压实至田间容重1.0 g/cm3。随后N100处理加入尿素溶液,并调节所有处理土壤含水量至50% 土壤孔隙含水量(WFPS)[9]。覆盖扎孔保鲜膜保持通气,于20℃培养箱中培养一年(365 d),培养期内定时采集气体和补充水分。
1.2 气体采集和N2O分析在培养期内共进行45次采气,培养初期采气频率为一天一次(1 ~ 7 d),之后每两天一次(9、11、13、16 d),待采气高峰结束后改为每周一次(17 ~ 99 d),后期每10 d一次(100 ~ 181 d),最后阶段两周一次直至培养结束。采气前将培养瓶通气30 min,密封后注入20 ml新鲜空气,混匀培养瓶内气体并抽出20 ml注入真空瓶作为第一针;密封培养6 h后用注射器采集20 ml气体样品注入真空瓶,作为第二针。使用气相色谱分析仪(Agilent 7890)测定N2O浓度,采用63Ni电子捕获检测器检测,N2O标准气体购于国家标准物质中心。N2O排放通量根据培养期间(6 h)浓度变化和培养瓶内气体体积计算。
1.3 土壤和有机肥性质测定土壤和有机肥中全碳(TC)和全氮(TN)含量采用碳氮分析仪(Elementar Vario Max CN)测定;pH采用土水比1︰2.5(m︰V)测定;有机肥活性有机碳(LOC)含量用高锰酸钾氧化法测定;NH4+-N和NO3−-N由2 mol/L的氯化钾溶液浸提,用氧化镁-代氏合金蒸馏法测定;采用考马斯亮蓝法测定有机肥总蛋白质含量。有机肥主要化学性质见表 1。
|
|
表 1 有机肥的主要化学性质 Table 1 Chemical properties of manure |
利用固态13C核磁共振技术测定有机肥中有机碳的结构特征。得到的核磁共振图谱划分为7个代表不同有机碳官能团的化学位移:烷基碳(δ=0 ~ 45)、甲氧基碳(δ=45 ~ 60)、烷氧碳(δ=60 ~ 93)、双氧烷基碳(δ=93 ~ 110)、芳基碳(δ=110 ~ 142)、酚基碳(δ=142 ~ 160)和羰基碳(δ=160 ~ 190)。利用MestReNova软件对图谱进行积分,不同官能团的相对含量用对应区间积分面积占比来表示。根据已有研究[19]计算有机肥易分解性指标CC/MC(烷氧基碳/甲氧基碳)和难分解指标芳基度指数(Aromaticity)=(芳香碳+酚基碳)/(烷基碳+甲氧基碳+烷氧基碳+双氧烷基碳+芳香碳+酚基碳)×100。
采用碱性氧化铜水解法测定有机肥中木质素酚含量和组成,水解产生3种类型的木质素酚单体:香草基(vanillyl,V;包括香草醛、乙酰香草酮和香草酸)、丁香基(syringyl,S;包括丁香醛、乙酰丁香酮和丁香酸)和肉桂基(cinnamyl,C;包括p-香豆酸和阿魏酸)。木质素酚类单体衍生物用气相色谱仪(Agilent 6890)测定。总木质素酚含量(VSC)为各单体含量之和,表征木质素降解程度;香草基类单体在土壤中相对稳定,而肉桂基和丁香基类单体相对转化较快,因此比值V/VSC也用来指示木质素被微生物分解和利用的程度[20]。
1.5 统计与分析采用Microsoft Excel 2021进行数据计算;采用SPSS 22.0进行单因素方差分析比较不同处理间差异的显著性;采用SPSS 22.0和Origin 2021进行相关分析和回归分析N2O排放量与有机肥性质的关系;采用R 4.0.3进行随机森林分析得到影响N2O排放的主要因素;用Origin 2021和R 4.0.3软件进行绘图。
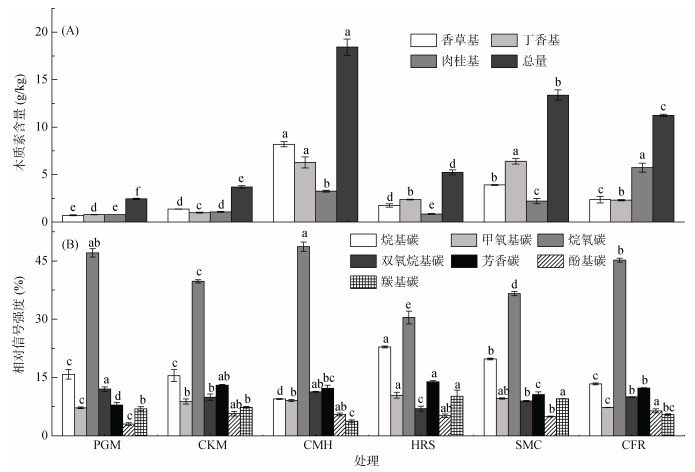
2 结果与分析 2.1 有机肥木质素含量及有机碳结构不同种类有机肥中总木质素酚含量存在显著差异(图 1A),其中CMH含量最高,PGM含量最低。木质素香草基和丁香基类单体均为CMH含量最高,肉桂基类单体则为CFR含量最高,3类单体含量的最小值均出现在PGM。13C核磁共振结果表明(图 1B),烷氧碳是相对含量最高的有机碳官能团,占比达36% ~ 48%,其次为烷基碳和芳基碳,酚基碳相对含量最低。不同有机肥对比发现,烷氧碳最大和最小含量占比分别出现在CMH和HRS,双氧烷基碳分别为PGM和HRS,芳香碳则分别为HRS和PGM。PGM的CC/MC指数最高、芳基度指数最低,说明其活性有机碳组分含量最高,可能具有更高的分解性。
|
(图柱上方小写字母不同表示不同有机肥间同一木质素酚单体和总木质素酚含量或有机官能团相对含量差异显著(P < 0.05)) 图 1 有机肥的木质素酚单体和总木质素酚含量(A)以及有机碳官能团的相对含量(B) Fig. 1 Contents of lignin phenols and monomer (A) and relative abundances of functional carbon groups (B) of manures |
不同处理N2O排放通量随培养时间呈相似的变化特征(图 2)。N2O排放峰值出现在培养第1天,不加氮情况下最大排放峰值出现在CKM,最小峰值为CMH处理的23.1 ng/(kg·h),与CK处理峰值25.6 ng/(kg·h)相近且显著低于其他处理。加氮处理N2O排放峰值为137.7 ~ 299.1 ng/(kg·h),显著高于不加氮处理,最大和最小峰值出现的处理与不加氮一致。随后,N2O排放通量急剧下降,至培养第23天出现另一排放峰。不加氮情况下,除CMH和HRS处理外,第23天峰值均低于第一天出现的峰值;相反,所有加氮处理第23天排放峰值均较低,仅为第1天排放峰的13 ~ 55%。之后直至培养结束,N2O排放通量虽仍有波动,但均保持在较低水平。

|
(–N:不加氮处理;+N:加氮处理,下同) 图 2 不加氮和加氮处理下添加不同有机肥土壤N2O排放通量的动态变化 Fig. 2 Dynamics of N2O emission fluxes from soils received different manures with or without N addition |
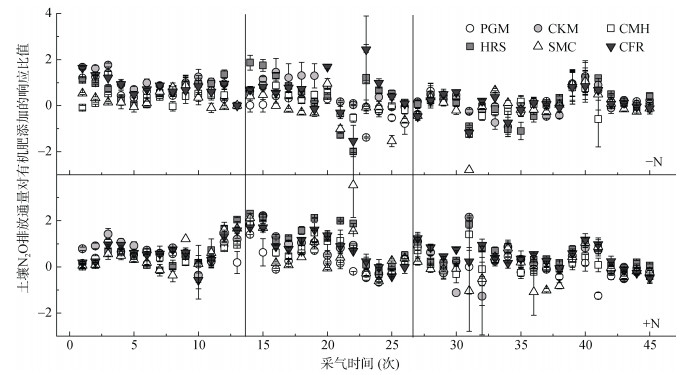
将各有机肥添加处理与CK处理N2O排放通量的比值进行对数转化(图 3),得到N2O排放通量对有机肥添加的响应比值(response ratio,RR)。按照其动态变化特征将整个培养期划分为3个阶段,分别为培养前期(第0 ~ 14次采气)、中期(第15 ~ 28次采气)和后期(第29 ~ 45次采气)。整个培养期,N2O排放通量的RR大多数大于0,小于0的情况主要出现在中后期。培养前期,除CMH和HRS外,其他有机肥处理N2O排放通量的RR均呈下降趋势;加氮情况下,各处理RR则呈波动上升趋势。然而,在培养中期加氮和不加氮处理的N2O排放通量对有机肥的响应RR均迅速下降,氮添加显著增强了有机肥对N2O排放的促进效应。各处理RR在培养后期表现为缓慢增加的波动变化趋势。
|
图 3 不同培养阶段不加氮和加氮处理下土壤N2O排放通量对有机肥添加响应比值的动态变化 Fig. 3 Dynamics of the response ratio of N2O emission fluxes to manure application with or without N addition |
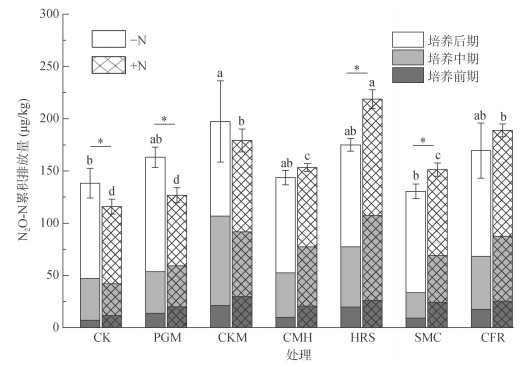
不加氮情况下,添加有机肥处理的N2O累积排放量为144 ~ 197 µg/kg(图 4);除SMC处理外,有机肥处理均高于对照CK(138 µg/kg),CKM处理达到显著水平。加氮情况下,所有有机肥处理均高于CK(116 µg/kg),除PGM处理外(127 µg/kg)均达显著水平;HRS处理N2O累积排放量最高,达到219 µg/kg。
|
(图中小写字母不同表示不加氮或加氮条件下各处理间差异显著;*表示同一有机肥处理加氮和不加氮处理间差异显著(P < 0.05)) 图 4 不加氮和加氮处理下添加不同有机肥土壤N2O累积排放量 Fig. 4 N2O cumulative emissions from soils received different manures with or without N addition |
计算整个培养期和不同阶段N2O累积排放量对有机肥添加的响应比值RR(图 5),在不加氮情况下不同有机肥处理前期RR均高于中后期,前期和中期RR的最高值出现在CKM有机肥,后期则为HRS。氮添加增强了全培养期有机肥对N2O排放的效应,主要是由于中期RR的增加。

|
(小写字母不同表示同一培养期不同有机肥处理间差异显著(P < 0.05)) 图 5 不同培养阶段不加氮和加氮处理下土壤N2O累积排放量对有机肥添加的响应比值 Fig. 5 Response ratios of soil N2O cumulative emissions to manure application with or without N addition at different incubation stages |
与不加氮相比,加氮显著降低了CK、PGM处理的N2O累积排放量,显著提高了HRS和SMC处理的累积排放量(图 4)。氮添加对CK、PGM和CKM处理N2O累积排放量表现为负效应,其他处理则为正效应,HRS、SMC和CFR的效应显著高于CK处理(表 2)。回归分析表明,不同有机肥处理N2O累积排放量对氮添加的响应随有机肥C/N、TC和LOC增加而显著增强(图 6)。
|
|
表 2 施用不同有机肥情况下N2O累积排放量对氮添加的响应 Table 2 Response ratios of N2O cumulative emissions to nitrogen addition under different manure treatments |

|
图 6 不同有机肥处理下土壤N2O排放对氮添加响应与有机肥C/N(A)(HRS处理不计入计算)、全碳(B)、活性有机碳(C)的关系 Fig. 6 Relationships between the effect of nitrogen addition on soil N2O emissions under different manure treatments and C/N(A), TC(B) and LOC(C) |
在不加氮和加氮情况下,随机森林模型分别解释了N2O全培养期排放量对有机肥响应比值(RR)73.8% 和75.6% 的变化。不加氮情况下有机肥的LOC和VSC含量是影响其对N2O排放效应的主要因素,而加氮处理中有机肥的VSC是影响N2O排放对其响应的最关键因素,且显著提高了TN的重要性(图 7)。加氮和不加氮处理中C/N对RR的影响均不显著。

|
图 7 影响全培养期N2O累积排放量对有机肥添加响应的重要因素(黑色表示该因子作用显著) Fig. 7 Relative importance of factors influencing the response ratio of N2O emissions to manure application during the whole incubation period |
对有机肥性质与不同阶段N2O累积排放量响应比值RR的相关分析表明(图 8),不加氮情况下培养前期RR与无机氮和蛋白质含量呈显著正相关关系,与TC、C/N、LOC和VSC呈显著负相关关系,其中与LOC和VSC的相关系数最高。在培养中期,RR与TN和芳基度呈显著正相关关系,与CC/MC呈显著负相关关系。培养后期RR与烷氧碳和双氧烷基碳呈显著负相关关系。

|
(图中* 表示相关性达到P < 0.05显著水平) 图 8 不同培养阶段不加氮和加氮处理下土壤N2O排放对有机肥添加的响应比值与有机肥性质的关系 Fig. 8 The relationships between the ratio of soil N2O fluxes response to manure application and the properties of manure at different incubation stages with or without N addition |
加氮降低了前期RR与LOC和VSC的相关性,不影响中期RR与有机肥性质的关系;加氮增强了后期RR与V/VSC的负相关关系及与蛋白质的正相关关系,但不影响烷氧碳和双氧烷基碳对RR的关系。
3 讨论 3.1 黑土N2O排放对施用有机肥的响应本研究中,施用有机肥总体上促进黑土N2O排放(除SMC处理外),平均增幅为23%(图 4)。理论上,有机肥施用带入大量有效碳氮,可以提高土壤硝化和反硝化微生物活性,诱导N2O产生;同时外源有机碳的输入提高土壤异养呼吸,产生更多厌氧微域,促进反硝化作用[10]。本研究中有机肥对N2O的促进作用增幅(23%)低于最新全球尺度meta分析的结果(33%)[6]。这可能是因为该试验是在模拟野外N2O高排放期平均含水量(50% WFPS)条件下进行,未达到反硝化作用发生的水分条件(70% ~ 90% WFPS),因此主导N2O产生的过程可能是硝化作用,而硝化作用产生N2O的能力远低于反硝化作用[21-22]。另外,在田间情况下,施用有机肥能够促进作物根系生长及活性,形成更加缺氧/厌氧的根际环境,进而增强土壤N2O排放对有机肥的正响应[6]。因此,本研究中有机肥添加对N2O排放的促进作用较低。
施用不同种类有机肥土壤N2O排放对氮添加的响应不同,主要是由于有机肥碳氮化学计量比尤其是活性碳含量的差异(图 6);另一方面,氮添加总体上增强了N2O排放对有机肥的响应(图 5)。在有机碳供应充足的土壤中,外源氮素的添加缓解了异养微生物同化作用和硝化作用对氮的竞争,促进N2O排放[23]。此外,尽管本试验设定的水分条件更利于硝化作用主导N2O产生,在有机肥分解形成的厌氧微域以及土壤团聚体内部可能具备反硝化作用进行的缺氧条件,施用高碳活性有机肥也可以通过刺激反硝化作用而促进氮肥来源中N2O的产生和排放。
本研究中,不加氮情况下,施用SMC有机肥并未增加N2O排放,相反导致一定程度的降低。这可能是因为SMC有机肥(14.77)与供试土壤(14.73)具有相似的C/N,更加符合土著微生物的代谢需求,导致微生物优先利用SMC有机肥中的活性有机物[24],从而增强异养微生物的呼吸,促进了对氮素的同化作用[25-26]。此外,SMC自身pH较高(8.21),施入土壤后可能促进了微生物生物量的增加,进而增强了氮素的固持同化作用[23]。更重要的是,SMC具有最高的活性有机碳和较高的总木质素酚含量,可能是导致N2O排放较低的主要诱因。
3.2 有机肥碳组分对不同阶段N2O排放的影响有机肥的活性有机碳和总木质素酚(而非碳氮计量比)是其影响N2O排放的主要因素(图 7),表明有机肥的组分特征对调控其影响整个培养期N2O的排放起决定性作用。Chen等[27]研究发现,有机碳的结构是影响其在土壤中分解和氮素释放速率的重要因素。有机碳内在分子结构和微生物可利用性的差异[15],导致不同阶段碳组分与N2O排放之间的耦合关系和强度不同。
培养前期,N2O排放对有机肥的响应比值(RR)显著高于中后期,主要是因为有机肥带入的无机氮(主要是NH4+)可以迅速被硝化微生物利用产生N2O(图 8)。培养前期RR与有机肥的活性有机碳含量呈显著负相关(图 8),可能是由于此时有机肥源活性碳成为微生物的主要底物,促进了异养微生物的代谢,增强对土壤NH4+的同化作用[25-26],造成与硝化微生物竞争利用氮底物,从而降低N2O排放;而此时有机肥的总木质素酚含量也与RR呈负相关关系。已有研究发现,在活性有机碳供应充足的情况下,木质素会通过共代谢作用被微生物利用[28],并且这种作用往往出现在有机物分解的前期[15]。因此,高木质素酚含量可能进一步促进异养微生物对NH4+同化。氮添加后减弱了RR与活性有机碳和木质素酚含量的负相关关系,进一步证实有机肥中活性碳组分诱导的氮同化作用是抑制有机肥对N2O排放正效应的重要机制。此外,丰富的活性碳底物也可能通过增强厌氧微域内N2O还原为N2[29],从而降低N2O排放,该机制的贡献可能较低,需要进一步结合15N技术进行量化区分。
培养中期RR与有机肥的CC/MC呈显著负相关关系。Bonanomi等[30]研究指出,CC/MC主要表征纤维素,特别是其中的活性部分。前期木质素与活性碳的共代谢作用破坏了包裹在纤维素外层的木质结构,微生物才得以对暴露在外的纤维素进一步降解[30]。因此,此时易降解的纤维素可能是有机肥中被分解的主要组分,进而调控氮素的同化作用并影响土壤N2O排放对有机肥的响应。与活性碳组分等可以直接被微生物利用的小分子物质不同,纤维素需要在胞外酶的作用下被分解成小分子物质后才能被微生物进一步利用,这降低了微生物对碳氮底物的利用效率[31]。因此,与前期相比,该培养阶段的RR总体呈降低的趋势(图 3)。同时,随着活性有机碳的不断消耗,稳定难降解的芳香类物质累积,从而降低了整体有机碳的可分解性[32],进而抑制同化作用,致使有机肥的芳基度与RR呈显著正相关关系。
培养后期,在不加氮情况下,烷氧碳和双氧烷基碳与RR呈显著负相关关系,表明纤维素和半纤维素进一步成为微生物的主要底物。与前期和中期不同的是,加氮显著改变有机肥性质对培养后期N2O排放的影响,RR与有机肥的V/VSC呈显著负相关关系,但是与蛋白质和全氮含量显著正相关。一方面,氮添加促进了前期和中期有机肥中活性碳底物的分解[15, 27],导致纤维素和半纤维素被更大程度地降解,使得木质素酚的稳定单体(V类)成为后期的主要碳底物;另一方面,氮添加缓解了中后期微生物的氮限制,降低了“氮挖掘”作用[33],减少了有机肥中含氮化合物的分解速率,使其在后期仍能作为硝化作用的氮底物来源,进而增强N2O排放对有机肥的响应。
总体来看,有机肥中总木质素酚和全氮含量是影响加氮土壤N2O排放最主要的因素(图 7)。PGM的全氮含量最低,SMC和CMH的总木质素酚含量最高,因此上述3种有机肥处理土壤N2O排放水平较低。前期研究发现,木质素是调控黑土中有机肥分解过程的重要因子,SMC和CMH的分解速率最低从而具有更高的残留效应[12]。因此,施用SMC和CMH有机肥对黑土有机碳提升和N2O减排具有积极作用。
4 结论本研究表明添加有机肥总体上促进了黑土N2O排放(除SMC处理外),有机肥中有机碳的组分特征是驱动N2O排放响应的重要因素。在硝化作用主导的好氧环境下,有机组分主要是通过影响微生物铵态氮同化与硝化作用之间的底物竞争关系,进而调控有机肥对N2O排放的效应方向及程度。不同培养时期内起主导作用的有机组分存在明显分异,关键组分由前期共代谢的活性有机碳与木质素酚,转为中后期的纤维素和半纤维素。施用低氮、高木质素酚的有机肥能够在一定程度上缓解N2O排放带来的气候负效应,更好实现黑土地固碳减排的目标。但考虑到室内培养和原位试验的差异,今后还需结合田间原位试验,以期更准确评价不同有机肥施用下黑土N2O的排放响应及有机组分特征与N2O排放的耦联效应,同时需进一步利用15N示踪和分子生物学技术阐明有机肥驱动的黑土N2O产生过程及其微生物机制。
| [1] |
Thangarajan R, Bolan N S, Tian G L, et al. Role of organic amendment application on greenhouse gas emission from soil[J]. Science of the Total Environment, 2013, 465: 72-96 DOI:10.1016/j.scitotenv.2013.01.031 (  0) 0) |
| [2] |
Zhou M, Butterbach-Bahl K, Vereecken H, et al. A meta-analysis of soil salinization effects on nitrogen pools, cycles and fluxes in coastal ecosystems[J]. Global Change Biology, 2017, 23(3): 1338-1352 DOI:10.1111/gcb.13430 (  0) 0) |
| [3] |
Diacono M, Montemurro F. Long-term effects of organic amendments on soil fertility: A review[J]. Agronomy for Sustainable Development, 2010, 30(2): 761-786 (  0) 0) |
| [4] |
Li B, Song H, Cao W, et al. Responses of soil organic carbon stock to animal manure application: A new global synthesis integrating the impacts of agricultural managements and environmental conditions[J]. Global Change Biology, 2021, 27(20): 5356-5367 DOI:10.1111/gcb.15731 (  0) 0) |
| [5] |
Lehmann J, Bossio D A, Kögel-Knabner I, et al. The concept and future prospects of soil health[J]. Nature Reviews Earth & Environment, 2020, 1(10): 544-553 (  0) 0) |
| [6] |
Zhou M, Zhu B, Wang S, et al. Stimulation of N2 O emission by manure application to agricultural soils may largely offset carbon benefits: A global meta-analysis[J]. Global Change Biology, 2017, 23(10): 4068-4083 DOI:10.1111/gcb.13648 (  0) 0) |
| [7] |
Thomson A J, Giannopoulos G, Pretty J, et al. Biological sources and sinks of nitrous oxide and strategies to mitigate emissions[J]. The Science of the Total Environment, 2012, 367(1593): 1157-1168 (  0) 0) |
| [8] |
Tian H, Yang J, Xu R, et al. Global soil nitrous oxide emissions since the preindustrial era estimated by an ensemble of terrestrial biosphere models: Magnitude, attribution, and uncertainty[J]. Global Change Biology, 2019, 25(2): 640-659 DOI:10.1111/gcb.14514 (  0) 0) |
| [9] |
Chen Z M, Ding W X, Luo Y Q, et al. Nitrous oxide emissions from cultivated black soil: A case study in Northeast China and global estimates using empirical model[J]. Global Biogeochemical Cycles, 2014, 28(11): 1311-1326 DOI:10.1002/2014GB004871 (  0) 0) |
| [10] |
Xia F, Mei K, Xu Y, et al. Response of N2O emission to manure application in field trials of agricultural soils across the globe[J]. Science of the Total Environment, 2020, 733: 139390 DOI:10.1016/j.scitotenv.2020.139390 (  0) 0) |
| [11] |
Chen H, Li X, Hu F, et al. Soil nitrous oxide emissions following crop residue addition: A meta-analysis[J]. Global Change Biology, 2013, 19(10): 2956-2964 DOI:10.1111/gcb.12274 (  0) 0) |
| [12] |
Xu Y H, Chen Z M, Ding W X, et al. Responses of manure decomposition to nitrogen addition: Role of chemical composition[J]. Science of the Total Environment, 2017, 587/588: 11-21 DOI:10.1016/j.scitotenv.2017.02.033 (  0) 0) |
| [13] |
Klemedtsson L, von Arnold K, Weslien P, et al. Soil CN ratio as a scalar parameter to predict nitrous oxide emissions[J]. Global Change Biology, 2005, 11(7): 1142-1147 DOI:10.1111/j.1365-2486.2005.00973.x (  0) 0) |
| [14] |
Huang Y, Zou J W, Zheng X H, et al. Nitrous oxide emissions as influenced by amendment of plant residues with different C: N ratios[J]. Soil Biology and Biochemistry, 2004, 36(6): 973-981 DOI:10.1016/j.soilbio.2004.02.009 (  0) 0) |
| [15] |
Rashti M R, Wang W J, Reeves S H, et al. Linking chemical and biochemical composition of plant materials to their effects on N2O emissions from a vegetable soil[J]. Soil Biology and Biochemistry, 2016, 103: 502-511 DOI:10.1016/j.soilbio.2016.09.019 (  0) 0) |
| [16] |
Yu Y Y, Guo Z T, Wu H B, et al. Spatial changes in soil organic carbon density and storage of cultivated soils in China from 1980 to 2000[J]. Global Biogeochemical Cycles, 2009, 23(2): GB2021 (  0) 0) |
| [17] |
苑亚茹, 邹文秀, 郝翔翔, 等. 黑土团聚体结合碳对不同有机肥施用量的响应[J]. 生态学报, 2019, 39(9): 3235-3242 (  0) 0) |
| [18] |
郝小雨, 周宝库, 马星竹, 等. 氮肥管理措施对黑土玉米田温室气体排放的影响[J]. 中国环境科学, 2015, 35(11): 3227-3238 (  0) 0) |
| [19] |
李娜, 盛明, 尤孟阳, 等. 应用13C核磁共振技术研究土壤有机质化学结构进展[J]. 土壤学报, 2019, 56(4): 796-812 (  0) 0) |
| [20] |
刘宁, 何红波, 解宏图, 等. 土壤中木质素的研究进展[J]. 土壤通报, 2011, 42(4): 991-996 (  0) 0) |
| [21] |
张楠, 苗淑杰, 乔云发, 等. 东北农田黑土N2O排放研究进展[J]. 土壤学报, 2022. http://kns.cnki.net/kcms/detail/32.1119.P.20220106.1711.006.html.
(  0) 0) |
| [22] |
蔡延江, 丁维新, 项剑. 土壤N2O和NO产生机制研究进展[J]. 土壤, 2012, 44(5): 712-718 (  0) 0) |
| [23] |
Li Z, Zeng Z, Song Z, et al. Vital roles of soil microbes in driving terrestrial nitrogen immobilization[J]. Global Change Biology, 2021, 27(9): 1848-1858 DOI:10.1111/gcb.15552 (  0) 0) |
| [24] |
魏圆云, 崔丽娟, 张曼胤, 等. 土壤有机碳矿化激发效应的微生物机制研究进展[J]. 生态学杂志, 2019, 38(4): 1202-1211 (  0) 0) |
| [25] |
王敬, 程谊, 蔡祖聪, 等. 长期施肥对农田土壤氮素关键转化过程的影响[J]. 土壤学报, 2016, 53(2): 292-304 (  0) 0) |
| [26] |
Chen R, Senbayram M, Blagodatsky S, et al. Soil C and N availability determine the priming effect: Microbial N mining and stoichiometric decomposition theories[J]. Global Change Biology, 2014, 20(7): 2356-2367 (  0) 0) |
| [27] |
Chen Z M, Xu Y H, Cusack D F, et al. Molecular insights into the inhibitory effect of nitrogen fertilization on manure decomposition[J]. Geoderma, 2019, 353: 104-115 (  0) 0) |
| [28] |
Blagodatskaya Е, Kuzyakov Y. Mechanisms of real and apparent priming effects and their dependence on soil microbial biomass and community structure: Critical review[J]. Biology and Fertility of Soils, 2008, 45(2): 115-131 (  0) 0) |
| [29] |
蔡延江, 丁维新, 项剑. 农田土壤N2O和NO排放的影响因素及其作用机制[J]. 土壤, 2012, 44(6): 881-887 (  0) 0) |
| [30] |
Bonanomi G, Incerti G, Giannino F, et al. Litter quality assessed by solid state 13C NMR spectroscopy predicts decay rate better than C/N and Lignin/N ratios[J]. Soil Biology and Biochemistry, 2013, 56: 40-48 (  0) 0) |
| [31] |
Hu Y T, Zheng Q, Noll L, et al. Direct measurement of the in situ decomposition of microbial-derived soil organic matter[J]. Soil Biology and Biochemistry, 2020, 141: 107660 (  0) 0) |
| [32] |
Berg B, Matzner E. Effect of N deposition on decomposition of plant litter and soil organic matter in forest systems[J]. Environmental Reviews, 1997, 5(1): 1-25 (  0) 0) |
| [33] |
Jung J Y, Lal R, Ussiri D A N. Changes in CO2, 13C abundance, inorganic nitrogen, β-glucosidase, and oxidative enzyme activities of soil during the decomposition of switchgrass root carbon as affected by inorganic nitrogen additions[J]. Biology and Fertility of Soils, 2011, 47(7): 801-81 (  0) 0) |
2. School of Applied Meteorology, Nanjing University of Information Science & Technology, Nanjing 210044, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China
 2023, Vol. 55
2023, Vol. 55


