2. 中国科学院大学, 北京 100049;
3. 江苏省污染场地土壤与地下水修复工程实验室, 南京 210008;
4. 西南科技大学环境与资源学院, 四川绵阳 621002
随着我国城市化进程中“退二进三”和“产业转移”政策落实步伐的加快,重污染行业大批关闭和搬迁,导致城市及周边出现大量遗留污染地块。焦化作为我国“土十条”中八大重点监管行业之一,在京津冀及周边地区量大面广,场地及周边土壤与地下水污染突出,已严重危及公众健康和生态安全。多环芳烃(PAHs)是焦化厂生产过程中最典型的污染物之一,企业生产过程中废水池等设施的渗漏,是造成土壤和地下水PAHs污染的主要原因[1]。
萘(naphthalene,C10H8)是由两个苯环组成的一种结构最简单的PAHs,稳定的芳香环结构使其很难从环境中去除,引起了广泛的关注[2]。萘在水中的溶解度较低(31.7 mg/L)[3],容易在土壤中积聚,并逐渐释放到地下水中,持续污染地下水[4]。萘在我国PAHs污染场地中检出率和含量都较高[5-6]。对京津冀5个典型焦化厂污染场地详细调查数据表明,萘在土壤中超标率为1.92% ~ 15.73%,地下水中超标率为3.70% ~ 22.86%。西南某焦化场地土壤中萘含量为0.024 ~ 2 820 mg/kg[7]。因此,迫切需要一种安全、高效且经济的方法来去除土壤和地下水中的萘。
高级氧化技术以化学氧化为基础,利用自由基[8] (如羟基自由基(·OH)、硫酸根自由基(SO4–·)和超氧自由基(O2–·)等)将高抗性和高毒性的有机物分解为危害性小的矿化产物,甚至是二氧化碳和水[9],在持久性有机污染控制方面显示出良好的效果[8],已用于环境中药物和个人护理品[10]、杀虫剂[11]、PAHs(包括萘)[12]等持久性有机污染治理。
目前,国内外学者已对高级氧化技术去除污染土壤和地下水中萘做了较多研究,相关进展还未见综述报道。本文系统归纳了用于萘污染土壤和地下水修复的高级氧化技术的原理和特性,回顾了现有研究中用于催化降解萘的活化剂的降解效果和影响因素,阐述了现有多种氧化剂联合使用或高级氧化技术–微生物协同修复的研究现状,最后展望了未来的研究动态,以期为土壤和地下水中萘的原位高级氧化修复技术提供理论基础。
1 土壤和地下水中萘的高级氧化研究进展高级氧化技术能够在常温常压条件下通过氢提取、电子转移或自由基加成3种机理生成·OH、SO4–·等强氧化性自由基[13],非选择性且高效地氧化大部分有机污染物[11]。常用于降解萘的高级氧化方法包括芬顿、臭氧和过硫酸盐氧化等[14]。1993年Hsu等[15]的研究首次将高级氧化技术用于土壤中萘的去除,使用的氧化剂为臭氧。臭氧既可以直接降解萘,也可以与水或过渡金属离子及其氧化物反应,生成·OH以降解萘,但是臭氧的氧化还原电位低于·OH[16],氧化性较弱。1995年研究人员首次将主要氧化活性物质为·OH的芬顿体系用于土壤中萘的氧化研究[17]。由于芬顿体系中活化过氧化氢生成的·OH的稳定性差,随后,能生成稳定性更强的SO4–·的活化过硫酸盐被广泛用于萘的降解[18]。近30年来,针对土壤和地下水中萘的高级氧化去除研究仍然较少,能够查阅的相关文献共计34篇(截至2022年4月30日),其中较多研究聚焦于活化过硫酸盐,其次是芬顿体系,针对于臭氧的研究很少。不同于废水处理,复杂的土壤结构以及成分使得土壤和地下水中萘的氧化十分困难。土壤的多孔结构使得萘会通过孔填充作用进入土壤颗粒所形成的孔隙中,使萘难以与液相的氧化剂接触[19]。其次,土壤中复杂的成分,例如有机质和黏土矿物都会对萘产生吸附,降低了萘的氧化效率,并且吸附强度随着萘存在于土壤中时间的延长而增大[20-23]。另外,土壤有机质的存在会导致氧化剂的消耗。
针对以上特点,目前,土壤和地下水中萘的高级氧化去除主要有以下两种研究思路:一是增大水相中萘的浓度,借助化学或物理手段促进与土壤结合的萘的溶出同时氧化将萘去除。常用的化学手段包括使用表面活性剂[24]、小分子酸[25-26]或者直接使用氧化剂[27]增大萘的溶出,物理手段包括使用超声[3]和加热[28]促进萘溶出的同时加速其分解。二是改善氧化剂的氧化性能,提升活化剂/氧化剂体系的利用效率,包括使用纳米零价铁[29]、铁螯合剂[24]以及铁矿物[30-32]作为活化剂促进萘的氧化去除。目前,土壤和地下水中萘的高级氧化研究进展详见表 1。
|
|
表 1 萘的高级氧化主要研究进展总结 Table 1 Summary of main research progresses on advanced oxidation of naphthalene |
大量研究表明,芬顿试剂(即过氧化氢和亚铁盐的结合,E0=+2.80 V)能够有效氧化多种有机污染物[39-41]。Fe2+活化过氧化氢分解生成的·OH,可以有效降解有机污染物,但其最适pH为3 ~ 4,不适用于实际地下环境条件。由于均相芬顿体系过氧化氢利用效率低,pH条件限制以及含铁污泥的产生,使得非均相芬顿受到广泛关注。
Kawahara等[17]最早(1995年)使用芬顿试剂对土壤中PAHs进行降解,研究表明电子能够在含铁黏土矿物中的铁离子与吸附在矿物表面的PAHs之间转移,被氧化的铁离子使黏土膨胀,自由基进入黏土孔隙并与包裹在其内部的萘反应,实现萘的降解。这证明黏土矿物在去除土壤中萘的过程中起重要作用。后续研究进一步表明,虽然黏土层由于渗透性低使得原位氧化修复困难,但是广泛存在其中的黏土矿物本身含有可变价金属离子,在地下的还原环境中含Fe2+的黏土能够催化芳香污染物的原位降解,并且矿物的吸附效果对降解起促进作用[30,32]。为充分利用土壤矿物的催化效果,外加能量的类芬顿体系被用于土壤和地下水中萘的氧化。在传统芬顿体系处理萘污染土壤过程中加入超声处理,既可以通过在土壤颗粒表面以及溶液中引起空化促进萘解吸,也可以产热以及通过加速Fe3+向Fe2+的转化催化自由基生成,通过热解或自由基氧化的方式降解萘[3]。电芬顿反应能够在阴极原位生成过氧化氢,将Fe3+还原为Fe2+,促进自由基生成对萘进行氧化,含铁量较高(2 mmol/L)的地下条件能够为过氧化氢的氧化提供更多的铁催化剂,更利于萘完全去除[42]。Yang等[43]在实际地下水溶液中使用经典芬顿体系对萘进行降解,结果表明地下水的pH缓冲能力和碳酸氢根(HCO3–)的存在会抑制萘的降解,另外,地下水中的天然有机质也会消耗自由基,抑制萘的降解,但是仍可以通过增大氧化剂和活化剂的投加量完全去除地下水中的萘。
为了解决均相芬顿体系中铁形态变化导致的芬顿体系适用pH范围较窄以及电子传递速度较慢的问题,非均相催化剂被用于活化过氧化氢,该氧化反应发生在固液界面上,减少了金属阳离子的损耗[44-45]。Zhao等[26]将有机酸(如柠檬酸、草酸等)和铁的络合物用作芬顿反应催化剂去除土壤中PAHs,络合态避免了反应过程中铁泥的产生;同时,柠檬酸和草酸能够促进土壤中结合态的PAHs的释放,使萘能够有效开环降解。土壤性质和污染物的分布情况也是影响土壤中萘去除效果的重要因素[46]。
芳香化合物的C=C断裂和开环主要涉及羟基化和电荷转移两种机理,开环后产生羧酸混合物,随后转化为小分子酸[33]。研究表明,芬顿体系对萘的降解主要中间产物是·OH攻击萘的α位点生成的1-萘酚,另外,·OH与O2–·共同作用生成醛类和酸类物质进一步开环[34,36],其可能的降解机理如图 1所示。
1.2 臭氧氧化臭氧(O3,E0=+2.07 V)既是一种亲电试剂,也是一种亲核试剂,具有极高的氧化能力[47]和选择性,主要攻击富电子官能团,如双键、胺和活化的芳环[48],反应生成副产物·OH。因此,臭氧反应本身被认为是高级氧化或类高级氧化过程[49]。
1993年即有研究使用臭氧去除土壤中的萘,研究表明,使用臭氧对潮湿土壤进行排气能够有效去除土壤中的萘[15]。Masten等[35]使用干燥的土壤也得出相同的结论,并且发现,相对于其他液态氧化剂,气态的臭氧在非饱和土壤中有更强的扩散能力,更容易分散到土壤孔隙中对萘进行氧化,而其在水中的溶解度较低,水分存在会降低臭氧在土壤中的扩散系数,因此臭氧氧化更适用于包气带土壤,而不适用于饱和的含水层。因此,后续对实际土壤和地下水中萘的去除研究逐渐减少。进一步研究表明,臭氧浓度越高对萘的氧化效率越高,pH升高能够促进臭氧生成·OH,但在pH 3 ~ 9的条件下仍以臭氧直接氧化萘的双苯环为主、自由基氧化为辅对萘进行降解[50]。萘与臭氧反应速度很快,在1 min时萘的降解基本达到平衡,推测原因是臭氧极易破坏萘的双苯环结构,并且臭氧浓度越高,PAHs的半衰期越短[51]。
Legube等[52]研究表明,一个臭氧分子与萘反应时,既能进行亲电取代也能发生偶极环加成,两个臭氧分子与萘反应时能够同时在1,2和3,4键进行偶极环加成反应。PAHs氧化试验表明,溶液中的PAHs会直接被臭氧氧化,或者被臭氧与水反应后生成的自由基所氧化[53]。土壤和地下水中的臭氧能够攻击萘使其开环,后在臭氧和自由基(如·OH)的共同作用下有效氧化萘,生成含醛类和羧基的中间产物,其水溶性更强进而更易被矿化,该过程中臭氧起主要作用[54],其氧化机理如图 2所示。
1.3 过硫酸盐氧化过硫酸盐(PS,E0=+2.01 V),包括过单硫酸盐(PMS)和过二硫酸盐(PDS),其分子中含有过氧基O–O,在常温下较稳定,对PAHs降解效果不明显,但在不同活化条件下,O–O键断裂,生成氧化性更强的SO4–·和·OH,降解能力大幅提升[55]。SO4–·的氧化还原电位(E0=+2.5 ~ +3.1 V)高于·OH(E0=+1.8 ~ +2.7 V),且SO4–·的半衰期(40 μs)远长于·OH(< 1 μs),使得活化过硫酸盐的氧化性优于芬顿和类芬顿体系[55]。
最早开始研究的过硫酸盐活化剂为铁及含铁化合物。过量的Fe2+会与SO4–·快速反应,浪费过硫酸盐[18,29,56],为防止Fe2+向Fe3+的快速转化,可以通过改变铁离子形态对溶液中的Fe2+浓度进行控制。研究表明,Fe2+会吸附在土壤表面构成非均相催化剂,活化过硫酸盐以降解萘,此时溶解态Fe2+易与土壤中的羧酸类物质形成高度稳定的络合物,难以被·OH破坏,对萘去除率的影响不大[57-58]。后续研究多聚焦于非均相活化剂活化过硫酸盐氧化萘[59-60]。为提高铁基催化剂的反应活性,比表面积更大的纳米零价铁被用于活化过硫酸盐降解地下水中的萘,但是反应后纳米零价铁表面会形成硫酸亚铁层使其钝化,可持续性较差[29]。Yan等[24]研究表明,使用铁螯合物Fe-EDTA(乙二胺四乙酸)活化过硫酸盐对萘的去除效果较好,其中EDTA不仅可以降低铁离子对pH的依赖性,同时能够溶解部分土壤有机质,增大萘的溶解度。然而,螯合剂EDTA不能被生物降解并可随地下水迁移,可能会造成地下水的二次污染。同时,过硫酸盐的存在会造成土壤pH降低,使得大量金属离子溶出且土壤结构被破坏,也会造成萘从土壤中的溶出增加,从而被过硫酸盐氧化去除。部分过硫酸盐被用于氧化螯合剂而消耗,造成氧化剂的浪费[24]。土壤有机质也会消耗部分过硫酸盐,降低萘的降解效率[56]。实际地下水中Cl–、HCO3–等浓度较高,会抑制萘的降解,Zeng等[25]研究表明,这种不利影响可以通过提高活化剂和氧化剂的浓度来消除,与前人的研究结论一致[43]。
除了通过改善活化剂的活化性能来促进萘在土壤和地下水中的氧化,也可以通过外加能量的物理方式,加速萘的解吸同时促进Fe3+向Fe2+的转化[61]。过硫酸盐的热活化温度一般在40 ~ 99℃,温度升高能够促进萘的解吸,同时活化过硫酸盐生成SO4–·、·OH和1O2等氧化活性物质,提高萘的降解率,该反应中中间产物会与萘竞争消耗氧化剂[30]。超声处理中萘更容易在水–气泡界面积累,增大萘与氧化剂的接触面积,使其具有更快的分解速率[46]。另外,现有研究对萘在固液气三相中的转化对降解的影响关注较少。对4 h内萘在密封系统中的行为探究表明,土壤与水相接触后,有75% 的萘会吸附于土壤中,23% 的萘溶于水相,反应后水相中约98% 的萘被去除,由于水相和气相之间的质量转移,水相中萘的降解也会降低空气中萘的含量,反应后可以去除系统中97% 的萘,其中被降解的萘约62%[61]。
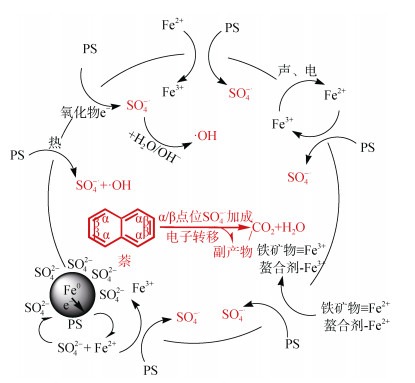
活化过硫酸盐氧化反应原理主要是SO4–·与PAHs通过电子转移和加成反应进行氧化。如图 3所示,过硫酸盐在Fe2+等活化条件下,对萘的氧化途径可能是自由基先在α或β位攻击萘环生成羟基化产物,而后进一步发生羰基化、加氢甲酰化或羧基化生成中间产物[29]。
目前,针对土壤和地下水中萘的高级氧化去除研究多集中于减少土壤基质对萘的吸附和提高活化剂的活化效率两方面,很少有研究聚焦于解决土壤有机质对氧化剂的消耗问题,针对于萘等低浓度高毒性PAHs的特异性氧化技术还有待进一步研究。
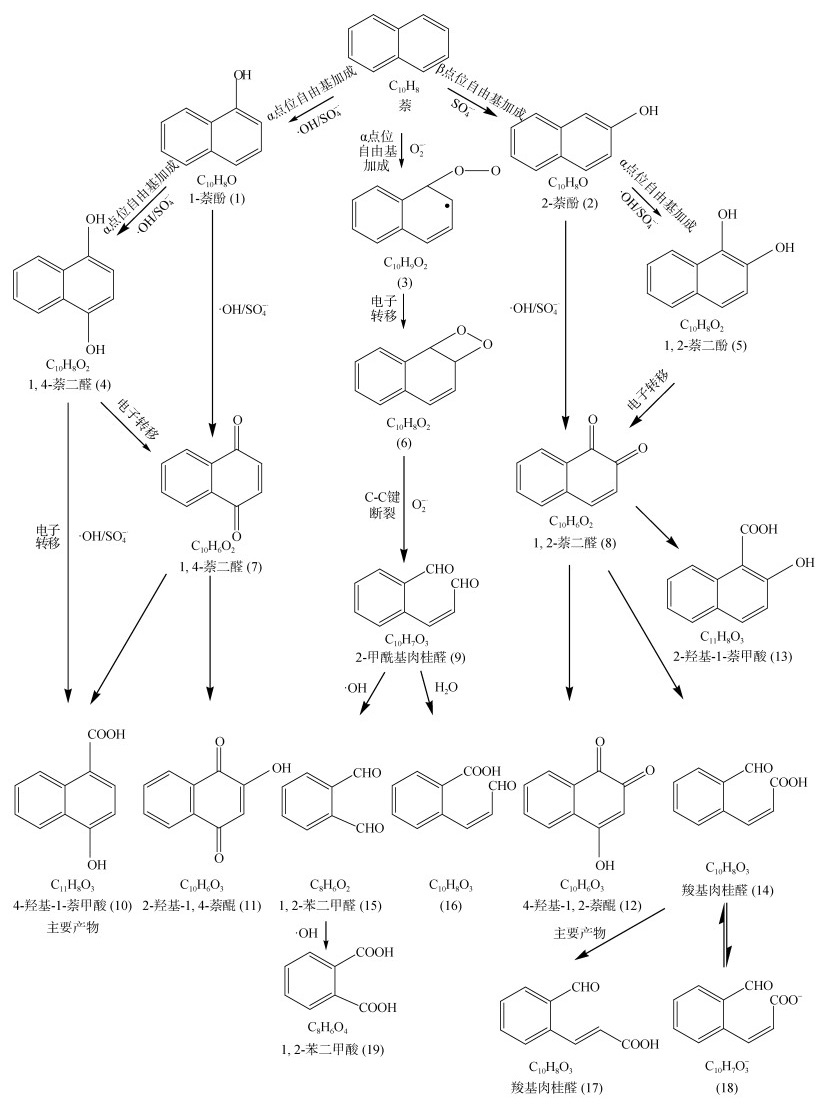
1.4 不同高级氧化技术的比较高级氧化过程中萘可能的降解途径如图 4所示。芬顿以及臭氧氧化体系生成的·OH,可以通过与萘的α位点进行加成反应以及后续的电子转移过程对萘进行降解,但分解速率过快,导致大量自由基的浪费。过硫酸盐的自由基释放速率相对较慢,其生成的SO4–·能够有效作用于萘的α、β点位,发生加成反应,进而通过电子转移对萘进行有效降解。So等[28]首先检测出图 4中的中间产物4-羟基-1-萘甲酸(10)、2-羟基-1, 4萘醌(11)、4-羟基-1, 2萘醌(12)和2-羟基-1-萘甲酸(13)。在整个反应过程中,生成的自由基与过氧化物反应会生成O2–·,O2–·的氧化还原电位较低、存在时间短、浓度低,只用于少量萘的降解[62]。
|
图 4 不同氧化剂氧化萘的降解途径[28,34] Fig. 4 Proposed degradation pathways of naphthalene oxidation by different oxidants |
上述内容总结了单一的氧化体系对萘的氧化效果,不同的试验条件和参数设置使得很难对不同研究中多种氧化剂的氧化效果进行比较,因此部分学者对不同氧化体系中萘的降解进行了比较研究。芬顿体系能够释放大量的·OH,由于其非选择性,会同时氧化土壤中的有机质,造成土壤C/N比及pH降低,更适用于处理天然pH > 6.2的土壤[63]。此外,由于芬顿体系反应速率快,高浓度的过氧化氢分解反应放热会导致土壤温度急剧升高,土壤微生物死亡,不利于微生物降解[63]。研究表明,活化过硫酸盐处理后,PAHs污染土壤pH降低2个单位,总有机碳含量降低50%,且土壤微生物群落丰度及生物多样性均降低[64]。此外,当PAHs去除率相当时,活化过硫酸盐体系的处理价格远高于芬顿体系[37]。与芬顿和类芬顿反应相比,高锰酸盐虽然不能生成自由基,但是由于其较高的氧化活性(E0=+1.80 V),也被用于PAHs的降解,由于不涉及自由基的形成和淬灭,其氧化PAHs的pH适用范围更广,且作用持续时间更长[46]。将类芬顿体系、过硫酸盐和高锰酸盐在不同条件下对16种PAHs的氧化效果进行比较,结果表明,高锰酸盐对污染土壤中PAHs的氧化显示出了一定的选择性,其对PAHs的氧化效率远高于土壤中可提取态有机质[46,65]。然而,高锰酸钾不能将PAHs完全矿化,只能改变其极性结构,从而增大其水溶性和天然生物降解性[66]。
1.5 不同高级氧化技术联合降解研究表明,由于自由基生成速度过快,MnO4-与过氧化氢联用时对PAHs的降解效率弱于其单独使用,而过氧化氢与过硫酸盐联合使用,使得自由基的生成速率适中,使用低剂量的氧化剂也能对PAHs的降解起到较好效果[67]。Li等[68]采用菱铁矿催化的过氧化氢/过硫酸盐体系氧化萘也得到相同的结论,过氧化氢的高反应性和过硫酸盐的稳定性对萘的降解具有协同作用,该体系中pH对降解率的影响比菱铁矿的添加量更显著,酸性条件下萘的降解效率更高。添加过量氧化剂能够避免中间产物醛、酮、醌等含氧PAHs的产生和残留[65]。除了氧化剂之间的联合使用外,还有学者对高级氧化法与其他方法联用降解萘进行了研究。生物降解能够将存在于土壤孔隙中难以与氧化剂接触的PAHs有效降解,但是由于土壤和地下水中PAHs生物有效性低、缺乏PAHs降解菌且PAHs生物降解时间较长[69],所以常将降解速度快、效率高的高级氧化法作为微生物降解的前处理或后处理过程,协同去除萘。将臭氧作为耦合微生物降解的前处理过程,臭氧先与土壤颗粒表面吸附的萘快速反应,该部分萘被完全氧化后,土壤颗粒微孔内的萘很难释放,降解速率下降,后续可继续使用微生物对萘进行降解[38]。适当增加臭氧通入量及时间利于萘的降解,但过量的臭氧以及其过长的处理时间会抑制后续微生物处理[38]。将生物降解与纳米零价铁/过氧化氢类芬顿体系联合使用,萘能够作为微生物的碳源,从而被降解,但不能被完全矿化,随后用纳米零价铁/过氧化氢类芬顿体系可将其代谢产物1-萘酚和1,4-萘二酮完全矿化[70]。Ramteke等[71]将芬顿与超声搅拌联用作为微生物降解萘的预处理过程,氧化和超声将萘降解为更利于微生物利用和分解的小分子,增大了微生物的有氧降解速率,与传统方法相比降解率提高了20% ~ 30%。可见,将高级氧化技术与微生物修复联用在修复萘污染土壤和地下水方面潜力巨大。
2 结论与展望现有基于土壤和地下水中萘的高级氧化研究都聚焦在各种氧化剂、活化剂以及联合使用等条件上的优化,已从传统的均相氧化逐步过渡到非均相氧化。不同的氧化剂都能通过高级氧化有效降解萘,但由于实际土壤和地下水成分复杂,原位修复条件下氧化剂和与土壤或其他组分结合的萘难以充分接触,无法实现土壤和地下水中萘的绿色、高效、可持续修复。因此,未来研究应该着重解决以下问题:
1) 加强场地实用性研究,充分考虑萘的特性对其在土壤和地下水中降解效果的影响。针对萘的挥发性及疏水性,其在三相之间的转化对地下水和土壤中萘降解效果的影响还有待探究。应采用与实际土壤和地下水相近的试验设置方法进行影响因素评价,为后续工程化应用提供实际支持。
2) 强化萘高级氧化降解机理及安全性的研究,探究氧化剂及其活化剂和氧化过程中生成的副产物对环境的影响。现有研究缺乏对萘降解中间产物及其降解效果的探究,另外,针对常用高级氧化活化剂的迁移规律及环境影响的研究较少,其投入使用后对生态环境的影响尚不清楚。
3) 与其他修复技术联用,如作为微生物降解的预处理或后处理过程,提高微生物降解效率同时减少氧化剂投加量,提高降解产物的矿化率。
4) 拓宽氧化剂的使用范围,提高氧化剂的利用率。提高氧化反应的电子传输效率、扩大pH适用范围、优化催化剂与氧化剂的投加量、提高活化剂对萘的专一性作用等有待进一步研究。
5) 对萘–苯复合污染进行降解机理及效果研究。作为焦化厂主要副产物,萘和苯也是焦化场地主要地下水关注污染物,且苯超标区域往往伴随着萘超标,呈现明显的共溶迁移特征,但是目前对于萘–苯复合污染降解机理研究尚处空白。
| [1] |
周若凡, 吴艳辉. 典型焦化场地污染特征研究进展[J]. 山东化工, 2020, 49(14): 51–52, 56 DOI:10.3969/j.issn.1008-021X.2020.14.019 (  0) 0) |
| [2] |
张默, 贾明云, 卞永荣, 等. 不同温度玉米秸秆生物炭对萘的吸附动力学特征与机理[J]. 土壤学报, 2015, 52(5): 1106-1115 (  0) 0) |
| [3] |
Virkutyte J, Vičkačkaite V, Padarauskas A. Sono-oxidation of soils: Degradation of naphthalene by sono-Fenton-like process[J]. Journal of Soils and Sediments, 2010, 10(3): 526-536 DOI:10.1007/s11368-009-0153-2 (  0) 0) |
| [4] |
孙清芳, 冯玉杰, 武晓威, 等. 松花江流域萘的多介质环境迁移与归趋模拟[J]. 哈尔滨工业大学学报, 2013, 45(4): 64-68 (  0) 0) |
| [5] |
曹云者, 韩梅, 夏凤英, 等. 采用健康风险评价模型研究场地土壤有机污染物环境标准取值的区域差异及其影响因素[J]. 农业环境科学学报, 2010, 29(2): 270-275 (  0) 0) |
| [6] |
程家丽, 黄启飞, 魏世强, 等. 我国环境介质中多环芳烃的分布及其生态风险[J]. 环境工程学报, 2007, 1(4): 138-144 DOI:10.3969/j.issn.1673-9108.2007.04.032 (  0) 0) |
| [7] |
王培俊, 刘俐, 李发生, 等. 西南某焦化场地土壤中典型污染物的特征分布[J]. 煤炭学报, 2011, 36(9): 1587-1592 DOI:10.13225/j.cnki.jccs.2011.09.036 (  0) 0) |
| [8] |
Duan X G, Sun H Q, Shao Z P, et al. Nonradical reactions in environmental remediation processes: Uncertainty and challenges[J]. Applied Catalysis B: Environmental, 2018, 224: 973-982 DOI:10.1016/j.apcatb.2017.11.051 (  0) 0) |
| [9] |
Ike I A, Linden K G, Orbell J D, et al. Critical review of the science and sustainability of persulphate advanced oxidation processes[J]. Chemical Engineering Journal, 2018, 338: 651-669 DOI:10.1016/j.cej.2018.01.034 (  0) 0) |
| [10] |
Kanakaraju D, Glass B D, Oelgemöller M. Advanced oxidation process-mediated removal of pharmaceuticals from water: A review[J]. Journal of Environmental Management, 2018, 219: 189-207 (  0) 0) |
| [11] |
Babu D S, Srivastava V, Nidheesh P V, et al. Detoxification of water and wastewater by advanced oxidation processes[J]. Science of the Total Environment, 2019, 696: 133961 DOI:10.1016/j.scitotenv.2019.133961 (  0) 0) |
| [12] |
Mojiri A, Zhou J L, Ohashi A, et al. Comprehensive review of polycyclic aromatic hydrocarbons in water sources, their effects and treatments[J]. Science of the Total Environment, 2019, 696: 133971 DOI:10.1016/j.scitotenv.2019.133971 (  0) 0) |
| [13] |
Glaze W H, Kang J W, Chapin D H. The chemistry of water treatment processes involving ozone, hydrogen peroxide and ultraviolet radiation[J]. Ozone: Science & Engineering, 1987, 9(4): 335-352 (  0) 0) |
| [14] |
Hu X B, Liu B Z, Deng Y H, et al. Adsorption and heterogeneous Fenton degradation of 17α-methyltestosterone on nano Fe3O4/MWCNTs in aqueous solution[J]. Applied Catalysis B: Environmental, 2011, 107(3/4): 274-283 (  0) 0) |
| [15] |
Hsu I Y, Davies S H R, Masten S J. The use of ozone for the removal of residual trichloroethylene from unsaturated soils[C]. The Proceedings of the 48th Annual Purdue University Industrial Waste Conference, 10-12 May, 1993.
(  0) 0) |
| [16] |
Aguilar C M, Rodríguez J L, Chairez I, et al. Naphthalene degradation by catalytic ozonation based on nickel oxide: Study of the ethanol as cosolvent[J]. Environmental Science and Pollution Research, 2017, 24(33): 25550-25560 DOI:10.1007/s11356-016-6134-2 (  0) 0) |
| [17] |
Kawahara F K, Davila B, Al-Abed S R, et al. Polynuclear aromatic hydrocarbon (PAH) release from soil during treatment with Fenton's reagent[J]. Chemosphere, 1995, 31(9): 4131-4142 DOI:10.1016/0045-6535(95)80013-B (  0) 0) |
| [18] |
Liang C J, Guo Y Y. Mass transfer and chemical oxidation of naphthalene particles with zerovalent iron activated persulfate[J]. Environmental Science & Technology, 2010, 44(21): 8203-8208 (  0) 0) |
| [19] |
杨勇, 张蒋维, 陈恺, 等. 化学氧化法治理焦化厂PAHs污染土壤[J]. 环境工程学报, 2016, 10(1): 427-431 (  0) 0) |
| [20] |
Weber W J Jr, McGinley P M, Katz L E. A distributed reactivity model for sorption by soils and sediments. 1. Conceptual basis and equilibrium assessments[J]. Environmental Science & Technology, 1992, 26(10): 1955-1962 (  0) 0) |
| [21] |
Weber W J, Huang W L. A distributed reactivity model for sorption by soils and sediments. 4. intraparticle heterogeneity and phase-distribution relationships under nonequilibrium conditions[J]. Environmental Science & Technology, 1996, 30(3): 881-888 (  0) 0) |
| [22] |
Amellal N, Portal J M, Berthelin J. Effect of soil structure on the bioavailability of polycyclic aromatic hydrocarbons within aggregates of a contaminated soil[J]. Applied Geochemistry, 2001, 16(14): 1611-1619 DOI:10.1016/S0883-2927(01)00034-8 (  0) 0) |
| [23] |
Bogan B W, Trbovic V. Effect of sequestration on PAH degradability with Fenton's reagent: Roles of total organic carbon, humin, and soil porosity[J]. Journal of Hazardous Materials, 2003, 100(1/2/3): 285-300 (  0) 0) |
| [24] |
Yan D Y S, Lo I M C. Removal effectiveness and mechanisms of naphthalene and heavy metals from artificially contaminated soil by iron chelate-activated persulfate[J]. Environmental Pollution, 2013, 178: 15-22 DOI:10.1016/j.envpol.2013.02.030 (  0) 0) |
| [25] |
Zeng G L, Yang R M, Fu X R, et al. Naphthalene degradation in aqueous solution by Fe(II) activated persulfate coupled with citric acid[J]. Separation and Purification Technology, 2021, 264: 118441 DOI:10.1016/j.seppur.2021.118441 (  0) 0) |
| [26] |
Zhao X Q, Qin L, Gatheru Waigi M, et al. Removal of bound PAH residues in contaminated soils by Fenton oxidation[J]. Catalysts, 2019, 9(7): 619 DOI:10.3390/catal9070619 (  0) 0) |
| [27] |
Sra K S, Thomson N R, Barker J F. Persulfate injection into a gasoline source zone[J]. Journal of Contaminant Hydrology, 2013, 150: 35-44 DOI:10.1016/j.jconhyd.2013.03.007 (  0) 0) |
| [28] |
So H L, Chu W, Wang Y H. Naphthalene degradation by Fe2+/Oxone/UV - Applying an unconventional kinetics model and studying the reaction mechanism[J]. Chemosphere, 2019, 218: 110-118 DOI:10.1016/j.chemosphere.2018.11.091 (  0) 0) |
| [29] |
Al-Shamsi M A, Thomson N R. Treatment of organic compounds by activated persulfate using nanoscale zerovalent iron[J]. Industrial & Engineering Chemistry Research, 2013, 52(38): 13564-13571 (  0) 0) |
| [30] |
So H L, Chu W, Xu W C. Photocatalysis of naphthalene by Fe3O4/Oxone/UV: Simultaneous radical and non-radical pathways[J]. Journal of Environmental Chemical Engineering, 2021, 9(2): 105076 DOI:10.1016/j.jece.2021.105076 (  0) 0) |
| [31] |
Liu X X, Yuan S H, Zhang P, et al. Reduced nontronite-activated H2O2 for contaminants degradation: The beneficial role of clayed fractions in ISCO treatments[J]. Journal of Hazardous Materials, 2020, 386: 121945 DOI:10.1016/j.jhazmat.2019.121945 (  0) 0) |
| [32] |
Costa R C C, Moura F C C, Ardisson J D, et al. Highly active heterogeneous Fenton-like systems based on Fe0/ Fe3O4 composites prepared by controlled reduction of iron oxides[J]. Applied Catalysis B: Environmental, 2008, 83(1/2): 131-139 (  0) 0) |
| [33] |
Brillas E, Garcia-Segura S. Benchmarking recent advances and innovative technology approaches of Fenton, photo-Fenton, electro-Fenton, and related processes: A review on the relevance of phenol as model molecule[J]. Separation and Purification Technology, 2020, 237: 116337 DOI:10.1016/j.seppur.2019.116337 (  0) 0) |
| [34] |
Li L, Lai C, Huang F L, et al. Degradation of naphthalene with magnetic bio-char activate hydrogen peroxide: Synergism of bio-char and Fe-Mn binary oxides[J]. Water Research, 2019, 160: 238-248 DOI:10.1016/j.watres.2019.05.081 (  0) 0) |
| [35] |
Masten S J, Davies S H R. Efficacy of in situ for the remediation of PAH contaminated soils[J]. Journal of Contaminant Hydrology, 1997, 28(4): 327-335 DOI:10.1016/S0169-7722(97)00019-3 (  0) 0) |
| [36] |
Tran L H, Drogui P, Mercier G, et al. Comparison between Fenton oxidation process and electrochemical oxidation for PAH removal from an amphoteric surfactant solution[J]. Journal of Applied Electrochemistry, 2010, 40(8): 1493-1510 DOI:10.1007/s10800-010-0128-4 (  0) 0) |
| [37] |
Xu Y Z, Che T, Li Y J, et al. Remediation of polycyclic aromatic hydrocarbons by sulfate radical advanced oxidation: Evaluation of efficiency and ecological impact[J]. Ecotoxicology and Environmental Safety, 2021, 223: 112594 DOI:10.1016/j.ecoenv.2021.112594 (  0) 0) |
| [38] |
蔡月华, 张丹, 姜林, 等. O3预处理耦合微生物降解修复PAHs污染土壤[J]. 环境科学研究, 2014, 27(12): 1493-1498 (  0) 0) |
| [39] |
Mirzaei A, Chen Z, Haghighat F, et al. Removal of pharmaceuticals from water by homo/heterogonous Fenton-type processes - A review[J]. Chemosphere, 2017, 174: 665-688 DOI:10.1016/j.chemosphere.2017.02.019 (  0) 0) |
| [40] |
Clarizia L, Russo D, Di Somma I, et al. Homogeneous photo-Fenton processes at near neutral pH: A review[J]. Applied Catalysis B: Environmental, 2017, 209: 358-371 DOI:10.1016/j.apcatb.2017.03.011 (  0) 0) |
| [41] |
Arnold S M, Hickey W J, Harris R F. Degradation of atrazine by Fenton's reagent: Condition optimization and product quantification[J]. Environmental Science & Technology, 1995, 29(8): 2083-2089 (  0) 0) |
| [42] |
McQuillan R V, Stevens G W, Mumford K A. Assessment of the electro-Fenton pathway for the removal of naphthalene from contaminated waters in remote regions[J]. Science of the Total Environment, 2021, 762: 143155 DOI:10.1016/j.scitotenv.2020.143155 (  0) 0) |
| [43] |
Yang R M, Zeng G L, Xu Z Q, et al. Comparison of naphthalene removal performance using H2O2, sodium percarbonate and calcium peroxide oxidants activated by ferrous ions and degradation mechanism[J]. Chemosphere, 2021, 283: 131209 DOI:10.1016/j.chemosphere.2021.131209 (  0) 0) |
| [44] |
Zhu Y P, Zhu R L, Xi Y F, et al. Strategies for enhancing the heterogeneous Fenton catalytic reactivity: A review[J]. Applied Catalysis B: Environmental, 2019, 255: 117739 DOI:10.1016/j.apcatb.2019.05.041 (  0) 0) |
| [45] |
Ribeiro R S, Silva A M T, Figueiredo J L, et al. Catalytic wet peroxide oxidation: A route towards the application of hybrid magnetic carbon nanocomposites for the degradation of organic pollutants. A review[J]. Applied Catalysis B: Environmental, 2016, 187: 428-460 DOI:10.1016/j.apcatb.2016.01.033 (  0) 0) |
| [46] |
Biache C, Lorgeoux C, Andriatsihoarana S, et al. Effect of pre-heating on the chemical oxidation efficiency: Implications for the PAH availability measurement in contaminated soils[J]. Journal of Hazardous Materials, 2015, 286: 55-63 DOI:10.1016/j.jhazmat.2014.12.041 (  0) 0) |
| [47] |
Miklos D B, Remy C, Jekel M, et al. Evaluation of advanced oxidation processes for water and wastewater treatment - A critical review[J]. Water Research, 2018, 139: 118-131 DOI:10.1016/j.watres.2018.03.042 (  0) 0) |
| [48] |
Merényi G, Lind J, Naumov S, et al. Reaction of ozone with hydrogen peroxide (peroxone process): A revision of current mechanistic concepts based on thermokinetic and quantum-chemical considerations[J]. Environmental Science & Technology, 2010, 44(9): 3505-3507 (  0) 0) |
| [49] |
Buffle M O, von Gunten U. Phenols and amine induced HO• generation during the initial phase of natural water ozonation[J]. Environmental Science & Technology, 2006, 40(9): 3057-3063 (  0) 0) |
| [50] |
Lu S, Liu L B, Demissie H, et al. Design and application of metal-organic frameworks and derivatives as heterogeneous Fenton-like catalysts for organic wastewater treatment: A review[J]. Environment International, 2021, 146: 106273 DOI:10.1016/j.envint.2020.106273 (  0) 0) |
| [51] |
李淑琪. 臭氧氧化技术去除水中萘的研究[D]. 北京: 中国地质大学(北京), 2020.
(  0) 0) |
| [52] |
Legube B, Guyon S, Sugimitsu H, et al. Ozonation du naphtalene en milieu aqueux—I. Consommation d'ozone et produits de reaction[J]. Water Research, 1986, 20(2): 197-208 DOI:10.1016/0043-1354(86)90009-6 (  0) 0) |
| [53] |
Beltran F J, Ovejero G, Encinar J M, et al. Oxidation of polynuclear aromatic hydrocarbons in water. 1. ozonation[J]. Industrial & Engineering Chemistry Research, 1995, 34(5): 1596-1606 (  0) 0) |
| [54] |
Wang H W, Li X Y, Hao Z P, et al. Transformation of dissolved organic matter in concentrated leachate from nanofiltration during ozone-based oxidation processes (O3, O3/H2O2 and O3/UV)[J]. Journal of Environmental Management, 2017, 191: 244-251 DOI:10.1016/j.jenvman.2017.01.021 (  0) 0) |
| [55] |
Ushani U, Lu X Q, Wang J H, et al. Sulfate radicals-based advanced oxidation technology in various environmental remediation: A state-of-the-art review[J]. Chemical Engineering Journal, 2020, 402: 126232 DOI:10.1016/j.cej.2020.126232 (  0) 0) |
| [56] |
邸莎, 张超艳, 颜增光, 等. 过硫酸钠对我国典型土壤中多环芳烃氧化降解效果的影响[J]. 环境科学研究, 2018, 31(1): 95-101 (  0) 0) |
| [57] |
Ganiyu S O, Zhou M H, Martínez-Huitle C A. Heterogeneous electro-Fenton and photoelectro-Fenton processes: A critical review of fundamental principles and application for water/wastewater treatment[J]. Applied Catalysis B: Environmental, 2018, 235: 103-129 (  0) 0) |
| [58] |
Han D S, Yun Y B, Ko S O. Effect of the presence of soil on the ferrous catalyzed sodium persulfate oxidation of naphthalene[J]. Journal of Soil & Groundwater Environment, 2010, 15(1): 29-38 (  0) 0) |
| [59] |
Gao Y Q, Gao N Y, Yin D Q, et al. Oxidation of the β-blocker propranolol by UV/persulfate: Effect, mechanism and toxicity investigation[J]. Chemosphere, 2018, 201: 50-58 (  0) 0) |
| [60] |
尹汉雄, 唐玉朝, 黄显怀, 等. 紫外光强化Fe(Ⅱ)-EDTA活化过硫酸盐降解直接耐酸大红4BS[J]. 环境科学研究, 2017, 30(7): 1105-1111 (  0) 0) |
| [61] |
Mendes G P, Magalhães V M A, Soares L C R, et al. Treatability studies of naphthalene in soil, water and air with persulfate activated by iron(II)[J]. Journal of Environmental Sciences, 2020, 90: 67-77 (  0) 0) |
| [62] |
Lair A, Ferronato C, Chovelon J M, et al. Naphthalene degradation in water by heterogeneous photocatalysis: An investigation of the influence of inorganic anions[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2008, 193(2/3): 193-203 (  0) 0) |
| [63] |
Cheng M, Zeng G M, Huang D L, et al. Hydroxyl radicals based advanced oxidation processes (AOPs) for remediation of soils contaminated with organic compounds: A review[J]. Chemical Engineering Journal, 2016, 284: 582-598 (  0) 0) |
| [64] |
Lai X J, Ning X N, Chen J Y, et al. Comparison of the Fe2+/H2O2 and Fe2+/PMS systems in simulated sludge: Removal of PAHs, migration of elements and formation of chlorination by-products[J]. Journal of Hazardous Materials, 2020, 398: 122826 (  0) 0) |
| [65] |
Boulangé M, Lorgeoux C, Biache C, et al. Fenton-like and potassium permanganate oxidations of PAH-contaminated soils: Impact of oxidant doses on PAH and polar PAC (polycyclic aromatic compound) behavior[J]. Chemosphere, 2019, 224: 437-444 (  0) 0) |
| [66] |
Rauscher L, Sakulthaew C, Comfort S. Using slow-release permanganate candles to remediate PAH-contaminated water[J]. Journal of Hazardous Materials, 2012, 241/242: 441-449 (  0) 0) |
| [67] |
Ferrarese E, Andreottola G, Oprea I A. Remediation of PAH-contaminated sediments by chemical oxidation[J]. Journal of Hazardous Materials, 2008, 152(1): 128-139 (  0) 0) |
| [68] |
Li Y H, Zhao L, Chen F L, et al. Oxidation of nine petroleum hydrocarbon compounds by combined hydrogen peroxide/sodium persulfate catalyzed by siderite[J]. Environmental Science and Pollution Research, 2020, 27(20): 25655-25663 (  0) 0) |
| [69] |
苏梦缘, 王红旗, 李艺, 等. 多环芳烃降解菌菌群构建及其适宜降解环境条件的确定[J]. 环境工程学报, 2017, 11(2): 1192-1198 (  0) 0) |
| [70] |
Yu B, Jin X Y, Kuang Y, et al. An integrated biodegradation and nano-oxidation used for the remediation of naphthalene from aqueous solution[J]. Chemosphere, 2015, 141: 205-211 (  0) 0) |
| [71] |
Ramteke L P, Gogate P R. Treatment of toluene, benzene, naphthalene and xylene (BTNXs) containing wastewater using improved biological oxidation with pretreatment using Fenton/ultrasound based processes[J]. Journal of Industrial and Engineering Chemistry, 2015, 28: 247-260 (  0) 0) |
2. Chinese Academy of Sciences, Beijing 100049, China;
3. Jiangsu Engineering Laboratory of Soil and Groundwater Remediation of Contaminated Sites, Nanjing 210008, China;
4. College of Environment and Resources, Southwest University of Science and Technology, Mianyang, Sichuan 621002, China
 2023, Vol. 55
2023, Vol. 55