2. 中国科学院大学, 北京 100049;
3. 南京林业大学林学院, 南京 210037;
4. 扬州大学环境科学与工程学院, 扬州 225009
秸秆还田被认为是保持土壤质量、维系土壤养分平衡以及减少焚烧造成大气污染的重要举措[1-2]。但是由于稻季秸秆还田造成大量的CH4排放[3-4],因此秸秆“麦季还田,稻季不还田”被认为是减少稻田CH4排放的有效途径[3]。然而N2O作为另一种重要的温室气体,其在百年尺度上的全球升温潜能超过CO2的310倍[5]。Li等人[6]发现全球范围内秸秆还田显著增加了29.70% 的N2O排放量。并且稻麦轮作系统下麦季开始秸秆还田同样可能提高水稻季的N2O排放量[7]。因此,农业生产中开发出对环境损害较少的秸秆还田替代方案尤为重要。
近年来,生物质炭(生物质在缺氧条件下裂解产生的高含碳难分解物质)在改善土壤质量、提高作物生产力和增加土壤固碳能力等方面的积极作用得到广泛认可[8-9]。同样生物质炭对减少N2O排放也有很多报道[10-11]。Liu等人[12]通过全球数据统计分析发现短期生物质炭施用可减少32% 的土壤N2O排放。这主要归因于生物质炭施用:①增加对土壤无机氮(NH4+和NO3–)的吸附和固定[13],减少硝化和反硝化底物;②改善土壤通气性,抑制反硝化过程[14];③通过提高土壤pH促进N2O还原酶活性以及生物质炭的电子传递催化N2O还原为氮气(N2)[14-15];④释放对微生物有毒性的化合物(如乙烯),抑制硝化和反硝化过程[16]。但是,也有研究发现生物质炭施用引起了土壤N2O排放的增加,并认为可能与土壤NH4+-N、NO3–-N和可溶性有机碳(DOC)含量增加促进了土壤硝化和反硝化产N2O的能力有关[17]。
生物质炭在土壤中历经复杂的物理、化学和生物学老化过程,表面的有机物质、孔隙结构以及官能团数量和种类会逐步发生变化。Duan等人[18]发现新鲜生物质炭可以实现N2O的减排,而老化生物质炭更大的羧基和羟基官能团密度可以诱导增强硝化和反硝化作用进而刺激N2O排放。Liu等人[19]研究结果也表明生物质炭对N2O排放的抑制作用仅在初期表现突出,随着时间的推移抑制作用趋于减弱,作者将其归因于生物质炭表面的活性官能团与金属结合老化,无法在产生N2O的氧化还原反应中充当电子供体。土壤N素有效性的不断变化可能间接影响土壤N2O排放过程。Song等人[20]在0.5 ~ 3 a的生物质炭施用时长对N2O排放量的影响研究中发现,生物质炭对N2O的减排作用随着试验时长的增加而减小,并在2 ~ 3 a时间段增加了N2O排放量。同时水稻植株氮吸收、土壤NH3挥发和氮淋溶对生物质炭连续施用时长的响应并不一致,这可能间接影响N2O的排放[21–23]。因此开展生物质炭长期施用对N2O排放影响研究具有重要意义。
1 材料与方法 1.1 试验田概况及生物质炭性质试验田位于江苏省扬州市小纪镇宗村村(32°35′5″N, 119°42′0″E),该地区属于亚热带温湿气候带,海拔5 m,年平均气温14.0 ℃,无霜期213 d,年降水量1 058 mm,蒸发量1 100 mm。土壤类型为下位砂姜土,砂粒(0.02 ~ 2 mm)、粉粒(0.002 ~ 0.02 mm)、黏粒(< 0.002 mm)质量分数分别为:20%、58% 和22%。生物质炭是由玉米秸秆在400 ℃下通过慢速热解的专利设备[24]生产。土壤、玉米秸秆和生物质炭特性见表 1。
|
|
表 1 土壤、玉米秸秆及生物质炭的基本性质 Table 1 Basic properties of soil, maize stalks and their derived biochar |
试验从2010年麦季开始。试验包括5个处理:无秸秆还田和生物质炭施用(CK);6 t/(hm2·a) 秸秆还田(CS);2.4 t/(hm2·a) 生物质炭施用(BC1);6 t/(hm2·a) 生物质炭施用(BC2);12 t/(hm2·a) 生物质炭施用(BC3)。CS处理秸秆还田量约为当地单位面积玉米秸秆生物量,BC1处理生物质炭施用量相当于CS处理秸秆全部炭化后的量。玉米秸秆和生物质炭均只在麦季施用,在小麦播种前将玉米秸秆或生物质炭均匀地翻耕到0 ~ 15 cm土层中,截至2021年稻季已经进行了11次玉米秸秆和生物质炭的施用。试验布局为完全随机设计,每个处理3个重复,共15个小区,小区之间相隔0.5 m。每个小区(2.5 m×4 m)有独立的灌水和排水口。水稻品种为南粳40(Oryza sativa L., cv. Nanjing 40),5月中旬开始育秧,6月中旬将秧苗移植到试验小区中,密度为24穴/m2,每穴3株秧苗。氮肥施用量为N 200 kg/hm2,以尿素形式分3次施用,秧苗移栽前35%,分蘖期35%,抽穗期30%;磷肥施用量为P2O5 70 kg/hm2;钾肥为K2O 70 kg/hm2作为基肥一次施入。田间水分管理方式为淹水–烤田–间歇灌溉,移栽后第38 ~ 46天烤田,第47天复水。其他田间管理遵循当地的农艺管理方式,包括耕作、防虫害和杂草控制。水稻生长期约120 d,10月下旬收割,每个小区割取1 m2(24穴)的水稻(不包括边界水稻植株)以供测产。
1.3 土壤N2O排放的测定采用静态箱–气相色谱法测定土壤N2O排放量。每个处理设有0.5 m×0.4 m由聚乙烯板做成的底座(埋入土深0.2 m),底座上端边缘有水槽。采气前将高为0.6 m或1.2 m的采气箱(根据水稻高度选用合适的尺寸)罩于底座上,并在水槽内加水使体系密闭。箱顶连有三通阀,通过注射器与三通阀连接采集气体。每次采样时,从每个小区采气箱中采集3个气样,时间间隔为20 min,每个气样30 mL,全部注入预先抽真空的20 mL气瓶内。在整个稻季,于施肥后每1 ~ 2 d采集一批气体样品,持续12 d,其后每7 ~ 10 d采集一批气样,采集时间为上午8:30—11:30。气体样品在实验室用气相色谱仪(岛津GC2014C)测定N2O浓度。
1.4 土壤样品分析2021年水稻收获后,在每个小区用土钻(直径2.5 cm)以五点取样法采集5个样点的0 ~ 15 cm的土壤样品,混匀后装于自封袋中用冰盒带回实验室,挑出根系、石子、植物残渣等,根据样品分析标准将土壤样品分成3份,分别进行自然风干,以及保存在4 ℃和-20 ℃冰箱中。土壤无机氮(NH4+和NO3–)含量、微生物生物量碳和微生物生物量氮(SMBC和SMBN)含量以及反硝化酶活性(DEA)立即进行测定。用Mettler-Toledo pH计测定土壤pH,土壤与水的比例为1:2.5(m/V);使用碳酸氢钠提取、钼蓝比色法测定土壤有效磷(AP)含量;用乙酸铵提取、火焰光度法测定速效钾(AK)含量。取一部分过100目筛网的土壤样品用H2O2-H2SO4混合溶液消煮,消煮后水溶液用火焰光度法测定土壤全钾(TK)含量,全自动间断化学分析仪(SmartChem 200,意大利)测量土壤全氮(TN)和全磷(TP)含量。土壤碱解氮(AN)含量用直接碱解扩散法测定;土壤无机氮(NH4+-N和NO3–-N)含量采用2 mol/L KCl浸提–流动分析仪比色法测定;土壤可溶性有机碳(DOC)和总溶解氮(DN)含量采用0.5 mol/L K2SO4浸提后TOC-TN分析仪测定;土壤总有机碳(TOC)含量采用重铬酸钾外加热法测定;可溶性有机氮(DON)为总溶解氮含量与NH4+-N和NO3–-N含量之差;易氧化碳(ROC)采用高锰酸钾氧化法和比色法测定[25];DEA采用乙炔抑制法测定[26];SMBC和SMBN通过氯仿熏蒸提取法测定;土壤阳离子交换量(CEC)使用乙酸铵交换法、全自动凯氏定氮仪测定[27]。
1.5 数据统计分析采用SPSS 18.0进行单因素方差分析,最小显著性差异法进行多重比较(P < 0.05)。其余统计分析使用R3.6.2和R4.0.4进行。不同土壤性质对N2O累积排放量的相对重要性通过“randomForest”包[28]进行加权随机森林分析(RF),并通过“rfPermute”包[29]评估预测变量的重要性。用“plspm”包[30]偏最小二乘路径分析法(PLS-PM)分析土壤特性、N2O排放量和水稻产量之间的关系。数据测定结果均以平均值±标准偏差表示(3次重复)。
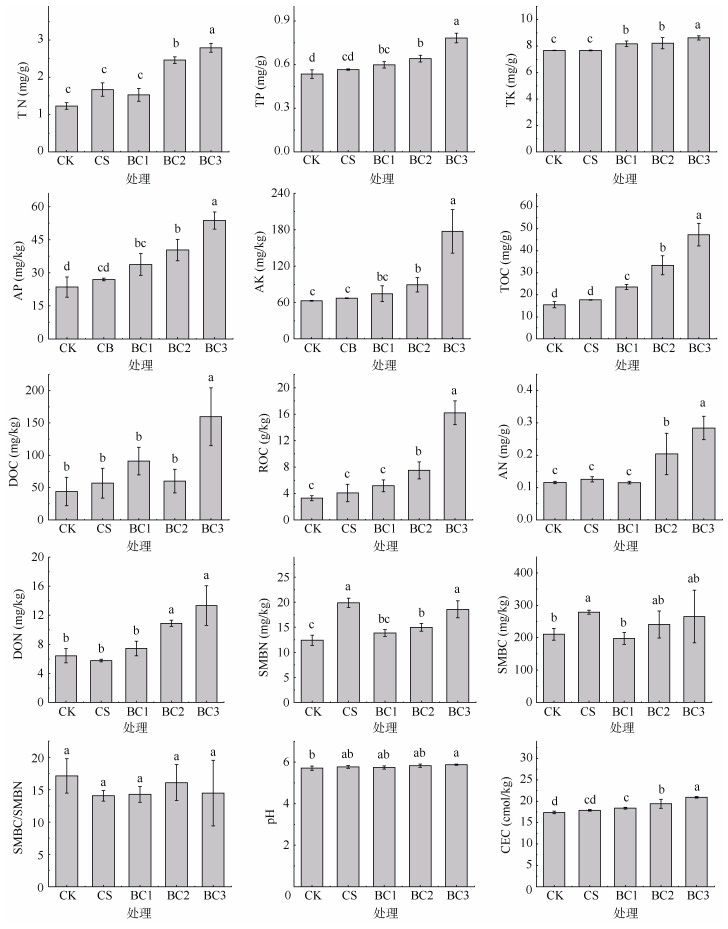
2 结果 2.1 土壤性质和水稻产量长期连续施用生物质炭显著改善了土壤理化性质。由图 1可知,相较于CK,3种剂量生物质炭施用下土壤的TN、TP和TK含量分别平均增加了83.67%、26.07% 和8.64%;与此同时,土壤速效养分AN、AP和AK的含量也随生物质炭施用量的增加而增加。施用3种剂量生物质炭分别平均提高土壤DOC和DON含量64.01% 和135.50%,提高SMBC和SMBN含量11.47% 和27.53%,以及土壤TOC和ROC含量124.29% 和191.88%。长期连续秸秆还田和中等或低剂量(BC1或BC2)生物质炭施用对土壤pH的影响较小。施用生物质炭显著提高土壤CEC 5.76% ~ 20.35%,并且土壤CEC与生物质炭施用剂量呈正相关关系。相较于CK,CS处理分别显著提高了60.35% 和32.47% 的SMBN和SMBC含量,在所有处理中提升幅度最大。相对于CS处理,BC1处理的土壤TK和TOC含量分别显著提高了6.42% 和32.73%(图 1)。长期连续秸秆还田和生物质炭施用对水稻产量的影响较小,均未达到显著水平(表 2)。
|
(图中小写字母不同表示处理间差异显著(P < 0.05),下同) 图 1 长期连续玉米秸秆还田和生物质炭施用对土壤性质的影响 Fig. 1 Effcets of long-term continuous maize straw returning and biochar application on soil properties |
|
|
表 2 长期连续玉米秸秆还田和生物质炭施用对稻季土壤N2O总排放量、阶段累积排放量及水稻产量的影响 Table 2 Effcets of long-term continuous maize straw returning and biochar application on seasonal soil N2O emission, periodic cumulative N2O emissions and rice yield in rice season |
施用生物质炭对土壤NH4+-N和NO3–-N的影响呈现不同规律(图 2)。两次追肥后第7天(水稻移栽后第22和56天)土壤NH4+-N含量均随生物质炭施用量增加而增加,但是两次追肥后第30天(水稻移栽后第46和79天)不同处理间没有差异。收获时BC3处理土壤NH4+-N含量显著低于CK处理,并且土壤NH4+-N含量随生物质炭施用量的增加而减少。不同的是,土壤NO3–-N含量在水稻生长季均保持与生物质炭施用量的正相关关系。并且相对于分蘖肥施用后第7天CK和BC3处理的土壤NO3–-N含量,分蘖肥施用后第30天CK和BC3处理土壤NO3–-N含量分别增加77.49% 和164.55%。总体而言,长期连续生物质炭施用有效提高土壤无机氮(NH4+-N和NO3–-N)含量14.18% ~ 92.13%,其中BC2和BC3处理达到显著水平。

|
(实线箭头数量由少到多分别代表基肥、分蘖肥和穗肥的施用时间。水稻移栽后第22天和第46天分别为分蘖肥施用后的第7天和第30天,水稻移栽后第56天和第79天分别为穗肥施用后的第7天和第30天。图中大写字母不同表示同一处理水稻移栽后不同时期差异显著(P < 0.05),小写字母不同表示水稻移栽后同一时期不同处理间差异显著(P < 0.05),下图同) 图 2 水稻生长季土壤NH4+-N和NO3–-N含量随时间变化情况 Fig. 2 Dynamics of soil NH4+-N and NO3–-N concentrations over time during rice growing season |
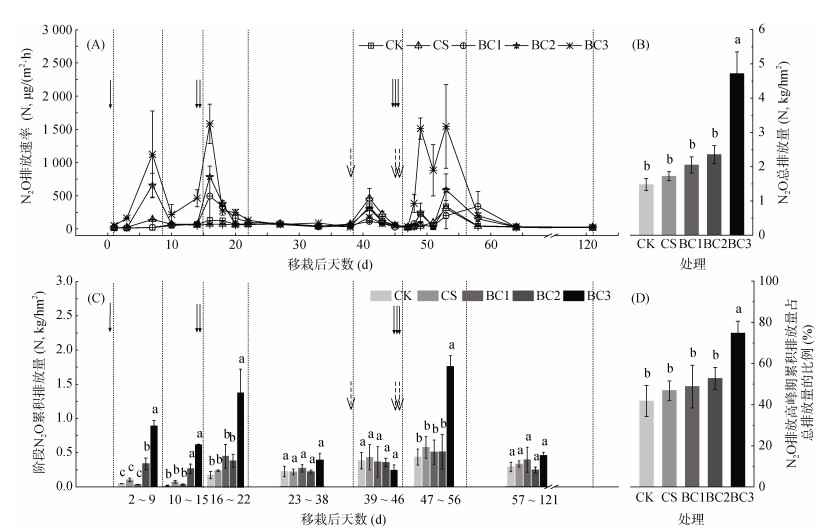
不同处理间N2O排放的动态规律相似,均表现为施肥后较短时间内以及季中排水阶段N2O排放量增多,其他时期排放量较少(图 3A、3C)。长期连续秸秆还田和生物质炭施用有增加土壤N2O累积排放量的趋势,相较于CK,CS处理提高了25.54% 的N2O累积排放量。N2O累积排放量随生物质炭施用量的增加而增加,其中高剂量生物质炭施用(BC3处理)对N2O增排效应尤为明显,相较于CK显著提高245.31%(图 3B)。
|
(水稻生长季土壤N2O排放速率;B. 水稻生长季土壤N2O总排放量;C. 水稻移栽后不同阶段土壤N2O累积排放量;D. 3次施肥后土壤N2O排放高峰期(3次施肥后7 d或10 d内)累积排放量占总排放量的比例。实线箭头数量由少到多分别代表基肥、分蘖肥和穗肥的施用时间,单虚线箭头代表拷田排水开始时间,双虚线箭头代表复水时间) 图 3 长期连续玉米秸秆还田和生物质炭施用对稻季土壤N2O排放的影响 Fig. 3 Effcets of long-term continuous maize straw returning and biochar application on soil N2O emissions in rice season |
水稻生长期N2O排放主要集中在施肥后7 d或10 d内和季中排水阶段。施肥后7 d或10 d内为N2O排放高峰期,由施肥和季中排水引起的N2O累积排放量分别占总排放量的41.72 % ~ 74.73% 和4.52% ~ 24.73%,其中第3次施肥(穗肥)后N2O排放高峰期累积排放量占比最高(图 3C、表 2)。3次施肥后N2O排放高峰期的累积排放量占总排放量的比例随生物质炭施加量的增加而增加,BC3处理这一比例高达80%(图 3D)。在季中排水阶段,施用生物质炭处理土壤N2O排放量低于CK,但是并没有达到显著水平,季中排水阶段N2O累积排放量和生物质炭施用量之间呈负相关关系(图 3C)。
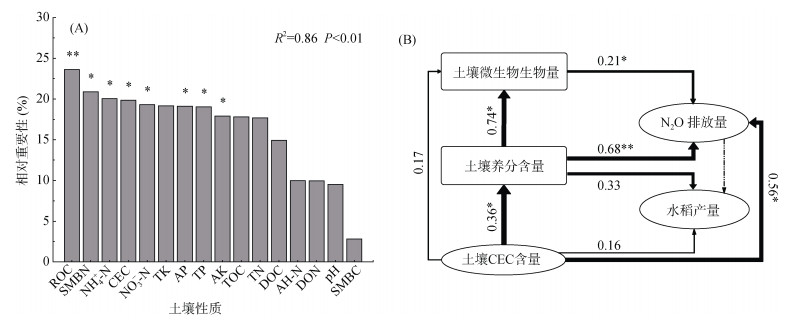
2.3 土壤N2O排放量和水稻产量与土壤性质的关系随机森林模型显示土壤ROC、SMBN、NH4+-N、CEC和NO3–-N含量对土壤N2O排放的影响相较于其他理化性质更为重要(图 4A)。同样PLS-PM分析中土壤N2O排放量也主要受土壤养分含量、土壤微生物生物量以及土壤CEC的影响(图 4B)。土壤养分含量对水稻产量具有正效应,但未达到显著水平;土壤N2O排放量、CEC对水稻产量的影响较小(图 4B)。
|
(A. 最佳随机森林模型评估土壤性质对土壤N2O排放的相对重要性;B. 偏最小二乘路径分析(PLS-PM)研究生物质炭施用处理下土壤性质、N2O排放量和水稻产量之间的关系,方框和椭圆框分别代表潜变量和观测变量。土壤养分含量包括AN、AP、AK、ROC、DOC、DON和无机氮含量;土壤微生物生物量包括SMBN和SMBC。实线和虚线分别表示正效应和负效应。*表示变量或者路径达P < 0.05显著水平,**表示达P < 0.01显著水平) 图 4 土壤N2O排放量和水稻产量与土壤性质之间的关系 Fig. 4 Relationship between soil N2O emissions and rice yield to soil properties |
就短期研究而言,生物质炭对土壤性质如土壤pH、SOC、TN和AN的积极作用已经得到了广泛报道[31-32]。在本研究中,中等和高剂量生物质炭施用(6 t/(hm2·a) 和12 t/(hm2·a))显著提高了土壤AP、AK、AN、NH4+-N和DON等养分含量(图 1、图 2)。这首先是由于生物质炭本身含有比土壤更高的养分含量,如TP、TK、AP和AK含量(表 1);其次生物质炭表面带有的负电荷官能团可以通过增加土壤CEC来持留更多养分。土壤CEC每增加1.00 cmol/kg,可增加0.39 g/kg K+或0.14 g/kg NH4+-N的吸持量。本研究不同剂量生物质炭施用下CEC提高了1.00 ~ 3.53 cmol/kg(图 1),因此0 ~ 15 cm耕层土壤最多可增加684.45 ~ 2416.11 kg/hm2 K+的吸持量,或者245.70 ~ 867.32 kg/hm2 NH4+-N的吸持量。另一方面,施用生物质炭明显提高SMBN和SMBC含量。这可能是由于每年新鲜生物质炭施用为土壤提供了额外的活性碳,土壤微生物活动最为敏感的组分ROC和DOC含量的显著提升为土壤微生物繁殖提供了丰富营养和能量来源(图 1)。同时生物质炭的老化可以增加生物质炭的总孔隙体积,为微生物提供更好的栖息地[33]。因此长期连续施用生物质炭有利于提高土壤养分供应能力,实现土壤微生物数量的增多和群落结构的持续变化。
秸秆直接还田(CS)和经炭化后还田(BC1)对土壤微生物活性、土壤有机质的矿化和温室气体排放的影响均有较大差异。本研究中,相较于CS处理,BC1处理显著提高了32.73% 的土壤TOC含量(图 1)。这是因为秸秆-C主要为活性碳,而生物质炭-C以芳香化的惰性C存在,难以被微生物利用分解(CS处理的SMBN和SMBC含量明显高于秸秆炭化还田处理,图 1)。刘本娟等人[34]将生物质炭和秸秆培养368 d后发现,生物质炭-C和秸秆-C的降解量分别为生物质炭和秸秆含碳量的0.16% ~ 0.25% 和29% ~ 37%。另一方面,秸秆直接添加到土壤中具有较强的正激发效应。Yin等人[35]发现秸秆直接添加到土壤中比经炭化后添加降低了6.61% 的土壤原有有机质含量。稻田淹水环境下秸秆直接还田还将提高CH4排放量,秸秆-C转化为CH4-C转化率约为2.98% ~ 18%[36-37],而生物质炭-C转化为CH4-C转化率仅为0.03%[37]。Liu等人[36]发现6 t/(hm2·a) 秸秆直接还田和等量秸秆炭化还田的土壤C累积速率分别为0.5 t/(hm2·a) 和1.4 t/(hm2·a)。因此土壤中添加生物质炭是增加土壤碳库的有效手段。另一方面,两种不同秸秆还田方式下秸秆/生物质炭的矿质养分的含量及其有效性也不尽相同。相较于CS处理,BC1处理提高了土壤TP和TK含量(图 1)。秸秆中的磷主要以有机磷形式存在,炭化后秸秆中的有机磷转化为无机磷,部分与Al、Fe、Ca和Mg结合成为难溶解的Al-P、Fe-P、Ca-P和Mg-P[38-39]。同时炭化过程中秸秆中可溶性钾部分转化为复杂结构和石墨化结构钾保留在生物质炭中并难以被淋溶损失[40]。
提高作物产量被认为是秸秆以及生物质炭应用于农业生产中的最大益处。但是我们发现长期连续秸秆还田和生物质炭施用并没有显著提高水稻产量(表 2)。PLS-PM模型显示土壤养分含量对水稻产量不具有显著影响(图 4B),这可能是由于本研究供试土壤本身肥力较高限制了产量的进一步提高。El-Naggar等人[41]认为生物质炭施用于持水能力较低或者肥力下降的土壤中可以实现作物增产。在具有良好耕作条件、土壤养分供应能力较强的土壤中应用则可能无法实现增产[9]。Liu等人[19]在6a的田间试验中同样发现在具有良好培育条件的农田中施用生物质炭对水稻产量没有影响,但是可以通过提高土壤持水能力提高小麦产量。
3.2 长期连续玉米秸秆还田和生物质炭施用对N2O排放的影响结果表明长期连续秸秆还田和中等和低剂量(2.4 t/(hm2·a) 和6 t/(hm2·a))生物质炭连续施用11a,对水稻生长季N2O累积排放量的影响不大,然而高剂量生物质炭施用(12 t/(hm2·a))显著增加了245.31% 的N2O累积排放量(图 3B、表3)。相较于CK,BC3处理的N2O总排放量和施氮肥后N2O排放高峰期的累积排放量分别提高了3.84 kg/hm2和3.36 kg/hm2(以N2O-N计),同时BC3处理在3次施肥后N2O排放高峰期的累积排放量占总排放量的比例高达80%(图 3B ~ 3D)。显而易见,高剂量生物质炭施用下N2O排放量的增加主要体现在施肥后的排放高峰期内。这与该时期内土壤无机氮底物变化驱动的土壤硝化和反硝化过程产生N2O以及微生物在土壤N素循环过程中的催化作用相关[42]。
水稻生长季中,施肥后耕层土壤NH4+-N含量快速增加,施加生物质炭引起土壤CEC的增加使土壤可以吸持更多的NH4+[43](图 2)。水稻生长期分蘖肥施用后第7天施加生物质炭处理显著提高土壤NH4+-N含量,但是第30天各处理间无显著差异。同时相较于分蘖肥施用后第7天不同处理的土壤NO3–-N含量,分蘖肥施用后第30天各处理土壤NO3–-N含量均有所增加,但是BC3处理的增加幅度显著高于其他处理(图 2)。因此高剂量生物质炭的施用引起的高NH4+-N持留促进了土壤硝化作用。季中排水期间(水稻移栽后38 ~ 46 d)耕层土壤水分含量逐步降低,土壤硝化作用占主导,NH4+-N继续向NO3–-N转化。同时,施加生物质炭改善土壤通气性,抑制反硝化产生N2O[44],因此季中排水阶段生物质炭施用处理下N2O排放量低于CK(图 3A、3C)。季中排水结束后,BC3处理更高的土壤NO3–-N含量(第46天BC3处理的土壤NO3–-N含量在水稻生长季中居于最高水平,图 2)和反硝化酶活性促进了土壤反硝化过程产生N2O(图 5)。与此同时,穗肥的施用再次为土壤硝化过程提供充足底物,BC3处理高NH4+持留的特性促进硝化过程产生更多的N2O(图 3A)。因此穗肥施用后的N2O排放高峰期BC3处理累积排放量的显著增多主要由土壤NH4+-N和NO3–-N含量的大幅增加促进了土壤硝化和反硝化过程产生N2O。在随后的土壤干湿交替阶段,土壤以硝化作用为主导,但由于土壤NH4+-N含量较低,各处理N2O排放速率均居于较低水平,处理间没有显著差异(图 3A)。因此,高剂量生物质炭连续施用显著提高了土壤N2O排放量的主要原因是土壤CEC的显著增加带来的高NH4+持留促进了施肥后N2O排放高峰期土壤硝化过程产生N2O(图 4B)。
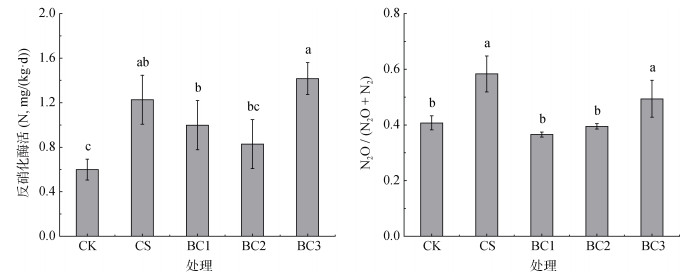
|
图 5 不同处理下的反硝化酶活性和N2O产生速率 Fig. 5 Denitrifying enzyme activities and N2O production rates under different treatments |
土壤微生物的催化参与产生N2O的所有生物过程,包括自养或异养硝化以及反硝化作用。在较低的pH和比较高的含水率环境下土壤异养硝化作用也是产生N2O的主要途径[10]。CS处理相较于CK较高的N2O排放量可能由于秸秆分解产生了更多的DOC和ROC,以及较高的SMBC和SMBN(图 1)刺激土壤异养呼吸和相关异养硝化细菌的活性[45],进而促进了土壤N2O的排放。相较于其他时期,季中排水结束前BC3处理土壤NO3–-N含量的大幅提升(图 2),以及高剂量生物质炭施用下土壤反硝化酶活性和N2O产生速率的显著提高促进了土壤反硝化过程产生N2O(图 5),这可能是由于生物质炭的老化伴随有表面官能团与金属离子的结合,导致在反硝化过程中竞争电子的能力减弱,进而对完全反硝化的促进作用减小[18-19]。老化生物质炭更大的羟基和羧基官能团密度和更丰富的孔隙结构允许更多的营养物质在生物质炭表面保留下来[18],同时每年新鲜生物质炭施用向土壤带入大量活性养分(表 1),促进了土壤微生物量的增多和活性的增强(图 1),进一步催化了产生N2O的相关生物过程。总而言之,高剂量生物质炭施用下土壤CEC的显著增加提升了对NH4+-N的持留,促进土壤硝化过程产生N2O,同时丰富的土壤养分供应和友好的微生物生长环境下微生物数量和活性的增加提高了土壤N循环速率并刺激了N2O排放的相关生物过程。
4 结论在稻麦轮作条件下,麦季长期连续中等和高剂量生物质炭施用(6 t/(hm2·a) 和12 t/(hm2·a))提高了稻田土壤养分供应能力,显著增加了AP、AK、AN、TOC、ROC、DON和SMBN含量。相对于秸秆直接还田,等量秸秆炭化还田分别显著提高6.42% 和32.73% 的土壤TK和TOC含量。另一方面,施用高剂量生物质炭显著提高了水稻季N2O累积排放量(245.31%),这主要是由于高剂量生物质炭施用处理比对照提高了20.35% 的土壤CEC,在氮肥施入后持留了更多的NH4+,进而促进了土壤硝化过程产生N2O,同时更友好的微生物生长条件(丰富的养分供应和良好的栖息环境)提高了土壤微生物的数量和活性,加速了土壤N循环速率。
致谢: 本研究的大田试验得到了江都FACE实验站徐美云的帮助,在此表示衷心感谢。
| [1] |
Yin H J, Zhao W Q, Li T, et al. Balancing straw returning and chemical fertilizers in China: Role of straw nutrient resources[J]. Renewable and Sustainable Energy Reviews, 2018, 81: 2695-2702 DOI:10.1016/j.rser.2017.06.076 (  0) 0) |
| [2] |
Ren J Q, Yu P X, Xu X H. Straw utilization in china— Status and recommendations[J]. Sustainability, 2019, 11(6): 1762 DOI:10.3390/su11061762 (  0) 0) |
| [3] |
Xie Z B, Liu G, Bei Q C, et al. CO2 mitigation potential in farmland of China by altering current organic matter amendment pattern[J]. Science China Earth Sciences, 2010, 53(9): 1351-1357 DOI:10.1007/s11430-010-4014-z (  0) 0) |
| [4] |
李露, 周自强, 潘晓健, 等. 不同时期施用生物炭对稻田N2O和CH4排放的影响[J]. 土壤学报, 2015, 52(4): 839-848 (  0) 0) |
| [5] |
Alexander L, Allen S, Bindoff N, et al. Climate change 2013: The physical science basis, in contribution of Working Group Ⅰ (WGI) to the Fifth Assessment Report (AR5) of the Intergovernmental Panel on Climate Change (IPCC)[M]//Climate Change 2013: The physical Science Basis. 2013.
(  0) 0) |
| [6] |
Li Z J, Reichel R, Xu Z F, et al. Return of crop residues to arable land stimulates N2O emission but mitigates NO3− leaching: A meta-analysis[J]. Agronomy for Sustainable Development, 2021, 41(5): 66 DOI:10.1007/s13593-021-00715-x (  0) 0) |
| [7] |
王保君, 胡乃娟, 顾泽海, 等. 稻秆还田方式对稻麦轮作农田CH4和N2O排放的影响[J]. 南京农业大学学报, 2017, 40(3): 367-375 (  0) 0) |
| [8] |
Sarfraz R, Hussain A, Sabir A, et al. Role of biochar and plant growth promoting rhizobacteria to enhance soil carbon sequestration—A review[J]. Environmental Monitoring and Assessment, 2019, 191(4): 251 DOI:10.1007/s10661-019-7400-9 (  0) 0) |
| [9] |
Hussain M, Farooq M, Nawaz A, et al. Biochar for crop production: Potential benefits and risks[J]. Journal of Soils and Sediments, 2017, 17(3): 685-716 DOI:10.1007/s11368-016-1360-2 (  0) 0) |
| [10] |
Li W, Xie H X, Ren Z H, et al. Response of N2O emissions to N fertilizer reduction combined with biochar application in a rain-fed winter wheat ecosystem[J]. Agriculture, Ecosystems & Environment, 2022, 333: 107968 (  0) 0) |
| [11] |
Case S D C, McNamara N P, Reay D S, et al. The effect of biochar addition on N2O and CO2 emissions from a sandy loam soil - The role of soil aeration[J]. Soil Biology and Biochemistry, 2012, 51: 125-134 DOI:10.1016/j.soilbio.2012.03.017 (  0) 0) |
| [12] |
Liu Q, Zhang Y H, Liu B J, et al. How does biochar influence soil N cycle? A meta-analysis[J]. Plant and Soil, 2018, 426(1): 211-225 (  0) 0) |
| [13] |
Zhang L Y, Jing Y M, Chen C R, et al. Effects of biochar application on soil nitrogen transformation, microbial functional genes, enzyme activity, and plant nitrogen uptake: A meta-analysis of field studies[J]. GCB Bioenergy, 2021, 13(12): 1859-1873 DOI:10.1111/gcbb.12898 (  0) 0) |
| [14] |
Su X X, Wang Y Y, He Q, et al. Biochar remediates denitrification process and N2O emission in pesticide chlorothalonil-polluted soil: Role of electron transport chain[J]. Chemical Engineering Journal, 2019, 370: 587-594 DOI:10.1016/j.cej.2019.03.195 (  0) 0) |
| [15] |
Joseph S, Cowie A L, Van Zwieten L, et al. How biochar works, and when it doesn't: A review of mechanisms controlling soil and plant responses to biochar[J]. GCB Bioenergy, 2021, 13(11): 1731-1764 DOI:10.1111/gcbb.12885 (  0) 0) |
| [16] |
Spokas K A, Novak J M, Venterea R T. Biochar's role as an alternative N-fertilizer: Ammonia capture[J]. Plant and Soil, 2012, 350(1): 35-42 (  0) 0) |
| [17] |
Lorenz K, Lal R. Biochar application to soil for climate change mitigation by soil organic carbon sequestration[J]. Journal of Plant Nutrition and Soil Science, 2014, 177(5): 651-670 DOI:10.1002/jpln.201400058 (  0) 0) |
| [18] |
Duan P P, Zhang X, Zhang Q Q, et al. Field-aged biochar stimulated N2O production from greenhouse vegetable production soils by nitrification and denitrification[J]. Science of the Total Environment, 2018, 642: 1303-1310 DOI:10.1016/j.scitotenv.2018.06.166 (  0) 0) |
| [19] |
Liu X Y, Zhou J S, Chi Z Z, et al. Biochar provided limited benefits for rice yield and greenhouse gas mitigation six years following an amendment in a fertile rice paddy[J]. CATENA, 2019, 179: 20-28 DOI:10.1016/j.catena.2019.03.033 (  0) 0) |
| [20] |
Song X Z, Pan G X, Zhang C, et al. Effects of biochar application on fluxes of three biogenic greenhouse gases: A meta-analysis[J]. Ecosystem Health and Sustainability, 2016, 2(2): e01202 DOI:10.1002/ehs2.1202 (  0) 0) |
| [21] |
Huang M, Fan L, Chen J N, et al. Continuous applications of biochar to rice: Effects on nitrogen uptake and utilization[J]. Scientific Reports, 2018, 8: 11461 DOI:10.1038/s41598-018-29877-7 (  0) 0) |
| [22] |
Dong Y B, Wu Z, Zhang X, et al. Dynamic responses of ammonia volatilization to different rates of fresh and field-aged biochar in a rice-wheat rotation system[J]. Field Crops Research, 2019, 241: 107568 DOI:10.1016/j.fcr.2019.107568 (  0) 0) |
| [23] |
Feng Y Y, Feng Y F, Liu Q, et al. How does biochar aging affect NH3 volatilization and GHGs emissions from agricultural soils?[J]. Environmental Pollution, 2022, 294: 118598 DOI:10.1016/j.envpol.2021.118598 (  0) 0) |
| [24] |
谢祖彬, 卑其成, 刘刚, 等. 一种秸秆制炭装置: CN200920232191.9[P]. 2010–06–16.
(  0) 0) |
| [25] |
Qi L, Pokharel P, Ni C S, et al. Biochar changes thermal activation of greenhouse gas emissions in a rice-lettuce rotation microcosm experiment[J]. Journal of Cleaner Production, 2020, 247: 119148 DOI:10.1016/j.jclepro.2019.119148 (  0) 0) |
| [26] |
Smith M S, Tiedje J M. Phases of denitrification following oxygen depletion in soil[J]. Soil Biology and Biochemistry, 1979, 11(3): 261-267 DOI:10.1016/0038-0717(79)90071-3 (  0) 0) |
| [27] |
中国林业科学研究院林业研究所. 森林土壤阳离子交换量的测定: LY/T 1243—1999[S]. 北京: 中国标准出版社, 1999.
(  0) 0) |
| [28] |
Liaw A, Wiener M. Classification and regression by randomForest[J]. R News, 2002, 2(3): 18-22 (  0) 0) |
| [29] |
Archer E. rfPermute: Estimate permutation p-values for random forest importance metrics[Z]. https://github.com/EricArcher/rfPermute.
(  0) 0) |
| [30] |
Bertrand F, Sanchez G, Trinchera L, et al. plspm: Tools for Partial Least Squares Path Modeling (PLS-PM)[Z]. https://cran.r-project.org/web/packages/plspm/index.html.
(  0) 0) |
| [31] |
Murtaza G, Ahmed Z, Usman M, et al. Biochar induced modifications in soil properties and its impacts on crop growth and production[J]. Journal of Plant Nutrition, 2021, 44(11): 1677-1691 (  0) 0) |
| [32] |
Ali S, Rizwan M, Qayyum M F, et al. Biochar soil amendment on alleviation of drought and salt stress in plants: A critical review[J]. Environmental Science and Pollution Research, 2017, 24(14): 12700-12712 DOI:10.1007/s11356-017-8904-x (  0) 0) |
| [33] |
Lehmann J, Rillig M C, Thies J, et al. Biochar effects on soil biota - A review[J]. Soil Biology and Biochemistry, 2011, 43(9): 1812-1836 DOI:10.1016/j.soilbio.2011.04.022 (  0) 0) |
| [34] |
刘本娟, 谢祖彬, 刘琦, 等. 生物质炭引起的土壤碳激发效应与土壤理化特性的相关性[J]. 土壤, 2021, 53(2): 343-353 (  0) 0) |
| [35] |
Yin Y F, He X H, Gao R, et al. Effects of rice straw and its biochar addition on soil labile carbon and soil organic carbon[J]. Journal of Integrative Agriculture, 2014, 13(3): 491-498 DOI:10.1016/S2095-3119(13)60704-2 (  0) 0) |
| [36] |
Liu Q, Liu B J, Ambus P, et al. Carbon footprint of rice production under biochar amendment - a case study in a Chinese rice cropping system[J]. GCB Bioenergy, 2016, 8(1): 148-159 DOI:10.1111/gcbb.12248 (  0) 0) |
| [37] |
Knoblauch C, Maarifat A A, Pfeiffer E M, et al. Degradability of black carbon and its impact on trace gas fluxes and carbon turnover in paddy soils[J]. Soil Biology and Biochemistry, 2011, 43(9): 1768-1778 DOI:10.1016/j.soilbio.2010.07.012 (  0) 0) |
| [38] |
Dai L C, Li H, Tan F R, et al. Biochar: A potential route for recycling of phosphorus in agricultural residues[J]. GCB Bioenergy, 2016, 8(5): 852-858 DOI:10.1111/gcbb.12365 (  0) 0) |
| [39] |
Wang Y, Lin Y X, Chiu P C, et al. Phosphorus release behaviors of poultry litter biochar as a soil amendment[J]. Science of the Total Environment, 2015, 512/513: 454-463 DOI:10.1016/j.scitotenv.2015.01.093 (  0) 0) |
| [40] |
Tan Z X, Liu L Y, Zhang L M, et al. Mechanistic study of the influence of pyrolysis conditions on potassium speciation in biochar "preparation-application" process[J]. Science of the Total Environment, 2017, 599/600: 207-216 DOI:10.1016/j.scitotenv.2017.04.235 (  0) 0) |
| [41] |
El-Naggar A, Lee S S, Rinklebe J, et al. Biochar application to low fertility soils: A review of current status, and future prospects[J]. Geoderma, 2019, 337: 536-554 DOI:10.1016/j.geoderma.2018.09.034 (  0) 0) |
| [42] |
Xu C, Han X, Ru S H, et al. Crop straw incorporation interacts with N fertilizer on N2O emissions in an intensively cropped farmland[J]. Geoderma, 2019, 341: 129-137 DOI:10.1016/j.geoderma.2019.01.014 (  0) 0) |
| [43] |
Atkinson C J, Fitzgerald J D, Hipps N A. Potential mechanisms for achieving agricultural benefits from biochar application to temperate soils: A review[J]. Plant and Soil, 2010, 337(1): 1-18 (  0) 0) |
| [44] |
Pan F X, Chapman S J, Li Y Y, et al. Straw amendment to paddy soil stimulates denitrification but biochar amendment promotes anaerobic ammonia oxidation[J]. Journal of Soils and Sediments, 2017, 17(10): 2428-2437 DOI:10.1007/s11368-017-1694-4 (  0) 0) |
| [45] |
Liu J Y, Shen J L, Li Y, et al. Effects of biochar amendment on the net greenhouse gas emission and greenhouse gas intensity in a Chinese double rice cropping system[J]. European Journal of Soil Biology, 2014, 65: 30-39 DOI:10.1016/j.ejsobi.2014.09.001 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. College of Forestry, Nanjing Forestry University, Nanjing 210037, China;
4. College of Environmental Science and Engeneering, Yangzhou University, Yangzhou, Jiangsu 225009, China
 2023, Vol. 55
2023, Vol. 55


