2. 江苏省农业气象重点实验室, 南京 210044
随着农药、垃圾及工业废弃物等不断进入土壤,土壤重金属污染日益加剧[1-2]。《全国土壤污染状况调查公报》[3]显示,我国土壤总的点位超标率为16.1%,其中镉(Cd)的点位超标率高达7%。土壤Cd污染已对我国水稻生产带来巨大压力[4-5]。据研究,土壤Cd污染影响水稻的光合特性进而抑制水稻的生长发育[6]。土壤Cd污染降低了水稻叶片净光合速率(Pn)、气孔导度(Gs)、蒸腾速率(Tr)和胞间CO2浓度(Ci)等光合参数,并使水稻叶片的光系统Ⅱ(PSⅡ)反应中心受到伤害,从而导致水稻的根长、苗高及生物量降低[7]。Cd对水稻光合特性的影响与Cd浓度密切相关。李陈贞等[6]研究表明,随着Cd浓度的增加,水稻光合作用PSⅡ的初始荧光参数(F0) 逐渐增加,而潜在最大光化学效率(Fv/Fm)、实际量子产量(ΦPSⅡ)和表观电子传递速率(ETR)逐渐降低。
近年来,全球气候变暖一直是人们首要关注的气候问题之一。IPCC第六次评估报告显示,2011—2020年全球地表温度比1850—1900年高1.09 ℃[8]。全球气候变暖已经严重影响了水稻生长发育乃至产量。余欣等[9]研究表明,高温处理显著降低了水稻叶绿素、Pn、Gs、Ci和Tr等光合参数。在水稻不同的生长期中,抽穗期的光合特性对高温更加敏感,高温抑制了抽穗期水稻的光合作用,导致水稻干物质积累和产量下降[10-11]。高温也会影响水稻的光合系统,水稻遭受高温胁迫后,剑叶的PSⅡ、Fv/Fm和ΦPSⅡ均下降,使叶片的光能剩余[12]。杜尧东等[13]研究指出,高温处理后水稻的ETR、Fv/Fm、ΦPSⅡ、光化学猝灭系数(qP) 和PSⅡ光化学反应下降,且高温对叶绿素荧光的影响与水稻的生长期密切相关。
通过以上研究可知,土壤Cd污染和温度变化影响了水稻光合特性及其生长发育。随着气候变暖,Cd污染稻田的水稻生长发育往往受Cd污染和温度双重因素的影响,但目前的研究大多集中于单一因素,因此迫切需要了解两者的复合作用对水稻生长发育的影响及其机理。基于此,本研究通过添加外源Cd,分析不同温度处理下抽穗期水稻光合参数、荧光参数的差异,并结合快速叶绿素荧光动力学曲线分析探究外源Cd和温度变化复合作用对水稻抽穗期光合特性及其生长的影响和机理,以期为气候变化下Cd污染稻田水稻的高产稳产栽培及安全生产提供理论依据。
1 材料与方法 1.1 试验材料本试验在南京信息工程大学农业气象试验站进行。前期试验比较了不同浓度Cd处理对不同品种水稻生长的影响,发现武运粳30号和新两优6号的耐Cd能力差异较大,为便于比较不同品种水稻的差异,本研究选择这两个品种作为研究对象。采集南京信息工程大学农业气象试验站表层土(0 ~ 20 cm)作为供试土壤,土壤风干,挑拣出杂质,砸碎,然后过5 mm塑料筛后混匀备用。供试土壤pH 7.6,有机质10.12 g/kg,全氮1.26 g/kg,有效磷18.92 mg/kg,速效钾112 mg/kg,总Cd 0.8 mg/kg。
1.2 试验设计试验设置3个变温处理(夜晚温度比白天低5 ℃),分别为:30 ℃/25 ℃(CK)、33 ℃/28 ℃(T1)和36 ℃/31 ℃(T2);2个Cd处理:不添加外源Cd(Cd0)和添加2 mg/kg的外源Cd(Cd2)。每个处理3个重复。
称取2 kg土壤,按照设置的Cd处理添加CdCl2溶液,混匀后,于聚氯乙烯(PVC)盆中(盆高15.5 cm,上直径16.2 cm,下直径13.4 cm)放置一个月。然后向每盆中加入尿素、磷酸二氢钾和氯化钾作为基肥。供试种子用质量比为30% 的双氧水浸泡消毒15 min,然后用去离子水冲洗干净,并放在30 ℃的培养箱中过夜,次日移至吸水纸上,并不断补充水分使其保持湿润。当种子发芽5 d后,在每盆土壤中移栽7棵生长状况较好、长势大致相同的幼苗,成活后保留长势一致的5棵苗,然后分别放入不同温度设置的人工气候箱(RXZ-1000C-CO2,宁波江南仪器厂;光照12 h/黑暗12 h,光照强度为6 000 lx,相对湿度70%)中进行培养。
1.3 抽穗期水稻光合参数的测定在水稻的抽穗期,使用光合仪(Li-6400XT,美国LI-COR公司)测定水稻叶片的净光合速率(Pn)、气孔导度(Gs)、胞间CO2浓度(Ci)和蒸腾速率(Tr)4个光合参数。使用手持便携式SPAD仪(SPAD-502PLUS,日本)测定水稻主茎倒数第二功能叶的叶绿素相对含量(SPAD值),每盆选取3片稻叶,且每片稻叶测定3次,取平均值作为该处理的SPAD值。
在水稻抽穗期,每盆选取长势大致相同的3株主茎剑叶,暗适应20 min后,使用植物效率分析仪(Pocket PEA,英国Hansatech公司)测定水稻的荧光动力学曲线(OJIP曲线)和初始荧光(F0)、可变荧光(Fv)和最大荧光(Fm)等叶绿素荧光参数,记录时间为1 s,每盆测定3次。对OJIP曲线进行JIP-test分析,得到4个比活度参数,即单位反应中心吸收的光能(ABS/RC)、单位反应中心热耗散的能量(DIO/RC)、单位反应中心捕获的用于还原QA的能量(TRO/RC)和单位反应中心用于电子传递的能量(ETO/RC),具体计算参照李岩宸等[14]的研究
1.4 数据处理试验数据用Microsoft Excel 2010进行基本处理,计算各处理的平均值和标准差。使用SPSS 19.0软件进行不同Cd浓度、不同温度及不同品种间的单因素方差分析(one-way AVOVA)和双因素方差分析(two-way AVOVA),并进行多重(Duncan)比较(P < 0.05);使用Microsoft Excel 2010绘制光合指标和荧光参数有关的图表。
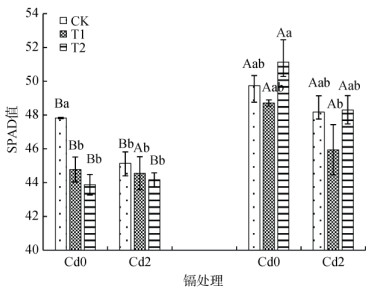
2 结果与分析 2.1 温度和Cd处理对水稻SPAD值的影响温度和Cd的复合作用未显著影响武运粳30号和新两优6号的SPAD值(图 1和表 1)。外源Cd显著降低了新两优6号的SPAD值(P < 0.05)。除T2外,外源Cd也降低了武运粳30号的SPAD值。在CK、T1和T2温度处理下,Cd2处理分别使新两优6号的SPAD值降低了4.74%、5.02% 和6.46%。增温处理显著降低了武运粳30的SPAD值,但未显著影响新两优6号的SPAD值。在Cd0处理下,与CK相比,T1和T2处理分别使武运粳30号的SPAD值显著降低6.37% 和8.25%。比较武运粳30号和新两优6号可知,除T1-Cd2处理外,新两优6号的SPAD值都显著大于武运粳30号。
|
(图中小写字母不同表示同一水稻品种不同Cd和温度处理间差异显著(P < 0.05),大写字母不同表示同一Cd和温度处理不同水稻品种间差异显著(P < 0.05,下同) 图 1 不同温度和Cd处理对不同品种水稻SPAD值的影响 Fig. 1 SPADs of different rice varieties under different temperatures and Cd concentrations |
|
|
表 1 Cd和温度影响下水稻光合参数的方差分析 Table 1 Two-way ANOVA of rice photosynthetic indexes under different Cd concentrations and temperatures |
温度和Cd的复合作用未显著影响武运粳30号和新两优6号的Pn,但显著影响了新两优6号的Gs和Tr(图 2和表 1)。与CK-Cd0处理相比,T2-Cd2复合处理使新两优6号的Gs和Tr分别显著降低了15.73% 和20.18%(P < 0.05)。外源Cd显著降低了武运粳30号和新两优6号的Pn(图 2和表 1),同时外源Cd也显著影响了新两优6号的Ci、Gs和Tr。增温处理显著影响新两优6号的Pn,但未显著影响武运粳30号的Pn。同时增温处理也显著影响武运粳30号和新两优6号的Gs和Tr(表 1)。在相同的Cd处理下,增温增加了武运粳30号和新两优6号的Tr,并增加了武运粳30号的Gs(图 2)。比较武运粳30号和新两优6号发现,新两优6号的Pn大于武运粳30号,在CK-Cd0和T1-Cd0处理下达到显著水平。新两优6号的其他光合参数在大部分处理下都大于武运粳30号。

|
图 2 不同温度和Cd处理对不同品种水稻光合指标的影响 Fig. 2 Rice photosynthetic indexes under different temperatures and Cd concentrations |
叶绿素荧光分析广泛应用于研究各种非生物胁迫,当植物遇到不同的逆境胁迫后,荧光动力学标准曲线(OJIP)会表现出不同的变化,其中O、L、K、J、I相分别对应0.05、0.1、0.3、2、30 ms时的荧光,P相是最大荧光。
图 3为水稻叶绿素标准化荧光动力学曲线图,为更清晰地比较不同处理间的荧光差异,以CK-Cd0为对照,用其他处理的标准化荧光与对照的差值重新作图,结果见图 4。由图 3和图 4可知,在温度和Cd的复合作用下,武运粳30号和新两优6号的OJIP曲线的变化趋势与规律大致相同。外源Cd的添加使武运粳30号出现了K点。除CK-Cd2外,新两优6号也出现了K点。

|
(A为武运粳30号,B为新两优6号;O、L、K、J、I相分别对应0.05、0.1、0.3、2、30 ms时的荧光,P相是最大荧光;下图同) 图 3 水稻叶绿素标准化荧光动力学曲线 Fig. 3 Kinetics curves of Chlorophyll fluorescence of rice after standardization |
|
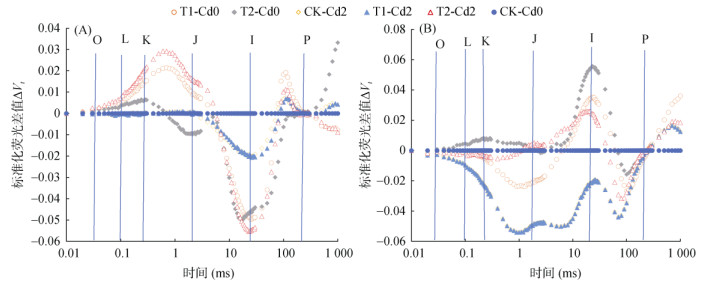
图 4 水稻叶绿素标准化荧光差值 Fig. 4 Differences of standardized chlorophyll fluorescence in rice |
外源Cd和增温单一处理对水稻的OJIP形状产生影响。对于武运粳30号,外源Cd使T1温度下O点到J点的荧光下降,而使T2温度下O点到J点的荧光升高;并且外源Cd使T2温度下K点的荧光上升,I点的荧光降低。而对于新两优6号,外源Cd使O点到J点的荧光降低,K点和I点的荧光也降低。对于武运粳30号,除T2-Cd0外,增温处理使O点到J点的荧光增加,I点荧光减少,并且增温使ΔK>0。而对于新两优6号,除T2-Cd2外,增温使O点到J点的荧光减少,ΔK < 0;除T1-Cd2外,增温处理下,I点荧光增加。
2.4 温度和Cd处理对水稻荧光参数和反应中心比活性参数的影响Fv/Fm值的大小通常可以表示植物受外界胁迫的程度。由表 2可知,外源Cd和温度的复合作用未显著影响武运粳30号和新两优6号的Fv/Fm。增温处理显著减小了武运粳30号的Fv/Fm值,但未显著影响新两优6号的Fv/Fm值。外源Cd处理未显著影响武运粳30号和新两优6号的Fv/Fm值。除CK-Cd0和T1-Cd0处理外,新两优6号的Fv/Fm值大于武运粳30号。
|
|
表 2 不同温度和Cd处理对不同品种水稻荧光参数和反应中心比活性参数的影响 Table 2 Fluorescence parameters of different rice varieties under different temperatures and Cd concentrations |
温度和Cd的复合作用未显著影响武运粳30号和新两优6号的比活性参数ABS/RC、TRo/RC、ET0/RC和DIo/RC。Cd处理显著降低了新两优6号的比活度参数(P < 0.05),但未显著影响武运粳30号的比活度参数。增温处理显著增加了武运粳30号的比活度参数,并未显著影响新两优6号的比活度参数。比较不同品种间比活性参数得知,武运粳30号在Cd2-T2处理下的ABS/RC、DIo/RC、TRo/RC和ETo/RC均显著大于新两优6号。
2.5 温度和Cd处理对水稻生物量的影响温度和Cd的复合作用显著降低了新两优6号根生物量(P < 0.05),但未显著影响武运粳30号的根生物量和两品种的茎叶生物量。与CK-Cd0相比,T1-Cd2和T2-Cd2处理使新两优6号的根生物量分别显著减少了54.38% 和51.25%(表 3)。在相同温度下,Cd2处理显著降低了新两优6号的茎叶和根生物量。在相同Cd处理下,增温显著减少了武运粳30号茎叶生物量和新两优6号的根生物量。比较武运粳30号和新两优6号得知,大部分处理的新两优6号的茎叶和根生物量大于武运粳30号,其中,CK-Cd0、T1-Cd0、T2-Cd0处理下的茎叶生物量及T2-Cd0处理下的根生物量都达到显著水平(P < 0.05)。
|
|
表 3 不同温度和Cd处理对武运粳30号和新两优6号各部位生物量的影响 Table 3 Biomass of Wuyungeng 30 and Xinliangyou 6 under different temperatures and Cd concentrations |
光合作用是植物生长发育的重要生理过程,受高温、重金属胁迫等环境因子的影响。本研究结果表明,外源Cd显著降低了武运粳30号和新两优6号的Pn,这主要与外源Cd对两个品种SPAD、Ci、Gs和Tr的影响有关。据研究,SPAD是影响水稻Pn的重要因素,Pn与SPAD值呈正相关关系[15]。Cd处理降低武运粳30号和新两优6号的SPAD值是两品种Pn降低的原因之一(图 1)。胁迫条件对光合作用的限制因素主要分为气孔限制和非气孔限制[13, 16]。气孔限制因素认为,在胁迫条件下,若植物叶片Gs和 Ci 降低引起Pn的下降,则说明了植物的光合作用受到气孔限制;当Ci 和Gs升高,而Pn下降,则说明植物的光合作用受到非气孔限制[17]。本研究中,外源Cd增加了除T1外的武运粳30号的Ci及除T2外的Gs,而降低了新两优6号的Ci 和Gs(图 2)。外源Cd可能使武运粳30号的光合器官受到损伤,叶绿素合成酶活性降低,光合作用受到抑制,从而降低净光合速率而Cd处理可能抑制新两优6号水稻叶片气孔的打开,光合作用所需的CO2供应不足,从而抑制了水稻的光合作用[6, 18]。这表明Cd胁迫主要通过非气孔因素限制武运粳30号的光合作用,而通过气孔因素限制新两优6号的光合作用。
OJIP曲线对光、热、寒冷、干旱、重金属或盐胁迫等各种环境的改变非常敏感,受到的环境胁迫不同,植物的OJIP曲线的变化趋势也不同。通过OJIP的变化轨迹,可以更好地了解PSⅡ的原始光化学反应及光合机构电子传递状态等过程[19]。在本研究中,增温均影响了两种水稻叶片的荧光动力学曲线的走向,这与前人研究[20]结论一致。增温条件下,除T2-Cd0处理外,武运粳30号的OJIP荧光诱导曲线的O点至J点荧光强度增加,这与部分反应中心因为QA的减少而关闭有关[19]。而新两优6号的OJIP曲线O点至J点荧光强度减少,这则说明水稻PSⅡ反应中心的闭合需要更多的时间,其次是次级电子的捕获和缓慢还原[21],那么荧光强度到达Fm所需的时间也就更长。Cd胁迫也对光合过程的光化学效率有负面影响。Cd能同时影响PSⅡ的供体侧和受体侧。在供体侧,它抑制放氧复合体OEC,而在受体侧,抑制了质体醌QA和泛醌QB之间的电子传递[22]。有研究表明,如果OJIP曲线中的J相荧光上升,并且出现拐点K(300 μs),则说明PSⅡ受体侧的QA到QB的电子传递受阻,PSⅡ供体侧的OEC发生了解离[14]。本研究表明,Cd处理使T2温度下武运粳30号叶片的ΔK和ΔJ略大于0,这说明Cd既损伤了PSⅡ供体侧OEC,也影响了受体侧的电子传递,但ΔI小于0,说明了PSⅡ受损后逐渐恢复;而新两优6号的ΔK和ΔJ小于0,说明水稻叶片的PSⅡ供体侧的放氧复合体未受影响, 而QA与QB之间的电子传递受到轻度抑制[23]。本研究中,不同品种的水稻受到的损伤程度不同,所对应的适应机制也不同。武运粳30号的PSⅡ反应中心受损程度大,其主要通过耗散剩下的激发能减轻伤害,而新两优6号受到的胁迫较小,叶片的PSⅡ反应中心部分发生可逆性失活,启动了自我保护机制,形成能量陷阱,PSⅡ反应中心吸收了光能但不传递电子,当环境胁迫减缓或解除后,已失活的反应中心又能恢复活性[23-24]。
当受到胁迫时,Fv/Fm显著下降,PSⅡ反应中心失活,所以常用Fv/Fm值的变化来判断植物是否受到抑制[25-26]。本研究中,增温显著降低了武运粳30号的Fv/Fm,但未显著影响新两优6号的Fv/Fm。这个结果表明,武运粳30号和新两优6号对温度具有不同的耐受能力,新两优6号对增温具有较强的耐受能力,但武运粳30号对增温的耐受能力较差。Cd处理下武运粳30号的SPAD值下降幅度比新两优6号小,而温度处理下武运粳30号的SPAD值下降幅度比新两优6号大,可以进一步解释武运粳30号和新两优6号对温度和Cd耐受能力的差异。通过分析比活性参数,能够更清楚地了解植物对光能的吸收、转化和耗散等情况[14]。本研究中,增温显著提高武运粳30号的ABS/RC、DIo/RC、TRo/RC、ETo/RC。在增温条件下,水稻通过增加热耗散能够防止电子传递链的过分还原,从而避免光合机构的过度破坏[27-28]。这说明增温使水稻吸收的光能增加,但用于电子传递的光能的增加有限,剩下的光能则通过热耗散进行消耗,以此减缓由PSⅡ反应中心活性降低造成的伤害[29]。Cd处理则显著降低了新两优6号大部分的比活性参数,说明了Cd胁迫抑制了水稻叶片的自我保护机制,通过热耗散消耗的光能减少,多余的光能所激发的电子转化成活性氧的比重提高,部分反应中心发生了不可逆性失活,进而影响水稻叶片对光能的吸收、传递与利用[30]。遭受温度和Cd的双重作用后,两种水稻均启动了自我保护机制,减轻了Cd胁迫造成的负面影响,从而使水稻的比活性参数变化不明显。
增温或Cd处理影响作物光合作用进程,抑制作物光合产物的形成和运输。本研究中,增温或Cd的单一处理显著降低了武运粳30号的茎叶生物量。这可能是增温或Cd处理通过影响了类囊体结构,直接损伤了叶绿体和线粒体结构,造成细胞膜解体从而改变光合特性,本研究中增温或Cd处理降低武运粳30号的叶绿素含量及净光合速率证实了这一猜测[31-32]。另一方面,增温或Cd处理破坏了水稻叶片PSⅡ反应中心活性,降低了最大光化学效率,增加了热耗散的能量,从而导致水稻物质积累减少[33]。温度或Cd处理虽然也显著降低了新两优6号茎叶生物量,但与武运粳30号相比,增温处理使新两优6号的茎叶生物量降低幅度较小。这主要与新两优6号对增温具有较高的耐受能力,增温处理对新两优6号的SPAD、Pn、Fv/Fm及比活动参数的影响较小有关。
4 结论Cd和增温处理对水稻光合参数的影响与水稻品种有关。添加外源Cd显著降低了新两优6号的SPAD值和两品种的Pn;大部分Cd和温度处理下,新两优6号的SPAD值和Pn大于武运粳30号。Cd和温度的复合作用未显著影响两品种的Fv/Fm和比活性参数。外源Cd处理未显著影响新两优6号的Fv/Fm值,但降低了新两优6号的比活度参数ABS/RC、TRo/RC、ETo/RC和DIo/RC(P < 0.05);增温处理显著降低了武运粳30号的Fv/Fm,而增加了比活动性参数。Cd和增温处理都减少了武运粳30号和新两优6号的茎叶和根生物量,但两者的复合作用对生物量的影响与水稻品种有关。根据温度和Cd处理对武运粳30号和新两优6号光合参数、荧光参数及生物量的影响结果可以得出武运粳30号对Cd具有较强的抗性而新两优6号对温度有较强的抗性。通过本研究可知,土壤Cd污染和增温对水稻光合作用及其生长具有一定的影响,且影响程度与水稻品种有关。本研究的结果将为气候变化下中低Cd污染稻田水稻的高产稳产及其管理提供理论依据。
| [1] |
刘娟, 张乃明, 于泓, 等. 重金属污染对水稻土微生物及酶活性影响研究进展[J]. 土壤, 2021, 53(6): 1152-1159 DOI:10.13758/j.cnki.tr.2021.06.007 (  0) 0) |
| [2] |
张雨, 汪家家, 夏冰, 等. 外源秸秆对污染土壤氧化还原过程水分散性胶体态重金属的影响[J]. 土壤学报, 2024, 61(1): 163-173 (  0) 0) |
| [3] |
环境保护部, 国土资源部. 全国土壤污染状况调查公报[R]. 2014. https://www.mee.gov.cn/gkml/sthjbgw/qt/201404/W020140417558995804588.pdf.
(  0) 0) |
| [4] |
罗秋红, 吴俊, 柏斌, 等. 水稻镉吸收与转运机理的研究进展[J]. 土壤, 2021, 53(6): 1142-1151 DOI:10.13758/j.cnki.tr.2021.06.006 (  0) 0) |
| [5] |
涂峰, 胡鹏杰, 李振炫, 等. 苏南地区Cd低积累水稻品种筛选及土壤Cd安全阈值推导[J]. 土壤学报, 2023, 60(2): 1-11 (  0) 0) |
| [6] |
李陈贞, 孙亚莉, 刘红梅, 等. 镉胁迫下不同水稻品种幼苗生长及光合性能的差异[J]. 湖南农业大学学报(自然科学版), 2021, 47(2): 147-152 (  0) 0) |
| [7] |
孙亚莉, 刘红梅, 徐庆国. 镉胁迫对不同水稻品种苗期光合特性与生理生化特性的影响[J]. 华北农学报, 2017, 32(4): 176-181 (  0) 0) |
| [8] |
Change Intergovernmental Panel on Climate. Climate change 2021 – The physical science basis[M].
Cambridge University Press, Cambridge, UK, 2023
(  0) 0) |
| [9] |
余欣, 童飞, 詹妮, 等. 干旱–高温交叉胁迫对水稻幼苗光合特性的影响[J]. 干旱地区农业研究, 2022, 40(3): 72-78 (  0) 0) |
| [10] |
尤翠翠, 贺一哲, 徐鹏, 等. 高温胁迫对水稻生长发育的伤害效应及其防御对策[J]. 浙江农业学报, 2023, 35(1): 10-22 (  0) 0) |
| [11] |
李兴华, 张盛, 周强, 等. 抽穗期高温对不同品种水稻产量的影响及差异[J]. 中国农学通报, 2019, 35(9): 1-6 (  0) 0) |
| [12] |
张文怡, 白涛, 何东, 等. 抽穗期高温胁迫对水稻花药花粉和光合特性的影响[J]. 湖南农业大学学报(自然科学版), 2022, 48(4): 379-385 (  0) 0) |
| [13] |
杜尧东, 李键陵, 王华, 等. 高温胁迫对水稻剑叶光合和叶绿素荧光特征的影响[J]. 生态学杂志, 2012, 31(10): 2541-2548 (  0) 0) |
| [14] |
李岩宸, 杨再强, 杨立, 等. 苗期高温高湿条件对黄瓜叶片光系统Ⅱ中心叶绿素荧光特性的影响[J]. 中国农业气象, 2022, 43(11): 912-922 (  0) 0) |
| [15] |
王弼琨, 于德彬, 赵洪颜, 等. 超高产大豆发育期不同节位叶片净光合速率与SPAD值变化分析[J]. 大豆科学, 2022, 41(2): 172-178 (  0) 0) |
| [16] |
杨泽粟, 张强, 郝小翠. 自然条件下半干旱雨养春小麦生育后期旗叶光合的气孔和非气孔限制[J]. 中国生态农业学报, 2015, 23(2): 174-182 (  0) 0) |
| [17] |
高冠龙, 冯起, 张小由, 等. 植物叶片光合作用的气孔与非气孔限制研究综述[J]. 干旱区研究, 2018, 35(4): 929-937 (  0) 0) |
| [18] |
张洪, 赵丽娟, 王创云. 土壤中镉离子对红芸豆幼苗叶绿素荧光的影响[J]. 山西农业科学, 2019, 47(11): 1999-2002 (  0) 0) |
| [19] |
胡雪华, 闫霄枫, 胡文海. 短时强光对绿萝快速叶绿素荧光诱导动力学特性的影响[J]. 井冈山大学学报(自然科学版), 2022, 43(6): 33-39 (  0) 0) |
| [20] |
Mathur S, Jajoo A, Mehta P, et al. Analysis of elevated temperature-induced inhibition of photosystem Ⅱ using chlorophyll a fluorescence induction kinetics in wheat leaves (Triticum aestivum)[J]. Plant Biology, 2011, 13(1): 1-6 (  0) 0) |
| [21] |
Mathur S, Jajoo A. Arbuscular mycorrhizal fungi protects maize plants from high temperature stress by regulating photosystem Ⅱ heterogeneity[J]. Industrial Crops and Products, 2020, 143: 111934 (  0) 0) |
| [22] |
Sigfridsson K G V, Bernát G, Mamedov F, et al. Molecular interference of Cd2+ with photosystem Ⅱ[J]. Biochimica et Biophysica Acta (BBA) - Bioenergetics, 2004, 1659(1): 19-31 (  0) 0) |
| [23] |
刘英, 雷少刚, 宫传刚, 等. 采煤沉陷裂缝区土壤含水量变化对柠条叶片叶绿素荧光的响应[J]. 生态学报, 2019, 39(9): 3267-3276 (  0) 0) |
| [24] |
Y Lee H, -N Hong Y, Chow W S. Photoinactivation of photosystem Ⅱ complexes and photoprotection by non-functional neighbours in Capsicum annuum L. leaves[J]. Planta, 2001, 212(3): 332-342 (  0) 0) |
| [25] |
苗婷婷, 曹志华, 刘俊龙, 等. 淹水胁迫对2个薄壳山核桃品种苗期生长及叶绿素荧光特性的影响[J]. 江苏农业科学, 2022, 50(16): 138-146 (  0) 0) |
| [26] |
Kalaji H M, Jajoo A, Oukarroum A, et al. Chlorophyll a fluorescence as a tool to monitor physiological status of plants under abiotic stress conditions[J]. Acta Physiologiae Plantarum, 2016, 38(4): 102 (  0) 0) |
| [27] |
Janeczko A, Koscielniak J, Pilipowicz M, et al. Protection of winter rape photosystem 2 by 24-epibrassinolide under cadmium stress[J]. Photosynthetica, 2005, 43(2): 293-298 (  0) 0) |
| [28] |
铁得祥, 胡红玲, 喻秀艳, 等. 桢楠幼树光合特性对镉胁迫的响应[J]. 生态学报, 2020, 40(11): 3738-3746 (  0) 0) |
| [29] |
赵霞, 杨华伟, 刘然方, 等. 水稻热耗散对逆境的响应[J]. 中国水稻科学, 2016, 30(4): 431-440 (  0) 0) |
| [30] |
孟力力, 闻婧, 张俊, 等. Cd2+胁迫对鸡爪槭PSⅡ叶绿素荧光动力学特性的影响[J]. 江苏农业学报, 2014, 30(2): 398-404 (  0) 0) |
| [31] |
刘春溪, 孙备, 王国骄, 等. 开放式增温对粳稻光合作用和叶绿素荧光参数的影响[J]. 生态环境学报, 2018, 27(9): 1665-1672 (  0) 0) |
| [32] |
刘尚佳, 吕尧, 曹逼力, 等. 高温渍涝胁迫对姜叶片光合作用和氮代谢的影响[J]. 园艺学报, 2022, 49(5): 1073-1080 (  0) 0) |
| [33] |
吴思佳, 李仁英, 谢晓金, 等. 抽穗期高温对水稻叶片光合特性、叶绿素荧光特性和产量构成因素的影响[J]. 南方农业学报, 2021, 52(1): 20-27 (  0) 0) |
2. Jiangsu Key Laboratory of Agricultural Meteorology, Nanjing 210044, China
 2024, Vol. 56
2024, Vol. 56

