2. 绿色智能复合肥研究院, 合肥 230001;
3. 哈尔滨工业大学环境学院, 哈尔滨 150090;
4. 中国农业大学资源与环境学院/中国农业大学国家绿色农业发展研究院, 北京 100193;
5. 中盐安徽红四方肥业股份有限公司, 合肥 230001
氮素是植物生长的必需元素,氮肥在全球农业生产中发挥着重要作用。国际肥料协会(IFA)的评估显示[1],中国的作物氮肥消耗量约占全球的1/4,而氮肥利用率仅为40% 左右,相比发达国家低10% ~ 20%[2-3]。在大量使用氮肥的情况下,大部分的氮素并没有被作物有效吸收,而是以氨挥发、硝酸盐淋洗等形式损失[4],给大气和水体环境带来了严重污染[5]。为了降低环境污染风险,提高氮肥利用率变得至关重要,也是推动农业绿色可持续发展的重要举措。
目前,施用硝化抑制剂是提高氮肥利用率的有效途径之一[6]。硝化抑制剂可以抑制土壤中铵态氮(NH4+-N)向硝态氮(NO3–-N)的转化,延长NH4+-N在土壤中的留存时间,减少由硝化作用产生的氮素损失。李学文等[7]研究发现,添加硝化抑制剂处理能减少约17.30% 总氮和5.13% NO3–-N的淋失。硝化抑制剂施入土壤60 d后,小粉土和青紫泥土壤中NH4+-N含量分别提高了52.70% 和57.50%,NO3–-N含量分别降低了58.30% 和65.90%,添加硝化抑制剂处理的氮肥利用率比对照提高了1.78倍和2.23倍[8]。当前市场上的硝化抑制剂种类较多,其中DMPP(3,4-二甲基吡唑磷酸盐)因其微量高效、绿色无毒无污染的作用特点,被广泛应用于稳定性肥料生产。与其他硝化抑制剂相比,DMPP可以在更少的用量下达到较好的硝化抑制效果。有研究结果表明,DMPP的用量只需DCD(双氰胺)的1/10,抑制效果就可超过DCD,且DMPP的抑制持续时间更长[9]。但添加硝化抑制剂在某些环境条件下会有增加氨挥发的风险[10]。如有研究表明,使用DMPP将增加5.30% 的氨挥发[11]。但也有学者发现,DMPP对土壤氨挥发损失没有显著影响[12]。这可能是由于DMPP的作用效果会受土壤类型及氮肥含量等多种因素的影响。刘发波等[13]研究表明,土壤中的氮素施用量和土壤pH是影响硝化抑制剂DMPP调节氮素转化的主要因素。另外,多形态氮素配施对于提高氮肥利用率同样具有重要意义。研究表明,与尿素相比,一次性施用同等氮量的草酰胺可以显著提高粮食作物产量[14-15]。新型脲铵氮肥的施用也能有效减少氮素的挥发,并对土壤起到一定的调节作用[16]。然而,不同形态氮肥在不同土壤中的转化过程和速率可能导致与DMPP配施后效果不同。因此,综合利用不同土壤条件,选择硝化抑制剂和不同形态氮素配施,对于提高氮肥利用率、降低环境污染风险具有重要意义。这些举措也将有助于实现农业的绿色可持续发展,从而促进社会、经济和生态的全面发展。
综上,本研究选取硝化抑制剂DMPP分别与不同氮素形态的肥料(脲铵氮肥、复合肥、硫硝酸铵、草酰胺)进行配施,通过土壤培养试验,研究了不同pH土壤中NH4+-N、NO3–-N、氨挥发浓度的动态变化,以明确DMPP在不同土壤条件下与不同氮肥配施的作用效果,为基于不同氮素形态的稳定性肥料产业化提供理论支持。
1 材料与方法 1.1 供试土壤供试土壤为南方水稻土和北方小麦土。南方水稻土采自安徽省北灵村(31°32'32'' N,117°23'20'' E),土壤类型属潴育型水稻土;北方小麦土采自中国农业大学曲周实验站(36°51'50'' N,115°0'58'' E),土壤类型属盐化潮土。以上2种类型土壤均取自农田耕作表层(0 ~ 20 cm)。采用“五点取样法”进行取样,将新鲜土样带回实验室混合均匀,经人工筛除杂物(如石块、植物和植物根系等)后,自然风干研磨,过2 mm筛装袋备用。土壤基本理化性质测定方法参照鲁如坤《土壤农化分析》进行处理与测定[17]。供试土壤基本理化性质见表 1。
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physiochemical properties of tested soil |
供试硝化抑制剂为DMPP,由武威金仓生物科技有限公司提供,有效成分含量≥99.0%。供试氮肥分别为复合肥(CF,含N量150 g/kg)、硫硝酸铵(ASN,分析纯,含N量260 g/kg)、脲铵氮肥(UA,含N量280 g/kg)、草酰胺(OA,分析纯,含N量320 g/kg)。
1.3 试验设计采用室内土壤培养方法,称取50.00 g风干土壤于培养瓶(250 mL)中,调节土壤含水量为60% WFPS (water filled pore space,土壤孔隙含水量),室温预培养4 d后进行肥料处理。每种土壤设置8个处理,试验设计见表 2。肥料添加量为N 0.10 g/kg,DMPP添加量根据行业推荐标准NY/T 3504—2019 《肥料增效剂硝化抑制剂及使用规程》[18]对DMPP的使用量要求,设置为所施肥料中酰胺态氮和铵态氮总量的0.80%,每个处理重复3次。土壤培养在室温条件下持续10 d。培养期间,每2 d采用称重法补充水分,使土壤含水量保持在60%WFPS。
|
|
表 2 试验设计 Table 2 Experimental design |
氨挥发采用“静态吸收法”测定[19],试验设计与处理设置和上述土壤培养相同,肥料添加量为N 0.50 g/kg。室温下培养10 d,每隔12 h记录一次NH3挥发量。
1.4 样品采集及测定NH3采集与测定:累积氨挥发量采用氨检测管检测[20]。在密封的橡胶塞上打孔,连接氨检测管(NH3-100,华安气体检测科技有限公司,鹤壁)。未与氨气反应时,检测管内指示粉为桔黄色,使用时用开管器将气体检测管的两端打开,指示粉与氨气反应变成灰黑色,直接读数即为从培养开始到读数时间内的累积氨挥发量。
土壤样品采集与测定:分别在培养1、3、5、10 d,对土壤培养试验各处理进行破坏性取样,称取10.0 g土于100 mL离心管中,加入50 mL的1 mol/L的KCl溶液,在室温条件下振荡1 h后过滤,采用流动分析仪(AA3,中通科技发展有限公司,天津)测定滤液中NH4+-N、NO3–-N含量,同时测定土壤含水量,用于土壤NH4+-N、NO3–-N含量的计算。
1.5 数据处理与统计分析采用Excel 2016进行数据基础整理;利用SPSS 26.0进行统计分析,包括进行Pearson相关系数的计算、运用单因素方差分析(One-way ANOVA)检验处理间的差异性;采用Origin 2022进行图表制作。
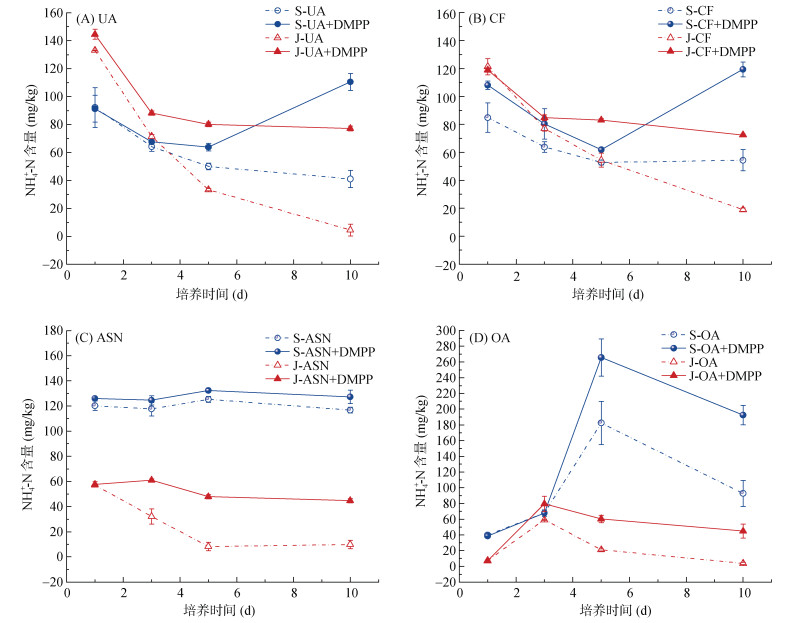
2 结果与分析 2.1 DMPP与不同氮肥配施对不同土壤无机氮动态变化的影响由图 1可知,DMPP与不同氮肥配施对不同土壤中NH4+-N的含量变化表现出不同的影响。对于脲铵氮肥和复合肥处理(图 1A、1B),培养期间NH4+-N的含量变化趋势基本一致,未添加DMPP的处理土壤NH4+-N的含量呈下降趋势,且在碱性土壤下下降速度更快。整个培养周期内,未添加DMPP的脲铵氮肥处理酸性土壤中NH4+-N含量减少55%,碱性土壤中NH4+-N含量降低97%;未添加DMPP的复合肥处理酸性土壤中NH4+-N含量减少了40%,碱性土壤中NH4+-N含量减少了84%,是酸性土壤的两倍。添加DMPP后土壤NH4+-N的含量下降趋势明显趋于平缓,且在酸性土壤中培养5 d后NH4+-N的含量突然回升,显著高于未添加DMPP的处理。硫硝酸铵与草酰胺处理的NH4+-N含量变化与脲铵氮肥和复合肥处理表现出显著不同的趋势。硫硝酸铵处理中(图 1C),在整个培养期间酸性土壤中NH4+-N含量几乎无明显变化;在碱性土壤中呈现先下降后趋于平稳的趋势,且添加DMPP的处理NH4+-N平均含量显著高于不添加DMPP的处理。DMPP与草酰胺配施时(图 1D),土壤NH4+-N含量在两种土壤条件下各处理均呈现先升高后降低的趋势,不同的是酸性土中在培养5 d时出现峰值,碱性土中土壤NH4+-N含量峰值则提前至培养3 d时出现,可能是碱性条件下,施用草酰胺处理的土壤硝化强度在培养3 d后快速增强,导致3 d后NH4+-N含量快速降低。
|
图 1 DMPP与不同氮肥配施处理下不同土壤NH4+-N含量变化过程 Fig. 1 NH4+-N contents in soils under combined applications of DMPP with different nitrogen fertilizers |
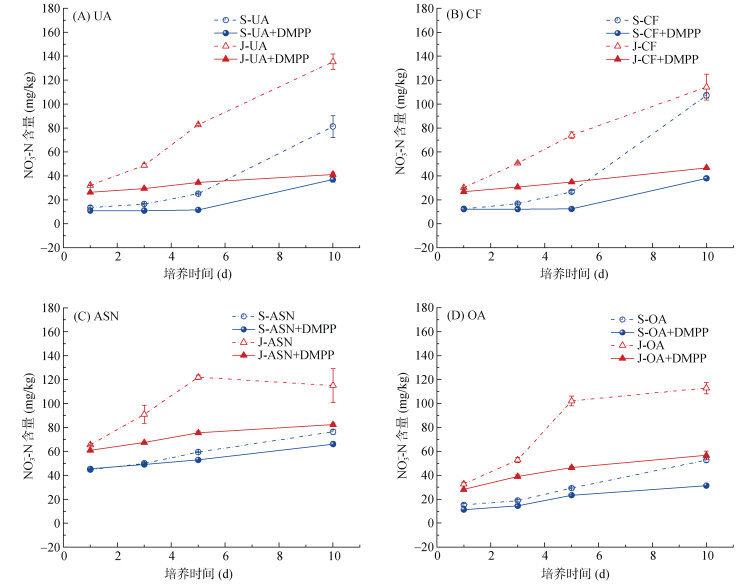
由图 2可知,DMPP与不同氮肥配施可显著降低土壤中NO3–-N的含量。各处理土壤NO3–-N含量均表现为随着培养时间增加而逐渐升高的趋势,但添加DMPP后增速显著放缓。未添加DMPP的脲铵氮肥处理(图 2 A)NO3–-N含量在酸性土与碱性土中均以培养5 ~ 10 d时增加速度最快;在酸性土中,培养结束时未添加DMPP的处理NO3–-N含量相比培养开始时增加了5.06倍,而添加DMPP的处理NO3–-N含量相比培养开始时只增加了2.38倍,DMPP添加显著降低了NH4+-N向NO3–-N的转化速度。DMPP与不同氮肥配施在培养后期,NO3–-N含量增加速度以酸性条件下未添加DMPP的复合肥处理最快。在培养期间,不含DMPP的处理NH4+-N快速转化成NO3–-N,特别是在酸性土壤中培养5 ~ 10 d时增长迅速,而在碱性土壤中快速增长时间则提前至培养3 ~ 5 d时,说明碱性土壤中硝化作用相对于酸性土壤中更加剧烈。
|
图 2 DMPP与不同氮肥配施处理下不同土壤NO3–-N含量变化过程 Fig. 2 NO3–-N contents in soils under combined applications of DMPP with different nitrogen fertilizers |
DMPP与不同氮源配施所表现出的硝化抑制效果有显著差异(表 3)。在酸性土中,DMPP与脲铵氮肥、复合肥和硫硝酸铵配施处理的硝化抑制率随培养时间逐渐上升,说明DMPP的作用效果逐渐增强。而DMPP与草酰胺配施处理则先降低后升高,5 d时硝化抑制能力最弱,但培养期间硝化抑制率均在20% 以上。培养结束(10 d)时,酸性土中添加DMPP处理的硝化抑制效果为复合肥 > 脲铵氮肥 > 草酰胺 > 硫硝酸铵,复合肥添加DMPP处理最高硝化抑制率为64.5%,约为硫硝酸铵添加DMPP处理的5倍。
|
|
表 3 DMPP与不同氮肥配施对不同土壤硝化作用的影响 Table 3 Nitrifications in soils under combined applications of DMPP with different nitrogen fertilizers |
在碱性土壤中,DMPP与脲铵氮肥和复合肥配施处理的硝化抑制率同样呈现出随培养时间推移逐渐升高的趋势。而DMPP与硫硝酸铵配施和草酰胺配施处理的硝化抑制率则表现出先升高后降低的变化趋势,硝化抑制活性在培养5 d时最强,此时,除硫硝酸铵处理外,其他各处理的硝化抑制率均达到50% 以上。整体上,在整个培养周期结束时,碱性土中DMPP与不同氮肥配施的硝化抑制率表现为脲铵氮肥 > 复合肥 > 草酰胺 > 硫硝酸铵,脲铵氮肥添加DMPP处理最高硝化抑制率为69.6%。
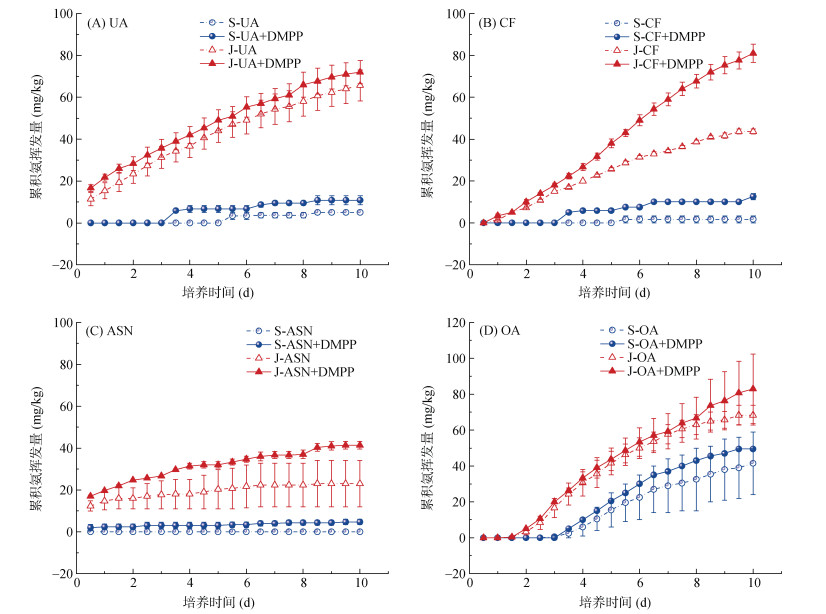
2.3 DMPP与不同氮肥配施对不同土壤氨挥发动态变化的影响DMPP与不同氮肥配施对土壤氨挥发动态变化的影响在碱性土中相似(图 3),氨挥发量均表现为随培养时间持续增加的趋势。而在酸性土中表现则有所不同,与碱性土中相比,除草酰胺处理外,其余处理的氨挥发现象非常微弱,对于硫硝酸铵处理(图 3C),未添加DMPP处理在整个培养期间几乎无氨挥发现象,添加DMPP处理检测到微弱的氨挥发现象;脲铵氮肥与复合肥处理(图 3A、3B)在培养3 d后才检测到氨挥发,且添加DMPP处理比未添加DMPP处理出现氨挥发现象更早,DMPP的使用使脲铵氮肥和复合肥处理的氨挥发出现时间提前了60 h。培养试验结束时,各肥料处理中,碱性土条件下氨挥发累积量均显著高于酸性土。在脲铵氮肥、硫硝酸铵和草酰胺处理中,相同土壤条件下添加DMPP处理与未添加DMPP处理间累积氨挥发量差异均不显著;但在复合肥处理中,不同土壤条件下添加DMPP处理累积氨挥发量均显著高于未添加DMPP处理。与酸性土相比,碱性土中氮肥的氨挥发现象较为显著,与未添加DMPP处理相比,DMPP的施用平均提高13.38% ~ 63.38% 氨挥发量。
|
图 3 硝化抑制剂与不同氮肥配施对不同土壤氨挥发的影响 Fig. 3 Ammonia volatilization in soils under combined applications of DMPP with different nitrogen fertilizers |
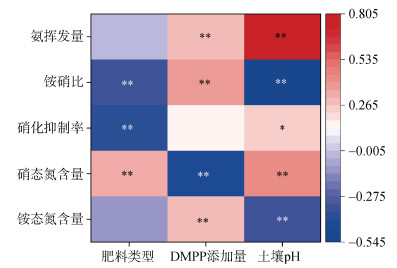
对所有处理的土壤NH4+-N含量、NO3–-N含量、硝化抑制率、铵硝比、氨挥发量与肥料类型、DMPP添加量、土壤pH进行Pearson相关性分析(图 4)发现,本试验条件下,土壤NH4+-N含量与DMPP添加量呈极显著正相关(P < 0.01),与土壤pH呈极显著负相关。而土壤NO3–-N含量与肥料类型和土壤pH表现为极显著正相关,与DMPP添加量则呈极显著负相关。DMPP对土壤的硝化抑制活性与配施的肥料类型呈极显著负相关,与土壤pH呈显著正相关(P < 0.05)。铵硝比与肥料类型和土壤pH呈极显著负相关,与DMPP添加量呈极显著正相关。氨挥发量与DMPP添加量和土壤pH呈极显著正相关。
|
(图中*、**分别表示在P < 0.05、P < 0.01水平显著相关) 图 4 氮素转化与不同变量之间的Pearson相关性 Fig. 4 Pearson correlations between nitrogen conversion and different variables |
本研究结果表明,DMPP与氮肥配施显著抑制了土壤硝化过程,这与前人的研究结果相似。Lan等[21]研究表明,1% 的DMPP可减缓土壤总硝化速率50.30% ~ 56.60%;赵宇晴等[22]的研究也指出,DMPP与氮肥配施显著降低了土壤中NO3–-N的累积量,降幅在13.07% ~ 62.32%;李学红等[23]亦指出,与尿素合用的DMPP能有效抑制NH4+-N硝化,从而减少氮素的损失。因此,结合硝化抑制剂的氮肥施用策略被证实是有效抑制土壤硝化作用的途径。本试验中,在酸性土壤条件下施用DMPP与尿素和复合肥的处理显示,至培养5 d时NH4+-N含量上升,NO3–-N含量亦相应增加,这可能是由于在本试验条件下,DMPP与脲铵氮肥和复合肥配施刺激了土壤微生物群落活性变化,促进了土壤中有机氮的矿化,从而转化出更多的NH4+-N和NO3–-N。
从研究结果来看,DMPP与硫硝酸铵配施对土壤硝化过程的抑制效果最差,这可能是由于DMPP的使用量受肥料中酰胺态氮和NH4+-N总量的影响,而硫硝酸铵中除含有部分NH4+-N外,还有一部分氮素为NO3–-N,DMPP对NO3–-N不发挥作用,外加肥料本身NO3–-N含量的加持,导致测定结果中DMPP与硫硝酸铵配施的整体硝化抑制效果最差[24]。因此,在稳定性肥料生产过程中要充分考虑肥料所含氮素形态,并选择适宜的肥料类型以最大限度地发挥DMPP的优势。
本研究进一步表明,在碱性土壤环境中,各类氮肥配施DMPP的硝化抑制效果优于酸性土壤中,这与已有文献报道相吻合,可能是由于碱性土壤中硝化细菌活性较强、土壤本底硝化速率较高所导致的[25-26]。DMPP的作用效率不仅受土壤pH影响,而且与配施氮肥的氮素形态相关。不同形态氮素在土壤中的转化机制不同,这或许解释了DMPP与不同类型氮肥配施所展示的差异化作用效果。在碱性土壤中,酰胺态氮和NH+ 4-N在转化过程中受硝化作用影响较大,而NO3–-N因不易被土壤吸附而易被淋失[27-28]。因此,向酰胺态氮肥与铵态氮肥中添加DMPP在碱性土壤条件下能更为有效地抑制硝化作用,减少氮肥流失。综合以上因素,硝化抑制剂与不同氮肥配施在不同土壤条件下将展现不同的作用效果。
3.2 DMPP与不同氮肥配施对土壤氨挥发的影响DMPP对硝化过程的抑制作用可能导致铵态氮肥或酰胺态氮肥更多地以氨的形式挥发损失,加剧氨挥发损失的风险[11]。在高珊等[29]的研究中,60% 田间持水量条件下,施用DMPP使土壤累积氨挥发量显著增加9.60% ~ 20.70%。然而,本研究结果发现,DMPP与硫硝酸铵配施时对氨挥发的影响较小。苏芳等[30]研究也发现,在尿素和硫硝酸铵的对比中,硫硝酸铵的氨挥发损失比尿素少8.30%。这可能是由于硫硝酸铵属生理酸性肥料,施用后能降低土壤pH,减弱了土壤NH4+-N的氨挥发趋势。在氨挥发较强的碱性土壤中,或进行肥料配方设计时,可以考虑使用硫硝酸铵替代常用氮肥,以降低氨挥发损失。
本研究显示,草酰胺处理的土壤在培养前3 d氨挥发现象不明显,在培养3 ~ 10 d时氨挥发量迅速增加。这可能与草酰胺中的酰胺态氮需要先经过土壤中脲酶以及微生物的作用,水解成碳酸铵或碳酸氢铵等NH4+-N有关[27]。沈晓忆等[31]研究发现,单施尿素会促进主导土壤硝化过程的氨氧化细菌(AOB)迅速繁殖,加快硝化作用的发生,而硝化抑制剂与尿素配施则抑制了AOB的生长,对反硝化细菌的影响则相反,有轻微促进作用。因此,使用硝化抑制剂时最好与其他氨挥发减排措施相结合,以更好地发挥其增效减排作用。
土壤pH对硝化抑制剂作用效果的影响较为复杂。一般来说,在pH较高的土壤上,硝化活性也较高,有利于DMPP硝化抑制效果的发挥。但此时土壤微生物的活性也较高,可能对DMPP的作用效果产生影响,也可能增加土壤氨挥发的风险。本研究结果表明,在碱性环境下,铵态氮肥的氨挥发损失更为严重,这可能是由于在碱性土壤条件下,肥料中的NH4+会与更多的OH–反应生成NH3,加剧氨挥发损失[32]。在徐丽萍等[33]的氨挥发试验中,土壤pH由大到小为潮土 > 灰漠土 > 红壤,培养28 d时的累积氨挥发量大小与pH一致,潮土累积氨挥发量最大,为0.53 mg/kg,红壤仅为0.10 mg/kg。本研究结果表明,土壤pH与氨挥发量呈极显著的正相关关系(r=0.803),这表明土壤pH越高,氨挥发量越大,这与前人研究结果一致[34]。因此,在添加硝化抑制剂的稳定性肥料生产和推广过程中,需要综合考虑氮素形态、土壤条件等因素的影响,因地制宜选用硝化抑制剂与氮肥配施。
4 结论DMPP与不同类型的氮肥配施均能有效抑制土壤中NH4+-N向NO3–-N的转化,从而减少NO3–-N的淋洗损失风险,且在碱性土壤中的效果优于在酸性土壤中的效果。然而,DMPP的添加会增加土壤氨挥发的风险,不过这也与肥料类型、DMPP添加量以及土壤pH等条件有关。碱性土壤中的氨挥发量显著高于酸性土壤。草酰胺处理中以酰胺态氮为主的情况下,氨挥发的增加最为显著。另外,DMPP与以NO3–-N为主的酸性氮肥硫硝酸铵配施时,对土壤氨挥发的影响并不显著。肥料类型对土壤中铵硝变化有显著影响,而DMPP的添加量和土壤的pH也对土壤中铵硝的变化和氨挥发产生重要影响。因此,未来的研究应该在多种氮源养分供应的背景下,基于硝化抑制剂进行氮阻控研究,以更好地评估硝化抑制剂的有效性,并推动其推广和应用。
| [1] |
Heffer P, Gruère A, Roberts T. Assessment of fertilizer use by crop at the global level 2014-2014/15[R]. International Fertilizer Industry Association. 2017.
(  0) 0) |
| [2] |
任科宇, 段英华, 徐明岗, 等. 施用有机肥对我国作物氮肥利用率影响的整合分析[J]. 中国农业科学, 2019, 52(17): 2983-2996 (  0) 0) |
| [3] |
巨晓棠, 张福锁. 关于氮肥利用率的思考[J]. 生态环境, 2003, 12(2): 192-197 (  0) 0) |
| [4] |
巨晓棠. 氮肥有效率的概念及意义——兼论对传统氮肥利用率的理解误区[J]. 土壤学报, 2014, 51(5): 921-933 (  0) 0) |
| [5] |
周伟, 吕腾飞, 杨志平, 等. 氮肥种类及运筹技术调控土壤氮素损失的研究进展[J]. 应用生态学报, 2016, 27(9): 3051-3058 (  0) 0) |
| [6] |
贾树龙. 氮肥增效剂的作用与应用技术[J]. 河北农业科技, 1998(3): 25 (  0) 0) |
| [7] |
李学文, 李树营, 王齐龙, 等. 减氮配施脲酶/硝化抑制剂对冬瓜品质、产量和土壤氮磷淋失的影响[J]. 中国瓜菜, 2021, 34(1): 55-59 (  0) 0) |
| [8] |
俞巧钢, 陈英旭. 3,4-二甲基吡唑磷酸盐对菜地土壤氮素形态转化的影响[J]. 水土保持学报, 2010, 24(3): 123-126 (  0) 0) |
| [9] |
曾祥明, 肖焱波, 段慧明. 硝化抑制剂DMPP在肥料上的应用[J]. 长江蔬菜, 2015(7): 64-65 (  0) 0) |
| [10] |
Qiao C L, Liu L L, Hu S J, et al. How inhibiting nitrification affects nitrogen cycle and reduces environmental impacts of anthropogenic nitrogen input[J]. Global Change Biology, 2015, 21(3): 1249-1257 (  0) 0) |
| [11] |
马芬, 杨荣全, 郭李萍. 控制氮肥施用引起的活性氮气体排放: 脲酶/硝化抑制剂研究进展与展望[J]. 农业环境科学学报, 2020, 39(4): 908-922 (  0) 0) |
| [12] |
Pan B B, Lam S K, Mosier A, et al. Ammonia volatilization from synthetic fertilizers and its mitigation strategies: A global synthesis[J]. Agriculture, Ecosystems & Environment, 2016, 232: 283-289 (  0) 0) |
| [13] |
刘发波, 马笑, 张芬, 等. 硝化抑制剂对我国蔬菜生产产量、氮肥利用率和氧化亚氮减排效应的影响: Meta分析[J]. 环境科学, 2022, 43(11): 5140-5148 (  0) 0) |
| [14] |
李俊, 陈驰, 张弘, 等. 缓释肥料草酰胺合成工艺及其性能[J]. 江苏农业科学, 2019, 47(21): 290-293 (  0) 0) |
| [15] |
段付岗, 段勤国. 草酰胺和尿素的相似性与差异性研究及建议[J]. 中氮肥, 2021(6): 1-6 (  0) 0) |
| [16] |
胡波. 脲铵氮肥是提高氮肥利用率的有效途径[J]. 中国农资, 2013(13): 25 (  0) 0) |
| [17] |
鲁如坤. 土壤农化分析方法[M].
中国农业科技出版社, 北京, 1999
(  0) 0) |
| [18] |
中华人民共和国农业农村部. 肥料增效剂硝化抑制剂使用规程: NY/T 3504—2019[S]. 北京: 中国标准出版社, 2019.
(  0) 0) |
| [19] |
孙克君, 毛小云, 卢其明, 等. 几种控释氮肥减少氨挥发的效果及影响因素研究[J]. 应用生态学报, 2004, 15(12): 2347-2350 (  0) 0) |
| [20] |
吴艳香. 土壤氨挥发方法优选及不同pH值的影响[J]. 贵州科学, 2017, 35(5): 85-90 (  0) 0) |
| [21] |
Lan T, Li M X, He X Q, et al. Effects of synthetic nitrification inhibitor (3,4-dimethylpyrazole phosphate; DMPP) and biological nitrification inhibitor (methyl 3-(4-hydroxyphenyl) propionate; MHPP) on the gross N nitrification rate and ammonia oxidizers in two contrasting soils[J]. Biology and Fertility of Soils, 2022, 58(3): 333-344 (  0) 0) |
| [22] |
赵宇晴, 杨迎, 田晓楠, 等. 减氮配施硝化抑制剂与菌剂对温室黄瓜产量品质和土壤氮素损失的影响[J]. 水土保持学报, 2023, 37(4): 367-277 (  0) 0) |
| [23] |
李学红, 李东坡, 武志杰, 等. 添加NBPT/DMPP/CP的高效稳定性尿素在黑土和褐土中的施用效应[J]. 植物营养与肥料学报, 2021, 27(6): 957-968 (  0) 0) |
| [24] |
Cookson W R, Cornforth I S. Dicyandiamide slows nitrification in dairy cattle urine patches: Effects on soil solution composition, soil pH and pasture yield[J]. Soil Biology and Biochemistry, 2002, 34(10): 1461-1465 (  0) 0) |
| [25] |
刘发波, 郎明, 马笑, 等. 硝化抑制剂类型和剂量对不同类型土壤硝化抑制作用机理的研究[J]. 中国土壤与肥料, 2022(8): 66-75 (  0) 0) |
| [26] |
张昊青, 赵学强, 张玲玉, 等. 石灰和双氰胺对红壤酸化和硝化作用的影响及其机制[J]. 土壤学报, 2021, 58(1): 169-179 (  0) 0) |
| [27] |
段付岗. 草酰胺缓释氮肥的特性分析及建议[J]. 磷肥与复肥, 2021, 36(5): 18-20 (  0) 0) |
| [28] |
张庆利, 张民, 杨越超, 等. 碳酸氢铵和尿素在山东省主要土壤类型上的氨挥发特性研究[J]. 土壤通报, 2002, 33(1): 32-34 (  0) 0) |
| [29] |
高珊, 郭艳杰, 张丽娟, 等. 温室土壤不同含水量下施用DCD和DMPP对N2O排放及NH3挥发的影响[J]. 河北农业大学学报, 2019, 42(4): 95-101 (  0) 0) |
| [30] |
苏芳, 黄彬香, 丁新泉, 等. 不同氮肥形态的氨挥发损失比较[J]. 土壤, 2006, 38(6): 682-686 (  0) 0) |
| [31] |
沈晓忆, 夏围围, 张洁, 等. 硝化抑制剂与尿素配施对旱地土壤温室气体排放及硝化微生物的影响[J]. 土壤, 2021, 53(3): 512-521 DOI:10.13758/j.cnki.tr.2021.03.010 (  0) 0) |
| [32] |
田光明, 蔡祖聪, 曹金留, 等. 镇江丘陵区稻田化肥氮的氨挥发及其影响因素[J]. 土壤学报, 2001, 38(3): 324-332 (  0) 0) |
| [33] |
徐丽萍, 王旭, 侯晓娜, 等. 脲酶抑制剂NBPT对三种类型土壤中UAN氮溶液氮素转化和氨挥发的影响[J]. 中国土壤与肥料, 2022(3): 126-136 (  0) 0) |
| [34] |
Gao J C, Luo J F, Lindsey S, et al. Effects of soil properties on urea-N transformation and efficacy of nitrification inhibitor 3,4-dimethypyrazole phosphate (DMPP)[J]. Soil Science and Plant Nutrition, 2022, 68(1): 228-237 (  0) 0) |
2. Academy of Green Intelligent Compound Fertilizer, Hefei 230001, China;
3. School of Environment, Harbin Institute of Technology, Harbin 150090, China;
4. College of Resources and Environment, China Agricultural University / National Academy of Agriculture Green Development, China Agricultural University, Beijing 100193, China;
5. CNSIG Anhui Hongsifang Fertilizer Co., Ltd., Hefei 230001, China
 2024, Vol. 56
2024, Vol. 56


