2. 土壤与农业可持续发展全国重点实验室(中国科学院南京土壤研究所), 南京 211135
三氯乙烯(TCE)是一种广泛用于杀虫剂、涂料和金属脱脂剂等加工行业的有机溶剂[1],也是用于不锈钢制品清洁、衣物干洗等的去污溶剂[2],使用不当会导致TCE泄露,进而进入大气、水体和土壤中。TCE作为一种有机污染物具有“三致”效应和易挥发性,广泛存在于典型的有机污染场地中[3-4]。TCE也是污染场地检出率较高的一类有机污染物,但由于环境样品基质复杂且TCE含量较低,其很难通过仪器直接检测,因此,在进行仪器分析之前,需要对环境样品进行前处理。
目前有多种技术可用于环境样品的前处理,包括微波辅助萃取、固相微萃取(SPME)和磁固相萃取等[5]。其中,SPME技术以其操作简单、溶剂消耗量低、易与气相色谱或液相色谱联合等优势,已成为一种应用广泛的样品前处理技术。该技术主要是通过目标物在涂层材料与样品之间的分配平衡实现目标物的萃取。因此,萃取涂层材料的吸附特性对于固相微萃取效果至关重要。
当前市面上常用的涂层材料有聚二甲基硅氧烷和聚二甲基硅氧烷‒二乙烯基苯等,但其机械强度低、成本高,不利于样品的快速检测[6]。现已研发出的新型涂层材料,包括碳基材料[7]、有机骨架材料[8]、金属有机骨架材料[9]和分子印迹材料[10]等,其中,金属有机骨架材料合成方法简单和成本相对较低,且具有多孔性、高稳定性和耐高温等优点,常被用作有机污染物的吸附剂[11]。ZIF-67是含钴的一种金属有机骨架材料,富含官能团和多孔结构,然而将ZIF-67作为固相微萃取涂层用于TCE萃取的相关研究鲜有报道。
基于以上,本研究通过常温合成ZIF-67材料,研究其结构特征以及对气态TCE的吸附性能,并采用物理涂敷法制备ZIF-67固相微萃取纤维涂层,与气相色谱(GC-ECD)联用,研究该方法对水土体系中TCE的顶空固相微萃取性能,以为快速检测土壤和水体挥发性有机污染提供技术支持。
1 材料与方法 1.1 实验仪器与试剂实验仪器:Agilent 6820气相色谱仪配备ECD检测器(美国安捷伦科技有限公司)、Smartlab 9 X射线衍射仪(XRD,日本理学株式会社)、Nova NanoSEM450扫描电子显微镜仪(SEM,美国FEI公司)、Tecnai G2 F20 S-Twin透射电子显微镜仪(TEM,美国FEI公司)、IS5红外吸收光谱仪(FTIR,美国赛默飞世尔公司)、ASAP 2020 PLUS比表面积孔径分析仪(BET,美国麦克默瑞提克公司)、DF-101S恒温加热磁力搅拌器(上海力辰邦西仪器科技有限公司)、0.25 mm不锈钢银针(衡水济渡医疗器械专营店)、10 mL手动注射器(美国安捷伦科技有限公司)、50 μL气相进样针(哈美顿上海实验器材有限公司)、聚四氟搅拌子(南京斑马实验器材有限公司)、SPME装置头(上海新拓分析仪器科技有限公司)。
试剂:三氯乙烯、环己烷(分析纯)、2-甲基咪唑和硝酸钴,购于上海百灵威化学技术有限公司;无水乙醇(分析纯),购于无锡市亚盛化工有限公司;甲醇(色谱纯),购于美国天地试剂公司;氢氟酸,购于上海麦克林生化科技有限公司;中性硅酮密封胶,购于上海西卡管理有限公司。
供试土样:取自南京某区6 m和22 m深度土壤。
1.2 ZIF-67合成与形貌表征ZIF-67的合成方法参考Ethiraj等[12]方法,并做了一定的改进,具体步骤如下:先称取0.273 g硝酸钴(Co(NO3)2·6H2O,0.0938 mmol)溶于20 mL甲醇,置于50 mL锥形瓶中搅拌至完全溶解,记为A液;取0.616 g 2-甲基咪唑溶于20 mL甲醇,置于50 mL锥形瓶中搅拌至完全溶解,记为B液;在30 min内将A液缓慢滴入B液并搅拌3 h,随后静置3 h,离心沉淀后用甲醇洗涤置于70 ℃真空干燥箱过夜,研磨得到紫色粉末。
利用SEM、TEM、XRD、FTIR和BET技术表征涂层材料。SEM条件:电子束加速电压为20 kV;TEM条件:电子束加速电压为200 kV;XRD条件;配超高速检测器,管电压为40 kV和150 mA,衍射速率为2°/min,扫描范围为5° ~ 90°;FTIR条件:在400 ~ 4 000 cm–1范围内采集光谱,扫描32次;BET条件:相对压力(P/P0)0 ~ 1下测定材料在超低温77 K对氮气的吸附解吸。
1.3 ZIF-67和土壤对TCE的吸附试验 1.3.1 TCE饱和蒸气的制备与浓度计算TCE饱和蒸气的制备参考Tang等[13]方法,具体如下:用移液枪移取20 mL TCE注入5 L的带有垫片密封盖的玻璃瓶中,置于25 ℃生化培养箱内1 d左右使其达到平衡,保持玻璃瓶底部始终有液体存在,玻璃瓶上方即为TCE饱和蒸气。TCE饱和蒸气的浓度是先根据Antoine公式[14]计算出TCE在25℃下的饱和蒸气压,再根据理想气体状态方程转化的推导公式得出:PM=ρRT,式中,P为气体的压强(Pa),M为气体的摩尔质量(kg/mol),ρ为气体的浓度(kg/m3),R为摩尔气体常数(J/(mol·k)),T为热力学温度(K),由此,TCE在25℃下的饱和蒸气浓度为525 mg/L。
1.3.2 TCE标准水溶液的制备取TCE标准品约5 mL置于100 mL广口瓶中,添加去离子水至瓶口附近,随后将广口瓶置于25℃、140 r/min恒温摇床中,连续振荡1 d后保持25℃静置,此时广口瓶中液体分层,上层水溶液为饱和溶液,其浓度为1 198 mg/L[15]。然后,将TCE饱和溶液稀释为10 mg/L的标准溶液,作为萃取试验的储备液。
TCE的标线配制:分别取10 mg/L的标准溶液6、60、180、360、480 μL加入含有60 mL去离子水的盐水瓶中,配制浓度为1、10、30、60、80 ng/mL的TCE水溶液,放置于25 ℃的生化培养箱中平衡12 h待测,设置3组平行。
1.3.3 ZIF-67和土壤对TCE吸附试验ZIF-67材料或土壤对气态TCE的吸附等温线试验采用批平衡法[16]进行:称取3 mg ZIF-67或1 g土壤样品置于100 mL盐水瓶中,用注射器从盐水瓶中抽出一定体积的空气,同时注入相同体积的TCE饱和蒸气(1 ~ 10 mL),具体步骤参考Tang等[13]方法,盐水瓶用铝盖和聚四氟乙烯塞密封。试验设置3组平行,2组空白,制备的样品放在25 ℃的生化培养箱内平衡1 h,然后测定瓶中气相TCE浓度。
1.4 萃取纤维制备根据文献[17]报道的方法,采用物理涂敷法制备ZIF-67涂层纤维。首先,将不锈钢针(直径0.25 mm)一端(1 cm)用氢氟酸常温处理5 h,使其从光滑的银白色表面变成黑色粗糙多孔的表面,以利于与涂层材料的结合;再用乙醇和超纯水分别超声洗涤15 min,后将清洁后的不锈钢针在室温下干燥过夜。
固相微萃取纤维的制备参考程虎[18]的方法:称取0.25 g硅酮密封胶置于2 mL离心管,用1.2 mL环己烷稀释,于涡旋振荡仪振荡10 min,取上清液倒入新的2 mL离心管中;将氢氟酸处理过的不锈钢针的前端1 cm插入上述溶液中,旋转一周立即取出,于称量纸上擦拭去除多余的中性硅酮胶,然后插入ZIF-67粉末中,反复旋转并轻轻按压以获得均匀的涂层;取出并去除不锈钢针上多余的ZIF-67,置于烘箱中90 ℃固化20 min。重复以上步骤2次,得到ZIF-67固相微萃取纤维,然后将固相微萃取纤维固定在商业SPME装置上,并在氮气保护下于240 ℃的GC进样口中预处理1 h,备用。
1.5 SPME萃取试验 1.5.1 水体系中TCE的萃取条件为了研究水溶液中TCE的最佳萃取温度,取10 mg/L的TCE标准溶液6 μL加入到含有60 mL去离子水的盐水瓶中,配置成浓度为1 ng/mL的TCE水溶液,用聚四氟乙烯塞加铝盖密封,设置3组平行;将盐水瓶放入恒温加热磁力搅拌器中,将ZIF-67涂层纤维插入盐水瓶中,分别在20、40、60、80 ℃下静置萃取10 min;萃取完成后取出纤维并迅速插入GC-ECD进样口,静态解吸6 min后运行GC测定程序。
试验步骤同上,为了研究水溶液中TCE的最佳萃取时间,在最佳萃取温度条件下,萃取浓度为1 ng/mL的TCE水溶液,分别在静置和在167 r/min搅拌条件下萃取10、20、30、40和50 min后进行解吸测定。
同样,为了研究水溶液中TCE的最佳萃取搅拌速率,配制浓度为10 ng/mL的TCE水溶液,在最佳萃取温度和萃取时间下,分别以0、167、333、500、666 r/min的搅拌速率萃取10 min后进行解吸测定。
水溶液中TCE的萃取等温线:将60 mL去离子水加入到一系列盐水瓶中,分别加入10 mg/L浓度的TCE标准溶液6、60、180、360和480 μL,得到浓度分别为1、10、30、60、80 ng/mL的TCE水溶液,用聚四氟乙烯塞子加铝盖密封,放入25 ℃培养箱平衡12 h。萃取前,用50 μL的进样针从盐水瓶中抽取10 μL顶空气体于气相色谱进样分析,然后继续对TCE相同浓度批次的盐水瓶进行固相微萃取试验,将涂有ZIF-67的纤维插入盐水瓶中,在60 ℃温度下进行30 min的顶空萃取。萃取完成后,迅速取出萃取纤维并插入GC-ECD进样口,静态解吸6 min后运行GC测定程序。
1.5.2 水土体系中TCE的萃取条件水土体系中TCE的测定参考土壤和沉积物中挥发性有机物的测定方法(顶空/气相色谱‒质谱法(HJ642—2013)[19]),即在顶空进样之前向土壤或沉积物中加入氯化钠水溶液。因此,本研究分别取0.5 g烘干的6 m和22 m深度土壤加入到盐水瓶中,同时加入60 mL去离子水和6 μL浓度为10 mg/L的TCE水溶液,放入25 ℃摇床,平衡后,将涂有ZIF-67的纤维插入盐水瓶中,分别在20、40、60和80 ℃下静置萃取10 min。萃取完成后,迅速取出萃取纤维并插入GC-ECD进样口进行解吸测定。试验设置3组平行。
试验步骤同上,为了研究水土体系中TCE最佳萃取搅拌速率,在最佳萃取温度条件下,分别以0、167、333、500、666 r/min的搅拌速率萃取10 min后进行解吸测定。
同样,为了研究水土体系TCE萃取的动力学特征,在最佳萃取温度和搅拌速率下分别萃取10、20、30、40和50 min后进行解吸测定。
1.5.3 水体系和水土体系的加标回收试验水体系:选择南京江宁汤山街道仙桃云谷农业园附近一处地表水作为实际样品,取10 mg/L TCE标准溶液加入到上述水样中,配制成1、10、50 ng/mL 3个不同浓度的TCE水溶液,放入摇床平衡12 h待测。
水土体系:取南京江宁景明大街一处土壤,风干研磨过筛,先称取0.5 g置于100 mL盐水瓶中,加入60 mL去离子水混合均匀,再分别加入6、60、300 μL浓度为10 mg/L的TCE标准溶液,配制成TCE浓度为1、10、50 ng/mL的3个不同浓度的TCE水土溶液,加盖密封,放入摇床平衡12 h待测。
1.6 气相色谱分析条件TCE定量分析采用配备电子捕获检测器(ECD)和Cerity QA-QC化学工作站的Agilent 6820气相色谱仪(GC-ECD),配以HP-5MSI柱(30 m × 0.25 mm × 0.25 μm)测定TCE浓度。仪器条件:进样口和检测器的温度分别为240 ℃和300 ℃,柱箱程序温度为40 ℃,保持2 min,以20 ℃/min升温至80 ℃,保持2 min。
1.7 数据处理与统计分析利用Origin处理多组吸附等温线数据,并进行数据拟合,采用决定系数R2来检验模型的拟合程度。
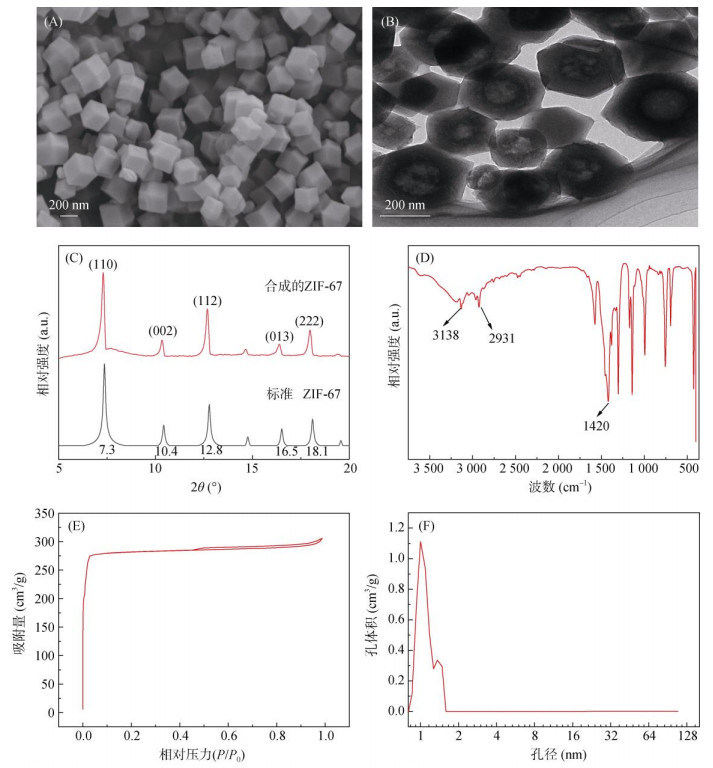
2 结果与讨论 2.1 ZIF-67材料的晶体结构和形貌特征ZIF-67的SEM图和TEM图如图 1A和图 1B所示。ZIF-67样品由纳米级晶体组成,粒径在100 ~ 300 nm,这些晶体具有相对光滑平坦的表面,并具有近似菱形十二面体形状。ZIF-67的XRD图谱如图 1C所示,本研究合成材料在7.3°、10.4°、12.8°、16.5°和18.1°处出现典型而尖锐的ZIF-67特征衍射峰,对应于ZIF-67的(110)、(002)、(112)、(013)和(222)晶面,所有特征峰与之前报道的标准ZIF-67特征衍射峰[20]相匹配,表明本研究在常温条件下成功合成了ZIF-67晶体。
|
图 1 ZIF-67材料的SEM图(A)、TEM图(B)、XRD图(C)、FTIR光谱图(D)、N2吸附解吸等温线(E)和孔径分布(F) Fig. 1 The Characteristics of ZIF-67 material: SEM(A), TEM(B), XRD(C), FTIR(D), N2 adsorption-desorption isotherm(E)and pore size distribution(F) |
ZIF-67的FTIR光谱如图 1D所示,在600 ~ 1 500 cm–1范围内的峰是咪唑基团的拉伸和弯曲振动,其中1 420 cm–1处为2-甲基咪唑中的C–H键伸缩振动产生的吸收峰;而在2 931 cm–1和3 138 cm–1处为脂族和芳香族咪唑基团的C–H伸缩振动峰。
ZIF-67的N2吸附–脱附等温线如图 1E所示,其吸附等温线属于Ⅰ型,在较低的相对压力下N2吸附量急剧增加,说明ZIF-67是微孔结构[21]。图 1F是样品的孔径分布曲线,ZIF-67的微孔孔径分布在0.8 ~ 2 nm范围内,属于微孔范围。ZIF-67的微孔体积为0.37 cm3/g,BET比表面积为1 132 m2/g。
不锈钢针和ZIF-67改性的不锈钢针表面形貌特征SEM图如图 2所示。ZIF-67在不锈钢针表面分布均匀,且涂敷后不锈钢针直径有所增加,由原来的256.44 μm (图 2A)增大到302.70 μm (图 2C),ZIF-67涂层厚度约为23 μm。进一步放大SEM观察倍数后,可以清晰地看到ZIF-67在不锈钢针表面上呈现无序堆积状态,形成缝隙,使得表面呈现粗糙多孔的特征(图 2B和图 2D),这种结构为TCE提供了丰富的吸附位点和空间,有助于提高其富集效果。

|
图 2 固相微萃取纤维的SEM图:放大1 000倍的不锈钢针(A);放大20 000倍的不锈钢针(B);放大800倍的ZIF-67涂层探针(C)和放大20 000倍的ZIF-67涂层探针(D) Fig. 2 The SEM images of solid phase microextraction fiberstainless steel needle magnified 1 000 times(A), stainless steel needle magnified 2 0000 times (B), ZIF-67 coated probe magnified 800 times (C)and ZIF-67 coated probe magnified 2 0000 times(D) |
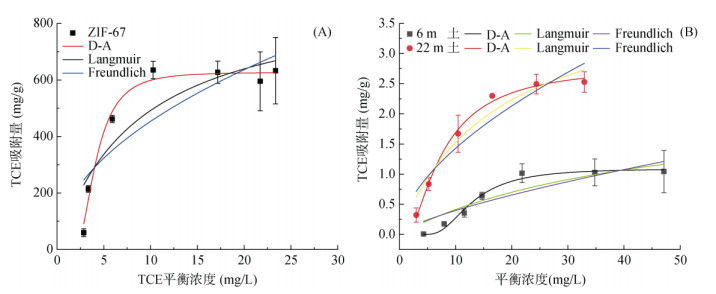
ZIF-67对气态TCE的吸附等温线如图 3所示,随着气相中TCE浓度的增加,ZIF-67材料对气态TCE的吸附量呈现出迅速增长的趋势,并在达到一定的浓度后进入平衡状态。为了更好地描述这一吸附过程,本文采用了3种等温模型Langmuir模型、Freundlich模型和Dubinin-Astakhov(D-A)模型的非线性形式进行拟合,具体的等温模型公式如表 1所示,其拟合参数如表 2所示。
|
图 3 TCE在ZIF-67上的吸附等温线(A)及TCE在不同深度土壤上的吸附等温线(B) Fig. 3 Adsorption isotherms of TCE on ZIF-67 (A) and adsorption isotherm of TCE on soils with various depths (B) |
|
|
表 1 3种吸附等温线模型 Table 1 Three adsorption isotherm models |
|
|
表 2 ZIF-67对TCE吸附等温模型拟合结果 Table 2 Fitting results of TCE adsorption isotherm models onto ZIF-67 |
从表 2和图 3可以看出,D-A模型对ZIF-67吸附TCE的等温线拟合效果最佳,相关系数高达0.98,这表明TCE在ZIF-67上的吸附机制主要遵循微孔填充理论。TCE的分子动力学直径为0.66 nm[22],略小于ZIF-67孔道直径,因此TCE可以有效进入ZIF-67微孔孔道。此外,ZIF-67具有较大的比表面积和微孔结构,可为TCE提供更多的吸附点位和空间。D-A模型计算的最大饱和吸附量达626 mg/g,远超过目前所报道的大多数材料,如疏水性超交联聚合物在干燥条件下吸附TCE的最大饱和吸附量为378 mg/g[23],生物质炭吸附TCE的最大饱和吸附量30.74 mg/g[24],Mg(OH)2负载的硫化纳米零价铁吸附TCE的最大饱和吸附量为253.55 mg/g[25]。
两种不同深度(6 m和22 m)的土壤对气态TCE的吸附等温线如图 4所示,随着气相中TCE浓度的增加,两种土壤对气态TCE的吸附量呈增长的趋势,并在达到一定的浓度后进入平衡状态,且D-A模型的非线性拟合最佳(R2 > 0.98)(表 2),且由于22 m深度的土壤对TCE的最大饱和吸附量大于6 m深度土壤对TCE的吸附量,说明22 m的土壤对TCE的吸附固定能力更强。大量的研究表明,土壤对挥发性有机污染物的吸附性能跟土壤有机质含量有关,即使土壤中的有机质经过氧化去除一部分,其吸附能力仍然受到土壤中有机质含量影响[26]。
|
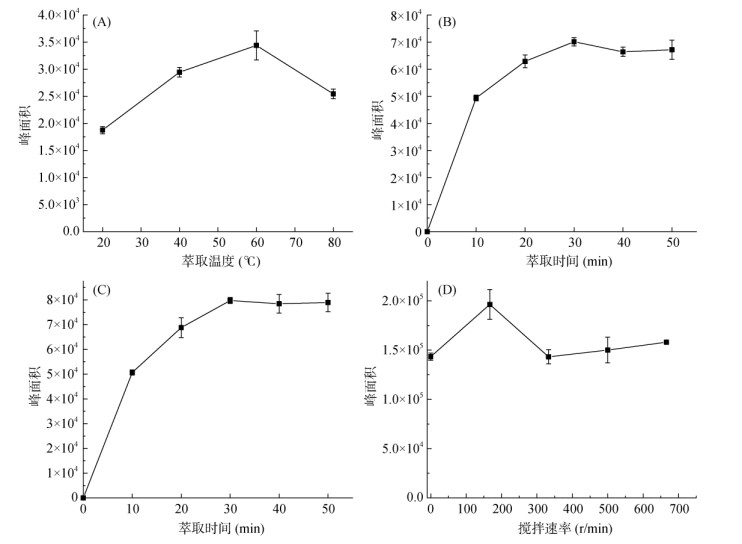
图 4 水体系中不同萃取温度(A)、静置条件下不同萃取时间(B)、搅拌速率为167 r/min条件下不同萃取时间(C)及不同搅拌速率(D)对ZIF-67涂层纤维顶空固相微萃取效率的影响 Fig. 4 Effects of different extraction temperatures (A), different extraction time under static conditions (B), different extraction time at a stirring rate of 167 r/min (C) and different stirring rates (D) in the water system on the TCE extraction efficiency of HS-SPME of the ZIF-67 coated fiber |
为了研究水体系中TCE固相微萃取最佳的萃取条件,本研究利用ZIF-67涂层纤维对1 ng/mL TCE水溶液进行萃取试验,考察萃取温度、萃取时间以及搅拌速率对TCE萃取效率的影响。在ZIF-67对TCE的吸附试验中,设置气相色谱进样口的温度为240 ℃,测定1个样品的运行时间为6 min,通过萃取预试验发现,用同一台气相色谱采用相同的程序升温时,在进样口解吸6 min,GC-ECD出峰效果很好。因此,后续进样方法采用相同的色谱检测条件,设置解吸温度为240 ℃,解吸时间为6 min。
水中不同萃取温度下ZIF-67涂层纤维对TCE萃取效率的影响如图 4A所示。随着温度升高,萃取效率逐渐提高,在萃取温度为60 ℃时,萃取效率达到最大值。这主要是由于随着温度升高,TCE更容易从水中挥发到顶空,从而有利于ZIF-67对气态TCE的吸附。然而当萃取温度进一步提高时,ZIF-67萃取纤维对TCE的萃取效率逐渐降低,这是由于温度过高,使得气态TCE容易从ZIF-67中热脱附进入顶空,不利于其对TCE的吸附萃取。因此,本研究确定水体系中ZIF-67涂层纤维对TCE的最佳萃取温度为60 ℃。
水体系中不同萃取时间下静置和搅拌速率为167 r/min条件下ZIF-67涂层纤维对TCE的萃取效果如图 4B和4C所示。可见,静置和搅拌速率167 r/min条件下的萃取效率变化趋势基本相同,但是在搅拌条件下的萃取效率略高于静置状态。随着萃取时间的增加,TCE的萃取效率逐渐升高,当萃取时间达到30 min,TCE的萃取效率达到最大,并趋于平衡;之后,随着萃取时间的继续延长,ZIF-67涂层纤维对TCE的萃取量基本保持不变。因此,试验确定水体系中ZIF-67涂层纤维对TCE的最佳萃取时间为30 min。
水体系中不同搅拌速率下ZIF-67涂层纤维对TCE的萃取效率如图 4D所示。当搅拌速率为167 r/min时,达到最佳萃取效率,搅拌速率大于167 r/min时,ZIF-67纤维涂层对TCE的萃取效率下降。这是由于搅拌速度过快,产生的气泡和涡流会降低TCE与涂层的接触[17]。因此,试验确定水体系中ZIF-67涂层纤维萃取TCE的最佳搅拌速率为167 r/min。
在水体系中TCE最佳萃取条件下,即萃取温度60 ℃、搅拌速率167 r/min、萃取时间30 min下,本研究对一系列不同浓度的TCE标准水溶液进行萃取分析,通过外标法,建立了对TCE的GC-ECD顶空萃取分析方法,分析结果如表 3所示,TCE在1 ~ 80 ng/mL浓度范围具有良好的线性关系,相关系数R2达到0.993 2,检出限为0.43 ng/mL,显示出高灵敏度。为了验证方法的准确性,进一步对1 ng/mL的TCE水溶液进行萃取测定(表 3),结果显示,采用单根ZIF-67涂层纤维平行测定3次,测定结果相对标准偏差(RSD)为2.3%;采用3支纤维进行测定时,RSD为7.2%,该方法具有较高的精密度和可靠性。以上结果表明,本研究建立的ZIF-67固相微萃取方法具有精确可靠、线性范围宽、富集能力强等优点。
|
|
表 3 基于ZIF-67涂层纤维的SPME-GC-ECD法测定TCE的分析参数(n=3) Table 3 Analytical parameters of SPME-GC-ECD for the determination of TCE based on ZIF-67 coated fiber |
为了进一步评估本研究方法在实际水样TCE萃取中的适用性,通过加标回收试验,考察了方法的准确度(表 4),结果显示,TCE加标回收率为69.6% ~ 101.8%,相对标准偏差≤4.1%,这表明该固相微萃取方法适用于实际环境水样TCE的分析。
|
|
表 4 TCE在环境水样中3个浓度水平下的加标回收率及精密度(n=3) Table 4 The recovery rates and precision of TCE at three levels in environmental water samples |
与水体系下试验类似,本研究利用ZIF-67涂层纤维对水土体系中TCE进行萃取,考察了萃取温度、萃取时间以及搅拌速率对萃取效率的影响,仪器各参数条件与水体系试验相同。
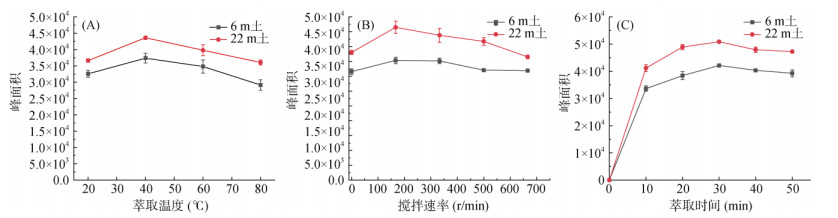
水土体系中不同取温度下ZIF-67涂层纤维对TCE萃取效率的影响如图 5A所示,随着温度升高,萃取效率升高,在60 ℃时达到最大值,然后逐渐下降。因此,试验确定60℃为水土体系下ZIF-67涂层纤维对TCE的最佳萃取温度。
|
图 5 水土体系中不同萃取温度(A)、不同搅拌速率(B)及不同萃取时间(C) 对ZIF-67涂层纤维顶空固相微萃取TCE效率的影响 Fig. 5 Effects of Different extraction temperatures (A), and different stirring ratesand (B), different extraction time(C) in the water-soil system on the TCE extraction efficiency of HS-SPME of the ZIF-67 coated fiber |
不同搅拌速率下ZIF-67涂层纤维对TCE的萃取效率如图 5B所示。当搅拌速率为167 r/min时,达到最佳萃取效率;当搅拌速率大于167 r/min时,纤维涂层的萃取效率下降。因此,试验确定水土体系下ZIF-67涂层纤维萃取TCE的最佳搅拌速率为167 r/min。
水土体系不同萃取时间下ZIF-67涂层纤维对TCE萃取效率如图 5C所示。随着萃取时间的增加,TCE的萃取效率逐渐升高,当萃取时间达到30 min时,TCE的萃取效率达到最大,并趋于平衡;之后,随着萃取时间的继续延长,ZIF-67纤维涂层对TCE的萃取量基本保持不变。因此,试验确定水土体系下ZIF-67涂层纤维对TCE的最佳萃取时间为30 min。
为了进一步评估该方法在实际土样中对TCE的萃取效果,在水土体系TCE最佳萃取条件(60℃、167 r/min、30 min)下对实际土样中的TCE进行萃取,加标回收试验显示,本研究建立的ZIF-67固相微萃取方法的加标回收率为84.01% ~ 111.83%,相对标准偏差≤5.28%(表 5),表明该固相微萃取方法可以用于土壤样品中TCE的萃取分析。
|
|
表 5 TCE在环境土样中3个水平下的加标回收率及精密度(n=3) Table 5 The recovery rates and precision of TCE at three levels in environmental soil samples |
与水体系中TCE的萃取效率相比(图 4和图 5),水土体系中TCE的萃取效率低于水体系,这一现象主要归因于土壤对TCE的吸附作用,即使增加萃取温度和萃取时间,仍有部分TCE因土壤的吸附而难以释放至空气中,从而影响了固相微萃取的效能。此外,土壤的吸附能力越强,其对TCE的萃取效率影响越大,导致萃取效率也越低。这是由于挥发性有机污染物在水土气三相间的分配是决定其运移的重要因素,且污染物与土壤间的非平衡吸附解吸是影响其运移的重要机制[27]。但是,无论水体系中还是水土体系中TCE的固相微萃取加标回收率仍然较高,说明本研究建立的ZIF-67固相微萃取方法适用于水、土体系中TCE的固相微萃取。
3 结论本研究常温条件下合成的ZIF-67材料,具有较高的比表面积和微孔结构,对TCE具有出色的吸附性能。TCE在ZIF-67材料的吸附等温线符合D-A模型,其最大饱和吸附量高达626 mg/g。通过物理涂敷法制备的ZIF-67固相微萃取涂层,与GC-ECD联用,是一种低检出限、高重复性的TCE检测方法。在水体系和水土体系中ZIF-67涂层纤维对TCE的最佳萃取温度均为60 ℃,最佳萃取时间均为30 min。土壤对TCE吸附能力越高,越不利于TCE的萃取。但是无论是水体系中还是水土体系中,TCE的固相微萃取加标回收率仍然较高,说明本研究建立的ZIF-67固相微萃取方法适用于水、土体系中TCE的固相微萃取,其可为水体和土壤中微量TCE的固相微萃取等提供技术参考。
| [1] |
Hou D B, Cui X D, Liu M, et al. Degradation of trichloroethylene by biochar supported nano zero-valent iron (BC-nZVI): The role of specific surface area and electrochemical properties[J]. Science of the Total Environment, 2024, 908: 168341 DOI:10.1016/j.scitotenv.2023.168341 (  0) 0) |
| [2] |
钱翌, 岳飞飞, 褚衍洋. 三氯乙烯环境污染修复技术研究进展[J]. 环境化学, 2012, 31(9): 1335-1343 (  0) 0) |
| [3] |
赵玲, 滕应, 骆永明. 我国有机氯农药场地污染现状与修复技术研究进展[J]. 土壤, 2018, 50(3): 435-445 DOI:10.13758/j.cnki.tr.2018.03.001 (  0) 0) |
| [4] |
葛锋, 张转霞, 扶恒, 等. 我国有机污染场地现状分析及展望[J]. 土壤, 2021, 53(6): 1132-1141 DOI:10.13758/j.cnki.tr.2021.06.005 (  0) 0) |
| [5] |
张悦, 宋志花, 王艺晓, 等. 基于色谱技术的典型环境污染物快速检测研究新进展[J]. 分析试验室, 2022, 41(3): 341-349 (  0) 0) |
| [6] |
杜洁, 孙鹏超, 张梦露, 等. 多孔氮化硼掺杂聚吡咯-2, 3, 3-三甲基吲哚固相微萃取涂层的制备及多环芳烃的检测[J]. 色谱, 2023, 41(9): 789-798 (  0) 0) |
| [7] |
况逸馨, 周素馨, 胡亚兰, 等. 衍生多孔碳材料在固相微萃取中的应用研究进展[J]. 色谱, 2022, 40(10): 882-888 (  0) 0) |
| [8] |
白璟, 林子俺. 共价有机骨架材料在样品前处理中的研究进展[J]. 色谱, 2019, 37(12): 1251-1260 (  0) 0) |
| [9] |
樊花, 刘红妹. 金属有机骨架及其复合材料在固相微萃取中的制备及应用[J]. 分析测试技术与仪器, 2019, 25(2): 78-85 (  0) 0) |
| [10] |
李金花, 温莹莹, 陈令新. 分子印迹聚合物固相萃取研究进展[J]. 色谱, 2013, 31(3): 181-184 (  0) 0) |
| [11] |
张贺, 李国良, 张可刚, 等. 金属有机骨架材料在吸附分离研究中的应用进展[J]. 化学学报, 2017, 75(9): 841-859 (  0) 0) |
| [12] |
Ethiraj J, Palla S, Reinsch H. Insights into high pressure gas adsorption properties of ZIF-67: Experimental and theoretical studies[J]. Microporous and Mesoporous Materials, 2020, 294: 109867 (  0) 0) |
| [13] |
Tang X J, Cao A C, Zhang Y, et al. Soil properties affect vapor-phase adsorption to regulate dimethyl disulfide diffusion in soil[J]. Science of the Total Environment, 2022, 825: 154012 (  0) 0) |
| [14] |
陈庚华, 杜志强, 韩世钧. 纯物质饱和蒸汽压数据的关联—用线性优化法求Antoine公式中的常数[J]. 浙江大学学报, 1985, 19(3): 92-97 (  0) 0) |
| [15] |
Scheutz C, Durant N D, Hansen M H, et al. Natural and enhanced anaerobic degradation of 1, 1, 1-trichloroethane and its degradation products in the subsurface–A critical review[J]. Water Research, 2011, 45(9): 2701-2723 (  0) 0) |
| [16] |
Wang Q X, Gao S D, Wang D, et al. Mechanisms for 1, 3-dichloropropene dissipation in biochar-amended soils[J]. Journal of Agricultural and Food Chemistry, 2016, 64(12): 2531-2540 (  0) 0) |
| [17] |
余晨. 基于共价有机骨架及其复合材料的固相微萃取探针的制备及其在环境分析中的应用[D]. 武汉: 武汉工程大学, 2022.
(  0) 0) |
| [18] |
程虎. 基于固相微萃取原位表征土壤有机污染物生物有效性与新型探针制备研究[D]. 北京: 中国科学院大学, 2019.
(  0) 0) |
| [19] |
环境保护部. 土壤和沉积物挥发性有机物的测定(顶空/气相色谱‒质谱法): HJ642-2013[S]. 北京: 中国标准出版社, 2013.
(  0) 0) |
| [20] |
Li Y B, Jin Z L, Zhao T S. Performance of ZIF-67–Derived fold polyhedrons for enhanced photocatalytic hydrogen evolution[J]. Chemical Engineering Journal, 2020, 382: 123051 (  0) 0) |
| [21] |
Tian Y, Li J X, Li X, et al. ZIF-8/ZIF-67 solid electrolyte ozone sensor at room temperature[J]. Sensors and Actuators A: Physical, 2023, 354: 114281 (  0) 0) |
| [22] |
Liu Y, Johnson N W, Liu C, et al. Mechanisms of 1, 4-dioxane biodegradation and adsorption by bio-zeolite in the presence of chlorinated solvents: Experimental and molecular dynamics simulation studies[J]. Environmental Science & Technology, 2019, 53(24): 14538-14547 (  0) 0) |
| [23] |
Lu S C, Liu Q L, Han R, et al. Potential applications of porous organic polymers as adsorbent for the adsorption of volatile organic compounds[J]. Journal of Environmental Sciences, 2021, 105: 184-203 (  0) 0) |
| [24] |
Ahmad M, Lee S S, Dou X M, et al. Effects of pyrolysis temperature on soybean stover- and peanut shell-derived biochar properties and TCE adsorption in water[J]. Bioresource Technology, 2012, 118: 536-544 (  0) 0) |
| [25] |
Zhang S B, Wang T X, Guo X, et al. Adsorption and reduction of trichloroethylene by sulfidated nanoscale zerovalent iron (S-nZVI) supported by Mg(OH)2[J]. Environmental Science and Pollution Research, 2023, 30(6): 14240-14252 (  0) 0) |
| [26] |
丁浩然, 王磊, 龙涛, 等. 活化过硫酸钠氧化土壤对挥发性有机污染物吸附特性的影响[J]. 土壤学报, 2015, 52(2): 336-344 (  0) 0) |
| [27] |
彭胜, 陈家军, 王红旗. 挥发性有机污染物在土壤中的运移机制与模型[J]. 土壤学报, 2001, 38(3): 315-323 (  0) 0) |
2. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 211135, China
 2025, Vol. 57
2025, Vol. 57


