2. 中国科学院大学, 北京 100049
东北地区作为我国重要的商品粮基地,因侵蚀作用导致氮、磷、钾及有机质等土壤养分大量流失,耕地生产力严重退化[1]。生物质炭和腐植酸是应用较多的提升土壤地力、改善土壤质量的外源有机物料[2-3]。生物质炭具有疏松多孔、比表面积大、含碳丰富等特性[4]。腐植酸同样为优质碳源,虽无生物质炭疏松多孔的结构与庞大的比表面积,但其作为生物刺激剂的一种,能够促进作物的自然生理代谢,增强营养物质的吸收及利用[5]。
研究表明,辽宁省棕壤地区农田氮肥利用率不足40%,约20% 的氮肥可能以氨(NH3)、氧化亚氮(N2O)等气态形式损失[6]。土壤NH3挥发是由尿素快速分解导致NH4+累积产生的。NH3是大气中最重要的还原型活性氮,也是形成次生无机铵盐的重要气体前驱体[7]。这类无机铵盐占PM2.5质量的40%,会对大气质量和人类健康造成不利影响[8]。N2O是一种具有高增温潜势的温室气体,会对臭氧层造成破坏[9]。虽然其在大气中的含量很低,但其温室效应是等质量CO2气体的265倍[10],具有较强的温室效应潜能,是农业源主要温室气体之一[11]。因此,降低农田NH3和N2O排放对改善生态环境和农业生产具有重要意义。
目前,许多研究通过应用硝化抑制剂调控氮素在土壤中的转化进程,以降低土壤NH3和N2O排放[12-13]。硝化抑制剂可以通过抑制硝化反应过程,延缓NH4+向NO3–的转化,减少因NO3–累积过多而造成的N2O排放量增加[14]。Friedl等[15]与Akiyama等[16]的研究均指出,3, 4-二甲基吡唑磷酸盐(DMPP)可以减少超过50% 的土壤N2O排放量。Meta分析结果显示,硝化抑制剂双氰胺(DCD)和DMPP分别显著减少了44.7% 和47.6% 的土壤N2O排放量[17]。高粱根系分泌物中的对羟基苯丙酸甲酯(MHPP)是一种近期发现的新型生物硝化抑制剂,已被证实在降低N2O排放方面具有一定的效果[18]。Yao等[19]研究指出,施用MHPP极大地降低了土壤N2O排放速率的峰值,其N2O总排放量比不施用MHPP低79%。相比于DCD和DMPP,MHPP对紫色土N2O产生速率表现出更强的抑制效果[20]。但也有研究指出,MHPP对N2O的减排效果没有化学硝化抑制剂显著[21]。且已有研究证明,单独施用硝化抑制剂易增加土壤NH3挥发风险[22]。然而,有机物料与硝化抑制剂配合施用对土壤氮素转化过程及氮素气态损失的影响尚不明确,值得进一步探讨。
基于以上,本研究以东北棕壤为研究对象,通过室内培养试验,探究了不同硝化抑制剂与不同有机物料配施对土壤氮素转化过程及N2O、NH3排放的影响及其机制,以期为减少我国东北棕壤氮素气态损失、提高氮肥利用率提供科学依据和技术支撑。
1 材料与方法 1.1 供试材料供试棕壤采自辽宁省铁岭市昌图县(42°48′33′′ N,123°58′55′′E)。该地属辽北低丘平原,中温带大陆性季风气候,日照充足,四季分明,雨热同季。利用梅花形采样法采集表层土壤(0~20 cm),晾晒风干,筛去砾石与植物根系等杂物,用四分法分样后研磨、过筛,取过10目和100目筛土样分别用于土壤培养试验及土壤基本理化性质测定。土壤基本理化性质见表 1。
|
|
表 1 供试土壤基本理化性质 Table 1 Physicochemical properties of tested soil |
供试脲酶抑制剂正丁基硫代磷酸三胺(NBPT)、生物来源硝化抑制剂对羟基苯丙酸甲酯(MHPP)由希恩思生物科技公司生产;化学合成硝化抑制剂3, 4-二甲基吡唑磷酸盐(DMPP)由乐研公司生产。供试腐植酸由中向旭耀公司提供,为碱性腐植酸。供试生物质炭为在500 ℃条件下由玉米秸秆采用限氧裂解技术制得。腐植酸、生物质炭基本性质见表 2。
|
|
表 2 腐植酸、生物质炭基本性质 Table 2 Basic properties of humic acid and biochar |
于2023年6—10月开展室内培养试验,共设置7个不同处理,分别为:尿素(U)、尿素+DMPP+ NBPT(UDN)、尿素+MHPP+NBPT(UMN)、尿素+ DMPP+NBPT+腐植酸(UDNH)、尿素+MHPP+NBPT+腐植酸(UMNH)、尿素+DMPP+NBPT+生物质炭(UDNB)、尿素+MHPP+NBPT+生物质炭(UMNB)每个处理设置3个重复。其中,尿素施用量为N 0.5 g/kg,生物质炭施用量为土壤质量的1.2%,DMPP、MHPP、NBPT和腐植酸的添加量分别为尿素氮量的1%、5%、1% 和100%。
试验前,将MHPP用酒精溶解后均匀喷洒于尿素颗粒表面,自然风干备用。试验过程具体为:取过10目筛的风干土样补充水分(土壤含水率小于20%)进行预培养,预培养结束后测定土壤含水率。然后,称取240 g (干土重)土样,按试验设计添加尿素、抑制剂等外源物质并充分混合均匀,置于培养瓶中,补充水分至20% 土壤含水率(田间持水量70%),采集初始土样;后用封口膜封口,封口膜均匀扎10个小孔,保证通气环境,于恒温(25±2)℃)遮光室内培养110 d。其间,每隔2~5 d用称重法补充各处理水分,以保证瓶内水分含量保持在目标含水量。试验于培养后的第3、5、8、12、18、30、51、70、90、110天采集气体样品,测定N2O排放速率;同时破坏性采样法采集土壤样品,用于测定土壤NH4+-N、NO3–-N含量,计算土壤硝化抑制率。此外,于培养前期(第3、5、8、12、18、30天)测定土壤尿素态氮含量及土壤酶活性,并测定培养前19 d内的土壤NH3挥发量。
1.3 测定指标与方法各指标测定遵循《土壤农业化学分析方法》[23]。具体方法如下:土壤尿素态氮含量采用乙酸苯汞浸提–分光光度法测定。土壤无机氮(NH4+-N、NO3–-N)含量通过1 mol/L KCl浸提,分别采用靛酚蓝比色、紫外分光光度法测定。脲酶活性采用尿素–柠檬酸盐缓冲液培养,改良靛酚蓝比色法测定。依据双抗体夹心法原理[24],对硝化、反硝化过程中的6种酶包括氨单加氧酶、一氧化氮还原酶、羟胺氧化酶、硝酸还原酶、亚硝酸还原酶以及氧化亚氮还原酶采用酶联免疫分析(ELISA)试剂盒(江苏酶免实业有限公司)进行处理,酶标分析仪(Infinite F50)测定。
NH3的采集与测定:采用封闭式硫酸吸收法。用10 mL 0.02 mol/L H2SO4累积吸收土壤培养过程中从土壤中挥发的NH3,吸收时间根据NH3挥发规律在24~72 h之间调整,使用靛酚蓝比色法测定吸收液中的NH4+-N含量,即为土壤NH3挥发量。N2O的采集与测定:采用遮光培养法。采样前将培养瓶连接到真空泵上,抽真空后通入空气,重复3次,使瓶内气体与大气相平衡;采集初始气体样本作为背景值;将培养瓶密封后置于25℃恒温恒湿培养箱中黑暗密闭培养6 h,用25 mL针筒注射器反复3次抽提后,采集20 mL气体注入真空瓶内,使用气相色谱分析仪(Agilen 7890)测定N2O浓度[25]。
1.4 数据处理与分析土壤NH3挥发速率:
| $ E = c \times V \times {\text{ts}} \times {10^3}/m $ | (1) |
式中:E为NH3挥发速率,μg/(kg·d)(以单质氮量计,下同):c为NH4+-N测定浓度,mg/L:V为测定样品的定容体积,mL;ts为分取倍数;103为换算系数;m为土壤质量,g。
土壤NH3累积排放量:
| $ M = E \times t $ | (2) |
式中:E为NH3挥发速率,μg/(kg·d),t为每次连续测定的时间,d。
土壤N2O排放速率:
| $ F = \rho \times \Delta C/\Delta t \times 273.15/\left( {273.15 + T} \right) \times V/m $ | (3) |
式中:F为N2O挥发速率,μg/(kg·h) (以单质氮量计,下同);ρ为标准状态下N2O的密度,1.25 kg/m3;ΔC/Δt为培养瓶内N2O浓度变化率,109/h;V为培养瓶体积,m3;T为环境气温,℃;m为土壤质量,kg。
土壤N2O累积排放量:
| $ M = {F_1} \times 24 + \mathop \sum \limits_{i = 2}^n \left( {{F_i} + {F_{i - 1}}} \right) / 2 \times \left( {{t_i} - {t_{i - 1}}} \right) \times 24 $ | (4) |
式中:F1为培养第1天的N2O排放速率;Fi和Fi-1分别为培养时间ti和ti-1的N2O排放速率。
土壤硝化抑制率:
| $ N = \left( {A - B} \right)/A \times 100\% $ | (5) |
式中:N为土壤硝化抑制率,%;A为不添加硝化抑制剂处理土壤培养后NO3– -N含量,mg/kg;B为添加硝化抑制剂处理土壤培养后NO3– -N含量,mg/kg。
采用Excel 2021和SPSS 26.0软件对数据进行处理与统计分析,并采用Duncan法进行多重比较(P < 0.05),运用Origin 2021软件作图。
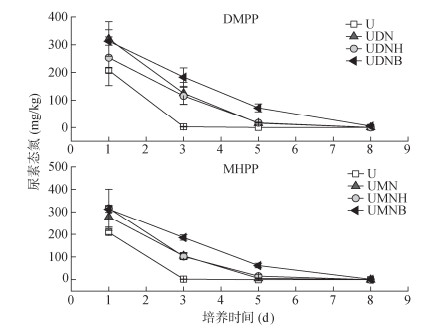
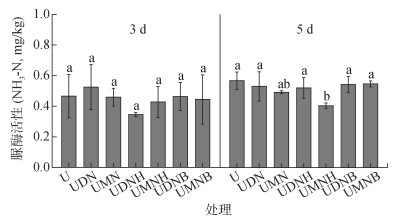
2 结果与分析 2.1 土壤中尿素态氮含量变化尿素施入土壤后的动态转化过程如图 1所示。各处理土壤尿素态氮含量均随时间的推移逐渐下降,在培养第8天时趋近于0,由此表明,第8天时尿素态氮几乎分解完全。DMPP处理组与MHPP处理组土壤尿素态氮含量变化趋势相近,均延缓了尿素的分解过程。其中,UDNB、UMNB处理在延缓尿素水解方面效果最佳。图 2为各处理施肥后第3、5天的土壤脲酶活性对比图。第3天时,各处理间脲酶活性无显著差异;第5天时,相较于U处理,各处理脲酶活性均有所下降,其中UMNH处理下降达显著水平。
|
(图中误差线表示3个重复的标准偏差;下同) 图 1 不同处理下土壤尿素态氮含量的变化趋势 Fig. 1 Trend of soil urea nitrogen content under different treatments |
|
(柱图上方不同小写字母表示不同处理间差异在P < 0.05水平下显著) 图 2 各处理培养前期土壤脲酶活性变化 Fig. 2 Changes in soil urease activity during the early stage of cultivation under each treatment |
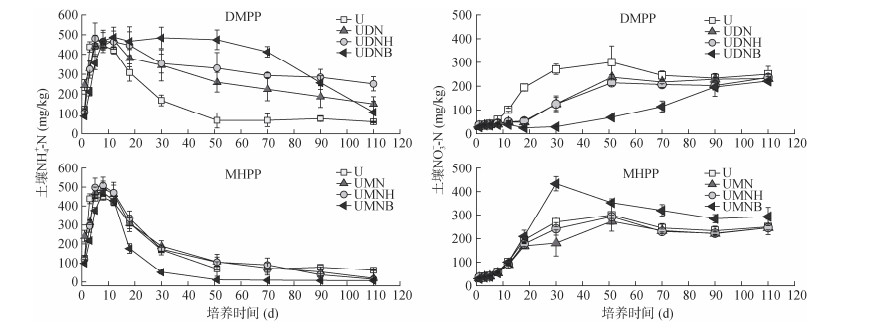
随着培养时间的推移,各处理土壤NH4+-N含量均表现出先增加后减少的趋势(图 3)。相较于U处理,UDN、UDNH、UDNB处理培养期内土壤NH4+-N含量始终处于较高水平。相较于UDN处理,UDNH、UDNB处理进一步延缓了NH4+-N的转化过程,UDNB处理中期(30~90 d)效果较好,UDNH处理后期(90 d后)效果更为稳定。MHPP处理组在延缓NH4+-N转化方面效果不及DMPP处理组。在整个培养期间,MHPP处理组的NH4+-N含量与U处理接近,一直处于较低水平,且处理间差异不大。
|
图 3 抑制剂与有机物料配施对土壤NH4+-N、NO3–-N转化的影响 Fig. 3 The effect of combined application of inhibitors and organic materials on transformations of NH4+-N and NO3–-N in soil |
土壤NO3–-N含量随时间的推移呈现先上升后略微下降的趋势。相较于U处理,UDN、UDNH、UDNB处理均抑制了土壤NO3–-N的形成。结合表 3可知,在培养的第18~30天,UDN、UDNH、UDNB处理对土壤硝化过程的抑制效率达到峰值,为72.40%~89.04%,抑制效果表现为UDNB > UDN > UDNH。UMN、UMNH、UMNB处理对土壤NO3–-N的抑制效果并不明显,硝化抑制率峰值仅为9.63%~ 33.00%(表 3)。值得注意的是,UMNB处理从培养的第12天起,硝化抑制效果已接近于0,培养后期未见硝化抑制效果,表明MHPP作用时间较短,后期有机物料对硝化过程的影响更大。
|
|
表 3 不同处理下的土壤硝化抑制率(%) Table 3 Soil nitrification inhibition rates under different treatments |
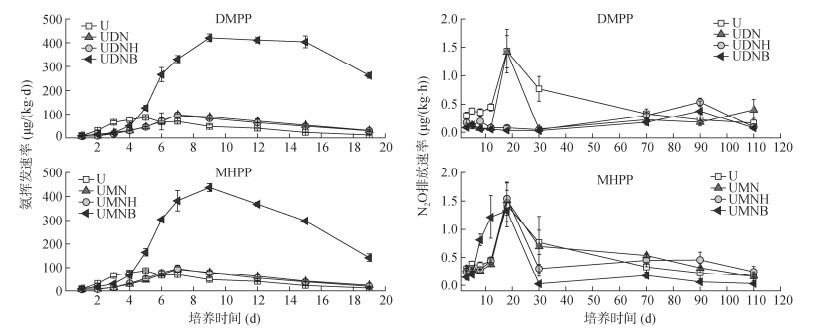
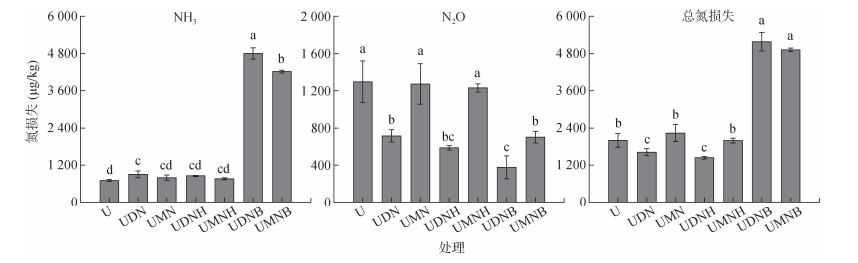
各处理的NH3挥发速率总体呈现出先上升后下降的趋势(图 4)。单施尿素(U)土壤NH3挥发速率在培养第5天时达到峰值,分别为0.087 μg/(kg·d)。DMPP处理组中,UDN、UDNH处理的变化趋势相同,土壤NH3挥发速率均在第7天时达到峰值,为0.098、0.096 μg/(kg·d);UDNB处理土壤NH3挥发速率显著高于其余各处理,且峰值时间出现推迟,在第9天时达到峰值,为0.42 μg/(kg·d)。MHPP处理组趋势与DMPP处理组相似,UMN、UMNH处理NH3挥发速率均在第7天达到峰值,分别为0.092、0.095 μg/(kg·d);UMNB处理在第9天达峰值,为0.44 μg/(kg·d)。结合土壤NH3排放总量可知(图 5),相较于U处理,各处理均增加了土壤NH3挥发损失风险。但UDNH、UMNH处理相较于UDN、UMN处理,有降低NH3排放的趋势。相反的,UDNB、UMNB处理显著提高了土壤NH3挥发量,增幅为496.92%、579.70%。由此表明,腐植酸有降低土壤NH3挥发的趋势,而生物质炭显著增加了土壤NH3挥发损失。
|
图 4 各处理土壤NH3挥发速率及N2O排放速率趋势 Fig. 4 Trends of NH3 volatilization rate and N2O emission rate under each treatment |
|
图 5 土壤气态氮损失总量对比 Fig. 5 Comparison of total loss of gaseous nitrogen in soil |
分析各处理施肥110 d内土壤N2O排放速率的变化趋势(图 4)发现,随着培养时间的推移,各处理土壤N2O排放速率总体均呈现先上升后下降的趋势。其中U、UDN处理土壤N2O排放速率峰值均出现在第18天,分别为1.43、1.42 μg/(kg·h)。UDNH、UDNB处理土壤N2O排放速率峰值均后移至第90天,分别为0.54、0.38 μg/(kg·h)。结合土壤N2O排放总量(图 5)可知,相较于U处理,DMPP处理组各处理均显著降低了土壤N2O排放量,降幅为44.83%~70.87%,且UDNB处理与UDN处理之间差异达显著水平,表明在施用抑制剂的基础上增施生物质炭可显著降低土壤N2O排放总量。MHPP处理组中,UMN、UMNH、UMNB处理土壤N2O排放速率均在第18天时出现峰值,分别为1.51、1.54和1.33 μg/(kg·h)。相较于U处理,UMN、UMNH、UMNB处理土壤N2O排放总量下降了1.82%~45.86%,其中UMNB处理与其他处理差异达显著水平。土壤总氮损失受NH3排放量的影响较大(图 5),相较于U处理,UDN、UDNH处理土壤总氮损失下降显著,UDNB、UMNB处理土壤总氮损失显著提高。
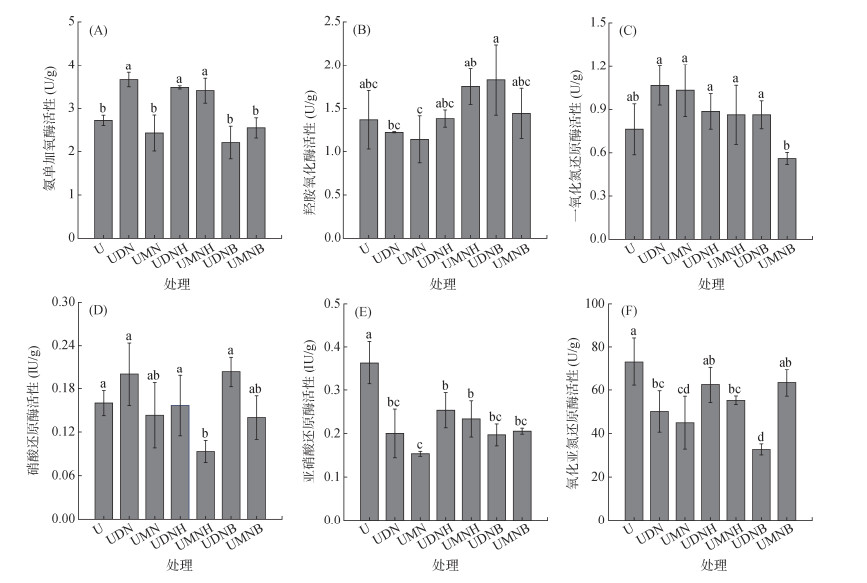
2.4 土壤中氮转化相关酶活性变化抑制剂与有机物料对培养第30天时土壤氮转化相关酶活性的影响如图 6所示。氨单加氧酶、羟胺氧化酶是控制土壤硝化过程的主要酶。UDN、UDNH、UMNH处理土壤氨单加氧酶活性显著高于U处理,增幅为25.14%~34.56%,其余各处理氨单加氧酶活性均较U处理有所下降,但差异未达显著水平。各处理羟胺氧化酶活性与U处理无显著差异,但UMNH、UDNB处理土壤羟胺氧化酶活性分别显著高于UMN和UDN处理。硝酸盐还原酶、亚硝酸盐还原酶、一氧化氮还原酶、氧化亚氮还原酶是控制土壤反硝化过程的关键酶。相较于U处理,除UMNB处理外,其余各处理土壤一氧化氮还原酶活性均有所上升,显著高于UMNB处理。UMNH处理硝酸还原酶活性较U处理显著下降41.67%,而UDN、UDNH、UDNB处理硝酸还原酶活性均显著高于UMNH处理。各处理土壤亚硝酸还原酶活性均显著低于U处理,降幅为30.28%~57.80%。除UDNH、UMNB处理外,其余各处理氧化亚氮还原酶活性均显著低于U处理,降幅为13.37%~55.35%。
|
图 6 培养第30天土壤氮转化相关酶活性对比 Fig. 6 Comparison of nitrogen conversion related enzyme activities on 30th day of cultivation |
本研究中,抑制剂与有机物料添加不仅延缓了尿素的分解过程,还抑制了土壤的硝化过程。其原因在于除对照(U)外,其余各处理均施用脲酶抑制剂NBPT,NBPT通过抑制土壤中的脲酶活性抑制了尿素的水解过程[26]。DMPP处理组硝化抑制率普遍高于MHPP处理组。DMPP作为化学合成硝化抑制剂,效果显著、作用时间长。而生物来源硝化抑制剂MHPP天然绿色,易被微生物降解利用,作用时间相对较短。且生物硝化抑制剂是植物–微生物根际互作中的特定化学信号物质,是植物根系感应到有利于硝化环境的因子后主动分泌的特定信号物质,用以调控根际硝化强度至适宜范围[27]。本研究为纯土壤体系,缺乏作物与土壤的互作关系,一定程度上限制了MHPP的硝化抑制效果。
与对照相比,抑制剂添加提高了土壤NH3挥发总量,其中UDN处理作用显著,这与已有研究结论相一致[22]。腐植酸与抑制剂配施对土壤NH3挥发无显著影响,但相比于单独施用抑制剂,腐植酸与抑制剂配施有降低土壤NH3挥发损失的趋势。有研究表明,腐植酸能以生物或非生物方式与土壤中的NH4+-N结合,增强土壤对NH4+-N的固持作用,从而减少氮素以NH3形式损失[28]。腐植酸分子中的羧基也能够提高土壤中NH4+-N的保留量[29]。生物质炭与抑制剂配施显著提高了土壤NH3挥发总量,增幅为496.9%~579.7%。土壤NH3挥发量与土壤NH4+-N含量呈正相关[30]。本研究中,生物质炭与DMPP配施极大程度上抑制了土壤硝化过程的进行,土壤NH4+-N含量显著提高,进而导致生物质炭处理NH3挥发量增加。此外,pH是制约土壤NH3排放的关键因素[31],二者之间呈正相关关系[32]。强碱性生物质炭的添加提高了土壤pH,致使UDNB、UMNB处理土壤NH3挥发量显著提高。生物质炭具有巨大的比表面积与丰富的孔隙度(表 2),施入土壤导致土壤容重降低,通气性增强,进一步加剧土壤NH3的排放[33]。
DMPP单施以及与腐植酸配施相较于对照均显著降低了土壤N2O排放总量,降幅分别为44.83% 和54.77%,而MHPP单施以及与腐植酸配施作用效果不显著,降幅仅分别为1.82% 和5.12%。土壤NO3–-N含量是制约土壤N2O排放的关键因素[34]。因DMPP具有较强的硝化抑制作用,土壤NO3–-N含量一直处于较低水平,N2O排放速率显著降低;而MHPP对土壤硝化过程的抑制效果并不显著,土壤NO3–-N含量较高,以至于N2O排放总量与对照处理差异不显著。此外,腐植酸还增加了土壤对NH4+-N的固持作用,降低了土壤硝化、反硝化过程中的氮素来源[26-27],进一步限制了土壤N2O的产生。本研究中,DMPP、MHPP单施以及DMPP与腐植酸配施,相较于对照,均显著降低了土壤亚硝酸还原酶活性。MHPP与腐植酸配施在降低土壤亚硝酸还原酶活性的同时,显著降低了土壤硝酸还原酶活性。硝酸还原酶、亚硝酸还原酶是反硝化过程的关键酶[35],二者活性的降低抑制了土壤反硝化过程,减少了土壤N2O的排放量。与对照相比,生物质炭与抑制剂配施显著降低了土壤N2O排放总量,降幅为45.86%~70.87%。前人研究表明,施用生物质炭可以降低反硝化产物中的N2O占比[36],最高可使反硝化产物比N2O/(N2O+N2)减少83.6%[37]。可能的机理是生物质炭能够改变与N2O还原相关的微生物群落和丰度[38];且生物质炭作为电子穿梭体,其还原性基团可以提供电子,促进微生物进行完全反硝化,降低土壤N2O排放量[39-40]。本研究中,生物质炭与抑制剂配施显著降低了土壤亚硝酸还原酶活性,抑制了土壤反硝化过程,降低了土壤N2O的产生。此外,pH是影响土壤N2O排放的因素之一,生物质炭添加后土壤pH上升,促使反硝化过程向着有利于N2的方向改变[41],进而降低了土壤N2O的排放总量。
4 结论棕壤中氮素转化与气态损失对不同抑制剂与有机物料的响应有明显差异。抑制剂不仅延缓了尿素态氮的分解,还抑制了土壤的硝化过程,且DMPP处理组效果优于MHPP处理组。抑制剂与有机物料能够通过改善土壤理化性质,影响土壤氮转化相关酶活性以及硝化与反硝化过程,进一步调节土壤NH3挥发和N2O排放。相比于对照,抑制剂提高了土壤氨挥发损失。抑制剂与腐植酸配施相较于抑制剂单独施用有降低土壤NH3挥发总量的趋势,但与生物质炭配施显著提高土壤NH3挥发总量。土壤N2O排放量主要受NO3– -N含量影响,MHPP处理组由于硝化抑制作用较弱,NO3– -N含量一直处于较高水平,致使土壤N2O排放量较对照降幅并不显著。相反,DMPP处理组由于较强的硝化抑制作用,显著降低了土壤N2O排放。生物质炭与抑制剂配合施用较抑制剂单独施用进一步降低了土壤N2O排放总量,腐植酸效果次之。但由于本试验为纯土壤体系,MHPP作为生物来源硝化抑制剂,在有无作物的培养体系中可能表现出截然不同的效果,抑制剂、有机物料与作物的互作关系对土壤氮素转化的影响值得进一步研究。总体而言,在东北地区偏酸性棕壤中施用DMPP减少了氮肥以N2O形式的气态损失,同时配施腐植酸减少了土壤NH3挥发总量,两者配合施用更有利于东北地区棕壤氮素固存。
| [1] |
张新乐, 钱蕾, 鲍依临, 等. 黑土区田块尺度耕地质量遥感监测与评价[J]. 土壤通报, 2020, 51(6): 1303-1312 (  0) 0) |
| [2] |
Wang Q, Hu X H, Ma Y H, et al. Enhancing sugar beet yield and quality in Northeast China: Investigating the synergistic impact of sugar mill filter mud and biochar on black soil[J]. Scientia Horticulturae, 2024, 326: 112680 DOI:10.1016/j.scienta.2023.112680 (  0) 0) |
| [3] |
Masmoudi S, Abid W, Medhioub K, et al. Compost derived from olive mill cake: Effects on isohumic soil quality based on humic acids characterization[J]. Heliyon, 2024, 10(16): e36456 DOI:10.1016/j.heliyon.2024.e36456 (  0) 0) |
| [4] |
Adak E, Halder S, Koley B, et al. An overview of the importance of biochar in sustainable agriculture[J]. Journal of Advances in Biology & Biotechnology, 2024, 27(6): 924-937 (  0) 0) |
| [5] |
Olubisi O J, Dick D P, Ojo A O, et al. Impact of urea-intercalated-biochar on N-release in soil and humified soil organic matter[J]. Journal of Sustainable Development, 2023, 16(3): 79 DOI:10.5539/jsd.v16n3p79 (  0) 0) |
| [6] |
Su C X, Kang R H, Huang W T, et al. Temporal patterns of N2O fluxes from a rainfed maize field in Northeast China[J]. Frontiers in Environmental Science, 2021, 9: 668084 DOI:10.3389/fenvs.2021.668084 (  0) 0) |
| [7] |
李淼, 遆超普, 彭凌云, 等. 不同区域旱地土壤氨挥发过程同位素δ15N变化规律[J]. 土壤学报, 2023, 60(3): 705-715 (  0) 0) |
| [8] |
Van Donkelaar A, Martin R V, Brauer M, et al. Global estimates of fine particulate matter using a combined geophysical-statistical method with information from satellites, models, and monitors[J]. Environmental Science & Technology, 2016, 50(7): 3762-3772 (  0) 0) |
| [9] |
杨钰, 赵永鉴, 宋晓桐, 等. 典型旱作农田土壤氧化亚氮排放的氨氧化微生物相对贡献[J]. 土壤学报, 2024, 61(5): 1398-1409 (  0) 0) |
| [10] |
Yuan X, Wang S L, Chen F S, et al. Non-additive effects of Chinese fir leaf litter mixtures of different ages on soil N2O emissions in a monoculture plantation treated with N and P additions[J]. Plant and Soil, 2025, 512(1): 209-221 (  0) 0) |
| [11] |
刘鑫慧, 李雅颖, 郑宁国, 等. 全球环境变化对土壤N2O排放影响的研究进展[J]. 土壤通报, 2023, 54(1): 213-222 (  0) 0) |
| [12] |
Guo B L, Zheng X Z, Yu J H, et al. Liming and nitrification inhibitor affects crop N uptake efficiency and N loss through changing soil N processes[J]. Biology and Fertility of Soils, 2022, 58(8): 949-959 DOI:10.1007/s00374-022-01674-5 (  0) 0) |
| [13] |
田发祥, 纪雄辉, 官迪, 等. 氮肥增效剂的研究进展[J]. 杂交水稻, 2020, 35(5): 7-13 (  0) 0) |
| [14] |
杨柳青, 季加敏, 巨晓棠. 硝化/脲酶抑制剂对石灰性潮土N2O减排效果及氮素转化的比较[J]. 农业环境科学学报, 2017, 36(3): 605-612 (  0) 0) |
| [15] |
Friedl J, Scheer C, Rowlings D W, et al. Effect of the nitrification inhibitor 3, 4-dimethylpyrazole phosphate (DMPP) on N-turnover, the N2O reductase-gene nosZ and N2O: N2 partitioning from agricultural soils[J]. Scientific Reports, 2020, 10(1): 2399 DOI:10.1038/s41598-020-59249-z (  0) 0) |
| [16] |
Akiyama H, Morimoto S, Hayatsu M, et al. Nitrification, ammonia-oxidizing communities, and N2O and CH4 fluxes in an imperfectly drained agricultural field fertilized with coated urea with and without dicyandiamide[J]. Biology and Fertility of Soils, 2013, 49(2): 213-223 DOI:10.1007/s00374-012-0713-2 (  0) 0) |
| [17] |
Yang M, Fang Y T, Sun D, et al. Efficiency of two nitrification inhibitors (dicyandiamide and 3, 4-dimethypyrazole phosphate) on soil nitrogen transformations and plant productivity: A meta-analysis[J]. Scientific Reports, 2016, 6: 22075 DOI:10.1038/srep22075 (  0) 0) |
| [18] |
Wang X, Bai J H, Xie T, et al. Effects of biological nitrification inhibitors on nitrogen use efficiency and greenhouse gas emissions in agricultural soils: A review[J]. Ecotoxicology and Environmental Safety, 2021, 220: 112338 DOI:10.1016/j.ecoenv.2021.112338 (  0) 0) |
| [19] |
Yao Y L, Zeng K, Song Y Z. Biological nitrification inhibitor for reducing N2O and NH3 emissions simultaneously under root zone fertilization in a Chinese rice field[J]. Environmental Pollution, 2020, 264: 114821 DOI:10.1016/j.envpol.2020.114821 (  0) 0) |
| [20] |
赖晶晶, 兰婷, 王启, 等. 硝化抑制剂对紫色土硝化作用及N2O排放的影响[J]. 农业环境科学学报, 2019, 38(6): 1420-1428 (  0) 0) |
| [21] |
周金泉, 张明超, 魏志军, 等. 高粱分泌硝化抑制物对羟基苯丙酸与质子泵的关系研究[J]. 土壤学报, 2015, 52(3): 620-627 (  0) 0) |
| [22] |
曾科, 王书伟, 朱文彬, 等. 不同硝化抑制剂对稻季N2O排放、NH3挥发和水稻产量的影响[J]. 土壤, 2023, 55(3): 503-511 DOI:10.13758/j.cnki.tr.2023.03.006 (  0) 0) |
| [23] |
鲁如坤. 土壤农业化学分析方法[M].
中国农业科技出版社, 北京, 1999: 156-249
(  0) 0) |
| [24] |
李海涛, 谢春梅, 刘成前, 等. UV-B增强后秸秆还田分解对土壤氮转化微生物及酶活性的影响[J]. 农业环境科学学报, 2024, 43(1): 111-121 (  0) 0) |
| [25] |
华瑶, 陆玉芳, 高维常, 等. 生物硝化抑制剂对黔西南黄壤硝化作用及N2O排放的影响[J]. 土壤, 2023, 55(3): 512-519 (  0) 0) |
| [26] |
史晓晴, 张鑫, 徐霄, 等. 脲酶抑制剂NBPT对水泡粪猪舍粪尿氮素转化及氨挥发的影响[J]. 中国农业大学学报, 2024, 29(12): 165-173 (  0) 0) |
| [27] |
陆玉芳, 施卫明. 生物硝化抑制剂的研究进展及其农业应用前景[J]. 土壤学报, 2021, 58(3): 545-557 (  0) 0) |
| [28] |
周爽, 其力莫格, 谭钧, 等. 腐植酸提高土壤氮磷钾养分利用效率的机制[J]. 腐植酸, 2015(2): 1-8 (  0) 0) |
| [29] |
Kasim S, Ahmed O H, Ab Majid N M, et al. Effect of organic based N fertilizer on dry matter (Zea mays L.), ammonium and nitrate recovery in an acid soil of Sarawak, Malaysia[J]. American Journal of Applied Sciences, 2009, 6(7): 1289-1294 DOI:10.3844/ajassp.2009.1289.1294 (  0) 0) |
| [30] |
史广宇, 吴贝贝, 胡嘉源, 等. 施加生物炭缓解土壤氮流失机理的研究进展[J]. 环境化学, 2025, 44(1): 149-163 (  0) 0) |
| [31] |
Rosliza S, Ahmed O H, Ab Majid N M. Controlling ammonia volatilization by mixing urea with humic acid, fulvic acid, triple superphosphate and muriate of potash[J]. American Journal of Environmental Sciences, 2009, 5(5): 605-609 DOI:10.3844/ajessp.2009.605.609 (  0) 0) |
| [32] |
Gul S, Whalen J K, Thomas B W, et al. Physico-chemical properties and microbial responses in biochar-amended soils: Mechanisms and future directions[J]. Agriculture, Ecosystems & Environment, 2015, 206: 46-59 (  0) 0) |
| [33] |
赵进, 赵旭, 王慎强, 等. 长期秸秆黑炭施加对石灰性潮土肥力、固碳及氨挥发的影响[J]. 应用生态学报, 2018, 29(1): 176-184 (  0) 0) |
| [34] |
张楠, 黎烨, 刘玉莲, 等. 有机肥组分特征对黑土N2O排放的影响研究[J]. 土壤, 2023, 55(1): 62-71 DOI:10.13758/j.cnki.tr.2023.01.008 (  0) 0) |
| [35] |
曹慧丽, 樊丹丹, 姚敏杰, 等. 土壤反硝化过程速率测定方法[J]. 应用与环境生物学报, 2021, 27(4): 1102-1109 (  0) 0) |
| [36] |
Song Y Z, Li Y F, Cai Y J, et al. Biochar decreases soil N2O emissions in Moso bamboo plantations through decreasing labile N concentrations, N-cycling enzyme activities and nitrification/denitrification rates[J]. Geoderma, 2019, 348: 135-145 DOI:10.1016/j.geoderma.2019.04.025 (  0) 0) |
| [37] |
高尚洁, 刘杏认, 徐春英, 等. 生物炭添加对土壤反硝化产物比的影响研究进展[J]. 中国农业气象, 2024, 45(7): 777-785 (  0) 0) |
| [38] |
Fungo B, Chen Z, Butterbach-Bahl K, et al. Nitrogen turnover and N2O/N2 ratio of three contrasting tropical soils amended with biochar[J]. Geoderma, 2019, 348: 12-20 DOI:10.1016/j.geoderma.2019.04.007 (  0) 0) |
| [39] |
Pascual M B, Sánchez-Monedero M Á, Cayuela M L, et al. Biochar as electron donor for reduction of N2O by Paracoccus denitrificans[J]. FEMS Microbiology Ecology, 2020, 96(8): fiaa133 DOI:10.1093/femsec/fiaa133 (  0) 0) |
| [40] |
Yuan H J, Zhang Z J, Li M Y, et al. Biochar's role as an electron shuttle for mediating soil N2O emissions[J]. Soil Biology and Biochemistry, 2019, 133: 94-96 DOI:10.1016/j.soilbio.2019.03.002 (  0) 0) |
| [41] |
Luz M C, Angel M S, Asunción R, et al. Biochar and denitrification in soils: When, how much and why does biochar reduce N2O emissions?[J]. Scientific Reports, 2013, 3(1): 1732 DOI:10.1038/srep01732 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China
 2026, Vol. 58
2026, Vol. 58


