2. 中国科学院大学, 北京 100049;
3. 广西欣港交通投资有限公司, 南宁 530000
随着全球城市化进程的加速,桥梁建设极大提升了交通便利并促进了地区经济增长。然而,这也对自然生态系统造成了严重威胁。例如,研究发现这种城市化进程对水稳性团聚体的粒径组成和稳定性都具有重要影响[1]。滨海湿地是典型的脆弱生态系统,对环境变化的响应极为敏感,尤其是红树林,常常受到桥梁建设的干扰[2]。红树林是分布在热带和亚热带地区潮间带的关键生态系统,为众多生物提供了栖息地,并在碳封存、海岸带侵蚀防护和生物多样性维持等方面发挥着重要作用[3-4]。
红树林土壤中蕴藏着丰富多样的微生物类群,包括细菌、古菌和真菌等,它们的多样性和稳定性对于维持红树林生态系统的健康和生态功能至关重要[5-6]。研究表明,桥梁建设深刻影响着红树林土壤微生物群落多样性和群落结构[7]。鉴于土壤微生物在养分循环、有机物分解和病原菌抑制中发挥的关键作用[8-10],了解桥梁建设造成的干扰对红树林土壤微生物群落的影响,对于保护和管理红树林生态系统至关重要。众所周知,土壤微生物群落对环境干扰极为敏感。桥梁建设可能会改变潮间带潮汐的动力学特征,阻碍物种在红树林生境之间的移动[11]。近期研究发现,桥梁建设显著降低了土壤细菌群落的多样性和微生物生物量[7]。然而,由于不同微生物类群(如细菌、古菌和真菌)形态特征和生态功能各异,因此原核生物和真菌可能对环境改变表现出不同的响应模式[12-13]。原核生物,包括细菌和古菌,具有简单的细胞结构和更高的生物量,通常具备更高的代谢多样性和适应能力,使其能更快速地响应环境变化[14]。相比之下,真菌则通过多细胞的菌丝网络能够在土壤中延伸更长的距离,发挥重要的土壤颗粒结合、有机物分解和营养循环作用[15]。然而,当前对于桥梁建设下这些重要微生物类群的响应规律仍知之甚少。
由此,本研究以广西当前正在建设的最长桥梁——龙门大桥作为研究样地,探究了不同桥梁施工方法(钢护筒围堰和钢桩板围堰)对红树林土壤原核生物和真菌群落的影响,以为基础设施建设背景下红树林生态系统保护提供重要的政策和管理建议。
1 材料与方法 1.1 样地设置与土壤样品采集研究样地位于广西钦州市龙门港镇(108°34′48″E,21°45′0″N)。该区域属于南亚热带海洋季风气候区,年平均气温为21.9 ℃,年平均降水量为2 234.8 mm。钦州湾潮汐以日潮为主,平均潮差2.55 m,最大潮差达5.49 m[16]。研究区域的红树林物种主要为桐花树(Aegiceras corniculatum),伴生种有秋茄(Kandelia obovata)和白骨壤(Avicennia marina)等[17]。
为探究桥梁建设对土壤微生物群落的潜在影响,分别在3个生境下采集土壤样品:两个处于不同桥梁建设方法下的区域(钢桩板围堰(Sheet pile cofferdam,SP)和钢护筒围堰(Steel casing pipe,SC))以及一个毗邻的未受扰动红树林区域(UD)。所有选定的采样点均具有相似的高程和潮汐特征。土壤样品于2023年5月采集,即桥墩施工开始6个月后采集,以便土壤微生物群落稳定。各生境内分别设置3个采样点,并在每个采样点周围随机采集3份土壤样品。土壤样品使用土钻(直径为5 cm、长度为20 cm)采集,随后,单个土柱充分混匀成一份样品。土壤样品用冰盒运输至实验室,用2 mm筛网去除杂质后分成两部分:一部分自然风干以供土壤理化性质分析,另一部分存放于–40 ℃冰箱用于土壤DNA提取。
1.2 土壤DNA提取与高通量测序土壤DNA提取采用FastDNA SPIN Kit(MP Biomedicals)试剂盒,并严格按照说明书操作。使用1% 琼脂糖凝胶电泳和NanoDropOne分光光度计评估提取的DNA质量和浓度。使用引物341F和805R对细菌16S rRNA基因的V3~V4高变区进行扩增[18],使用引物519F和915R对古菌16S rRNA基因的V4~V5高变区进行扩增[19],使用引物ITS1和ITS2对真菌的ITS1区进行扩增[20]。高通量测序在Illumina Miseq PE 300平台(Illumina)上进行。所有原始测序序列(raw reads)上传至国家基因组科学数据中心(National Genomics Data Center),其中,细菌的登录号为CRA014249,古菌为CRA014806,真菌为CRA014792。
分析前去除质量较差(读长<200 bp或平均质量评分<20)的原始测序序列,将获得的高质量测序序列(clean reads)通过UPARSE[21]和QIIME2[22]方法进行分析。其中,高质量测序序列以100% 的相似性阈值聚类为操作分类单元(OTU)[23]。古菌和细菌的代表性序列使用Silva数据库(v132)进行注释,真菌的代表性序列则使用UNITE数据库(v8.0)进行注释。所有测序序列均按样本抽平至统一深度(古菌为24 169,细菌为1 742,真菌为2 209),以便进行下游分析。
1.3 土壤理化性质测定土壤含水量(Soil water content,SWC)通过将20 g新鲜土壤在105 ℃下烘干至恒重来测定。土壤pH使用pH计(FE28,Mettler-Toledo)测量,水土质量比为2.5∶1。土壤电导率(Electrical conductivity,EC)使用电导率仪(Bante902P,Bante)在25 ℃下进行测定。土壤全碳(Total carbon,TC)和全氮(Total nitrogen,TN)使用Vario EL Ⅲ元素分析仪(Elementar)进行定量分析。土壤有机碳(Total organic carbon,TOC)使用重铬酸钾氧化法进行测定[24]。土壤有机质(Soil organic matter,SOM)采用失重法进行测定[25]。微生物生物量碳(Microbial biomass carbon,MBC)和微生物生物量氮(Microbial biomass nitrogen,MBN)使用氯仿熏蒸提取法进行测定[26]。
1.4 微生物共存网络分析各生境微生物共存网络基于Spearman相关矩阵进行构建[27]。网络构建过程中去除在土壤样品中出现频率低于20% 且相对丰度低于0.01% 的OTU(操作分类单元),最终,获得676个古菌、626个细菌和109个真菌OTU。然后,将Spearman r>0.8且P<0.05的相关性视为强共现,用于网络构建。每个生境中的网络属性使用ggClusterNet R包进行计算。网络中每个节点的网络角色使用rnetcarto R包进行识别,其中,连接者(connectors)、模块枢纽(module hubs)和网络枢纽(network hubs)被定义为核心物种。
1.5 数据处理与分析本研究使用物种丰富度(Richness)代表微生物群落的α多样性,并通过稀释曲线来判断样本量是否足够。物种丰富度与环境变量之间的相关性通过Spearman相关性进行评估。Venn图用于展示不同生境中独特和共享的OTU。主坐标分析(PCoA)用于评估微生物群落的相对差异,此分析基于Weighted UniFrac距离。置换多元方差分析(PERMANOVA)用于检验不同生境之间微生物群落的显著性差异。使用minerva R包计算环境因子与OTU相对丰度之间的相关性,最大信息系数(MIC)>0.4被视为显著相关。基于距离的冗余分析(db-RDA)用于识别影响土壤微生物群落的主要环境因子。环境变量之间的多重共线性通过Hmisc R包进行评估。为了理解生物多样性模式及其成因,利用adespatial R包将不同生境间的β多样性细分为替代和丰富度差异组分。基于Spearman相关分析的Mantel检验用于验证微生物群落组分与环境变量之间的关系。通过spaa R包计算每个OTU的Levin生态位宽度(Niche breadth,NB)指数,以进一步解释β多样性模式。微生物群落的稳定性通过平均变异度(Average variation degree,AVD)指数进行评估[28]。AVD值越低,表示微生物群落越稳定。使用Wilcoxon检验比较不同生境间微生物群落的显著差异(包括多样性、群落稳定性和生态位宽度等)。所有分析均在R软件(版本4.4.0)中进行,所有统计分析的显著性水平均设定为P<0.05。
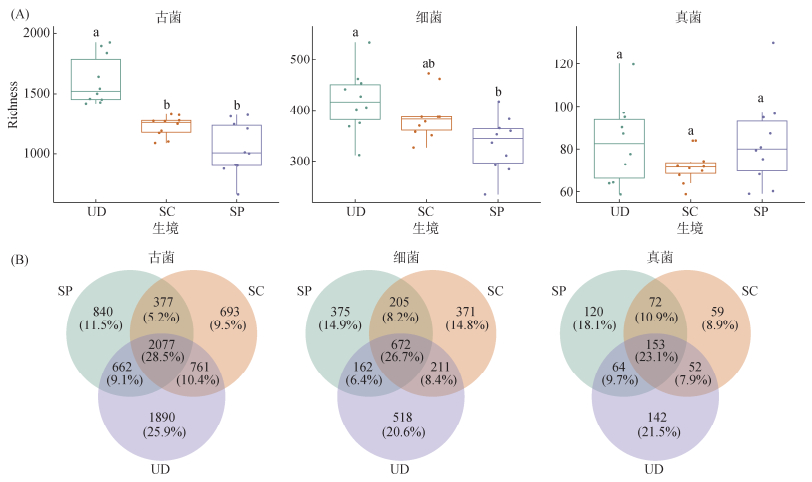
2 结果与分析 2.1 微生物α多样性及其驱动因子通过分析不同生境下微生物的物种丰富度(Richness),本研究揭示了古菌、细菌及真菌群落对桥梁建设响应的差异性(图 1)。UD生境的古菌和细菌群落丰富度均显著高于SC和SP生境(图 1A)。与UD生境相比,SP和SC生境的古菌丰富度分别下降了35.16% 和23.79%;SP和SC生境的细菌丰富度分别下降了20.33% 和7.42%。与前两者不同,UD、SC和SP三个生境间的真菌丰富度并未表现出显著性差异。
|
(UD:未扰动红树林土壤;SC:钢护筒围堰土壤;SP:钢桩板围堰土壤;图中不同小写字母表示各生境土壤间差异在P<0.05水平显著;下同) 图 1 不同生境下土壤微生物丰富度(A)及共有与特有OTU(B) Fig. 1 Soil microbial richness (A) and shared and unique OTUs (B) across different habitats |
Venn图(图 1B)分析显示,UD生境中各微生物类群的独有OTU占比均为最高,分别为:古菌(25.9%)、细菌(20.6%)和真菌(21.5%)。在受扰动的SP和SC生境中,虽然各微生物类群多样性整体下降,但仍鉴定出10%~20% 的独有OTU。
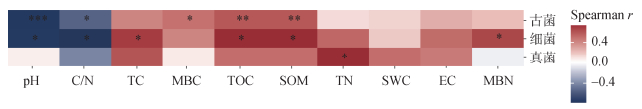
Spearman相关分析表明,微生物丰富度与土壤全碳(TC)、全氮(TN)、有机碳(TOC)及有机质(SOM)均表现出显著的正相关关系,而与C/N比呈现显著负相关关系(P<0.05)。此外,古菌和细菌丰富度受pH的显著抑制(图 2)。
|
(SWC:土壤含水量;EC:电导率;TC:土壤全碳;TN:土壤全氮;TOC:土壤有机碳;SOM:土壤有机质;MBC:微生物生物量碳;MBN:微生物生物量氮;*、**、***分别表示在P<0.05、P<0.01、P<0.001水平显著相关;下同) 图 2 微生物物种丰富度与环境因子之间的Spearman相关系数 Fig. 2 Spearman correlations between microbial richness and environmental variables |
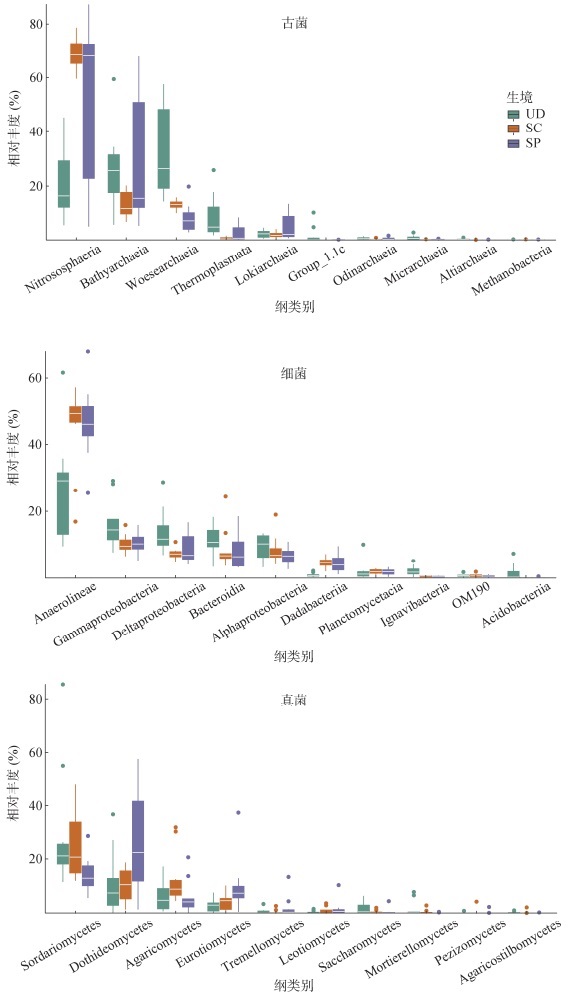
在纲(Class)水平上,不同生境土壤的微生物组成表现出显著的演变趋势(图 3)。古菌群落的优势类群为亚硝化球菌纲(Nitrososphaeria),且该纲在受扰动生境(SC:68.9%;SP:68.6%)中的相对丰度远高于UD生境(16.7%),成为扰动后的绝对优势类群。细菌群落以厌氧绳菌纲(Anaerolineae)为主要类群,其在SC和SP生境中的丰度较UD生境有明显提升。而真菌群落中粪壳菌纲(Sordariomycetes)在各生境中均占据主导地位。
|
图 3 不同生境下土壤古菌、细菌和真菌主要类群在纲水平上的相对丰度 Fig. 3 Relative abundance of dominant archaeal, bacterial, and fungal groups at the class level across different habitats |
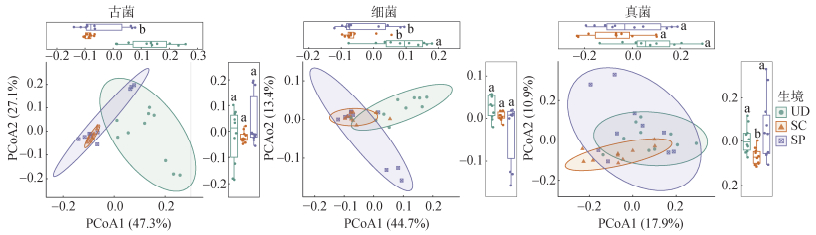
主坐标分析(图 4)与PERMANOVA检验(表 1)结果一致,证实桥梁建设显著改变了三大微生物类群的群落结构(P<0.001)。生境对古菌群落结构的解释度最高(R2=0.383),其次是细菌(R2=0.266),真菌群落受生境影响的解释度相对较低(R2=0.138)。主坐标分析(图 4)表明,原核生物(古菌与细菌)在SC和SP生境中的群落相似性较高(距离缩短),而真菌群落在SP生境中表现出更高的群落异质性。
|
图 4 不同生境下微生物群落差异主坐标分析 Fig. 4 Principal coordinates analysis of differences in microbial communities across different habitats |
|
|
表 1 不同生境微生物群落的置换多元方差分析(PERMANOVA) Table 1 PERMANOVA of soil microbial communities across different habitats |
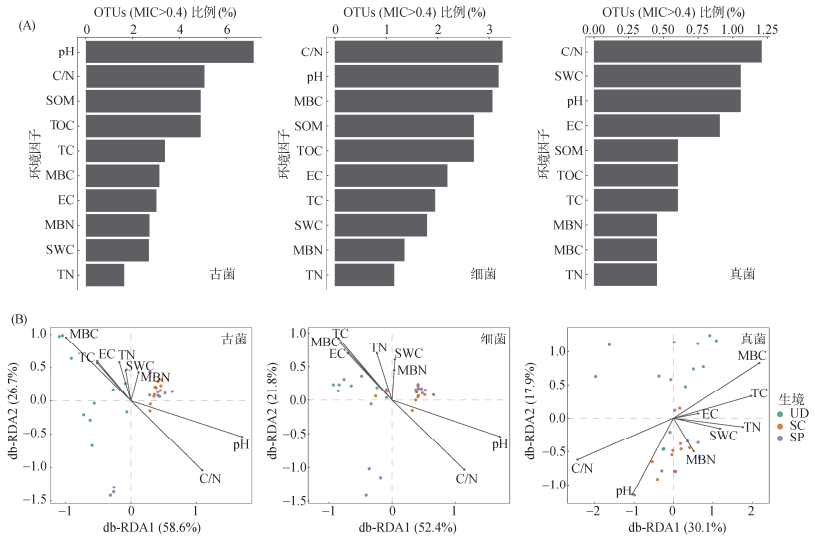
通过分析环境因子与OTU相对丰度的相关性(图 5A)及db-RDA排序(图 5B),揭示了驱动微生物群落变化的关键因子。土壤pH和C/N比是影响三大微生物群落结构的最主要环境因子。此外,微生物生物量碳(MBC)对古菌和细菌群落也具有显著的驱动作用。古菌对pH最为敏感,超过7% 的OTU与pH呈显著相关(MIC>0.4)。db-RDA分析显示,pH与C/N比共同解释了古菌群落的大部分变异(db-RDA1: 58.6%)。细菌与真菌的群落演变主要受C/N比驱动。细菌群落受TC、MBC、EC等多种肥力指标的协同影响,而真菌群落则表现出对pH和C/N比的特异性响应。
|
图 5 与环境因子显著相关的OTU比例(A)及微生物群落主要环境因子的冗余分析(db-RDA)(B) Fig. 5 Proportion of OTUs significantly correlated with environmental factors (A) and distance-based redundancy analysis (db-RDA) of the main environmental factors shaping microbial communities (B) |
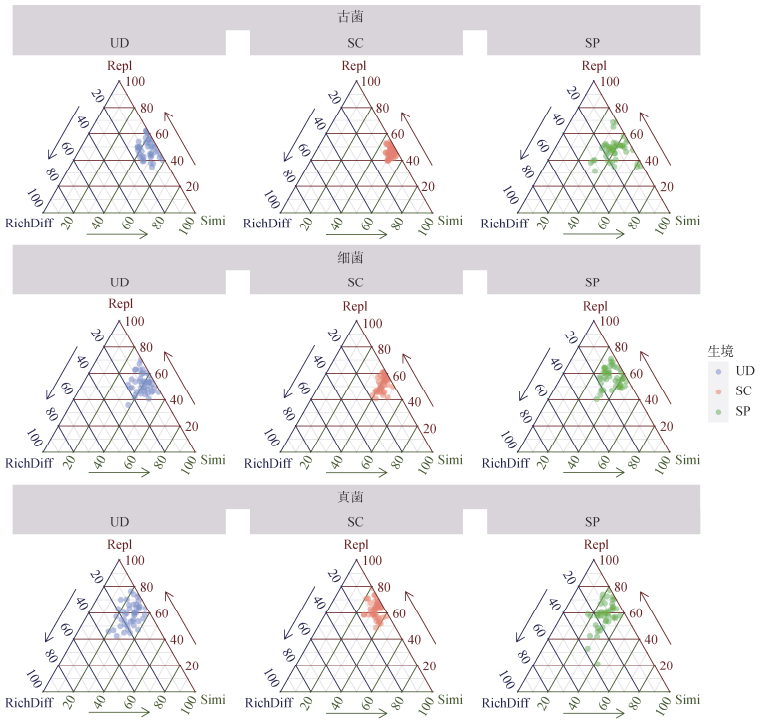
通过对β多样性进行分解(图 6、表 2)发现,在所有微生物类群中,物种替代(Repl)组分均占据主导地位,贡献率显著高于丰富度差异(RichDiff)。其中,真菌群落的β多样性最高(0.361),且主要由物种替代驱动(Repl占比84.5%)。三元图分析显示(图 6),相较于UD生境,SC生境中的物种替代比例有所降低,而SP生境中的丰富度差异组分占比则呈现增加趋势。
|
(Repl:物种替换;RichDiff:丰富度差异;Simi:相似性) 图 6 土壤微生物β多样性不同组分的差异 Fig. 6 Different components of soil microbial beta diversity |
|
|
表 2 微生物群落β多样性及其分解组分 Table 2 Beta diversity and its partitioning components of microbial communities. |
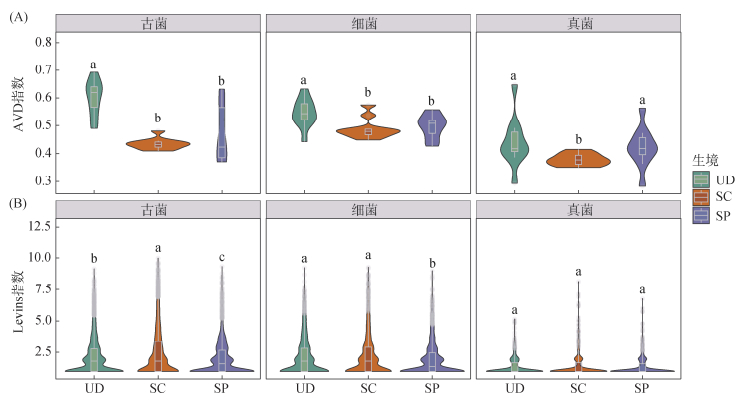
本研究利用群落变异程度(AVD)指数评估了群落稳定性(AVD值越低代表稳定性越强)(图 7A)。对于古菌和细菌群落,UD生境的AVD值显著高于SC和SP生境,表明在受干扰生境中,原核生物群落趋向于形成一种异质性较低的稳定状态。真菌群落的AVD值在SC生境中达到最低,表现出较强的群落稳定性。总体而言,真菌群落的平均AVD值显著低于古菌和细菌,显示出其对环境扰动具有更高的抗性。
|
图 7 不同生境土壤微生物群落的稳定性(A)和生态位宽度(B) Fig. 7 Stability of soil microbial community (A) and niche width (B) between different habitats |
生态位宽度(Levins指数)分析表明(图 7B),古菌和细菌的生态位宽度在SP生境中显著收缩,反映了施工区的物理化学环境限制了原核生物的资源获取范围。不同生境间真菌的生态位宽度无显著差异,维持在较低水平。这一结果与AVD分析一致,进一步证实真菌群落主要由生态位较窄的专性类群组成,且其群落结构在扰动下具有较高的稳定性。
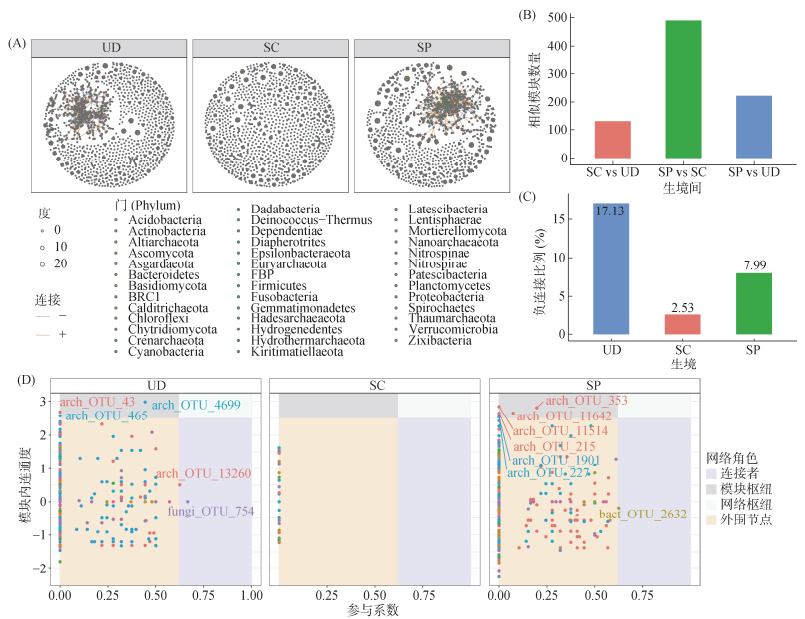
2.4 微生物共存网络特征通过构建不同生境下的微生物共存网络(图 8A),发现桥梁建设显著改变了微生物间的相互作用模式(表 3)。SP生境网络的平均度(6.74)显著高于UD(4.11)和SC(3.44)生境。SP生境的总边数(3 506)和节点数(1 040)均为最高。相似模块数量分析(图 8B)显示,SP与SC生境之间共享的模块数最多,反映了施工扰动对群落结构具有相似的筛选作用。网络中正、负相关连接的比例揭示了群落内相互作用的动态变化。在所有生境中,正相关连接占比均远超80%,表明微生物类群之间以合作或共栖关系为主(图 8C)。UD生境拥有最高比例的负相关连接(17.13%),相比之下,SC生境的负相关连接比例降至最低(2.53%),反映出施工干扰可能削弱了群落内部的竞争强度。利用模块内连通度和参与系数识别了网络中的核心物种(图 8D),发现不同生境的核心物种组成存在显著差异。在UD和SP生境中,识别出多个发挥重要连接作用的核心OTU。值得注意的是,大多数被识别为核心物种(如外围节点中的关键OTU和模块枢纽)的类群均为古菌。这表明古菌不仅在丰度上发生变化,更在维持微生物生态网络结构的稳定性和复杂性中发挥着不可替代的中枢作用。
|
图 8 不同生境之间的土壤微生物共存网络(A)、网络内相似模块数量(B)、负连接数占所有连接数的百分比(C)及每个节点在网络中的网络角色(D) Fig. 8 Microbial co-occurrence network among different habitats (A), number of similar modules within ecological networks between habitats (B), percentage of negative links to all links in network (C), and universal role of each node in networks (D) |
|
|
表 3 不同生境下土壤微生物共存网络的拓扑属性参数 Table 3 Topological attributes of soil microbial co-occurrence networks across different habitats |
红树林是地球上最重要的生态系统之一,然而,其正受到人类活动、气候变化加剧和土地利用变化等威胁[29]。人类活动,如桥梁建设可能会打破这些生态系统中微生物群落的动态平衡。因此,了解这些微生物群落如何响应人类活动,对制定有效的生态保护和管理策略至关重要。本研究揭示了红树林土壤细菌、古菌和真菌群落对桥梁建设的差异性响应及其环境主控因子,强调了在生态评估和保护策略中考虑这些差异的重要性。
本研究表明,与未受干扰红树林生境相比,受到桥梁施工影响的生境中细菌和古菌的α多样性显著下降,而真菌α多样性无显著差异,这表明原核生物群落对桥梁建设的干扰更为敏感。该发现与之前关于桥梁建设导致浙江舟岱大桥[30]和广西龙门大桥[7]土壤细菌α多样性降低的研究结论相吻合。微生物α多样性的下降可能归因于桥梁施工过程中对土壤理化性质和水文特征的改变。相比之下,真菌的α多样性在3种生境之间没有显著差异,表明真菌群落在不同生境间保持了相对稳定的α多样性,对环境干扰具有更高的稳定性。这种在扰动环境中的稳定性可能与真菌的生活策略和生态角色有关,包括与植物形成共生关系等[31-32]。
β多样性分析进一步揭示了原核生物和真菌群落的差异响应模式。桥梁建设降低了细菌和古菌的β多样性,表明这些群落在受到干扰的生境中趋向于同质化。这可能是由于环境条件的改变引起的选择压力增加,从而优先选择了一部分耐受物种,同时过滤了更敏感的微生物类群[33-34]。另一方面,真菌的β多样性在桥梁建设后有所增加,反映出不同生境中真菌群落组成的更大变异性。这可能是由于真菌能够利用多样的生态位并适应广泛的环境条件[32, 35-36]。将β多样性划分为物种替代和丰富度差异组分有助于揭示群落组装过程[37-38]。结果显示,物种替代而非丰富度差异的变化主导了微生物群落在生境中的组成变化。这一发现强调了土壤生物群落的动态特性,其中物种替换在受干扰后的群落重组中发挥着关键作用[39-40]。在原核生物群落中观察到的更高物种替代表明,这些微生物在应对环境变化时更容易发生群落重组,而真菌群落则表现出更高的稳定性和更少的更替。生态网络分析表明,在所有生境中,正相关的相互作用占主导地位,进一步支持了以上结果。而在未受干扰生境中,负相关连接比例最高(17.13%),表明在受到干扰的生境中微生物网络更加趋向于合作。此外,负责维持网络连通性和稳定性的关键物种可能由于桥梁建设活动而丢失,从而进一步促进了原核生物群落的同质化。相比自然生境,桥梁建设下的生境共享了更多的生态模块,这些模块往往具有普适的生存策略和关键生态功能,能够在不同环境中维持群落稳定性,因此利用核心模块将有助于开展生态修复与生态系统功能提升。
土壤理化性质与微生物丰富度之间存在显著相关性。例如,微生物丰富度与土壤C/N比呈显著负相关,与土壤全碳和全氮含量呈显著正相关。这些相关性突显了养分可用性和土壤理化性质在塑造微生物群落中的重要性。微生物对这些环境因素的不同响应进一步强调了原核生物和真菌在生态功能和适应策略上的差异。土壤pH、C/N比和微生物生物量碳被确定为微生物群落结构的关键调节因子。其中,pH对古菌的显著影响表明,古菌对土壤酸度变化极为敏感。此外,桥梁建设下的微生物群落趋向于更大的群落稳定性,这可能源于桥梁建设活动施加的选择压力,导致能够在压力下维持群落功能的耐受物种占主导地位[41]。古菌和细菌群落的生态位宽度在不同生境中也存在差异,而真菌则未显示出这种差异,表明真菌相较于原核生物在环境变化中具有更强的适应能力和稳定性。
原核生物和真菌群落对桥梁建设干扰的差异性响应表明,保护措施应重点关注维持那些有利于多样化及敏感微生物群落生存的生境条件,特别是在基础设施快速发展的地区。因为不稳定的微生物群落通常具有较高的生态韧性和多功能性,能够在环境变化和干扰发生时迅速响应和调整。鉴于土壤微生物在养分循环、有机物分解和病原菌抑制中的关键作用,维持微生物多样性对红树林生态系统的整体健康和功能至关重要[42-43]。因此,管理实践应旨在减少物理干扰和土壤理化性质的变化,通过保护和恢复自然栖息地中的多样化环境特征(如水文和土壤结构等),为微生物群落提供更多的生境选择。此外,在基础设施建设中采取生态工程措施,如绿色桥梁、生态走廊等,可为微生物群落提供生物多样性补充。例如,相比钢板桩围堰,使用侵入性较小的建设方法(如钢护筒围堰),可以帮助维持红树林土壤微生物多样性。
然而,尽管本研究揭示了桥梁建设对红树林土壤微生物群落影响,但仍需进一步研究以充分理解驱动这些变化的潜在机制。长期跟踪微生物群落随时间、空间的动态变化对于捕捉群落对干扰的时间响应至关重要[44]。通过深入探究土壤微生物群落如何响应人类活动干扰,将为在持续人类活动下红树林生态系统的健康与功能保护提供科学依据。
4 结论桥梁建设显著降低了红树林土壤古菌和细菌的丰富度,但真菌群落表现出更强的环境耐受性。施工干扰导致土壤pH和C/N比发生显著变化,进而重塑了微生物群落结构,使古菌中的亚硝化球菌纲在受干扰生境中占据绝对优势。虽然微生物通过增强共存网络的复杂性和发挥古菌的核心连接作用来应对扰动,但群落内部竞争关系的显著减少预示了生态系统稳定性的下降。因此,未来施工过程中应重点保护独有物种,并加强对土壤pH和有机质含量的动态监测与精准修复,从而缓解工程建设对土壤微生态功能的负面影响。
致谢: 感谢贾利强、蒋树勤、李莘哲和李红旗在试验设计和现场采样等方面提供的帮助。
| [1] |
殷金忠, 唐蛟, 潘飞飞, 等. 城市近郊土地利用变化对土壤团聚体及其结合有机碳的影响[J]. 土壤, 2024, 56(1): 49-55 DOI:10.13758/j.cnki.tr.2024.01.007 (  0) 0) |
| [2] |
Mombauer D. The bridge between land and sea[EB/OL]. Earth Island Journal, (2019-09-25)[2025-12-15]. https://www.earthisland.org/journal/index.php/articles/entry/bridge-between-land-and-sea-mangroves-sri-lanka/.
(  0) 0) |
| [3] |
Curnick D J, Pettorelli N, Amir A A, et al. The value of small mangrove patches[J]. Science, 2019, 363(6424): 239 DOI:10.1126/science.aaw0809 (  0) 0) |
| [4] |
李静泰, 闫丹丹, 么秀颖, 等. 中国滨海湿地碳储量估算[J]. 土壤学报, 2023, 60(3): 800-814 (  0) 0) |
| [5] |
Liu M, Huang H Q, Bao S X, et al. Microbial community structure of soils in Bamenwan mangrove wetland[J]. Scientific Reports, 2019, 9: 8406 DOI:10.1038/s41598-019-44788-x (  0) 0) |
| [6] |
Wang F F, Guo R, Zhang N, et al. Soil organic carbon storages and bacterial communities along a restored mangrove soil chronosequence in the Jiulong River Estuary: From tidal flats to mangrove afforestation[J]. Fundamental Research, 2023, 3(6): 880-889 DOI:10.1016/j.fmre.2022.08.019 (  0) 0) |
| [7] |
Gao G F, He Y, Li J S, et al. Sea-crossing bridge construction interference reduced soil microbial biomass and diversity in mangrove ecosystems[J]. Soil Ecology Letters, 2024, 7(1): 240257 (  0) 0) |
| [8] |
Trivedi P, Anderson I C, Singh B K. Microbial modulators of soil carbon storage: Integrating genomic and metabolic knowledge for global prediction[J]. Trends in Microbiology, 2013, 21(12): 641-651 DOI:10.1016/j.tim.2013.09.005 (  0) 0) |
| [9] |
Delgado-Baquerizo M, Reich P B, Trivedi C, et al. Multiple elements of soil biodiversity drive ecosystem functions across biomes[J]. Nature Ecology & Evolution, 2020, 4(2): 210-220 (  0) 0) |
| [10] |
Banerjee S, van der Heijden M G A. Soil microbiomes and one health[J]. Nature Reviews Microbiology, 2023, 21(1): 6-20 DOI:10.1038/s41579-022-00779-w (  0) 0) |
| [11] |
Li Q, Qian R, Gao J F, et al. Environmental impacts and risks of bridges and tunnels across lakes: An overview[J]. Journal of Environmental Management, 2022, 319: 115684 DOI:10.1016/j.jenvman.2022.115684 (  0) 0) |
| [12] |
Luis P, Saint-Genis G, Vallon L, et al. Contrasted ecological niches shape fungal and prokaryotic community structure in mangroves sediments[J]. Environmental Microbiology, 2019, 21(4): 1407-1424 DOI:10.1111/1462-2920.14571 (  0) 0) |
| [13] |
Voříšková J, Elberling B, Priemé A. Fast response of fungal and prokaryotic communities to climate change manipulation in two contrasting tundra soils[J]. Environmental Microbiome, 2019, 14(1): 6 DOI:10.1186/s40793-019-0344-4 (  0) 0) |
| [14] |
Gupta R, Gupta N. Prokaryotic cell structure and function[M]//Fundamentals of Bacterial Physiology and Metabolism. Singapore: Springer Singapore, 2021: 43–79.
(  0) 0) |
| [15] |
Morton J B. Fungi[M]//Gentry T J, Fuhrmann J J, Zuberer D A. Principles and Applications of Soil Microbiology. 3rd ed. Amsterdam: Elsevier, 2021: 149-170.
(  0) 0) |
| [16] |
Li D, Tang C, Hou X Y, et al. Morphological changes in the Qinzhou Bay, southwest China[J]. Journal of Coastal Conservation, 2019, 23(4): 829-841 DOI:10.1007/s11852-018-0600-6 (  0) 0) |
| [17] |
Huang X, Wang X P, Li X Z, et al. Occurrence and transfer of heavy metals in sediments and plants of Aegiceras corniculatum community in the Qinzhou Bay, southwestern China[J]. Acta Oceanologica Sinica, 2020, 39(2): 79-88 DOI:10.1007/s13131-020-1555-7 (  0) 0) |
| [18] |
Yang L Y, Zhou S Y D, Lin C S, et al. Effects of biofertilizer on soil microbial diversity and antibiotic resistance genes[J]. Science of the Total Environment, 2022, 820: 153170 DOI:10.1016/j.scitotenv.2022.153170 (  0) 0) |
| [19] |
Hugoni M, Domaizon I, Taib N, et al. Temporal dynamics of active Archaea in oxygen-depleted zones of two deep lakes[J]. Environmental Microbiology Reports, 2015, 7(2): 321-329 DOI:10.1111/1758-2229.12251 (  0) 0) |
| [20] |
Yang T, Adams J M, Shi Y, et al. Soil fungal diversity in natural grasslands of the Tibetan Plateau: Associations with plant diversity and productivity[J]. The New Phytologist, 2017, 215(2): 756-765 DOI:10.1111/nph.14606 (  0) 0) |
| [21] |
Edgar R C. UPARSE: Highly accurate OTU sequences from microbial amplicon reads[J]. Nature Methods, 2013, 10(10): 996-998 DOI:10.1038/nmeth.2604 (  0) 0) |
| [22] |
Bolyen E, Rideout J R, Dillon M R, et al. Reproducible, interactive, scalable and extensible microbiome data science using QIIME 2[J]. Nature Biotechnology, 2019, 37(8): 852-857 DOI:10.1038/s41587-019-0209-9 (  0) 0) |
| [23] |
Edgar R C. Updating the 97% identity threshold for 16S ribosomal RNA OTUs[J]. Bioinformatics, 2018, 34(14): 2371-2375 DOI:10.1093/bioinformatics/bty113 (  0) 0) |
| [24] |
Nelson D, Sommers L E. Total carbon, organic carbon, and organic matter[M]. Methods of soil analysis: Part 2 chemical and microbiological properties, Madison: American Society of Agronomy, Soil Science Society of America, 1983, 9: 539-579.
(  0) 0) |
| [25] |
Salehi M H, Beni O H, Harchegani H B, et al. Refining soil organic matter determination by loss-on-ignition[J]. Pedosphere, 2011, 21(4): 473-482 DOI:10.1016/S1002-0160(11)60149-5 (  0) 0) |
| [26] |
Oren A, Rotbart N, Borisover M, et al. Chloroform fumigation extraction for measuring soil microbial biomass: The validity of using samples approaching water saturation[J]. Geoderma, 2018, 319: 204-207 DOI:10.1016/j.geoderma.2018.01.007 (  0) 0) |
| [27] |
Wen T, Xie P H, Yang S D, et al. ggClusterNet: An R package for microbiome network analysis and modularity- based multiple network layouts[J]. iMeta, 2022, 1(3): e32 DOI:10.1002/imt2.32 (  0) 0) |
| [28] |
Xun W B, Liu Y P, Li W, et al. Specialized metabolic functions of keystone taxa sustain soil microbiome stability[J]. Microbiome, 2021, 9(1): 35 DOI:10.1186/s40168-020-00985-9 (  0) 0) |
| [29] |
McKee K L. Global change impacts on mangrove ecosystems: U. S. Geological Survey Fact Sheet 2004–3125[R/OL]. Reston, VA: U. S. Geological Survey, 2004. https://doi.org/10.3133/fs20043125.
(  0) 0) |
| [30] |
Li T, Lai X Y, Xiang J, et al. Ecological impacts of sea-crossing bridge construction on local sediment microbiome in East China[J]. Regional Studies in Marine Science, 2022, 53: 102363 DOI:10.1016/j.rsma.2022.102363 (  0) 0) |
| [31] |
Boddy L, Hiscox J. Fungal ecology: Principles and mechanisms of colonization and competition by saprotrophic fungi[J]. Microbiology Spectrum, 2016, 4(6) DOI:10.1128/microbiolspec.FUNK-0019-2016 (  0) 0) |
| [32] |
Bahram M, Netherway T. Fungi as mediators linking organisms and ecosystems[J]. FEMS Microbiology Reviews, 2022, 46(2): fuab058 DOI:10.1093/femsre/fuab058 (  0) 0) |
| [33] |
Huber P, Metz S, Unrein F, et al. Environmental heterogeneity determines the ecological processes that govern bacterial metacommunity assembly in a floodplain river system[J]. The ISME Journal, 2020, 14(12): 2951-2966 DOI:10.1038/s41396-020-0723-2 (  0) 0) |
| [34] |
Olden J D, Poff N L. Ecological processes driving biotic homogenization: Testing a mechanistic model using fish faunas[J]. Ecology, 2004, 85(7): 1867-1875 DOI:10.1890/03-3131 (  0) 0) |
| [35] |
Naranjo-Ortiz M A, Gabaldón T. Fungal evolution: Major ecological adaptations and evolutionary transitions[J]. Biological Reviews, 2019, 94(4): 1443-1476 DOI:10.1111/brv.12510 (  0) 0) |
| [36] |
Kumar V, Sarma V V, Thambugala K M, et al. Ecology and evolution of marine fungi with their adaptation to climate change[J]. Frontiers in Microbiology, 2021, 12: 719000 DOI:10.3389/fmicb.2021.719000 (  0) 0) |
| [37] |
Legendre P. Interpreting the replacement and richness difference components of beta diversity[J]. Global Ecology and Biogeography, 2014, 23(11): 1324-1334 DOI:10.1111/geb.12207 (  0) 0) |
| [38] |
Seymour M, Roslin T, DeWaard J R, et al. Global arthropod beta-diversity is spatially and temporally structured by latitude[J]. Communications Biology, 2024, 7: 552 DOI:10.1038/s42003-024-06199-1 (  0) 0) |
| [39] |
Pinto-Junior H V, de Carvalho Müller L A, Neri A V. Turnover is the dominant process of taxonomic and functional β-diversity on Neotropical inselbergs[J]. Flora, 2023, 305: 152319 DOI:10.1016/j.flora.2023.152319 (  0) 0) |
| [40] |
Qin H, Dong G, Zhang F. Relative roles of the replacement and richness difference components of beta diversity following the ecological restoration of a mountain meadow, North China[J]. Ecological Informatics, 2019, 52: 159-165 DOI:10.1016/j.ecoinf.2019.05.009 (  0) 0) |
| [41] |
Baishya J, Wakeman C A. Selective pressures during chronic infection drive microbial competition and cooperation[J]. NPJ Biofilms and Microbiomes, 2019, 5: 16 DOI:10.1038/s41522-019-0089-2 (  0) 0) |
| [42] |
Candry P, Abrahamson B, Stahl D A, et al. Microbially mediated climate feedbacks from wetland ecosystems[J]. Global Change Biology, 2023, 29(18): 5169-5183 DOI:10.1111/gcb.16850 (  0) 0) |
| [43] |
孔亚丽, 秦华, 朱春权, 等. 土壤微生物影响土壤健康的作用机制研究进展[J]. 土壤学报, 2024, 61(2): 331-347 (  0) 0) |
| [44] |
康小虎, 刘鑫, 刘姗姗, 等. 不同时空尺度下土壤微生物群落分布及驱动因素研究进展[J]. 土壤, 2024, 56(4): 689-696 DOI:10.13758/j.cnki.tr.2024.04.001 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Guangxi Xingang Transportation Investment Co., Ltd., Nanning 530000, China
 2026, Vol. 58
2026, Vol. 58


