2. 中国科学院宁波城市环境观测研究站, 浙江宁波 315800
自工业革命以来,石油已成为人类需求量最大的能源之一,被视为国民经济的生命线,这也使石油污染成为全球性的环境问题[1]。据统计,目前我国石油年产量已超2.0×108 t,其中有近6×105 t无法回收而直接进入环境,污染海洋、土壤和水体,每年新增石油污染土壤近1.0×108 t[2]。研究显示,进入到土壤的石油污染物只有少量可以被降解,大部分长期残留在土壤中,改变土壤理化性质,对土壤微生物群落结构产生负面影响,通过食物链危及生态系统安全,甚至危害人类健康[3-4]。相关研究已经证实植物–丛枝菌根真菌(Arbuscularmycorrhizal fungi,AMF)共生有助于复杂有机污染物的降解[5],将丛枝菌根(Arbuscular mycorrhizal,AM)技术应用于石油污染土壤的修复具有经济、安全、绿色环保等诸多优点。本文从石油污染土壤修复技术、AM修复石油污染土壤的影响因素、AM对石油污染物的直接和间接去除机制等方面进行综述,并提出未来研究方向,以期推动该技术的广泛应用。
1 土壤石油污染修复技术概况石油污染土壤的修复主要包括物理、化学和生物三大修复技术[6]。物理修复技术主要包括土壤置换、气相抽提、超声清洗和热处理(蒸汽法、热脱附、焚烧法)等,这些方法的去除率可达65%~90%,其中热处理技术效果最好[6-7]。化学修复技术主要包括化学氧化、淋洗萃取和光催化降解等,这类方法的去除率为60%~90%,其中萃取法去除效果最好[8-9]。总体而言,物理和化学修复技术修复快速,但存在成本高、易造成二次污染,甚至影响土壤成分与功能等缺陷,在实际应用中常常受到限制[7]。生物修复技术主要利用植物和微生物,其优势包括处理成本相对较低且易操作、处理效果良好、对环境影响较小等,修复效率一般也能达到50%~80%,是土壤修复领域中较为经济和环保的一类修复技术[10-11]。但生物修复技术普遍存在修复时间过长,以及高浓度污染土壤可能使修复生物出现中毒现象等问题,阻碍了该技术的广泛应用[12-13]。AM修复技术是利用AMF和植物的共生体来促进土壤污染物的去除。一方面,AM通过减轻污染物质对植物的毒害,提高植物对不利环境的抵抗力,促进植物生长,从而提高污染物的降解效率[14];另一方面,AM也能直接或间接去除污染物,提高修复效率[15]。可见,AM修复技术能够在一定程度上克服微生物修复和植物修复的缺点,被认为是最有前途的新型土壤修复技术之一。然而,现如今AM修复技术在石油污染土壤中的应用仍然处于起步阶段[16]。
2 AM修复技术 2.1 AM及其功能AMF是自然界中最古老、最具有生态重要性的真菌之一,几乎存在于陆地上所有的生境中,并与80% 以上的维管植物形成共生体[17]。AMF侵入植物根部后,在植物根内、根外和根表面逐渐形成密集的菌丝网络,使植物根系和菌丝体相连,增加了植物养分和水分的吸收通道,从而增强干旱条件下植物的抗旱性,尤其提高植物在磷素限制的土壤条件下体内的磷含量。AM能够分泌一些酸性物质,活化土壤养分,促进植物对Zn、Cu、K、Mg、S、Mn等营养元素的吸收和利用,保障植物的生长发育[18]。AM还可以通过增加自身泡囊结构,提高植物的耐涝性。AMF密集的菌丝结构使其在必要时增加植物对水分的吸收,以此来缓解高盐和高温对植物的迫害[19]。AMF的菌丝和孢子在分解过程中产生一种特殊蛋白——球囊霉素,其分子结构中有寡糖链和蛋白质连接,且含有金属元素,它的黏附力可以复合土壤颗粒,有助于土壤团聚结构的稳定性,提高土壤的透气性和持水能力[20]。因此,AM所具有的促进植物吸收水分、养分,改良土壤结构和理化性质,提高植物抵抗逆境胁迫的能力,使学者们开始尝试将AM作为污染土壤的修复主体,开拓了植物修复技术的前景。
目前,AMF–植物生物修复技术已在矿山复垦、重金属污染治理、荒漠植被恢复等领域取得较多成功案例[21]。在有毒有机污染物污染土壤的治理中,主要应用于农药和多环芳烃(Polycyclic aromatic hydrocarbon,PAHs)污染的去除[22-23]。研究者在受石油污染的土壤中筛选出AMF孢子,发现在较高石油污染浓度下依然能形成AMF侵染(表 1),这些研究的发现为AM生物修复石油污染土壤奠定了基础,但关于石油污染土壤修复治理的报道相对较少。以国内研究为例,这些研究报道中石油污染土壤来源不同,石油产地不同,其组分和成分比例也会有很大差别,如有些学者研究AM修复石油污染的土壤直接采自油田、油井地区[34-36],有的学者则采用附近绿化地等土壤作为供试土壤,他们的石油从外采购,在实验室模拟配制石油污染土壤[37-39]。不同的原油性质,不同的污染浓度,都会影响修复效率[40]。Leyval和Binet [41]的研究表明,当土壤中的PAHs浓度达到5 g/kg时,只有AMF侵染的植物能够存活。黄玲玲等[34]发现,在陕西石油污染区生长的13种人工种植树种均形成AM;研究还发现,土壤石油烃浓度与森林根际土壤中球囊霉素含量正相关,与多酚氧化酶和过氧化氢酶活性显著正相关。此外,释放到土壤中的球囊霉素可使有机污染物从土壤颗粒中脱附出来,增强了有机污染物的生物有效性[42]。另有研究表明,球囊霉素的添加改变了土壤微生物群落结构,增加了降解有机污染物的功能细菌和基因的丰度,这些都有助于提高有机污染土壤的修复[43]。这些研究从不同角度证明了AMF–植物联合修复石油污染土壤具有可行性。自20世纪80年代以来,国内外学者将AM应用于石油污染的土壤修复,但AM对石油污染物的去除机制及其影响因素的研究尚处于起步阶段,有时不能达到理想的修复效果,需要更多学者进行积极的探索。
|
|
表 1 野外石油污染土壤中AMF资源 Table 1 Arbuscular mycorrhizal fungi isolated from field petroleum-contaminated soils |
AMF在石油污染胁迫下仍能侵染植物,是AM修复石油污染土壤的前提和基础。雒晓芳等[35]在植物–微生物的组合研究中设置3个污染水平,当石油烃浓度为1% 和3% 时,紫花苜蓿(Medicago sativa)、冰草(Agropyron cristatum)和冬小麦(Triticum aestivvm)可以正常生长,且在石油烃浓度为3% 时修复效率达到最大值。然而,当石油烃浓度为10% 时,微生物的生长受到显著抑制,植物生长缓慢,土壤脱氢酶活性降低,石油烃去除率也降低。王丽萍等[44]研究发现,2% 污染浓度下接种AMF对石油烃的降解率高于污染浓度为0.2% 的土壤。周利承等[39]研究也发现,相比于0.15% 污染浓度的土壤修复效果,紫花苜蓿接种摩西球囊霉(Glomus mosseae)对1.5% 的石油污染土壤的修复效率更高。虽然不同AMF受石油胁迫的浓度不同[24],通常情况下土壤中石油污染物在较低污染浓度下对AMF可能产生刺激作用,使其产孢量增加,AM修复效果随石油烃浓度增加而增加,但污染浓度过高将显著抑制AMF或植物生长。宗炯等[37]发现,污染浓度越高,对AMF侵染植物的抑制程度越大,高污染强度还会抑制AMF菌丝的延伸和孢子的形成,而低污染处理则促进了AMF菌丝和孢子的产生。山宝琴等[13]也发现,石油污染浓度低于4% 时,AMF孢子密度、侵染率随原油浓度的增加而增加;石油污染浓度高于5%,则水分不易渗入土壤,容易造成植物缺水而不能发芽或者出苗后黄化死亡。Alejandro-Córdova等[45]研究表明,土壤中原油浓度在6% 以下时,促进AMF菌丝生长,增加其孢子数量,但高于该浓度则严重抑制AMF的生长。此外,Małachowska-Jutsz和Kalka[46]报道,接种AMF处理对土壤石油组分中PAHs的去除率高于脂肪烃。Lu和Lu[47]对PAHs去除研究中发现,AMF对5环PAHs的降解效率高于2~4环PAHs。
综上,AM技术对石油污染浓度处于相对低水平范围内的土壤能够达到最理想修复效果,且该技术的优势可能在于它对毒性更强的PAHs类污染物质的降解效率更高。但目前较少研究对修复后土壤中不同石油组分的去除率进行测定,该技术是否对石油污染物中高毒组分具有更好的去除效果,有待开展更多的相应研究。
2.2.2 菌种和宿主植物对AM修复效率的影响AMF与宿主植物之间互惠互利关系的建立程度将直接影响污染土壤的修复效率。在以往研究中,AMF侵染率、植物自身的生物量和植株的高度等参数通常被用以衡量AMF和宿主植物之间的共生关系是否良好。在无污染情况下不同宿主植物与AMF菌种之间共生关系的建立程度存在差异。如马俊卿等[48]以玉米(Zea mays)、高粱(Sorghum bicolor)、三叶草(Trifolium pratense)、黑麦草(Lolium perenne)作为宿主,以聚丛根孢囊霉(Rhizophagus aggregatus)和幼套近明球囊霉(Claroideoglomus etunicatum)进行侵染,发现不同宿主对同一AMF菌种的扩繁效应不同,它们侵染率由高到低为玉米、高粱、三叶草、黑麦草;同一宿主对不同AMF的扩繁效应也不同,玉米和黑麦草对聚丛根孢囊霉的扩繁效应高于幼套近明球囊霉,三叶草和高粱对幼套近明球囊霉的扩繁效应高于聚丛根孢囊霉。宿主植物根系发达程度、宿主植物与AMF之间碳的分配和养分的传递,都会影响AMF扩繁效应。不同AMF对同一寄主植物侵染率在不同浓度石油污染土壤中也存在差异。如耿春女等[24]在比较3种AMF菌种对三叶草(Trifolium subterrasm)耐油性研究中发现,在0.5% 石油污染浓度下,摩西球囊霉的侵染率最高,显著增加了三叶草的根长和生物量;石油浓度为1% 时,三叶草对缩球囊霉(G. constrictum)的依赖性最大。王丽萍等[44]研究发现,玉米为宿主植物,0.2% 石油浓度下摩西球囊霉的侵染率高于地表球囊霉菌(G. versifome),且受摩西球囊霉侵染的玉米植株干重、根干重更大,而2% 石油浓度下地表球囊霉菌成为最适菌种,促进玉米生长。宿主植物与AMF之间存在最佳组合,使石油去除率达到最高。如山宝琴等[13]研究发现,接种同一AMF菌剂后,艾蒿(Artemisia argyi)植株干重增加最多,柠条(Caragana korshinskii)次之,虽然都对石油烃污染显现出较强的抵抗力,在石油烃降解率比较中,柠条却为最高,艾蒿的降解率不显著。Li等[49]发现接种到嵩柳(Salix viminalis)的摩西斗管囊霉(Funneliformis mosseae)、幼套近明球囊霉和根内根孢囊霉(Rhizophagus intraradices)对苯并芘的去除效率不同,且发现不同菌种根际有机酸含量和酶活性不同。此外,研究表明,宿主植物,尤其是根系间形成的空间,对AMF菌丝形态产生重要影响[50]。AMF侵染宿主植物后菌丝主要形成Arum型和Paris型两种形态,前者主要形成皮层细胞间菌丝和细胞内丛枝,后者主要形成细胞内菌丝和丛枝。研究表明,不同宿主植物接种同一AMF后形成的菌丝形态不同,不同AMF侵染同一宿主植物也会形成不同形态的菌丝,而菌丝形态的不同可能影响其功能[51-52]。
综上,根据土壤的实际情况选择合适的宿主植物,建立良好的互惠互利共生关系是发挥AM功能的关键。但单纯选择AMF侵染率或宿主植物生长指标筛选宿主植物或AMF菌种,可能并不能达到最高去除效率。在修复应用中应当针对被修复土壤的污染浓度选取适应性较强的AMF,且在能够促进宿主植物生长的前提下,还要关注菌丝形态、根际促生菌及相关酶活性的变化,才能最大程度地发挥宿主植物与AMF共生依赖关系随土壤条件恶化而增强的作用,最终实现石油污染土壤的高效修复。
2.2.3 接种方法对AM修复效率的影响由于原油成分的复杂性和难降解性,单一菌种可能无法完全降解石油烃污染物,并且修复效果难以持久。一些已报道研究发现,AMF和其他菌剂混合接种对石油烃的降解作用大于单一接种处理[53]。研究表明,某些细菌不仅能够直接降解土壤中的污染物,而且有助于AMF在污染土壤中的存活和扩繁,从而提高污染物的降解效率[54]。如王丽丽和杨谦[36]研究发现,混合接种枯草芽孢杆菌(Bacillus subtilis)和地斗管囊霉(F. geosporum)对石油污染土壤的修复效果优于单一菌剂接种。耿春女等[55]发现,AMF和细菌混合接种对柴油的降解显示出明显的协同效应。Xun等[56]在中等污染土壤研究中发现,植物根际促生菌不动杆菌(Acinetobacter sp.)和根内根孢囊霉处理植物的总石油烃降解率最高。王楚栋等[57]选用玉米接种摩西斗管囊霉,并添加动物源生物质炭来研究其对多氯联苯的修复效应,结果显示添加该生物质炭能够显著提高AMF侵染率。Abbaspour等[58]比较发现,接种AMF且添加生物质炭有效促进了石油的降解率。混接AMF和其他菌种或添加其他物质主要通过改善土壤营养状况,改变植物根际微生物群落结构和土壤酶活性提高石油污染物的去除率,但对AMF定殖生长影响却不相同。混接枯草芽孢杆菌并未提高AMF侵染率,但增加了宿主植物的生物量,枯草芽孢杆菌的存在可能使植株内丙二醛含量降低,从而提高对石油胁迫的抵御能力[36]。但混接根瘤菌不仅能提高AMF的侵染率,且显著增加宿主植物的生物量,这种协同效应在盐碱土中更为显著[59]。可见根际促生菌可能通过提高植株抗氧化能力或根系细胞渗透调节力,提高对逆境的抵御能力[60]。添加生物质炭提高了AMF侵染率,表明生物质炭的多孔结构改善了土壤通气性,有利于菌根生长,且生物质炭具有较大的比表面积,对有机污染物产生吸附作用。
此外,一些研究接种两种或两种以上AMF于石油污染土壤,修复效果却并不一致。如王丽萍等[44]将摩西球囊霉和地表球囊霉菌接种到玉米根系上,发现与单接种处理相比,双重接种显著提高了石油烃的降解效率。Gao等[61]的研究中也发现,接种2种AMF对菲和芘的降解更有效。而Malicka等[62]却发现单一菌种接种促进了植物生长,而混合菌种(F. caledonium、Diversispora varaderana和C. walkeri)接种对植物生长无影响,甚至阻碍植物生长。尽管许多AMF菌种生存于受石油污染土壤中,如无梗囊霉属(Acaulospora sp.)、原囊霉属(Archaeospora sp.)、近明球囊霉属(Claroideoglomus sp.)、多样孢囊霉属(Diversispora sp.)、根内根孢囊霉等(表 1),但不同AMF菌种对污染环境的抵御能力存在差异。如球囊霉目(Glomerales)将自身生物量分配给根内菌丝,以此避免与环境污染物之间接触来降低胁迫,而多样饱囊霉目(Diversisporales)菌种更多地产生根外菌丝[63],因此它在受污染土壤中的耐受力较弱。如与此类低耐受性的AMF菌种混合接种,不仅无法提高植物耐性,还会消耗部分本该用于耐受较高的AMF菌种生长的碳与养分,抑制耐受较高的AMF菌种的生长。因此,在这种组合混合接种情况下,反而不能促进植物生长,也不利于石油污染物的高效去除。
综上,单一或混合AMF菌种接种,或添加其他菌种和物质组合可能极大地影响AM技术对石油污染土壤的修复效果(表 2),在修复效率和经济成本的权衡下,选择石油胁迫下耐受性较高的AMF菌种,再适当添加协同修复物质将有助于提高石油污染土壤修复效率。
|
|
表 2 近年来将AM技术应用于石油污染土壤修复的研究案例 Table 2 Case studies of mycorrhizal technology in remediating petroleum-contaminated soil in recent years |
各种环境条件变化将会影响AMF的侵染、扩繁、生理代谢活动,以及与宿主植物的共生关系等,从而影响其对污染土壤的修复效应,其中以土壤养分、pH、水分、温度等影响最大[67]。土壤养分对AM的发育与功能有直接影响,营养元素和有机质等含量过高或过低时,都会显著降低AMF对宿主植物的侵染率,使AM修复效率受到影响[68]。pH对植物和AMF的生长都存在较大影响。邓杰等[69]发现,植物生长指标随pH降低而显著降低,接种AMF后缓解了酸胁迫对紫花苜蓿生长的影响。但pH过低会对AMF本身产生影响,如冯曾威等[70]在试验中设置了4个pH,分别为3.7、4.5、5.5和6.5,发现当pH低于5.5时,AMF丰度开始降低,植物生物量也开始降低,表明低pH显著抑制AMF与植物的共生作用。酸胁迫下,AMF可能通过诱导植物氧化应激反应来缓解酸对植物的伤害,但植物也减少了向AMF运输脂类物质,从而不利于AM形成[71]。土壤碱化通常伴随着盐分过高,会破坏土壤物理结构,使通风条件恶化,土壤养分的释放受到抑制。AMF可通过改变植物营养元素吸收、离子平衡、激素水平等来提高宿主植物对盐碱环境的适应性,但pH过高也会抑制AMF孢子的萌发、菌丝的生长及其在土壤中的延伸,减少AMF与植物根部接触的机会[72]。目前直接研究土壤酸碱性对AM修复石油污染土壤效果影响的文献报道较少,从以往修复试验用土来看,pH在7左右的修复效率较高,pH低于5或高于9,将会降低修复效率。土壤湿度也是AMF生长发育的一个重要影响因素,当土壤含水量过低,微生物不能得到充足的水分供应,细胞活性受到抑制;但过多的水分会充满土壤有效毛细孔隙而阻碍氧气的供应[73]。研究表明,当土壤含水量为田间持水量的50%~60% 时,AMF侵染率最高,含水量高于这个范围时侵染率将减少一半[74]。此外,AMF孢子的萌发和菌根的形成受到温度的影响,研究发现,AMF孢子密度和侵染率存在明显的季节变化,AMF侵染率和孢子密度秋季高于春季,冬季低于夏季,春夏交替时侵染率最高[75]。温度升高且降水减少会减弱植物与AMF的共生关系[76]。
综上,在实际修复应用中,应考虑各种环境因素的影响,AMF–植物修复技术在一定的养分条件、合适的土壤pH范围及水分含量下,在AMF最适生长的季节才能达到理想的修复效果。全球气候变化趋势下,在一些极端环境和土壤条件下,AMF–植物修复技术的应用潜力也是未来值得关注的研究方向。
3 AM对石油污染物的去除机制石油主要包括各种碳氢化合物(正构烷烃、异构烷烃、烯烃、环烷烃、芳香烃)、含氧化合物、含硫化合物、含氮化合物、沥青质、树脂等。但因原油来源不同,其中链烷烃大约占15%~60%,环烷烃占30%~60%,芳香烃占3%~30%[77]。研究发现,AMF可能通过自身代谢、固定稳定化作用直接去除石油污染物,还可以通过调节根际分泌物等作用增强根际微生物效应而间接去除石油污染物[5, 40]。
3.1 AM的直接去除作用AMF可能以石油污染物为碳源,通过自身的生命代谢方式将一些石油污染物分解为简单的有机物、碳水化合物、水和盐,从而降低石油污染物的毒性[78]。由于外生菌根(Ectomycorrhizal mycorrhiza,ECM)可实现纯培养生长,为其降解有机污染物提供研究条件,对有机污染物(包括农药、PAHs和石油等)的直接降解作用的发现主要来自ECM真菌的相关研究[79-80]。AMF是一种不能纯培养的专性活微生物,主要通过菌根侵染率、孢子数量等指标表征其与石油污染物去除的关系。Binet等[81]发现,土壤中PAHs经AM修复后,仅有0.11‰吸附于植物根系,0.16‰和0.001‰积累于植物根系和茎秆组织,而高达66% 通过微生物分解等途径消散,且接种AMF后使植物去除途径的占比更少。Volante等[82]发现,接种摩西球囊霉、球状巨孢囊霉(Gigaspora Margarita)和玫瑰红巨孢囊霉(Gi. Rosea)后,经灭菌、人工添加污染物的土壤中芳香烃类污染物浓度显著减少,认为该芳香烃类污染物的去除与AMF接种有直接关系。这些研究表明,接种AMF能够显著提高石油污染物的去除率,虽然不能直接证明AMF对烃类污染物的直接降解作用,但为AM技术修复石油污染土壤和优化降解条件提供了科学依据。
土壤中有机污染物的生物毒性与其存在形态有关,结合态比提取态的环境风险低,但这两种形态处于动态平衡,环境条件的改变会引起两者间的转化[83]。研究表明,AM的形成能改变土壤中有机污染物的形态,从而影响其生物安全性。如Gao等[42]首次发现,AMF产生的球囊霉素能够使PAHs从土壤颗粒解吸进入土壤溶液中,从而提高了PAHs的微生物可获得性,促进了PAHs的降解。另一方面,如果有机污染物能被封锁在土壤中,则生物毒害的可能性也会降低。研究发现,AM的某些生物结构能够积累有机污染物,从而减少它们向植物的迁移。如Gaspar等[43]在地斗管囊霉孢子中检测到PAHs,直接证明了孢子具有吸收和积累PAHs作用。Gao等[61]的研究也说明了AMF菌丝能够吸收土壤中的PAHs。Aranda等[84]也发现护卫根孢囊霉(R.custos)孢子和菌丝能够积累PAHs,并阻止PAHs进入植物根系。石油污染物大多是由烃类物质组成,烃类具有疏水性质,影响了植物对水分和其他无机营养的吸收,AMF能够吸收烃类物质,对植物的生长和最终的修复效率都有一定的提升。此外,AM具有的泡囊和根外附着胞等结构中脂类物质含量较高,可以增加它们对有机污染物的固定和吸附,改变其在植物体内的分布和迁移,从而降低根系中毒的风险[43]。
3.2 AM的间接去除作用根际是在物理、化学和生物学特性上不同于周围土体的植物根系表面的一个微域环境,AMF的菌丝能够进入植物根所不能进入的土壤孔隙里面,改良土壤结构,AM及其外延菌丝与土壤颗粒的紧密接触,使根际环境大大增加,菌根际的空间、养分和生态条件有效改善了微生物的生存环境,改变了微生物群落组成和功能,使具有降解活性的微生物可以快速增殖,从而促进微生物对污染物的降解[61, 85]。因此,根际污染物的降解修复越来越受到关注[37]。
AM可能改变根际微生物群落结构,从而影响有机污染物的去除。如Ingrid等[64]研究发现,接种异形根孢囊霉(R. irregularis)使根际革兰氏阳性细菌和阴性菌分别增加56% 和37%,提高了污染土壤中PAHs和烷烃的去除率。另一些研究发现,接种AMF使真菌比例增加。如王曙光等[86]报道,接种光壁无梗囊霉(A. laevis)和苏格兰斗管囊霉(F. caledonium)后菌丝际土壤中邻苯二甲酸二酯的去除率最高,而菌丝际微生物数量比对照组有所减少,但其中真菌的比例增加。李秋玲等[85]报道,接种AMF后提高了土壤中菲与芘的降解,同时发现土壤中细菌、真菌和放线菌数量都明显提高,其中真菌数量与PAHs去除率间正相关关系尤为显著。肖敏[87]在PAHs污染土壤的三隔室试验研究中也发现,菌根际和菌丝际土壤中细菌、真菌和放线菌的数量显著高于未接种处理,其中真菌数量增加最多。由此可见,根际真菌比例增加可能是接种AMF提高土壤中有机污染物去除率的原因之一。如Gramss等[88]发现,真菌对5~7环PAHs的去除率比细菌更强。接种AMF后其他真菌对有机污染物的去除贡献还需要更多研究来验证。
AMF侵染的植物根际微生物数量变化趋势不一致。接种AMF后可能抑制或增加根际土壤微生物数量,但菌丝际土壤中微生物数量通常是增加的。菌根际的微生物变化可能主要受植物根系分泌物的影响,如Rentz等[89]发现,有机酸、葡萄糖和谷氨酸等根际分泌物抑制了可降解菲的假单胞菌的活性。接种AMF后根系分泌物可能发生改变,如Li等[49]接种AMF使根际亚麻油酸、5-甲氧基水杨酸等有机酸浓度显著增加,且一些研究表明这些脂肪酸能够激发PAHs降解菌,或为其提供了共代谢底物[90],因此提高PAHs的去除率。AMF菌丝不断扩展,一些研究表明菌丝际为细菌,特别是根际促生菌提供了良好的生态位。秦华等[91]以美国南瓜(Cucubita pepo)为供试植物,用摩西斗管囊霉侵染发现菌丝际微生物量显著高于未接种对照组,且菌丝量与多氯联苯总量呈显著负相关,排除根际效应后发现菌丝也能够影响土壤中微生物群落,提高对多氯联苯的降解效率。菌根际与菌丝际间根系分泌物的种类与浓度、菌丝提供的空间等条件不同,都会使菌根际和菌丝际土壤中有机污染物的去除效果产生差异。
土壤酶是土壤的重要组成部分,主要包括在土壤中积累的酶活性,并且酶活性从土壤生物(微生物、动物活体、植物根)释放到土壤中。土壤酶可分为五大类:水解酶、氧化酶,还原酶、转移酶、裂解酶[92]。根据微生物对石油烃好氧降解机理的研究报道,石油烃类有机污染物进入微生物细胞膜后,首先通过氧化还原酶类和水解酶类的作用被降解。其中烷烃和环烷烃通过催化氧化酶的末端、次末端或双末端加氧氧化而转化为脂肪酸;芳香烃首先被单加氧酶、芳烃双加氧酶或苯酚羟化酶等催化转化为邻苯二酚中间产物,再通过邻苯二酚双加氧酶邻位或间位氧化开环裂解[93]。可见在此过程中,加氧酶和脱氢酶起着重要作用。Lu和Lu[47]研究发现接种苏格兰斗管囊霉提高了土壤中多酚氧化酶活性,且土壤中nidA基因拷贝数增加,表明PAHs降解相关的分枝杆菌也在快速增长。刘世亮等[94]发现,以紫花苜蓿为宿主植物接种苏格兰斗管囊霉后,土壤中多酚氧化酶活性增加显著,苯并芘的降解增强。肖敏[87]发现,在菲、芘污染的土壤中,由于摩西球囊霉和幼套近明球囊霉的接种,土壤中多酚氧化酶、酸性磷酸酶和过氧化氢酶活性增强。黄玲玲等[34]发现,过氧化氢酶活性随土壤中石油烃污染浓度的增加显著增加。张瑞芹等[95]发现,AM可促进根系的抗氧化酶活性。因此,AM可能通过促进相关酶的分泌而间接降解土壤中的有机污染物,包括一些不能被细菌单独降解的有机污染物。
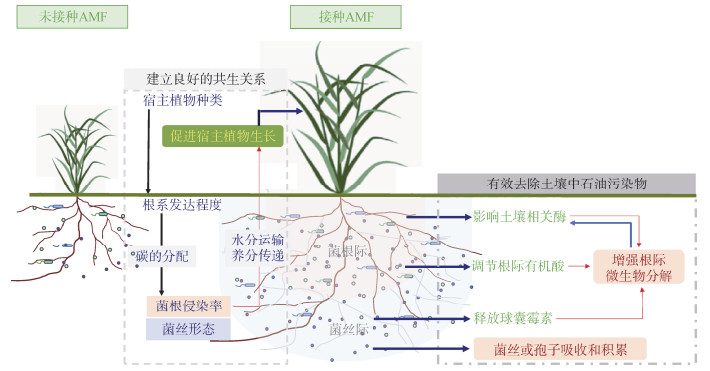
综上所述,AMF孢子和菌丝能够积累石油污染物,同时还能够分泌出球囊霉素等物质影响石油污染物在土壤中的生物活性,对土壤中石油污染物产生直接去除作用。AM通过调节根系分泌物,增强石油污染物降解相关酶活性,改变根际和菌丝际微生物群落结构等方面,间接影响土壤中石油污染的去除(图 1)。这些都对植物和土壤健康状况的提升以及根际微环境的改善具有重要意义,增强了该技术在石油污染土壤修复中的应用潜力。
|
图 1 AM在石油污染土壤修复中的作用机制 Fig. 1 Role mechanism of arbuscular mycorrhizae in remediating petroleum-contaminated soil |
随着AMF生理和生态功能研究的深入,AM技术在污染土壤的修复方面也取得了较好的应用示范效果,其在污染治理和环境保护领域有着广阔的应用前景。AMF与植物根系共生体不仅能够提高植物在石油污染土壤中的抗胁迫能力,而且还调节了根系分泌物和特定酶的产生,增强了根际其他微生物的活性,从而促进了土壤石油污染物的去除。AM修复技术集聚了植物修复和微生物修复技术的优点,但目前该技术还处于起步阶段,对石油污染物质的降解机制及实际应用情况了解甚少,今后可从以下5个方面作进一步的研究。
1) 开展AM对土壤中不同毒性石油组分的去除研究。石油污染物成分复杂,目前的研究中常以修复前后总石油烃含量的变化作为测定指标来检验AM的修复效率。可从修复前后石油烃具体成分的变化,特别是不同毒性的污染物质,以揭示AM在修复中的主要去除成分,从而深入了解其去除机制,挖掘其应用潜力。
2) 探究AMF菌丝形态对石油污染土壤修复的影响。针对石油污染土壤首先确定适应性较强的宿主植物,再来筛选共生依赖性强的AMF菌种,并从AMF菌丝形态等结构角度研究AM对污染物的降解、吸收、转移的比例贡献,建立AM形态结构与去除途径的相关关系,为AM技术修复效率的提高提供方向。
3) 开发AMF与其他根际有益微生物协同修复路径。研究AMF与细菌、其他菌根真菌或与多种有益微生物共接种,或引入其他物质等,更好地发挥协同作用和群落效应,构建AMF与其他有益菌的合成菌群并研发修复石油污染土壤的微生物菌剂。
4) 尝试AM应用于大面积石油污染土壤原位修复工程。AM技术对石油污染土壤的修复效应还与诸多其他环境因素相关,如土壤养分、水分、温度等条件,现有研究大多在实验室开展,对实际污染场地的修复实践甚少,全球变化下特定或极端环境下的修复效率是否能够得到保证,如何改善受限的环境条件,是该技术成功应用的关键。
| [1] |
Kalter V, Passow U. Quantitative review summarizing the effects of oil pollution on subarctic and Arctic marine invertebrates[J]. Environmental Pollution, 2023, 319: 120960 DOI:10.1016/j.envpol.2022.120960 (  0) 0) |
| [2] |
黄艺, 汪杰, 陈惠苑, 等. 中国主要产油区土壤石油污染及其毒性评估[M].
科学出版社, 北京, 2018: 1-6
(  0) 0) |
| [3] |
Gao H, Wu M L, Liu H, et al. Effect of petroleum hydrocarbon pollution levels on the soil microecosystem and ecological function[J]. Environmental Pollution, 2022, 293: 118511 DOI:10.1016/j.envpol.2021.118511 (  0) 0) |
| [4] |
Sharma K, Shah G, Singhal K, et al. Comprehensive insights into the impact of oil pollution on the environment[J]. Regional Studies in Marine Science, 2024, 74: 103516 DOI:10.1016/j.rsma.2024.103516 (  0) 0) |
| [5] |
Wang F Y, Adams C A, Yang W W, et al. Benefits of arbuscular mycorrhizal fungi in reducing organic contaminant residues in crops: Implications for cleaner agricultural production[J]. Critical Reviews in Environmental Science and Technology, 2020, 50(15): 1580-1612 DOI:10.1080/10643389.2019.1665945 (  0) 0) |
| [6] |
李俊, 胡健, 马文敏, 等. 石油污染土壤修复技术研究进展[J]. 生态学杂志, 2024, 43(8): 2502-2512 (  0) 0) |
| [7] |
O'Brien P L, DeSutter T M, Casey F X M, et al. Thermal remediation alters soil properties–a review[J]. Journal of Environmental Management, 2018, 206: 826-835 DOI:10.1016/j.jenvman.2017.11.052 (  0) 0) |
| [8] |
Ali N, Bilal M, Khan A, et al. Effective exploitation of anionic, nonionic, and nanoparticle-stabilized surfactant foams for petroleum hydrocarbon contaminated soil remediation[J]. Science of the Total Environment, 2020, 704: 135391 DOI:10.1016/j.scitotenv.2019.135391 (  0) 0) |
| [9] |
邓旭, 陈余道, 邓日添, 等. PS缓释处理岩溶水石油污染过程中电子受体的利用[J]. 环境工程学报, 2024, 18(6): 1531-1540 (  0) 0) |
| [10] |
杜亚鲁, 胡韬, 彭琳. 土壤石油污染的生物修复技术研究进展[J]. 环境科学与技术, 2017, 40(S1): 133-138 (  0) 0) |
| [11] |
Nwankwegu A S, Zhang L, Xie D T, et al. Bioaugmentation as a green technology for hydrocarbon pollution remediation. Problems and prospects[J]. Journal of Environmental Management, 2022, 304: 114313 DOI:10.1016/j.jenvman.2021.114313 (  0) 0) |
| [12] |
朱林海, 丁金枝, 王健健, 等. 石油污染对土壤–植物系统的生态效应[J]. 应用与环境生物学报, 2012, 18(2): 320-330 (  0) 0) |
| [13] |
山宝琴, 屈萌萌, 李皎, 等. 丛枝菌根真菌与植物共生修复陕北石油污染土壤[J]. 草业学报, 2016, 25(7): 87-94 (  0) 0) |
| [14] |
Dickson U J, Coffey M, Mortimer R J G, et al. Mycoremediation of petroleum contaminated soils: Progress, prospects and perspectives[J]. Environmental Science: Processes & Impacts, 2019, 21(9): 1446-1458 (  0) 0) |
| [15] |
程国玲, 孙晖, 杜葳. 菌根真菌对有机污染物的降解研究[J]. 土壤通报, 2007, 38(4): 799-803 (  0) 0) |
| [16] |
Hoang S A, Lamb D, Seshadri B, et al. Rhizoremediation as a green technology for the remediation of petroleum hydrocarbon-contaminated soils[J]. Journal of Hazardous Materials, 2021, 401: 123282 DOI:10.1016/j.jhazmat.2020.123282 (  0) 0) |
| [17] |
Genre A, Lanfranco L, Perotto S, et al. Unique and common traits in mycorrhizal symbioses[J]. Nature Reviews Microbiology, 2020, 18(11): 649-660 DOI:10.1038/s41579-020-0402-3 (  0) 0) |
| [18] |
Duan S L, Jin Z X, Zhang L, et al. Mechanisms of cooperation in the plants-arbuscular mycorrhizal fungi-bacteria continuum[J]. The ISME Journal, 2025, 19(1): wraf023 DOI:10.1093/ismejo/wraf023 (  0) 0) |
| [19] |
Tang B, Man J, Lehmann A, et al. Arbuscular mycorrhizal fungi benefit plants in response to major global change factors[J]. Ecology Letters, 2023, 26(12): 2087-2097 (  0) 0) |
| [20] |
Holátko J, Brtnický M, Kučerík J, et al. Glomalin–Truths, myths, and the future of this elusive soil glycoprotein[J]. Soil Biology and Biochemistry, 2021, 153: 108116 DOI:10.1016/j.soilbio.2020.108116 (  0) 0) |
| [21] |
陈保冬, 于萌, 郝志鹏, 等. 丛枝菌根真菌应用技术研究进展[J]. 应用生态学报, 2019, 30(3): 1035-1046 (  0) 0) |
| [22] |
Rajtor M, Piotrowska-Seget Z. Prospects for arbuscular mycorrhizal fungi (AMF) to assist in phytoremediation of soil hydrocarbon contaminants[J]. Chemosphere, 2016, 162: 105-116 DOI:10.1016/j.chemosphere.2016.07.071 (  0) 0) |
| [23] |
严康, 楼骏, 汪海珍, 等. 污染场地研究现状与发展趋势: 基于知识图谱的分析[J]. 土壤学报, 2021, 58(5): 1234-1245 (  0) 0) |
| [24] |
耿春女, 李培军, 陈素华, 等. 不同AM真菌对三叶草耐油性的影响[J]. 应用与环境生物学报, 2002, 8(6): 648-652 (  0) 0) |
| [25] |
王春丽. 石油污染土壤中丛枝菌根菌的分布及其对石油的降解效应[D]. 泰安: 山东农业大学, 2005: 49–55.
(  0) 0) |
| [26] |
黄继(如生), 唐明, 牛振川, 等. 四川遂宁地区石油污染土壤中丛枝菌根真菌[J]. 生态学杂志, 2007, 26(9): 1389-1392 (  0) 0) |
| [27] |
Cabello M N. Hydrocarbon pollution: Its effect on native arbuscular mycorrhizal fungi (AMF)[J]. FEMS Microbiology Ecology, 1997, 22(3): 233-236 DOI:10.1111/j.1574-6941.1997.tb00375.x (  0) 0) |
| [28] |
Hassan S E, Bell T H, Stefani F O P, et al. Contrasting the community structure of arbuscular mycorrhizal fungi from hydrocarbon-contaminated and uncontaminated soils following willow (Salix spp. L.) planting[J]. PLoS One, 2014, 9(7): e102838 DOI:10.1371/journal.pone.0102838 (  0) 0) |
| [29] |
Lee S J, Kong M X, St-Arnaud M, et al. Arbuscular mycorrhizal fungal communities of native plant species under high petroleum hydrocarbon contamination highlights Rhizophagus as a key tolerant genus[J]. Microorganisms, 2020, 8(6): 872 DOI:10.3390/microorganisms8060872 (  0) 0) |
| [30] |
Garcés-Ruiz M, Senés-Guerrero C, Declerck S, et al. Arbuscular mycorrhizal fungal community composition in Carludovica palmata, Costus scaber and Euterpe precatoria from weathered oil ponds in the Ecuadorian Amazon[J]. Frontiers in Microbiology, 2017, 8: 2134 DOI:10.3389/fmicb.2017.02134 (  0) 0) |
| [31] |
Ryszka P, Zarzyka-Ryszka M, Anielska T, et al. Arbuscular mycorrhizal fungi from petroleum-impacted sites in the Polish Carpathians[J]. International Biodeterioration & Biodegradation, 2019, 138: 50-56 (  0) 0) |
| [32] |
Dagher D J, de la Providencia I E, Pitre F E, et al. Arbuscular mycorrhizal fungal assemblages significantly shifted upon bacterial inoculation in non-contaminated and petroleum-contaminated environments[J]. Microorganisms, 2020, 8(4): 602 DOI:10.3390/microorganisms8040602 (  0) 0) |
| [33] |
Iffis B, St-Arnaud M, Hijri M. Petroleum hydrocarbon contamination, plant identity and arbuscular mycorrhizal fungal (AMF) community determine assemblages of the AMF spore-associated microbes[J]. Environmental Microbiology, 2016, 18(8): 2689-2704 DOI:10.1111/1462-2920.13438 (  0) 0) |
| [34] |
黄玲玲, 李莎, 唐明. 石油污染土壤中不同人工林木根际丛枝菌根真菌与球囊霉素的研究[J]. 西北植物学报, 2012, 32(3): 573-578 (  0) 0) |
| [35] |
雒晓芳, 陈丽华, 杨成波, 等. 植物–微生物联合修复石油污染土壤的实验室模拟[J]. 兰州大学学报(自然科学版), 2015, 51(3): 411-417 (  0) 0) |
| [36] |
王丽丽, 杨谦. 接种枯草芽孢杆菌和丛枝菌根真菌促进红三叶修复石油污染土壤[J]. 江苏农业科学, 2016, 45(5): 526–528, 529 (  0) 0) |
| [37] |
宗炯, 朱雪竹, 凌婉婷, 等. 多环芳烃污染对丛枝菌根真菌生物学性状的影响[J]. 农业环境科学学报, 2014, 33(2): 305-312 (  0) 0) |
| [38] |
白雪梅, 王甲敏, 陈开芳, 等. 接种AM真菌对利用冰草降解土壤石油污染的效果研究[J]. 延安大学学报(自然科学版), 2017, 36(4): 34-37 (  0) 0) |
| [39] |
周利承, 曹梦珂, 郑晨露, 等. 接种丛枝菌根真菌对紫花苜蓿修复石油污染土壤的潜在作用[J]. 应用与环境生物学报, 2020, 26(5): 1129-1137 (  0) 0) |
| [40] |
骆永明. 有机污染土壤的修复机制与技术发展[M].
科学出版社, 北京, 2016
(  0) 0) |
| [41] |
Leyval C, Binet P. Effect of polyaromatic hydrocarbons in soil on arbuscular mycorrhizal plants[J]. Journal of Environmental Quality, 1998, 27(2): 402-407 (  0) 0) |
| [42] |
Gao Y Z, Zong J, Que H, et al. Inoculation with arbuscular mycorrhizal fungi increases glomalin-related soil protein content and PAH removal in soils planted with Medicago sativa L[J]. Soil Biology and Biochemistry, 2017, 115: 148-151 DOI:10.1016/j.soilbio.2017.08.023 (  0) 0) |
| [43] |
Gaspar M, Cabello M, Cazau M, et al. Effect of phenanthrene and Rhodotorula glutinis on arbuscular mycorrhizal fungus colonization of maize roots[J]. Mycorrhiza, 2002, 12(2): 55-59 DOI:10.1007/s00572-001-0147-4 (  0) 0) |
| [44] |
王丽萍, 郭光霞, 华素兰, 等. 丛枝菌根真菌–植物对石油污染土壤修复实验研究[J]. 中国矿业大学学报, 2009, 38(1): 91-95 (  0) 0) |
| [45] |
Alejandro-Córdova A, Rivera-Cruz M C, Hernández-Cuevas L V, et al. Responses of arbuscular mycorrhizal fungi and grass Leersia hexandra swartz exposed to soil with crude oil[J]. Water, Air, & Soil Pollution, 2017, 228(2): 65 (  0) 0) |
| [46] |
Małachowska-Jutsz A, Kalka J. Influence of mycorrhizal fungi on remediation of soil contaminated by petroleum hydrocarbons[J]. Fresenius Environmental Bulletin, 2010, 19: 3217-3223 (  0) 0) |
| [47] |
Lu Y F, Lu M. Remediation of PAH-contaminated soil by the combination of tall fescue, arbuscular mycorrhizal fungus and epigeic earthworms[J]. Journal of Hazardous Materials, 2015, 285: 535-541 DOI:10.1016/j.jhazmat.2014.07.021 (  0) 0) |
| [48] |
马俊卿, 侯宁, 孙晨瑜, 等. 宿主不同对丛枝菌根真菌扩繁效应的影响[J]. 中国农学通报, 2022, 38(1): 7-14 (  0) 0) |
| [49] |
Li X, Kang X F, Zou J Z, et al. Allochthonous arbuscular mycorrhizal fungi promote Salix viminalis L.-mediated phytoremediation of polycyclic aromatic hydrocarbons characterized by increasing the release of organic acids and enzymes in soils[J]. Ecotoxicology and Environmental Safety, 2023, 249: 114461 DOI:10.1016/j.ecoenv.2022.114461 (  0) 0) |
| [50] |
Brundrett M, Kendrick B. The roots and mycorrhizas of herbaceous woodland plants: I. Quantitative aspects of morphology[J]. The New Phytologist, 1990, 114(3): 457-468 DOI:10.1111/j.1469-8137.1990.tb00414.x (  0) 0) |
| [51] |
Cavagnaro T R, Gao L L, Smith F A, et al. Morphology of arbuscular mycorrhizas is influenced by fungal identity[J]. New Phytologist, 2001, 151(2): 469-475 DOI:10.1046/j.0028-646x.2001.00191.x (  0) 0) |
| [52] |
Giesemann P, Rasmussen H N, Liebel H T, et al. Discreet heterotrophs: Green plants that receive fungal carbon through Paris-type arbuscular mycorrhiza[J]. New Phytologist, 2020, 226(4): 960-966 DOI:10.1111/nph.16367 (  0) 0) |
| [53] |
何翊, 魏薇, 吴海. 菌剂–菌根联合修复石油污染土壤的实验研究[J]. 土壤, 2004, 36(6): 675-677 (  0) 0) |
| [54] |
Bento R A, Saggin-Júnior O J, Pitard R M, et al. Selection of leguminous trees associated with symbiont microorganisms for phytoremediation of petroleum-contaminated soil[J]. Water, Air, & Soil Pollution, 2012, 223(9): 5659-5671 (  0) 0) |
| [55] |
耿春女, 李培军, 陈素华, 等. 不同丛枝菌根真菌对万寿菊生长及柴油降解率的影响[J]. 应用生态学报, 2003, 14(10): 1775-1779 (  0) 0) |
| [56] |
Xun F F, Xie B M, Liu S S, et al. Effect of plant growth-promoting bacteria (PGPR) and arbuscular mycorrhizal fungi (AMF) inoculation on oats in saline-alkali soil contaminated by petroleum to enhance phytoremediation[J]. Environmental Science and Pollution Research, 2015, 22(1): 598-608 DOI:10.1007/s11356-014-3396-4 (  0) 0) |
| [57] |
王楚栋, 单明娟, 陆扣萍, 等. 丛枝菌根真菌及猪炭对多氯联苯污染土壤的联合修复作用[J]. 环境科学学报, 2018, 38(10): 4157-4164 (  0) 0) |
| [58] |
Abbaspour A, Zohrabi F, Dorostkar V, et al. Remediation of an oil-contaminated soil by two native plants treated with biochar and mycorrhizae[J]. Journal of Environmental Management, 2020, 254: 109755 DOI:10.1016/j.jenvman.2019.109755 (  0) 0) |
| [59] |
邢易梅, 蕫理, 战力峰, 等. 混合接种摩西球囊霉和根瘤菌对紫花苜蓿耐碱能力的影响[J]. 草业学报, 2020, 29(9): 136-145 (  0) 0) |
| [60] |
秦敬泽, 秦泽峰, 倪刚, 等. AMF和PGPR单独或"跨界"互作促进植物耐盐性的研究进展[J]. 植物营养与肥料学报, 2024, 30(7): 1354-1366 (  0) 0) |
| [61] |
Gao Y Z, Cheng Z X, Ling W T, et al. Arbuscular mycorrhizal fungal hyphae contribute to the uptake of polycyclic aromatic hydrocarbons by plant roots[J]. Bioresource Technology, 2010, 101(18): 6895-6901 DOI:10.1016/j.biortech.2010.03.122 (  0) 0) |
| [62] |
Malicka M, Magurno F, Posta K, et al. Differences in the effects of single and mixed species of AMF on the growth and oxidative stress defense in Lolium perenne exposed to hydrocarbons[J]. Ecotoxicology and Environmental Safety, 2021, 217: 112252 DOI:10.1016/j.ecoenv.2021.112252 (  0) 0) |
| [63] |
Aguilar-Trigueros C A, Hempel S, Powell J R, et al. Bridging reproductive and microbial ecology: A case study in arbuscular mycorrhizal fungi[J]. The ISME Journal, 2019, 13(4): 873-884 DOI:10.1038/s41396-018-0314-7 (  0) 0) |
| [64] |
Ingrid L, Lounès-Hadj Sahraoui A, Frédéric L, et al. Arbuscular mycorrhizal wheat inoculation promotes alkane and polycyclic aromatic hydrocarbon biodegradation: Microcosm experiment on aged-contaminated soil[J]. Environmental Pollution, 2016, 213: 549-560 DOI:10.1016/j.envpol.2016.02.056 (  0) 0) |
| [65] |
杨燕. 油蒿及其根围丛枝菌根真菌共生修复石油污染土壤潜力研究[D]. 延安: 延安大学, 2020.
(  0) 0) |
| [66] |
Alarcón A, Davies F T Jr, Autenrieth R L, et al. Arbuscular mycorrhiza and petroleum-degrading microorganisms enhance phytoremediation of petroleum-contaminated soil[J]. International Journal of Phytoremediation, 2008, 10(4): 251-263 DOI:10.1080/15226510802096002 (  0) 0) |
| [67] |
刘润进, 李晓林. 丛枝菌根及其应用[M].
科学出版社, 北京, 2000
(  0) 0) |
| [68] |
段海霞, 罗崇亮, 师茜, 等. 丛枝菌根真菌对植物–土壤系统的影响研究进展[J]. 生态学报, 2025, 45(1): 475-491 (  0) 0) |
| [69] |
邓杰, 李芳, 古丽君, 等. 不同土壤pH下AM真菌对苜蓿苗期生长的影响[J]. 草业科学, 2019, 36(11): 2854-2862 (  0) 0) |
| [70] |
冯曾威, 王宁, 朱红惠, 等. 低pH影响丛枝菌根真菌丛枝发育和磷的吸收[J]. 菌物学报, 2017, 36(7): 950-962 (  0) 0) |
| [71] |
Feng Z W, Liu X D, Feng G D, et al. Linking lipid transfer with reduced arbuscule formation in tomato roots colonized by arbuscular mycorrhizal fungus under low pH stress[J]. Environmental Microbiology, 2020, 22(3): 1036-1051 DOI:10.1111/1462-2920.14810 (  0) 0) |
| [72] |
丁胜利. AM真菌提高牧草在盐碱化土壤中耐受性的作用机制[D]. 呼和浩特: 内蒙古大学, 2021.
(  0) 0) |
| [73] |
Wu Y B, Cheng Z B, Wu C W, et al. Water conditions and arbuscular mycorrhizal symbiosis affect the phytoremediation of petroleum-contaminated soil by Phragmites australis[J]. Environmental Technology & Innovation, 2023, 32: 103437 (  0) 0) |
| [74] |
Reid C P. Effect of soil moisture on VA mycorrhizae formation//Robles C, Barea J, ed. Arbuscular mycorrhizae and quality[M]. International Conference on Mycorrhizal 2nd. Uppasla: Sweden University of Agricultural Sciences Press, 1998.
(  0) 0) |
| [75] |
Hewins C R, Carrino-Kyker S R, Burke D J. Seasonal variation in mycorrhizal fungi colonizing roots of Allium tricoccum (wild leek) in a mature mixed hardwood forest[J]. Mycorrhiza, 2015, 25(6): 469-483 DOI:10.1007/s00572-015-0628-5 (  0) 0) |
| [76] |
Xie T, Lin Y W, Li X R. Responses of the arbuscular mycorrhizal fungi community to warming coupled with increased drought in an arid desert region[J]. Geoderma, 2024, 441: 116744 DOI:10.1016/j.geoderma.2023.116744 (  0) 0) |
| [77] |
Adebiyi F M. Air quality and management in petroleum refining industry: A review[J]. Environmental Chemistry and Ecotoxicology, 2022, 4: 89-96 DOI:10.1016/j.enceco.2022.02.001 (  0) 0) |
| [78] |
Meharg A A, Cairney J W G. Ectomycorrhizas—extending the capabilities of rhizosphere remediation[J]. Soil Biology and Biochemistry, 2000, 32(11/12): 1475-1484 (  0) 0) |
| [79] |
程国玲, 李培军, 王凤友, 等. 几种纯培养外生菌根真菌对矿物油的降解效果[J]. 中国环境科学, 2003, 23(1): 74-76 (  0) 0) |
| [80] |
Assad R, Reshi Z A, Rashid I, et al. Role of ectomycorrhizal biotechnology in pesticide remediation[M]//Bhat R, Hakeem K, Saud Al-Saud N. Bioremediation and biotechnology. Vol 3. Cham: Springer, 2020.
(  0) 0) |
| [81] |
Binet P, Portal J M, Leyval C. Fate of polycyclic aromatic hydrocarbons (PAH) in the rhizosphere and mycorrhizosphere of ryegrass[J]. Plant and Soil, 2000, 227(1): 207-213 (  0) 0) |
| [82] |
Volante A, Lingua G, Cesaro P, et al. Influence of three species of arbuscular mycorrhizal fungi on the persistence of aromatic hydrocarbons in contaminated substrates[J]. Mycorrhiza, 2005, 16(1): 43-50 DOI:10.1007/s00572-005-0012-y (  0) 0) |
| [83] |
Chen H Y, Tian Y X, Cai Y X, et al. A 50-year systemic review of bioavailability application in Soil environmental criteria and risk assessment[J]. Environmental Pollution, 2023, 335: 122272 DOI:10.1016/j.envpol.2023.122272 (  0) 0) |
| [84] |
Aranda E, Scervino J M, Godoy P, et al. Role of arbuscular mycorrhizal fungus Rhizophagus custos in the dissipation of PAHs under root-organ culture conditions[J]. Environmental Pollution, 2013, 181: 182-189 DOI:10.1016/j.envpol.2013.06.034 (  0) 0) |
| [85] |
李秋玲, 凌婉婷, 高彦征, 等. 丛枝菌根对土壤中多环芳烃降解的影响[J]. 农业环境科学学报, 2008, 27(5): 1705-1710 (  0) 0) |
| [86] |
王曙光, 林先贵, 尹睿. VA菌根对土壤中DEHP降解的影响[J]. 环境科学学报, 2002, 22(3): 369-373 (  0) 0) |
| [87] |
肖敏. 丛枝菌根修复多环芳烃污染土壤的几种酶活性研究[D]. 南京: 南京农业大学, 2009.
(  0) 0) |
| [88] |
Gramss G, Voigt K D, Kirsche B. Degradation of polycyclic aromatic hydrocarbons with three to seven aromatic rings by higher fungi in sterile and unsterile soils[J]. Biodegradation, 1999, 10(1): 51-62 DOI:10.1023/A:1008368923383 (  0) 0) |
| [89] |
Rentz J A, Alvarez P J J, Schnoor J L. Repression of Pseudomonas putida phenanthrene-degrading activity by plant root extracts and exudates[J]. Environmental Microbiology, 2004, 6(6): 574-583 DOI:10.1111/j.1462-2920.2004.00589.x (  0) 0) |
| [90] |
Zhao X, Li J B, Zhang D Y, et al. Mechanism of salicylic acid in promoting the rhizosphere benzo [a] pyrene biodegradation as revealed by DNA-stable isotope probing[J]. Science of the Total Environment, 2022, 810: 152202 DOI:10.1016/j.scitotenv.2021.152202 (  0) 0) |
| [91] |
秦华, 白建峰, 徐秋芳, 等. 丛枝菌根真菌菌丝对土壤微生物群落结构及多氯联苯降解的影响[J]. 土壤, 2015, 47(4): 704-710 (  0) 0) |
| [92] |
Nannipieri P, Bollag J M. Use of enzymes to detoxify pesticide-contaminated soils and waters[J]. Journal of Environmental Quality, 1991, 20(3): 510-517 (  0) 0) |
| [93] |
姬雨. 石油污染土壤细菌群落结构及难降解组分功能基因定量研究[D]. 西安: 长安大学, 2019.
(  0) 0) |
| [94] |
刘世亮, 骆永明, 丁克强, 等. 苯并[a]芘污染土壤的丛枝菌根真菌强化植物修复作用研究[J]. 土壤学报, 2004, 41(3): 336-342 (  0) 0) |
| [95] |
张瑞芹, 卢致霖, 陈洁雯, 等. AM真菌影响三叶草根系抗氧化酶活性的系统效应[J]. 微生物学通报, 2011, 38(3): 322-327 (  0) 0) |
2. Ningbo Research Center for Urban Environment, Chinese Academy of Sciences, Ningbo, Zhejiang 315800, China
 2026, Vol. 58
2026, Vol. 58

