2. 中国科学院大学南京学院, 南京 211135;
3. 中国科学院大学, 北京 100049;
4. 郑州轻工业大学烟草科学与工程学院, 郑州 450002
气候变化导致全球平均温度逐年升高,区域降水模式也随之改变,这对世界各地农业的可持续发展和现代农业水资源管理构成了重大挑战,尤其是在干旱和半干旱地区[1]。在自然变化和人类活动共同作用下,不同时空尺度中土壤水分运移与循环的变化也更加剧烈[2]。在中国,人均水资源占有量不足世界平均水平的1/4,干旱、半干旱地区约占国土面积的51%,无灌溉条件的旱地约占耕地面积的65%[3]。干旱胁迫会改变土壤养分、土壤生物学性状等,从而影响作物生长发育[4]。近年来,农林保水剂在农业和园林领域取得了显著的保水、保肥、改土效果[5-6],已成为应对农业干旱、提高水肥利用率、促进作物增产的重要手段[7]。有关农林保水剂农业应用效果的Meta分析表明,应用农林保水剂可使农业产量平均提高12.8%,水分生产力提高17.2%[8]。
然而,我国现行的行业标准NY/T 886—2022《农林保水剂》主要规定了农林保水剂的吸水倍数、吸盐水倍数、水分含量、pH和粒度5项技术指标,主要关注农林保水剂的吸水性能,缺乏对其保水性能的评价指标。在土壤学中,水势是决定土壤中水分流动方向的关键判据[9-11]。如果农林保水剂吸持水的水势低于土壤水势,即使农林保水剂吸水倍数高,其吸持的水分也无法进入土壤供植物吸收利用[12]。在一定的土壤环境下,农林保水剂中水的能量状态与水运动状态改变的难易程度直接相关,吸持水量只是农林保水剂吸持水分的某一瞬时状态,对于研究农林保水剂吸持水在土壤中的运动是不够的,还必须研究其水分所处的能量状态,因为水分能态的差异是水分在土壤中运动的驱动力[12]。水分在土壤中的时空动态对农业可持续发展、水资源高效管理等方面具有重要的应用价值[13]。
本研究主要参考土壤学中对土壤水能量状态的分析方法,依据热力学第一、第二定律,研究农林保水剂吸持水的能量状态,从功能转换的角度探究农林保水剂的保水性能并给出有效的评价指标,并且开展4种商业农林保水剂的保水性验证试验,以期为农业实践中农林保水剂的评估、选用提供科学依据。
1 材料与方法 1.1 供试土壤和保水剂纤维素购自山东科源生化有限公司,无水乙醇购自南京化学试剂股份有限公司,氯化钠购自国药集团化学试剂有限公司,均为分析纯;供试土壤为红壤,取自中国科学院鹰潭红壤生态实验站,为第四纪红黏土发育而来的典型红壤[14],基本理化性质见表 1。4种商业农林保水剂,分别为绿盟生态保水剂(广州绿盟生态科技有限公司,主要成分:聚丙烯酰胺,简称绿盟保水剂,编号Ⅰ)、氯星保水剂(欧联弘达(北京)工贸有限公司,主要成分:接枝玉米淀粉的聚丙烯酸钾,编号Ⅱ)、沃特保水剂(胜利油田长安控股集团有限公司,主要成分:接枝高岭土等矿物的聚丙烯酸钾,编号Ⅲ)、绿满天下保水剂(任丘市金誉化工有限公司,主要成分:接枝玉米淀粉的聚丙烯酸钠,简称绿满保水剂,编号Ⅳ)。
|
|
表 1 供试红壤基本理化性质 Table 1 Basic physicochemical properties of tested red soil |
土壤基本理化性质测定参考《土壤农化分析》[15]。土壤pH采用玻璃电极法测定(NY/T 1121.2—2006);土壤有机碳含量采用重铬酸钾氧化–外加热法测定(NY/T 1121.6—2006);土壤全氮含量采用硫酸–加速剂消解,凯氏定氮法测定(LY/T 1228—2015);土壤全磷含量采用NaOH碱熔,钼锑抗分光光度法测定(GB/T 9837—1988);土壤全钾含量采用NaOH碱熔,火焰光度计法测定(NY/T 87—1988);土壤碱解氮含量采用碱解扩散法测定(LY/T 1228—2015);土壤有效磷含量采用氟化铵–盐酸溶液浸提,钼锑抗比色法测定(NY/T 1121.7—2014);土壤速效钾含量采用乙酸铵浸提–火焰光度计测定(NY/T 889—2004);土壤含水率采用烘箱恒重法测定。
1.2.2 农林保水剂吸持水的能量类型农林保水剂吸持水的能量类型分析借鉴土壤学对土壤水势(能)的划分方法[12, 16]。通常情况下,农林保水剂吸持水的动能可以忽略,而其中水的能量可以用其势能来代替。根据农林保水剂与水之间不同的吸引力,将其吸持水的势能分为4类:①溶质势能(Es),农林保水剂内的离子吸引自由纯水导致自由纯水相比于标准参考状态的势能变化;②基质势能(Ev),农林保水剂的内外表面分子通过范德华力或氢键吸引自由纯水导致自由纯水相比于标准参考状态下的势能变化;③重力势能(Eg),农林保水剂吸持水由于受到重力导致其相比于标准参考状态下的势能变化;④压力势能(Ep),农林保水剂吸持水由于受到大气压力和周围水的静水压力导致其相比于标准参考状态下的势能变化。标准参考状态通常定义为自由(除了重力以外没有其他力)纯水在参考压力p0、参考温度T0和参考高度z0下的状态[12]。
一般情况下,农林保水剂吸持水的总水势能(Et)是上述各种水势能之和,总水势能(Et)可以通过公式(1)表示:
| $ {E_{\rm t}} = {E_{\rm s}} + {E_{\rm m} } + {E_{\rm g}} + {E_{\rm p}} $ | (1) |
在忽略农林保水剂结构破坏、恒压条件下,对农林保水剂吸水前后吸持水能量变化的热力学分析方法如下。
对农林保水剂开始吸水到吸水饱和这一过程进行分析,农林保水剂吸持的全部纯水可以视为一个封闭系统。根据热力学第一定律,农林保水剂吸持水的内能变化(dU)可表达为[17]:
| $ {\rm d}U = \mathtt{δ} Q + \mathtt{δ} W $ | (2) |
式中:dU表示系统内能的变化(J);δQ表示系统与环境之间以热的形式交换的能量(J);δW表示系统与环境之间以非热的方式交换的能量(J)。
在一般过程中,δW通常包括体积功、表面功、电功、场功和机械功[18],即:
| $ \mathtt{δ} W = - p{\rm d}V + \gamma {\rm d}{A_{\rm s}} + E{\rm d}q + {W_{\rm F}} + {W_{\rm m}} $ | (3) |
式中:p表示外压(pa),dV表示系统体积的改变(m3),–pdV表示体积功(J);γ表示当系统表面积增加一个单位时内能的增量(J/m2),dAs表示系统表面积的改变(m²),γdAs表示表面功(J);E表示系统的外加电势差(V),dq表示在该电势差下通过的电荷量(C),Edq表示电功(J);WF表示反抗场力功,例如重力场或电磁场(J);Wm表示机械功(J)。
对一个系统而言,除了传热和做功,向该系统引入或移出物质(dni)也能改变系统的内能[19-20],因此有:
| $ {\rm d}U = \mathtt{δ} Q - p{\rm d}V + \gamma {\rm d}{A_{\rm s}} + E{\rm d}q + {W_{\rm F}} + {W_{\rm m}} + \Sigma {\mu _{\rm i}}{\rm d}{n_{\rm i}} $ | (4) |
式中:μi是从系统中引入或移出组分i的化学势,这里指的是偏摩尔内能(J/mol);dni表示从系统中引入或移出的组分i的物质的量(mol)。
结合状态函数特征和热力学第二定律,对于系统有:
| $ {\rm d}U = T{\rm d}S - p{\rm d}V + \gamma {\rm d}{A_{\rm s}} + E{\rm d}q + {W_{\rm F}} + {W_{\rm m}} + \Sigma {\mu _{\rm i}}{\rm d}{n_{\rm i}} $ | (5) |
式中:T是系统的温度(K);S是系统的熵(J/K)。
对于农林保水剂吸持的全部纯水这一封闭系统,根据公式(5),在农林保水剂吸水过程中,不涉及电化学装置,不涉及在场内位置的改变(重力场位置变化可以忽略不计),不涉及系统物质的量的变化,因此有WF=Wm=Edq=∑μidni=0。于是对于农林保水剂吸持水有:
| $ {\rm d}U = T{\rm d}S - p{\rm d}V + \gamma {\rm d}{A_{\rm s}} $ | (6) |
将农林保水剂填满一个普通玻璃比色皿(容积:3.5 mL;规格:10 mm;尺寸:12.5 mm×12.5 mm×45 mm)并压实,再将农林保水剂倒入一个500 mL烧杯中,加入400 mL纯水,记录烧杯中农林保水剂吸水前后的液面高度,根据液面变化判断农林保水剂吸水前后体积变化,试验中用纤维素粉作空白对照,因为纤维素亲水性好但膨胀性差。全程使用同一组比色皿和烧杯。
1.2.5 农林保水剂吸水倍数取商业农林保水剂1.0 g,浸入1 000 mL纯水中,每隔1 h取样,用100目筛网滤干农林保水剂自由水分并称重(记为wt),再放回去离子水中继续吸水,以获得不同时间的吸水倍数(Water absorption capacity,WAC),连续监测9 h,待吸水满24 h后,用100目筛网滤干农林保水剂自由水分并称重,得最大吸水倍数(记为wm),吸水倍数(WAC)使用公式计算[21]:
| $ {\rm WAC}=W_{t}–1 $ | (7) |
式中:Wt 指在时间t时农林保水剂吸水凝胶的质量(g)。
1.2.6 农林保水剂保水能力取吸水饱和商业农林保水剂凝胶40 g,放入一个250 mL玻璃瓶中,再放入烘箱中,设置温度为60 ℃,每隔1 h定期称玻璃瓶总重,连续监测7 h;用40 g纯水代替农林保水剂凝胶作为空白对照,其余处理均相同,每组设3个平行。去除玻璃瓶质量,绘制保水剂的质量随时间变化曲线。水分保持能力(Water retention capability,WRC)可通过拟合保水剂质量变化曲线斜率k,根据公式(8)进行计算。
| $ {\rm WRC} = \frac{{{\rm WAC}_m}}{{\left| k \right|}} $ | (8) |
式中:k表示拟合的农林保水剂质量变化曲线的斜率;WACm表示商业农林保水剂的最大吸水倍数。本研究采用的农林保水性测试方法是基于常见的“烘箱加热蒸发法”[22]并结合农林保水剂能量分析设计的新方法。
1.2.7 农林保水剂在红壤中的保水能力将红壤依次过20目和30目筛网,保留20~30目的红壤。将50 g红壤加入250 mL玻璃瓶中,然后向玻璃瓶中添加吸水饱和商业农林保水剂凝胶20 g,再加入50 g红壤,之后将玻璃瓶放入烘箱中,设置温度为60 ℃,每隔1 h定期称重,连续监测7 h;用20 g纯水代替农林保水剂凝胶作为空白对照,其余处理均相同,每组设3个平行。去掉玻璃瓶质量,据此绘制红壤–农林保水剂凝胶体系的质量随时间变化曲线。
1.2.8 农林保水剂吸水过程热效应将200 mL无水乙醇倒入一个玻璃培养皿中(直径15 cm,壁高3 cm),在其中放一个500 mL玻璃烧杯,向烧杯中加入200 mL纯水。将一个数显温度计置于500 mL烧杯中测水温,另一个数显温度计置于玻璃培养皿中测乙醇温度。称取50 g商业农林保水剂倒入500 mL烧杯中,每隔1 min分别记录烧杯内纯水和玻璃培养皿中乙醇的温度,持续观测10 min。4种商业农林保水剂采用同一套试验装置。商业农林保水剂、纯水和无水乙醇的温度在试验前均平衡到空气温度(21℃)。
1.3 数据分析和绘图采用SPSS v27单因素方差分析(ANOVA)进行数据显著性检验;使用Origin 2024对数据进行绘图,拟合曲线函数时采用Origin中分析模块的线性拟合。
2 结果和讨论 2.1 农林保水剂吸水过程的热力学分析试验结果(图 1)显示,农林保水剂吸水后形成的水凝胶体积大于吸水前农林保水剂和纯水的总体积之和,表明存在对外体积功,因此−pdV<0。当水分子被农林保水剂表面的亲水基团吸持后,水分子从三维自由运动转变为表面的受限二维运动,导致纯水的运动自由度减少,从而降低水分子的熵(dS<0)[18]。在农林保水剂吸水过程中,水从液态转变为半固态,从自由流动状态变为相对固定的非流动状态,这一过程反映了随着系统从自由运动向相对固定转变,水分子无序性的损失(dS<0),至于TdS这一项的大小,需结合农林保水剂吸水热效应的结果进行讨论。纯水被农林保水剂吸持后,由于农林保水剂颗粒的分散性,形成了多种大小不一的水凝胶,与纯水的原始状态相比,农林保水剂吸持水的总表面积因形成大量水凝胶而增加,类似于水被分割成很多小块凝胶,导致水的表面能增加,γdAS>0。在农林保水剂吸水过程中,被农林保水剂吸持的纯水从液态转变为半固态,表明农林保水剂的结合力大于纯水分子间的作用力,最终导致农林保水剂吸持水比自由纯水具有更低的能量状态。综上有:dS<0、–pdV<0、γdAs>0、dU<0。

|
图 1 农林保水剂吸水形成水凝胶前后体积变化 Fig. 1 Volume changes of agro-forestry water-retaining agents before and after water absorption |
如果要将水从农林保水剂中分离出来,就需要对农林保水剂吸持水传递能量,以帮助其克服内能损失,这部分能量是dU,其积分形式记作ΔU,表示将农林保水剂吸持水分离出来并使其成为自由水所需的能量。实际上,将能量传递给埋在土壤中的农林保水剂吸持水只有两种方式:一种是传热,另一种是做功[23]。Williams等[24]指出,影响土壤水分保持特性的因素包括土壤颗粒大小分布、黏土矿物和有机质含量以及土壤容重。影响土壤水分保持能力的主要特性是土壤质地和结构[25],因为不同质地的土壤具有不同比例的颗粒组成,导致其表面能和整体能量状态各异。土壤水分的释放和储存受到植被覆盖、土壤质地和土壤湿度的强烈影响[26]。土壤特有的孔隙结构决定土壤水分分布的非均质性及动态变化特性[27]。由此可见,土壤的保水性有其自身的背景特性和状态,本质上反映的是土壤–水相互作用,一块土体对各种饱和农林保水剂水凝胶进行传热或做功的能力相对一致,可以使用土壤能量传递功率(P)来反映这种能力,即:
| $ \Delta U = Pt, t = \frac{{\Delta U}}{P} $ | (9) |
式中:P表示土壤能量传递功率,即单位时间一块土体所能向农林保水剂吸持水传递的能量(J/s);t表示在能量传递功率P时,农林保水剂吸持水的内能损失完全补偿所需的时间(s)。
因此可知,ΔU决定农林保水剂中的水完全离开农林保水剂的时间,也就是农林保水剂中的水完全进入到土壤中所需的时间,对应于农林保水剂的保水能力。因此可以在实验室中使用烘箱来测量ΔU,理论上可以将许多吸水饱和农林保水剂凝胶放在温度相同的烘箱中,控制传热条件一致并测量饱和农林保水剂凝胶失去所有水分所需的时间t,该时间t可以反映ΔU。吸水饱和农林保水剂凝胶的失水时间t也可以结合失水速率k和最大吸水倍数WACm计算得到,见公式(8),但公式(8)应用的前提条件是吸水饱和农林保水剂凝胶整个失水过程的失水速率k保持相对稳定。
2.2 农林保水剂热力学分析的试验验证为验证上述对农林保水剂吸持水的能量分析,试验测量了4种商业农林保水剂吸水饱和后的失水速率,结合吸水倍数计算农林保水剂的保水性能。同时,失水速率k可以反映农林保水剂中单位质量水的能量状态,斜率k的绝对值越大,表示失水速率越快,单位质量水分能量越高。由于农林保水剂的吸水倍数是随时间变化的,试验测定了4种商业农林保水剂的吸水平衡时间。研究发现,氯星保水剂、绿盟保水剂、沃特保水剂和绿满保水剂分别在6、4、4和1 h达到吸水平衡状态(图 2)。这表明,不同农林保水剂需要不同的时间以达到最大吸水倍数,各农林保水剂吸水/盐水倍数见表 2。
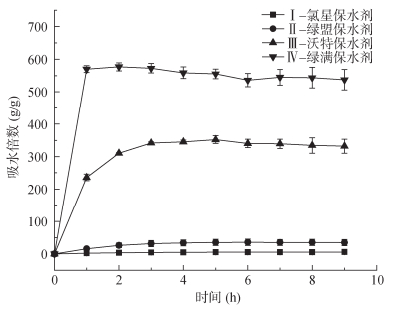
|
图 2 四种商业农林保水剂在去离子水中的吸水动力学曲线 Fig. 2 Water absorption kinetic curves of four commercial agro-forestry water-retaining agents in deionized water |
|
|
表 2 四种商业农林保水剂在去离子水中的最大吸水倍数 Table 2 Maximum water absorption ratios of four commercial agro-forestry water-retaining agents in deionized water |
由4种商业农林保水剂的水分损失曲线(图 3)可知,每种农林保水剂表现出相对稳定的水分损失速率,失水变化过程近乎线性,斜率反映了水分损失速率。由于饱和农林保水剂凝胶的初始温度为室温(约25 ℃),农林保水剂在放入60 ℃烘箱后的1 h内,存在吸热以达到烘箱温度(60 ℃)的阶段,故在此期间的水分损失速率低于烘箱温度(60 ℃)下的稳定失水速率,为了更准确地描绘农林保水剂的水分损失行为,选择从1 h开始绘图。在相同的环境温度(60 ℃)及传热条件下,4种饱和商业农林保水剂凝胶在相同时间内接受相同的热量,所以水分损失速率越快,表明单位质量的水能量状态越高。与纯水对照相比,所有农林保水剂的水分损失速率均较慢(图 3),这表明农林保水剂具有一定的保水能力,也反映了农林保水剂与灌溉处理之间的差异。不同商业农林保水剂单位时间失水速率的顺序为:绿满保水剂>沃特保水剂>氯星保水剂>绿盟保水剂。4种饱和农林保水剂的相对失水速率反映了这些凝胶中水的能量状态,因此,饱和农林保水剂中单位质量水的能量高低顺序为:绿满保水剂>沃特保水剂>氯星保水剂>绿盟保水剂。结合4种商业农林保水剂的吸水倍数,不同商业农林保水剂保水性优劣的顺序见表 3。由表 3中单位质量保水剂保水时间(通常取1 g或1 kg商业农林保水剂做吸水测试)可判断农林保水剂保水时效。一般来说,保水时间越长,农林保水剂保水效果越好。其中绿满保水剂虽然失水速率最快(2.19 g/h),但因其吸水倍数最大(545.92 g/g),其单位质量保水时间(250.42 h/g)仍然最高,保水性最优,这表明,农林保水剂可因其高吸水倍数而掩盖其高失水速率对保水性的负面影响。
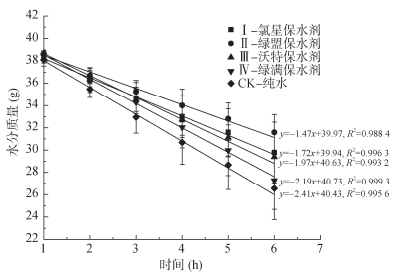
|
图 3 四种商业农林保水剂吸水饱和凝胶的失水曲线(60 ℃) Fig. 3 Water loss curves of gels of four commercial agro-forestry water-retaining agents after saturation (at 60 ℃) |
|
|
表 3 四种商业农林保水剂的保水性能 Table 3 Water retention performance of four commercial agro-forestry water-retaining agents |
通过热力学分析知道,当相同量的农林保水剂水凝胶进入土壤时,农林保水剂中水的能量状态越低,其保水能力越高。为了模拟田间条件,将相同质量吸水饱和的4种商业农林保水剂凝胶放入红壤中。由于土壤质地会影响农林保水剂的性能,为了消除土壤质地的影响,使用20~30目粒级的红壤进行试验。与模拟灌溉处理(CK)相比,加入相同质量的饱和农林保水剂凝胶减少了土壤水分蒸发并增加了土壤含水量(图 4)。
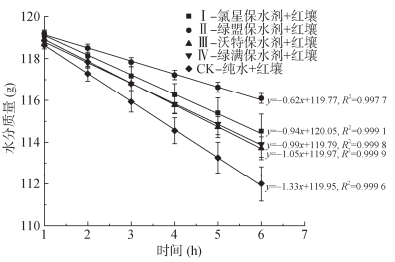
|
图 4 四种商业农林保水剂吸水饱和凝胶在红壤中的失水曲线(60 ℃) Fig. 4 Water loss curves of gels of four commercial agro-forestry water-retaining agents in red soil (at 60 ℃) |
4种饱和商业农林保水剂凝胶在红壤中的失水速率顺序与烘箱中的失水速率基本一致(仅沃特保水剂和绿满保水剂的顺序有所变化)。这表明,可通过室内农林保水剂的烘箱保水性测试结果预测其土壤实际保水效果。试验的误差应该是由于实验用烘箱内部温度不均匀造成的,更精确的验证实验需要高度均匀的温度环境和传热均匀的器皿,由于实验条件限制,只能给出初步验证结果。
2.3 农林保水剂吸水过程的热效应由图 5可知,4种商业农林保水剂在吸水过程中表现出3种不同的热效应。将农林保水剂及其所吸持的水视为系统,第一种热效应表现为农林保水剂吸水后,系统温度及其环境(乙醇)温度持续降低(氯星保水剂和绿盟保水剂);第二种热效应表现为农林保水剂吸水后,系统温度保持不变,但环境(乙醇)温度不断降低(沃特保水剂);第三种热效应表现为农林保水剂吸水后,系统温度和环境(乙醇)温度均不断升高(绿满保水剂)。
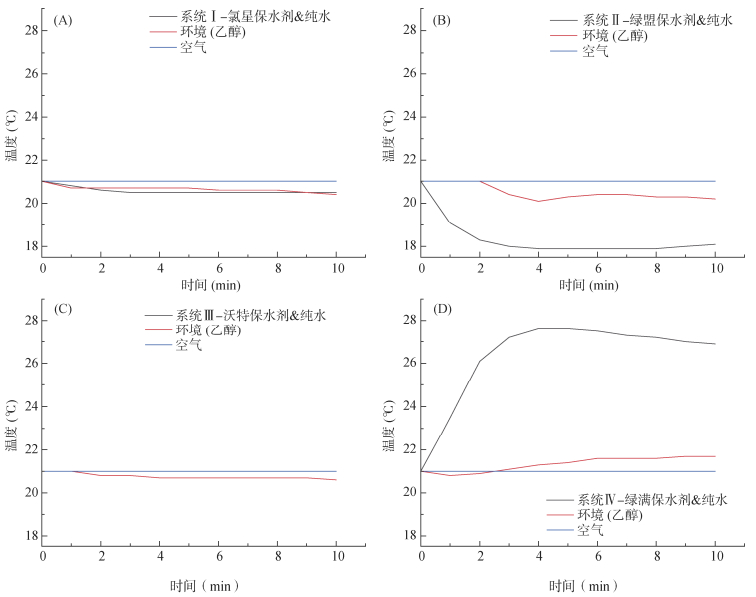
|
图 5 四种商业农林保水剂吸水过程中的热效应 Fig. 5 Heat effects during water absorption process of four commercial agro-forestry water-retaining agents |
试验期间空气温度一直为21 ℃,在农林保水剂的吸水过程中,无论是放热还是吸热,最终都会与空气达到热平衡。通过分析4种商业农林保水剂在吸水过程中的热效应,可以评估农林保水剂吸水过程中系统内能的变化。在吸水过程中,绿满保水剂系统温度升高,向环境(乙醇)释放热量,最后在与空气热平衡的过程中,将继续释放热量,导致系统内能下降。相比之下,绿盟保水剂系统和氯星保水剂系统在整个过程中持续从环境(乙醇)吸收热量,最后在与空气热平衡的过程中,还将继续从空气吸收热量,导致系统内能增加。沃特保水剂系统在整个过程中保持恒定的温度21 ℃,但持续吸收环境(乙醇)中的热量,当达到与空气温度平衡时,在整个吸水过程中吸收热量并增加系统内能。
农林保水剂通常是吸水性树脂,吸水后膨胀,吸水过程会增加农林保水剂(不包括吸收的水分)的势能,这一过程与水分子的作用密切相关。农林保水剂含有大量亲水基团,能够吸引大量水分子,水分子与农林保水剂分子之间的碰撞可以使这些分子克服分子间引力并得以扩展。水分子的动能在此过程中转化为农林保水剂的势能,水分子的动能减小,导致系统温度降低,随着系统温度下降,它会从周围环境(乙醇)中吸收热量,导致环境(乙醇)温度降低。这些分析阐明了上述农林保水剂(氯星保水剂、绿盟保水剂、沃特保水剂)吸水过程中的吸热现象。此外,电解质在水中溶解或反应产生的热量可能是上述3种热效应的另一个潜在原因。通常,农林保水剂含有丰富的亲水基团(–COOH,–SO3H,–NH2,–OH)[21],这些基团的离子化可以产生热效应。目前,占市场主导地位的保水剂是聚丙烯酸–丙烯酸钠聚合物[28]。对于聚丙烯酸类的农林保水剂,盐离子的存在使得其溶解于水时产生热效应。对于农林保水剂吸水过程最终的热效应取决于系统中吸热和放热的相对强度。观察到的第三个热效应可能是由于电解质溶解和化学反应的放热效应,导致绿满保水剂在吸水过程中释放大量热量。
3 结论通过对农林保水剂吸持水的能量分析,明确了农林保水剂吸持水存在溶质势能(Es)、基质势能(Em)、重力势能(Eg)、压力势能(Ep) 4种势能类型。热力学分析结果表明,农林保水剂吸持水的内能损失(ΔU)决定其在土壤中的保水性能。农林保水剂吸持水的内能损失越大,其保水效果越好,且农林保水剂在吸水过程中会对外做体积功,水分被农林保水剂吸持后熵值减小,表面积增大。通过4种商业农林保水剂的保水试验,验证了理论分析,并且发现农林保水剂吸水过程存在3种不同的热效应。研究结果为农林保水剂的选用提供了科学依据,为解决现行标准在农林保水剂保水性评价方面的不足提供了新的思路和方法。
| [1] |
Climate change 2014: Impacts, adaptation, and vulnerability: Part B: Regional aspects[R]. 2014. https://www.docin.com/p-1540954692.html
(  0) 0) |
| [2] |
李禹凝, 王金满, 张雅馥, 等. 干旱半干旱煤矿区土壤水分研究进展[J]. 土壤, 2023, 55(3): 494-502 DOI:10.13758/j.cnki.tr.2023.03.005 (  0) 0) |
| [3] |
张蕊, 白岗栓. 保水剂在农业生产中的应用及发展前景[J]. 农学学报, 2012, 2(7): 37–42, 78 (  0) 0) |
| [4] |
方静, 赵小庆, 史功赋, 等. 干旱胁迫对不同春小麦田产量及土壤特性的影响[J]. 土壤, 2024, 56(6): 1231-1239 DOI:10.13758/j.cnki.tr.2024.06.011 (  0) 0) |
| [5] |
Han Y G, Yang P L, Luo Y P, et al. Porosity change model for watered super absorbent polymer-treated soil[J]. Environmental Earth Sciences, 2010, 61(6): 1197-1205 DOI:10.1007/s12665-009-0443-4 (  0) 0) |
| [6] |
蒋美佳, 刘晓林, 冯钰梅, 等. 有机肥配施保水剂对紫色土水分入渗及氮素淋溶的影响[J]. 水土保持学报, 2019, 33(5): 99-104 (  0) 0) |
| [7] |
Hüttermann A, Orikiriza L J B, Agaba H. Application of superabsorbent polymers for improving the ecological chemistry of degraded or polluted lands[J]. CLEAN –Soil, Air, Water, 2009, 37(7): 517-526 DOI:10.1002/clen.200900048 (  0) 0) |
| [8] |
Zheng H F, Mei P P, Wang W D, et al. Effects of super absorbent polymer on crop yield, water productivity and soil properties: A global meta-analysis[J]. Agricultural Water Management, 2023, 282: 108290 DOI:10.1016/j.agwat.2023.108290 (  0) 0) |
| [9] |
Tang P S, Wang J S. A thermodynamic formulation of the water relations in an isolated living cell[J]. The Journal of Physical Chemistry, 1941, 45(3): 443-453 DOI:10.1021/j150408a010 (  0) 0) |
| [10] |
Kramer P J, Knipling E B, Miller L N. Terminology of cell-water relations[J]. Science, 1966, 153(3738): 889-890 DOI:10.1126/science.153.3738.889 (  0) 0) |
| [11] |
Slatyer R O, Taylor S A. Terminology in plant and soil-water relations[J]. Nature, 1960, 187(4741): 922-924 DOI:10.1038/187922a0 (  0) 0) |
| [12] |
邵明安, 王全九, 黄明斌. 土壤物理学[M].
高等教育出版社, 北京, 2006: 61
(  0) 0) |
| [13] |
郑曼迪, 刘忠, 许昭辉, 等. 基于微波遥感的土壤水分反演估算研究进展[J]. 土壤学报, 2024, 61(1): 16-28 (  0) 0) |
| [14] |
段春健, 宛颂, 叶桂萍, 等. 长期缺素施肥及石灰石膏施用对江西鹰潭红壤反硝化微生物功能基因丰度的影响[J]. 应用生态学报, 2021, 32(6): 2209-2216 (  0) 0) |
| [15] |
鲍士旦. 土壤农化分析(3版)[M].
中国农业出版社, 北京, 2000
(  0) 0) |
| [16] |
耿增超, 贾宏涛. 土壤学(2版)[M].
科学出版社, 北京, 2020: 84
(  0) 0) |
| [17] |
沈文霞, 淳远, 王喜章. 物理化学核心教程学习指导(2版)[M].
科学出版社, 北京, 2016: 88
(  0) 0) |
| [18] |
傅献彩, 侯文华. 物理化学-下册(6版)[M].
高等教育出版社, 北京, 2000: 78–79, 394
(  0) 0) |
| [19] |
Chen L Q. Chemical potential and Gibbs free energy[J]. MRS Bulletin, 2019, 44(7): 520-523 DOI:10.1557/mrs.2019.162 (  0) 0) |
| [20] |
Chen L Q. Chemical potential and Gibbs free energy Ⅱ: Q&A[J]. MRS Bulletin, 2022, 47(8): 753-758 DOI:10.1557/s43577-022-00405-3 (  0) 0) |
| [21] |
Hu X S, Wang Q, Liu Q, et al. Villus-like nanocomposite hydrogels with a super-high water absorption capacity[J]. Journal of Materials Chemistry A, 2020, 8(25): 12613-12622 DOI:10.1039/D0TA03907A (  0) 0) |
| [22] |
孙秀秀, 郑道君, 陈宣, 等. 10种不同农林保水剂保水及反复吸水性能评价[J]. 林业科技, 2022, 47(1): 35-39 (  0) 0) |
| [23] |
刘克哲, 张承琚, 刘建强, 等. 物理学-上卷(5版)[M].
高等教育出版社, 北京, 2018: 200
(  0) 0) |
| [24] |
Williams J, Prebble R E, Williams W T, et al. The influence of texture, structure and clay mineralogy on the soil moisture characteristic[J]. Australian Journal of Soil Research, 1983, 21(1): 15-32 DOI:10.1071/SR9830015 (  0) 0) |
| [25] |
Nimmo J R. Modeling structural influences on soil water retention[J]. Soil Science Society of America Journal, 1997, 61(3): 712-719 DOI:10.2136/sssaj1997.03615995006100030002x (  0) 0) |
| [26] |
Stumpp C, Hendry M J. Spatial and temporal dynamics of water flow and solute transport in a heterogeneous glacial till: The application of high-resolution profiles of δ18O and δ2H in pore waters[J]. Journal of Hydrology, 2012, 438/439: 203-214 DOI:10.1016/j.jhydrol.2012.03.024 (  0) 0) |
| [27] |
李保国, 周虎, 王钢, 等. 探索"透明"土壤体: 土壤孔隙学的时代已经启航[J]. 土壤学报, 2023, 60(5): 1221-1230 (  0) 0) |
| [28] |
邬一凡. 高吸水性树脂研究进展及发展趋势[J]. 化工新型材料, 2019, 47(5): 23–26, 31 (  0) 0) |
2. University of Chinese Academy of Sciences, Nanjing, Nanjing 211135, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. College of Tobacco Science and Engineering, Zhengzhou University of Light Industry, Zhengzhou 450002, China
 2026, Vol. 58
2026, Vol. 58


