2. 土壤与农业可持续发展全国重点实验室(中国科学院南京土壤研究所), 南京 211135;
3. 北京理工大学生命学院, 北京 100049;
4. 中国科学院大学, 北京 100049;
5. 江西农业大学国土资源与环境学院, 南昌 330045;
6. 江西水利电力大学水土保持学院, 南昌 330099
南方红壤丘陵区土壤面积约113万hm2,占全国国土总面积的11.8%,不合理施肥及长期集约化种植等人为因素加剧了红壤酸化[1]。土壤酸化导致农田钙、镁、钾等盐基离子淋失,同时铝、锰等离子活化[2],造成作物根系铝毒升高,植物养分利用效率降低[3]。与此同时,酸化还降低土壤微生物多样性和丰度,影响土壤微生物群落结构,造成有益微生物与有害微生物比例失衡,导致土传病害发生,最终威胁作物生长[4]。传统酸化红壤改良多依赖石灰等碱性物质,虽可短期提升pH[5],但其Ca2+饱和易引发土壤板结,且存在二次酸化风险[6-8]。
近年来,微生物菌剂[9]和微生物调控技术[10]等在土壤改良中的应用逐渐受到重视,但是仍面临微生物定殖率不高、与土著微生物竞争等问题。例如,根瘤菌可通过分泌有机酸来中和H+[11],解磷菌能活化沉积态磷[12]。然而,当土壤pH<4.5时,普通菌剂的定殖效率下降,严重影响其应用效果[13]。值得注意的是,外源菌剂与土著微生物的竞争排斥效应(如营养抢夺、抗生素分泌)也可能削弱微生物菌剂的改良效果[14]。
基因工程改造的耐酸枯草芽孢杆菌不仅具有环境适应优势,还可通过群体感应调控代谢途径,激活抗逆基因,维持胞内pH稳态[15];同时,耐酸枯草芽孢杆菌还可诱导植物系统抗性,增强根系对Al3+的排斥作用,提高植物耐铝毒能力[16]。此外,生物质炭在土壤改良中的直接应用较为广泛,其多级孔道结构与表面负电荷特性能作为功能微生物的理想载体[17]。王宣懿等[18]研究发现,生物质炭-芽孢杆菌(D2)联用可提高土壤有效磷含量;黎紫珊等[19]研究发现,生物质炭-蜡状芽孢杆菌(M)联用可提高土壤pH,增加土壤有效磷和钾含量。但是目前为止,生物质炭联合耐酸工程菌对红壤pH及土著微生物多样性的影响尚不明确。
本研究选用耐酸枯草芽孢杆菌作为微生物菌剂,玉米秸秆生物质炭材料作为附着载体,通过室内培育试验,探究野生型芽孢杆菌、耐酸芽孢杆菌单独施用或与生物质炭联用对红壤pH、养分含量及微生物多样性的影响,探明生物质炭与微生物菌剂的协同增效机制,以期为南方酸性红壤改良提供理论和技术参考。
1 材料与方法 1.1 供试土壤供试土壤样品采集于中国科学院红壤生态实验站(28°12′25′′N,116°55′4′′E),地处江西省鹰潭市余江区,属于中亚热带季风气候,年均气温17.6 ℃,年均降水量1 766 mm,采样地点5年内未进行耕作、播种和施肥等农事活动。供试土壤发育于第四纪红黏土。样品经风干处理后挑去肉眼可见的碎石块、植物残体,过2 mm筛后置于4 ℃冰箱备用。供试土壤的基本理化性质为pH 4.64,有机质16.0 g/kg,可溶性有机质157 mg/kg,全氮0.814 g/kg,全磷0.343 g/kg,全钾8.94 g/kg,速效氮80.8 mg/kg,有效磷11.2 mg/kg,速效钾15.1 mg/kg,交换性酸4.40 cmol/kg,交换性铝4.16 cmol/kg。
1.2 供试菌剂和生物质炭供试枯草芽孢杆菌野生型(Bacillussubtilis168,Bs-wt)及耐酸枯草芽孢杆菌工程菌(经Bs-wt基因组突变得到,Bs-m9)均由北京理工大学提供。挑选平板上的Bs-wt和Bs-m9单菌落接种至5 mL的LB液体培养基中,37 ℃、220 r/min振荡培养12 h,振荡培养结束后5 000 r/min离心4 min,弃去上清液,将剩下的菌泥用无菌水重悬,获得浓度约为1×108 CFU/mL菌悬液,置于4 ℃冰箱备用。
生物质炭购于河南立泽环保科技有限公司,原材料为玉米秸秆,通过高温分解法在500~600 ℃缺氧状态下高温热解所得。生物质炭的基本理化性质为有机碳含量510.9 g/kg,全氮8.51 g/kg,全磷2.34 g/kg,全钾15.76 g/kg,灰分含量8.43%。
1.3 试验设计试验设置6个处理:①空白对照(CK);②施用生物质炭(C);③施用枯草芽孢杆菌野生型Bs-wt菌悬液(Bwt);④施用耐酸枯草芽孢杆菌工程菌Bs-m9菌悬液(BN);⑤施用Bs-wt菌悬液+生物质炭(BwtC);⑥施用Bs-m9菌悬液+生物质炭(BNC),进行土培试验。每个处理风干土壤添加量为60 g,25 ℃避光培育60 d,试验期间土壤含水量保持在40% 左右,每天根据土壤水分损失情况,适当补充蒸馏水。在添加生物质炭和菌液的处理中,生物质炭和菌液的添加量均为土壤重量的1%[20]。BwtC、BNC处理中,菌液经生物质炭吸附预处理后混入土壤:菌液分3次滴加至生物质炭(每次翻拌至完全吸收),随后将附着有菌液的生物质炭均分为两份,先取50% 添加至土壤中翻拌2 min,剩余50% 装入无菌密封袋揉捏5 min;随后将两部分物料整体平铺为扇形,翻拌10 min至分散均匀。每个处理设6次重复,分别于培养第6天和第60天各破坏性取3个重复样本,进行土壤理化性质和微生物多样性分析。
1.4 土壤样品分析 1.4.1 土壤理化性质分析土壤样品基本理化性质的测定参照《土壤农化分析》[21]。土壤pH采用电位法测定,全氮(TN)采用凯氏定氮法测定,全磷(TP)采用氢氧化钠熔融-钼锑抗比色法测定,全钾(TK)采用氢氧化钠熔融-火焰光度法测定,速效氮(AN)采用碱解扩散法测定,有效磷(AP)采用盐酸-氟化铵浸提法(Bray法)测定,速效钾(AK)采用乙酸铵浸提-火焰光度法测定,有机质(SOM)采用重铬酸钾氧化-外加热法测定,可溶性有机碳(DOC)采用总有机碳(TOC)分析仪法测定,交换性酸采用氯化钾交换-中和滴定法测定,交换性铝采用氯化钾提取-分光光度法测定。
1.4.2 土壤微生物多样性分析使用土壤基因组DNA提取试剂盒(DP336,TianGen)提取土壤总DNA,经1% 琼脂糖凝胶电泳检验完整性,并通过NanoDrop2000分光光度计测定纯度(A260/A280= 1.8~2.0),合格样本保存于–80 ℃。随后对细菌16S rRNA V4~V5区(引物515F/806R)和真菌ITS1-5F区(引物ITS1F/ITS2R)进行PCR扩增。扩增程序为:95 ℃预变性3 min,95 ℃ 30 s、55 ℃ 30 s、72 ℃ 45 s,30个循环,之后72 ℃终延伸10 min。扩增产物经NEBNext Ultra Ⅱ DNA文库制备试剂盒构建文库,Qubit 2.0定量及qPCR质检后,利用Illumina NovaSeq 6000平台进行双端测序。原始数据经fastp质控过滤(Q20,N<5%)、FLASH拼接双端序列、DADA2去噪生成ASV特征表,最终基于Silva 138.1(16S rRNA)和UNITE v9.0(ITS)数据库通过QIIME2分类器进行物种注释(置信阈值≥80%)[22-23]。
1.5 数据统计试验数据采用SPSS 27.0与R(4.4.2) 软件进行统计分析。通过单因素方差分析(one-way ANOVA)检验不同处理间土壤理化性质的差异显著性。微生物多样性分析基于R平台进行:α多样性与β多样性计算借助microbiome和phyloseq包完成,群落组成差异通过vegan包的主坐标分析(PCoA)进行可视化呈现。进一步采用vegan包的冗余分析(RDA)探究土壤理化性质与微生物群落结构的相关性。
2 结果 2.1 不同处理对土壤理化性质的影响 2.1.1 培养第6天不同处理对土壤理化性质的影响培养第6天,与对照(CK)相比,生物质炭与Bs-m9菌液联用(BNC)处理显著改善了红壤理化性质(P<0.05):土壤pH从4.44升高至4.80,升高8.11%;交换性酸和交换性铝含量分别降低24.6% 和9.6%;SOM含量从15.37 g/kg增至25.22 g/kg,升高64.1%;DOC增幅为1.73%;TN、TP和TK含量分别升高14.1%、16.2% 和9.3%;AN、AP、AK含量分别升高22%、86.3% 和138.3%。而单一施加Bs-m9菌液(BN)处理pH仅升高4.73%,交换性铝含量增加7.7%,TP降低5.23%,TK降低5.01%,AN升高3%,AP降低7.7%,AK升高14.4%。
2.1.2 培养第60天不同处理对土壤理化性质的影响培养第60天,相较于CK,BNC处理对红壤理化性质的改良效应持续显著。BNC和BN处理土壤pH稳定于4.56,而单施生物质炭(C)处理下降2.0%;BNC处理交换性酸含量从4.61 cmol/kg降至3.76 cmol/kg(降幅18.4%,P<0.001),交换性铝含量从4.2 cmol/kg降至3.37 cmol/kg(降幅19.8%,P<0.001),显著优于BN处理(交换性酸减少2.2%,交换性铝增加2.1%);BNC处理SOM含量由14.07 g/kg增至23.03 g/kg(增幅63.7%,P<0.001),DOC含量从250.67 mg/kg降至238.67 mg/kg(降幅4.8%);BNC处理TN和TP含量分别增加14.8%(P<0.01)和10.2% (P<0.05),TK降低29.0%,BN处理降低13.7%;BNC处理AP和AK含量分别激增99.4%(P<0.001)和134.2%(P<0.001),显著优于BN处理(AP仅增9.2%,AK增加22.2%),BNC处理AN减少7.1%,而BN处理AN减少1.4%。
|
|
表 1 培养第6天不同处理下土壤理化性质 Table 1 Soil physicochemical properties under different treatments after 6-day incubation |
|
|
表 2 培养第60天不同处理下土壤理化性质 Table 2 Soil physicochemical properties under different treatments after 60-day incubation |
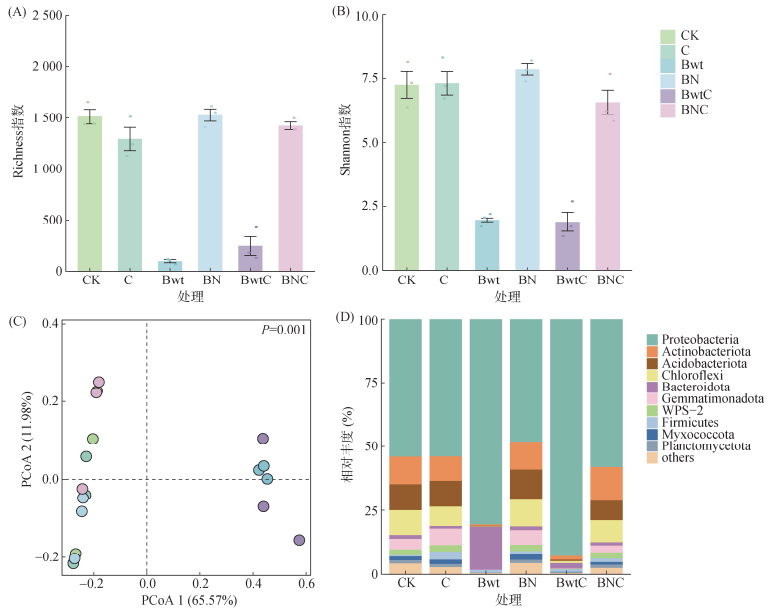
培养第6天,不同处理对细菌群落多样性的影响差异显著(图 1A、1B)。相较于对照CK,C处理细菌丰富度Richness指数降低14.41%,但香农指数(Shannon)上升0.82%;Bwt处理Richness和Shannon指数分别骤降93.43% 和72.83%;BN处理Richness略微提升0.99%,Shannon指数提升8.29%;BwtC处理Richness和Shannon指数分别下降83.73% 和73.85%;BNC处理对细菌多样性的负面影响最弱,Richness降低5.91%,Shannon指数下降9.33%。基于Bray-Curtis距离的主坐标分析(PCoA,图 1C)显示,第6天不同处理土壤细菌群落结构存在显著差异(P=0.001)。不同细菌门类的相对丰度存在显著差异(图 1D)。其中,变形菌门(Proteobacteria,43.3%~96.8%)为绝对优势类群;放线菌门(Actinobacteriota,0.4%~21.5%)、酸杆菌门(Acidobacteriota,0.1%~13.3%)、绿弯菌门(Chloroflexi,0.1%~12.1%)、WPS-2(0.0%~4.4%)在细菌群落中的丰度较高,占细菌总ASV的70%;其余门类主要由芽单胞菌门(Gemmatimonadota,0.0%~6.0%)、浮霉菌门(Planctomycetota,0.4%~1.8%)、黏细菌门(Myxococcota,0.1%~2.6%)及拟杆菌门(Bacteroidota,0.9%~22.0%)组成。相较于CK处理,C处理变形菌门丰度接近,酸杆菌门丰度小幅上升,绿弯菌门相对丰度降低;Bwt处理变形菌门增加49.55%,绿弯菌门与酸杆菌门分别降低97.8% 和98.1%;BwtC处理变形菌门丰度增加92.92%;BN处理变形菌门降低10.8%,酸杆菌门增加14.9%,绿弯菌门增加8.2%;BNC处理变形菌门丰度接近对照CK,WPS-2相对丰度提高15.68%,放线菌门达21.5%。
|
(A. 土壤细菌群落Richness指数变化趋势;B. 土壤细菌群落Shannon指数变化趋势;C. 基于Bray-Curtis距离矩阵的土壤细菌群落主坐标分析;D. 门水平丰度排名前10位的细菌相对丰度堆叠柱状图。相对丰度在每个处理中均小于1% 的物种合并为“others”。下同) 图 1 不同处理第6天土壤细菌多样性和门水平下细菌相对丰度 Fig. 1 Soil bacterial diversity and relative abundance at the phylum level under different treatments on day 6 |
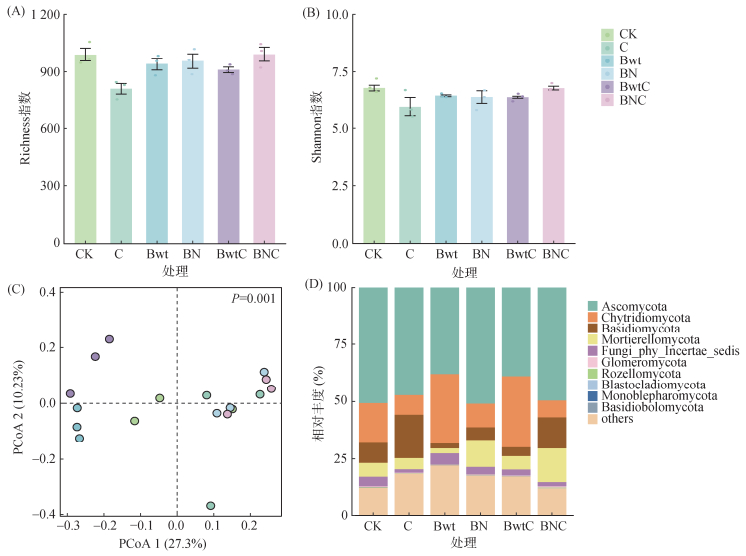
培养第6天,与CK相比,各处理对真菌群落多样性产生差异影响(图 2A、2B)。其中,C处理对真菌群落多样性表现出显著负影响,其Richness指数下降18.25%,Shannon指数下降12.24%;Bwt处理对两者的影响幅度较小,Richness和Shannon指数分别下降5.08% 和4.87%;BN处理Richness指数降幅为3.50%,但Shannon指数降幅为5.72%;BwtC处理Richness和Shannon指数分别下降8.20% 和5.90%;而BNC处理Richness指数略微上升0.20%,Shannon指数维持不变。PCoA结果表明(图 2C),不同处理下真菌群落存在显著差异(P=0.001)。不同真菌门类的相对丰度存在显著差异(图 2D)。其中,子囊菌门(Ascomycota,33.7%~59.4%)为绝对优势类群,壶菌门(Chytridiomycota,2.4%~36.6%)、担子菌门(Basidiomycota,2.5%~43.9%)、被孢霉门(Mortierello-mycota,2.6%~28.3%)及Fungi_phy_Incertae_sedis(1.0%~6.7%)在真菌群落中丰度较高。相较于CK,C处理子囊菌门丰度几乎维持不变,壶菌门丰度下降,担子菌门显著增加,被孢霉门略增;Bwt处理子囊菌门丰度降低,壶菌门丰度上升48.5%,担子菌门锐减75.9%,被孢霉门下降;BwtC处理子囊菌门恢复但仍较CK降低17.2%,壶菌门丰度较CK增加26.0%;BN处理壶菌门丰度下降57.4%,被孢霉门激增149.2%,担子菌门增加16.1%,子囊菌门接近CK;BNC处理子囊菌门丰度提升7.5%,担子菌门增加55.2%,被孢霉门显著提升110.2%。
|
(A. 土壤真菌群落Richness指数变化趋势;B. 土壤真菌群落Shannon指数变化趋势;C. 基于Bray-Curtis距离矩阵的土壤真菌群落主坐标分析;D. 门水平丰度排名前10位的真菌相对丰度堆叠柱状图) 图 2 不同处理第6天土壤真菌多样性和门水平下真菌相对丰度 Fig. 2 Soil fungal diversity and relative abundance at the phylum level under different treatments on day 6 |
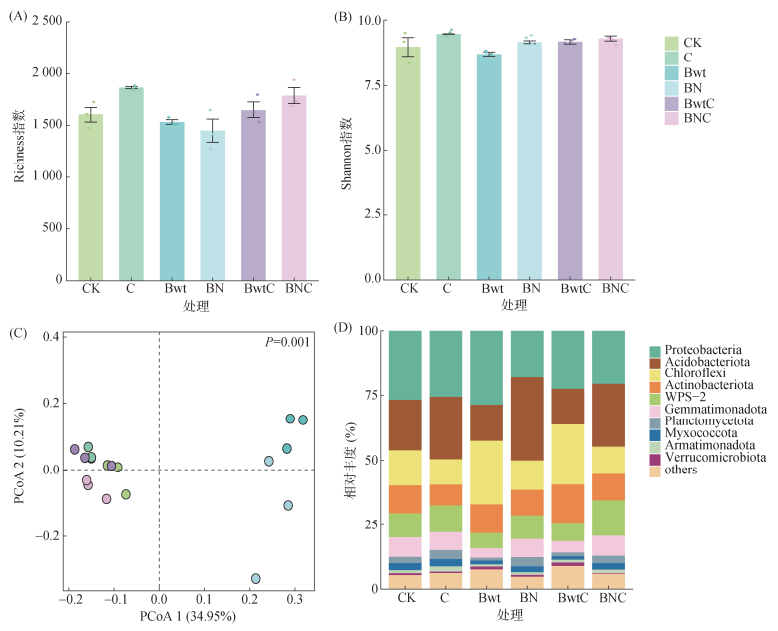
培养第60天,不同处理对细菌群落多样性的影响差异显著(图 3A、3B)。相较于CK,C处理Richness和Shannon指数分别上升16.35% 和5.52%;Bwt处理Richness指数下降4.48%,Shannon指数下降3.03%;BN处理Richness指数降低9.69%,但Shannon指数上升2.04%;BwtC处理Richness和Shannon指数分别上升3.10% 和2.26%;BNC处理Richness和Shannon指数分别提升11.62% 和3.60%。PCoA结果表明(图 3C),不同处理下细菌群落存在显著差异(P=0.001)。细菌门水平相对丰度显示(图 3D),变形菌门(Proteobacteria,17.2%~38.2%)、酸杆菌门(Acidobacteriota,12.7%~37.6%)、绿弯菌门(Chloroflexi,8.8%~25.5%)、放线菌门(Actinobacteriota,7.8%~21.5%)及WPS-2(5.6%~15.7%)为细菌群落主要优势类群;其余门类包括芽单胞菌门(Gemmatimonadota,3.6%~8.2%)、浮霉菌门(Planctomycetota,1.0%~4.8%)、黏细菌门(Myxococcota,1.2%~3.2%)、Armatimonadota (0.8%~2.0%)和疣微菌门(Verrucomicrobiota,0.3%~1.5%)。相较于CK,C处理中酸杆菌门丰度增加25.6%,绿弯菌门下降21.0%,变形菌门下降14.0%,WPS-2上升24.1%;Bwt处理绿弯菌门激增88.5%,变形菌门提升14.8%,酸杆菌门与WPS-2分别下降34.4% 和39.8%;BN处理酸杆菌门激增94.2%,变形菌门下降35.8%,绿弯菌门下降34.2%,WPS-2微降13.5%;BwtC处理绿弯菌门增长81.7%,放线菌门倍增99.4%,变形菌门与酸杆菌门分别下降26.5% 和56.5%;BNC处理WPS-2显著增加67.2%,酸杆菌门增长29.5%,变形菌门与绿弯菌门分别下降21.6% 和33.7%。
|
图 3 不同处理第60天土壤细菌多样性和门水平下细菌相对丰度 Fig. 3 Soil bacterial diversity and relative abundance under different treatments on day 60 |
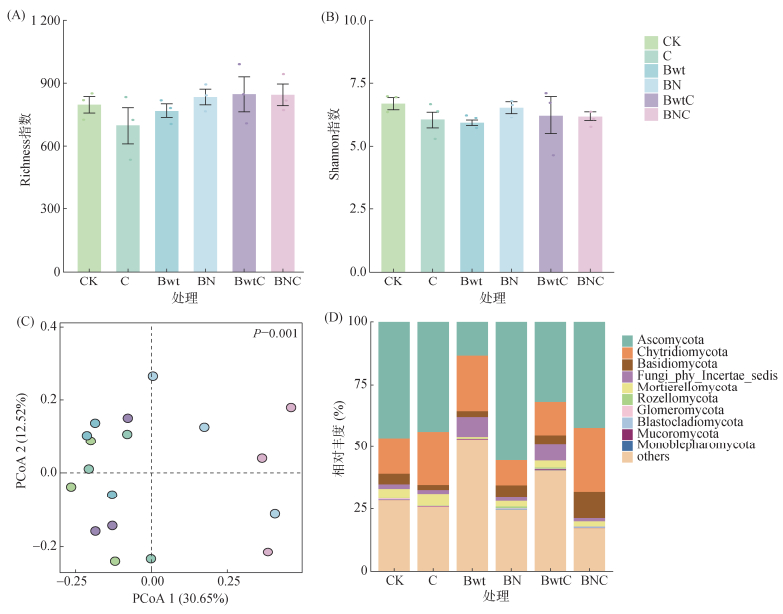
培养至第60天时,不同处理对真菌多样性的调控作用呈现显著性差异(图 4A、4B)。相较于CK,C处理Richness和Shannon指数分别显著下降12.66%、9.84%;Bwt处理Richness指数下降3.67%,Shannon指数下降11.66%;BN处理Richness指数上升4.50%,但Shannon指数下降2.39%;BwtC处理Richness指数上升6.09%,Shannon指数下降7.01%;BNC处理Richness指数上升5.75%,Shannon指数下降7.61%。PCoA结果表明(图 4C),不同处理下真菌群落存在显著差异(P=0.001)。不同真菌门类的相对丰度也存在显著差异(图 4D),子囊菌门(Ascomycota,8.4%~58.0%)为绝对优势类群,壶菌门(Chytridiomycota,4.7%~38.8%)、担子菌门(Basidiomycota,1.8%~22.2%)、被孢霉门(Mortierellomycota,0.4%~7.0%)及Fungi_phy_incertae_sedis(0.8%~9.4%)为主要优势亚类。相较于CK,C处理子囊菌门丰度下降12.7%,壶菌门和被孢霉门分别增加50.3% 和26.3%;BN处理子囊菌门与担子菌门协同增长18.9%、19.0%,壶菌门降低25.9%;BwtC处理Fungi_phy_incertae_sedis爆发性增长261.1%,子囊菌门锐减35.4%;而BNC处理担子菌门丰度显著提升207.1%;Bwt处理子囊菌门丰度异常骤降70.6%,壶菌门丰度上升55.2%。
|
图 4 不同处理第60天土壤真菌多样性和门水平下真菌相对丰度 Fig. 4 Soil fungal diversity and relative abundance at the phylum level under different treatments on day 60 |
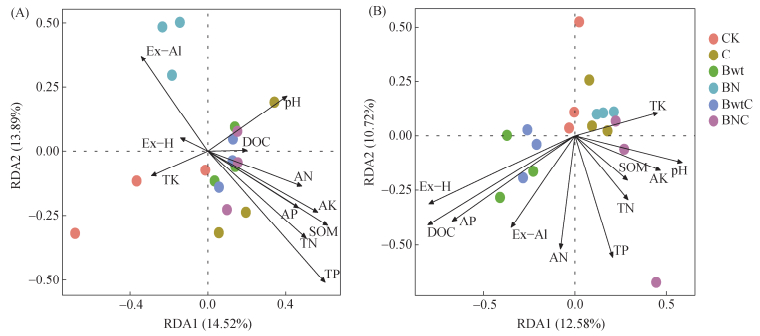
培养第6天时,RDA分析显示前两轴对细菌和真菌群落结构变化的累积解释度分别为28.41% 和23.3%(图 5)。TP、TN、SOM和交换性氢(Ex-H)是影响细菌群落组成结构的主要因素(表 3)。BN处理细菌群落与Ex-H呈正相关关系,但与TP、TN、SOM呈负相关;BNC处理细菌群落与SOM正相关,但与Ex-H呈负相关;二者分布距离较远,群落结构差异显著。pH、DOC、TP、AK和交换性铝(Ex-Al)是真菌群落组成结构核心驱动因子,BN、BNC处理真菌群落均与DOC、Ex-Al呈负相关;BN处理真菌群落与AK呈正相关,BNC处理真菌群落与pH、AK呈正相关。
|
(A.细菌群落;B.真菌群落。Ex-H:交换性氢;Ex-Al:交换性铝。下同) 图 5 第6天不同处理下土壤化学指标对细菌、真菌群落组成的影响 Fig. 5 The effect of soil chemical properties on bacterial and fungal community composition under different treatments on day 6 |
|
|
表 3 不同处理下土壤化学性质与细菌、真菌多样性基于RDA分析的变量方差分解 Table 3 Variance partitioning of soil chemical properties and bacterial and fungal diversity based on RDA analysis under different treatments |
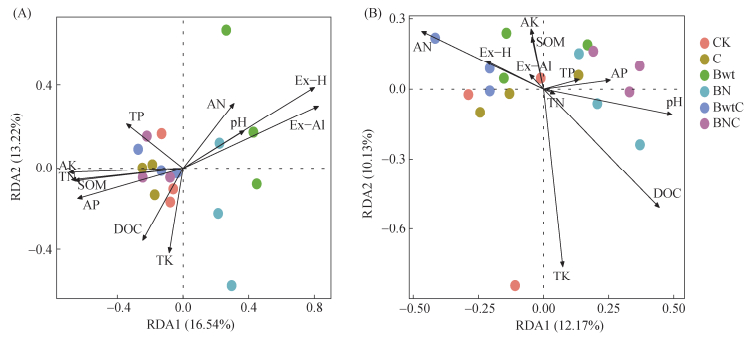
培养第60天时,RDA分析显示前两轴对细菌和真菌群落结构变化的累积解释度分别为29.76% 和22.3%(图 6)。SOM、TN、AK、Ex-H和Ex-Al是影响细菌群落组成结构的主要因素(表 3)。BN处理细菌群落与Ex-H、Ex-Al呈正相关;BNC处理细菌群落与SOM、TN、AK呈正相关,但与Ex-H、Ex-Al呈负相关;二者分布距离较远,群落结构差异显著。DOC和TK是真菌群落组成结构核心驱动因子,BN处理真菌群落与DOC呈正相关,而BNC处理真菌群落与DOC呈负相关。
|
图 6 第60天不同处理下土壤化学指标对细菌、真菌群落组成的影响 Fig. 6 The effect of soil chemical properties on bacterial and fungal community composition under different treatments on day 60 |
本研究发现,生物质炭与Bs-m9菌液联用(BNC处理)在第6天可使红壤pH显著提升0.36个单位,同时交换性酸和交换性铝含量呈持续降低趋势(第60天分别降低18.4% 和19.8%),与前人研究[24-27]一致,进一步证实了生物质炭与Bs-m9菌液的协同作用在改良土壤酸化方面的重要作用。主要原因可能是:①耐酸芽孢杆菌的直接作用。芽孢杆菌属可能通过碳代谢驱动有机酸(如柠檬酸)合成,螯合游离态Al3+,降低其活性,进而缓解酸铝毒害;更重要的是,芽孢杆菌可能通过乳酸降解[28-29]及潜在多酸协同代谢[30]减少土壤有机酸含量,同时可能通过代谢产碱(如NH3)直接中和酸性。②耐酸芽孢杆菌与生物质炭的协同作用。生物质炭通过多孔结构及表面官能团可对Al3+进行专性吸附,以及其碱性组分(灰分含量8.43%)的中和作用直接提升pH[31-33],有效缓解铝毒害[34];耐酸枯草芽孢杆菌与生物质炭联用时,生物质炭的多孔结构为芽孢杆菌提供适宜生长环境,并提供碳源促进其代谢活性,最终提升其酸化改良能力。长期(60 d)培养后pH提升效果减弱(与CK无差异),可能与外源菌定殖能力下降[35]、生物质炭碱性组分消耗及红壤缓冲系统抵消[36]有关。未来需通过菌株定殖强化(如包埋缓释)与复合改良剂开发,延长酸化改良的持续周期。此外,本研究还发现BwtC处理在整个培养期间红壤pH显著下降,这可能是由于Bs-wt未优化代谢通路,通过发酵代谢,产生较多的短链脂肪酸等酸性物质,抵消了碱性物质的中和效应;还有可能Bs-wt菌与土著产酸菌的营养竞争也能促使后者分泌更多有机酸。
3.2 生物质炭与Bs-m9菌液联用提高土壤微生物群落多样性微生物群落的多样性和均匀度是土壤健康的关键指标[37],较高的多样性和均匀度能够促进资源的高效利用,并增强微生物之间的互作,有利于增强土壤的自我修复能力和对环境胁迫的抵抗力[38-39]。本研究表明,生物质炭与Bs-m9菌液联用(BNC处理)显著提升了土壤微生物群落的多样性和均匀度,培养60 d的BNC处理细菌Richness指数较单施Bs-m9菌液(BN)处理提升16.44%,Shannon指数提高0.92%。这一结果与近年来微生物–增效材料的协同修复研究结论一致[29-32]。生物质炭与Bs-m9的联用可能通过改变土壤环境中的营养物质分布,提供有利的生态位,改变微生物竞争格局,从而促进群落多样性和均匀度的提高[40-41]。而更高的群落多样性和均匀度有助于微生物之间的资源共享和功能互补,增强了群落的整体功能性和生态稳定性。
3.3 生物质炭与Bs-m9菌液联用改变土壤微生物相对丰度本研究中,所有处理中都包含变形菌门(Proteobacteria)、酸杆菌门(Acidobacteriota)、绿弯菌门(Chloroflexi)和放线菌门(Actinobacteriota)等主要细菌门。其中变形菌门在所有处理中都是占比最高的细菌门,但BNC处理中其丰度的变化相对较小。其他主要细菌门的丰度存在显著差异。这一结果与前人研究中关于微生物群落稳定性与特定细菌门占比稳定性之间的关联相吻合[42-43]。具体而言,变形菌门通常被视为r-策略者,即快速生长和繁殖的细菌,它们在资源丰富的环境中占据优势[44]。在本研究中,BNC处理组中变形菌门占比的稳定可能反映了Bs-m9菌的添加对整体群落稳定性的积极影响。第60天BNC处理中拟杆菌门(Bacteroidota)的占比显著降低。拟杆菌门通常与有机物质的分解和营养循环密切相关[45-46],其占比的降低可能意味着Bs-m9工程菌对土壤元素循环,特别是有机物质分解过程的特定影响。此外,本研究还发现,随着处理时间的延长,所有处理中的细菌群落都经历了从r-策略向K-策略的转变,如酸杆菌门、绿弯菌门等寡营养型菌门丰度升高。BN与BNC处理组中这种转变的特征可能与单独施用,或者与生物质炭联合施用Bs-m9工程菌后特定生态功能密切相关。值得注意的是,BNC处理中WPS-2等适应性功能类群的特异性富集,其相对丰度在培育第6天和第60天较对照(CK)分别显著提升15.68% 和67.2%。这一动态变化揭示了生物质炭和Bs-m9工程菌联用对特定功能微生物的选择性激活效应,可能反映了其与土壤原有微生物之间的相互作用机制。
3.4 生物质炭与Bs-m9菌液联用影响微生物群落组成结构BNC处理通过生物质炭与菌剂的协同作用显著重塑了土壤微生物群落结构。培养第6天RDA分析显示,BNC处理微生物群落与土壤SOM呈显著正相关,表明生物质炭通过高碳含量(总碳量68.4%)[46-47]及多孔结构提升SOM稳定性[48](较CK提高22.3%),形成持续碳源供给体系。而BN与TP、TN的负相关性揭示其可能因养分竞争导致微生物生物量下降,BNC处理则通过生物质炭的保肥效应缓解了这一限制。至第60天,BNC处理的微生物群落呈现明显差异:细菌群落演替由初期SOM驱动转向TN与AK协同调控,反映生物质炭的养分缓释特性激活了氮转化及钾活化类群;真菌群落则从DOC依赖演变为TK响应,可能与真菌菌丝网络扩展增强矿物钾活化能力有关。此外,BNC处理通过pH提升(ΔpH=+0.37)显著扩展了真菌生态位,促进嗜中性真菌(如担子菌门)定殖,而BN处理真菌群落仍依赖易分解碳源(DOC),群落稳定性易受底物波动影响。
4 结论生物质炭与Bs-m9菌联用短期内(培养第6天)可提升土壤pH(0.36单位),并降低可交换铝浓度;随着培养时间延长(第60天),pH改良效果虽有所减弱,但仍优于单一处理,且对交换性铝的消减作用及微生物群落多样性调控呈现持续效应,在酸化红壤改良中具有较好的潜在应用价值。
| [1] |
Cai Z J, Wang B R, Xu M G, et al. Intensified soil acidification from chemical N fertilization and prevention by manure in an 18-year field experiment in the red soil of Southern China[J]. Journal of Soils and Sediments, 2015, 15(2): 260-270 DOI:10.1007/s11368-014-0989-y (  0) 0) |
| [2] |
高小龙. 土壤酸化和盐渍化的原因和预防对策[J]. 当代化工研究, 2022(18): 12-14 (  0) 0) |
| [3] |
朱灿, 程永生, 彭尽晖. 植物铝毒害研究进展[J]. 现代园艺, 2009(9): 4-6 (  0) 0) |
| [4] |
徐影, 于镇华, 李彦生, 等. 土壤酸化成因及其对农田土壤–微生物–作物系统影响的研究进展[J]. 土壤通报, 2024, 55(2): 562-572 (  0) 0) |
| [5] |
王梅. 钙-蒙脱石和石灰对两种酸性土壤的改良研究[D]. 重庆: 西南大学, 2018.
(  0) 0) |
| [6] |
曾廷廷, 蔡泽江, 王小利, 等. 酸性土壤施用石灰提高作物产量的整合分析[J]. 中国农业科学, 2017, 50(13): 2519-2527 (  0) 0) |
| [7] |
顾时国, 章道清, 牛永康, 等. 生物炭在土壤中的功能及其对土壤改良的研究进展[J]. 种子科技, 2024, 42(15): 133-135 (  0) 0) |
| [8] |
孟赐福, 傅庆林, 水建国, 等. 浙江中部红壤施用石灰对土壤交换性钙、镁及土壤酸度的影响[J]. 植物营养与肥料学报, 1999, 5(2): 129-136 (  0) 0) |
| [9] |
宋泽海, 田沛. 土壤微生物在土壤改良与修复中的作用概述[J]. 草业科学, 2024, 41(11): 2622-2636 (  0) 0) |
| [10] |
许冬宁, 吴晓青, 周方园, 等. 减少农田土壤氮损失的微生物调控技术研究进展[J]. 山东科学, 2024, 37(2): 117-126 (  0) 0) |
| [11] |
闫首龙, 李爽, 陈曦, 等. 生物炭固定化微生物修复石油烃污染研究进展[J]. 化学与生物工程, 2023, 40(9): 10–14, 26 (  0) 0) |
| [12] |
汪海峰, 王井亮, 王翀, 等. 一株肠源枯草芽孢杆菌的生长、抗逆和产酶特性分析[J]. 中国畜牧杂志, 2012, 48(17): 66-70 (  0) 0) |
| [13] |
Raklami A, Tahiri A I, Bechtaoui N, et al. Restoring the plant productivity of heavy metal-contaminated soil using phosphate sludge, marble waste, and beneficial microorganisms[J]. Journal of Environmental Sciences, 2021, 99: 210-221 DOI:10.1016/j.jes.2020.06.032 (  0) 0) |
| [14] |
鲁丽佳, 计丕霞, 陈全, 等. 生物炭提升土壤中解磷菌定殖及其解磷能力[J]. 材料导报, 2024, 38(21): 154-162 (  0) 0) |
| [15] |
闻诗歌, 李爽, 彭小锋, 等. 枯草芽孢杆菌抗菌脂肽的重组表达及应用研究进展[J]. 食品安全质量检测学报, 2024, 15(14): 105-114 (  0) 0) |
| [16] |
郑红丽, 周晓荣, 樊明寿. 燕麦根际有机磷细菌的分离及其有关生理特性的研究[J]. 干旱地区农业研究, 2007, 25(5): 1-6 (  0) 0) |
| [17] |
张韩, 龚霞. 生物炭与改性物质对土壤中重金属影响的研究进展[J]. 江西农业学报, 2025, 37(1): 18-27 (  0) 0) |
| [18] |
王宣懿, 梁媛, 袁楚齐, 等. P改性生物炭微生物复合材料磷释放特性与阿特拉津去除效果及机理研究[J]. 环境科学学报, 2024, 44(6): 20-30 (  0) 0) |
| [19] |
黎紫珊, 胡志文, 梅闯, 等. 稻秆生物炭和蜡状芽孢杆菌联合作用对土壤重金属形态转化及微生物群落的影响[J]. 环境工程, 2024, 42(10): 165-176 (  0) 0) |
| [20] |
王璞. 土壤中添加生物质炭对土壤及番茄生长指标影响的研究[D]. 太谷: 山西农业大学, 2015.
(  0) 0) |
| [21] |
鲍士旦. 土壤农化分析[M].
中国环境科学出版社, 北京, 1997: 8-19
(  0) 0) |
| [22] |
封俊豪, 刘小伟, 景煜都, 等. 增温对黄土高原草地土壤有机碳三库分解影响特征与机制[J/OL]. 土壤学报, 2025: 1–14. (2025–05–12). https://kns.cnki.net/KCMS/detail/detail.aspx?filename=TRXB20250508001&dbname=CJFD&dbcode=CJFQ.
(  0) 0) |
| [23] |
Liu Y X, Chen L, Ma T F, et al. EasyAmplicon: An easy-to-use, open-source, reproducible, and community-based pipeline for amplicon data analysis in microbiome research[J]. iMeta, 2023, 2(1): e83 DOI:10.1002/imt2.83 (  0) 0) |
| [24] |
赵学强, 潘贤章, 马海艺, 等. 中国酸性土壤利用的科学问题与策略[J]. 土壤学报, 2023, 60(5): 1248-1263 (  0) 0) |
| [25] |
王启, 高鹏飞, 姚佳, 等. 减氮配施炭基肥对土壤理化性质与马铃薯产量品质的影响[J]. 中国土壤与肥料, 2024(12): 84-93 (  0) 0) |
| [26] |
刘慧, 焦岩, 窦婉毓, 等. 减氮配施生物炭对土壤肥力和水稻产量的补偿效应与机制[J]. 农业机械学报, 2024, 55(9): 391–401, 469 (  0) 0) |
| [27] |
Tong D L, Xu R K. Ameliorating effects of fungus chaff and its biochar on soil acidity[J]. Communications in Soil Science and Plant Analysis, 2015, 46(15): 1913-1921 DOI:10.1080/00103624.2015.1068323 (  0) 0) |
| [28] |
毛志海, 殷想想, 占成, 等. 乳酸利用菌的筛选及生长特性研究[J]. 酿酒科技, 2023(1): 24–29, 34 (  0) 0) |
| [29] |
苏晓佳, 罗小叶, 王晓丹. 降酸微生物在发酵饮品领域应用研究进展[J]. 中国酿造, 2024, 43(12): 1-5 (  0) 0) |
| [30] |
Gu Q, Li Y X, Lou Y, et al. Selecting autochthonous lactic acid bacteria for co-inoculation in Chinese bayberry wine production: Stress response, starter cultures application and volatilomic study[J]. Food Research International, 2024, 178: 113976 DOI:10.1016/j.foodres.2024.113976 (  0) 0) |
| [31] |
王海洋, 夏昊, 李红霞, 等. 生物炭配施土壤改良剂对酸性土壤特性及烤烟品质的影响[J]. 云南农业大学学报(自然科学), 2024, 39(3): 79-89 (  0) 0) |
| [32] |
高静, 徐明岗, 李然, 等. 整合分析生物炭施用对土壤pH的影响[J]. 中国农业科技导报, 2023, 25(9): 186-196 (  0) 0) |
| [33] |
程明琨, 萧洪东, 李学文, 等. 减氮条件下生物质炭施用对珠三角地区生菜产量、品质及土壤性质的影响[J]. 土壤, 2023, 55(1): 37-44 DOI:10.13758/j.cnki.tr.2023.01.005 (  0) 0) |
| [34] |
Xia H, Riaz M, Babar S, et al. "Assessing the impact of biochar on microbes in acidic soils: Alleviating the toxicity of aluminum and acidity"[J]. Journal of Environmental Management, 2023, 345: 118796 DOI:10.1016/j.jenvman.2023.118796 (  0) 0) |
| [35] |
Bell T H, Callender K L, Whyte L G, et al. Microbial competition in polar soils: A review of an understudied but potentially important control on productivity[J]. Biology, 2013, 2(2): 533-554 DOI:10.3390/biology2020533 (  0) 0) |
| [36] |
Fernando D R, Marshall A T, Lynch J P. Foliar nutrient distribution patterns in sympatric maple species reflect contrasting sensitivity to excess manganese[J]. PLoS One, 2016, 11(7): e0157702 DOI:10.1371/journal.pone.0157702 (  0) 0) |
| [37] |
马晓丹. 内蒙古草原7种地带性针茅根际微生物群落的构建、更替及功能探究[D]. 呼和浩特: 内蒙古大学, 2023.
(  0) 0) |
| [38] |
张哲超. 耐盐碱根际促生菌与丛枝菌根真菌联合提高牧草盐碱耐受性的微生物机制研究[D]. 呼和浩特: 内蒙古大学, 2022.
(  0) 0) |
| [39] |
齐钊. 海南近岸珊瑚微生物组种间空间变化特征及对环境胁迫的响应研究[D]. 海口: 海南大学, 2023.
(  0) 0) |
| [40] |
Wang J Y, Xiong Z Q, Kuzyakov Y. Biochar stability in soil: Meta-analysis of decomposition and priming effects[J]. GCB Bioenergy, 2016, 8(3): 512-523 DOI:10.1111/gcbb.12266 (  0) 0) |
| [41] |
Masiello C A, Chen Y, Gao X D, et al. Biochar and microbial signaling: Production conditions determine effects on microbial communication[J]. Environmental Science & Technology, 2013, 47(20): 11496-11503 (  0) 0) |
| [42] |
Abdulsada Z, Kibbee R, Princz J, et al. Transformation of silver nanoparticles (AgNPs) during lime treatment of wastewater sludge and their impact on soil bacteria[J]. Nanomaterials, 2021, 11(9): 2330 DOI:10.3390/nano11092330 (  0) 0) |
| [43] |
刘晓霞, 金秉洁, 张敏, 等. 生物质炭用量对新垦耕地土壤肥力、细菌群落结构和功能以及作物生物量的影响[J]. 土壤, 2025, 57(1): 76-85 DOI:10.13758/j.cnki.tr.2025.01.009 (  0) 0) |
| [44] |
杨安娜, 李曾燕, 牟凌, 等. 上海大金山岛不同植被类型土壤细菌群落的变异[J]. 植物生态学报, 2024, 48(3): 377-389 (  0) 0) |
| [45] |
Naumoff D G, Dedysh S N. Lateral gene transfer between the Bacteroidetes and Acidobacteria: The case of α-l[J]. FEBS Letters, 2012, 586(21): 3843-3851 DOI:10.1016/j.febslet.2012.09.005 (  0) 0) |
| [46] |
Yang A N, Li Z Y, Mou L, et al. Variation in soil bacterial community across vegetation types in Dajinshan Island, Shanghai[J]. Chinese Journal of Plant Ecology, 2024, 48(3): 377-389 DOI:10.17521/cjpe.2023.0172 (  0) 0) |
| [47] |
Xiao Y, Wu Z J, Cui M, et al. Co-modification of biochar and bentonite for adsorption and stabilization of Pb2+ ions[J]. Journal of Inorganic Materials, 2021, 36(10): 1083 DOI:10.15541/jim20200745 (  0) 0) |
| [48] |
高德才, 张蕾, 刘强, 等. 生物黑炭对旱地土壤CO2、CH4、N2O排放及其环境效益的影响[J]. 生态学报, 2015, 35(11): 3615-3624 (  0) 0) |
2. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 211135, China;
3. School of Life Sciences, Beijing Institute of Technology, Beijing 100049, China;
4. University of Chinese Academy of Sciences, Beijing 100049, China;
5. College of Land Resource and Environment, Jiangxi Agricultural University, Nanchang 330045, China;
6. School of Soil and Water Conservation, Jiangxi University of Water Resources and Electric Power, Nanchang 330099, China
 2026, Vol. 58
2026, Vol. 58


