2. 福建师范大学福建省植物生理生态重点实验室, 福州 350007
可溶性有机质(Dissolved organic matter,DOM)作为土壤碳库中最具活性和流动性的有机组分,对土壤碳循环和有机质储存至关重要[1]。DOM组成不仅影响其在土壤中的迁移转化,更反映其稳定性和生物可利用性[2-3]。如植物源类腐殖质组分具有较大的分子量和复杂芳香结构,在土壤中较为持久,更多地贡献于碳汇,而微生物代谢主导的类蛋白质组分生物可利用性较高[4]。受微生物降解、矿物吸附、化学转化等影响,土壤DOM呈动态变化[5-6],进而影响其生态功能。已有研究揭示了DOM在不同大陆尺度[7]、海拔梯度[8]、土层深度[9]中的空间分异规律,但仍缺少对外源碳输入下土壤DOM动态的表征。因此,探究不同碳源添加下土壤DOM的动态变化将有助于加深对土壤碳循环过程的认识。
凋落物是森林土壤有机质输入和养分归还的重要途径[10],也是土壤DOM的主要来源[11]。凋落物输入会显著改变土壤DOM组成和性质[12]。但不同植物组织凋落物对土壤DOM的影响存在差异[13-14]。凋落叶和细根分别是植物地上与地下输入的重要碳源[15],二者在化学性质如C: N、木质素和纤维素含量方面存在显著差异,这些差异影响其在土壤中的分解[16],进而影响DOM含量、组成及其稳定性。然而,目前研究多聚焦单一碳源输入对土壤有机质形成的影响[17],而不同碳源添加下土壤DOM的动态变化尚未明晰。
生物质炭(Biochar,BC)是生物质在厌氧条件下经高温裂解产生的惰性炭,富含缩合芳香结构[18]。生物质炭具有比表面积大、吸附能力强、稳定性高等特点[19],可以改善土壤肥力、缓解土壤酸化[20],作为土壤改良剂近年在农业和林业中已得到广泛应用。已有研究表明,生物质炭可通过提高土壤pH,增加可溶性组分的释放,提高土壤DOM含量[21]。但也有研究发现,生物质炭的吸附作用也可能降低土壤DOM含量[22]。生物质炭施用可以改变DOM组成。Smebye等[23]研究报道,生物质炭添加优先吸附较小的脂肪族分子,增加了芳香烃的浸出,将DOM向更高分子量转化。然而,Eykelbosh等[24]发现,生物质炭添加优先保留了高分子量类腐殖质物质,对低分子量氨基酸类物质保留效果有限,增加了低分子量DOM的淋溶损失。此外,生物质炭在土壤中分解缓慢,能够以相对稳定的速率持续释放DOM,但其性质随老化过程改变[25],可能进一步影响DOM的动态变化。
杉木(Cunninghamia lanceolata [Lamb.] Hook.)是我国亚热带广泛栽培的针叶树种,位居人工林面积首位[26]。然而,南方土壤肥力较低,加之杉木连栽等集约经营模式进一步加剧了土壤肥力衰退[27]。在此背景下,将凋落物制备成生物质炭用于土壤改良,既实现森林资源循环利用,又有效改善土壤肥力,是行之有效的土壤管理策略。但以往的研究多聚焦于单一凋落物输入或单施生物质炭对土壤DOM的影响[28],而凋落叶、细根及生物质炭添加对土壤DOM影响的差异,尤其是动态变化鲜少报道。为此,本研究通过360 d的培养试验,结合紫外可见光谱与荧光光谱分析,探究杉木凋落叶、细根及生物质炭添加对土壤DOM含量和组成的影响,揭示不同碳源添加下土壤DOM的动态变化,为深入理解亚热带森林土壤碳循环提供科学依据。
1 材料与方法 1.1 采样点概况采样点位于福建省南平市武夷山国家公园(27° 33′N~27°54′ N,117°27′E~117°51′ E)。该区域为典型的亚热带季风气候,年均气温为12~18 ℃,年均相对湿度为82%~85%,年降水量约为1 900 mm[29]。本研究以海拔780 m处杉木人工林为主要对象,土壤类型为黄红壤。
1.2 试验材料2023年2月进行土壤样品采集,去除表层枯枝落叶,采集杉木人工林表层土壤(0~15 cm),新鲜土混合均匀后全部过2 mm筛,于4 ℃冰箱保存用于培养试验。土壤pH为4.08,全碳(TC)含量为23.09 g/kg,全氮(TN)含量为1.75 g/kg,可溶性有机碳(DOC)含量为10.34 mg/kg。
杉木细根和凋落叶用去离子水洗净,在60 ℃下烘干、粉碎后过2 mm筛,用于后续培养和生物质炭制备。生物质炭制备需将凋落物适量置于锡箔纸中放置于KTF管式炉中封闭,在350 ℃厌氧条件下热解2 h,冷却后过2 mm筛,充分混匀备用。外源碳的基本性质见表 1。
|
|
表 1 外源碳基本性质 Table 1 Basic properties of exogenous carbon |
试验设置4个处理:培养土不添加外源碳(CK);土壤+1% 生物质炭(SB);土壤+1% 细根(SR);土壤+1% 凋落叶(SL);每个处理16次重复。分别称取140 g (相当于干土质量100 g)过2 mm筛的新鲜土和相应添加量的杉木细根、凋落叶及其生物质炭,混合均匀后置于500 mL棕色培养瓶中,在设定为25 ℃的恒温培养箱中培养,通过称重法定期补充去离子水,使土壤水分保持在60% 最大田间持水量。分别于培养后30、90、180和360 d进行破坏性取样,每次取样4个重复,测定相关指标。
1.4 测定指标及方法土壤pH采用电位法测定(Mettler FE28,上海),水土质量比为2.5∶1;TC、TN含量采用元素分析仪(Elementar Vario EL III,德国)测定;土壤硝态氮(NO3–-N)和铵态氮(NH4+-N)含量用2 mol/L的KCl浸提,采用连续流动分析仪(Skalar San++,荷兰)测定。
土壤DOM浸提:将15 g过2 mm筛的新鲜土壤置于50 mL离心管中,加入30 mL超纯水,在25 ℃、250 r/min下振荡30 min,以尽量减少提取过程中DOM的降解;悬浮液在4 000 r/min下离心10 min,上清液通过0.45 μm滤膜过滤后立即进行分析。DOC含量采用总有机碳分析仪(TOC-VCPH,岛津,日本)测定。
土壤DOM光谱分析:紫外–可见吸收光谱采用紫外可见分光光度计(Shimadzu UV-2540,日本)测定;芳香化指数(SUVA254)为在254 nm波长的吸光度与DOC含量的比值,表征DOM芳香化程度;DOM的荧光发射光谱及三维荧光光谱均采用荧光分光光度计(F7000,Hitachi,日本)测定;荧光发射光谱腐殖化指数(HIX)为固定激发波长为254 nm时,435~ 480 nm波段发射光谱的峰面积(S435~480)与300~345 nm波段发射光谱的峰面积(S300~345)的比值。
1.5 数据处理采用SPSS 26.0软件对4个处理间土壤理化性质、DOC含量及光谱指标进行单因素方差分析(ANOVA),并利用最小显著差异(LSD)法进行多重比较。使用Matlab 2021b软件,基于DOM Flour工具箱进行平行因子分析,以确定DOM组分。切除瑞利散射和拉曼散射,排除异常值,通过裂半分析和残差分析验证平行因子模型的有效性。采用Origin 2021和Correlation Plot工具包绘制DOM与土壤理化性质的皮尔逊相关性热图。
2 结果与分析 2.1 不同碳源添加对土壤基本性质的影响不同处理土壤基本性质见表 2。随培养时间延长,土壤pH整体呈下降趋势,SB、SR和SL处理pH在30 d时显著高于CK(P < 0.05),后逐渐降低;SB处理pH从4.65逐步降至4.50,降幅仅3.1%。SB处理土壤TC含量最高,且随培养时间无显著变化;SR和SL处理次之,均显著高于CK(P < 0.05)。与CK相比,除30 d外,SB、SR和SL处理均显著提高土壤TN含量(P < 0.05),其中SL处理在360 d时最高(2.07 g/kg),显著高于SR和SB处理(P < 0.05)。SB处理土壤C∶N最高,且随培养时间无显著变化;SL和SR处理土壤C∶N随培养时间显著降低(P < 0.05)。各处理土壤NH4+-N含量在30 d时最高,后迅速下降并趋于稳定,且30 d时SB、SL和SR处理土壤NH4+-N含量均显著低于CK (P < 0.05)。土壤NO3–-N含量随培养时间显著提高(P < 0.05),360 d时SR处理土壤NO3–-N含量最高(91.50 mg/kg),SL处理次之,SB处理土壤NO3–-N含量显著低于SR和SL处理(P < 0.05)。
|
|
表 2 不同处理土壤基本性质 Table 2 Soil properties under different treatments |
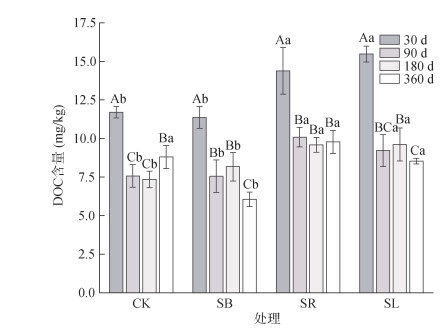
土壤DOC为土壤DOM的主要组成部分,本研究以土壤DOC含量表征土壤DOM含量变化。由图 1可知,30 d时各处理土壤DOC含量最高,90 d时土壤DOC含量显著降低(P < 0.05),180 d和360 d时土壤DOC含量变化幅度趋于稳定。与CK相比,SL和SR处理土壤DOC含量在30、90和180 d时显著增加(P < 0.05),而SB处理对土壤DOC含量无显著影响;360 d时,SB处理土壤DOC含量显著降低(P < 0.05)。
|
(图中大写字母不同表示同一碳源处理不同培养时间下差异显著(P < 0.05),小写字母不同表示相同时间不同碳源处理间差异显著(P < 0.05),下图同) 图 1 不同处理土壤DOC含量 Fig. 1 Soil DOC contents under different treatments |
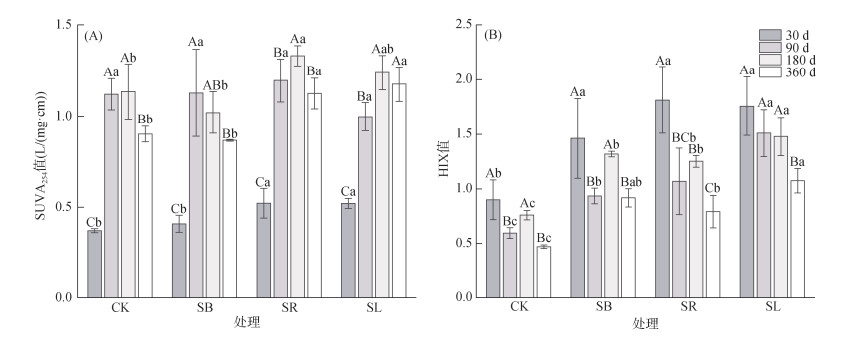
由图 2可知,SUVA254值随培养时间呈先升高后降低的趋势,30、180和360 d时,SL和SR处理SUVA254值均显著高于CK(P < 0.05),而SB处理与CK无显著差异。除180 d外,各处理HIX值整体呈下降趋势。与CK相比,SB、SR和SL处理显著提高HIX值(P < 0.05)。
|
(A. 土壤DOM芳香化指数(SUVA254);B. 土壤DOM腐殖化指数(HIX)) 图 2 不同处理土壤DOM光谱特性 Fig. 2 Spectral characteristics of soil DOM under different treatments |
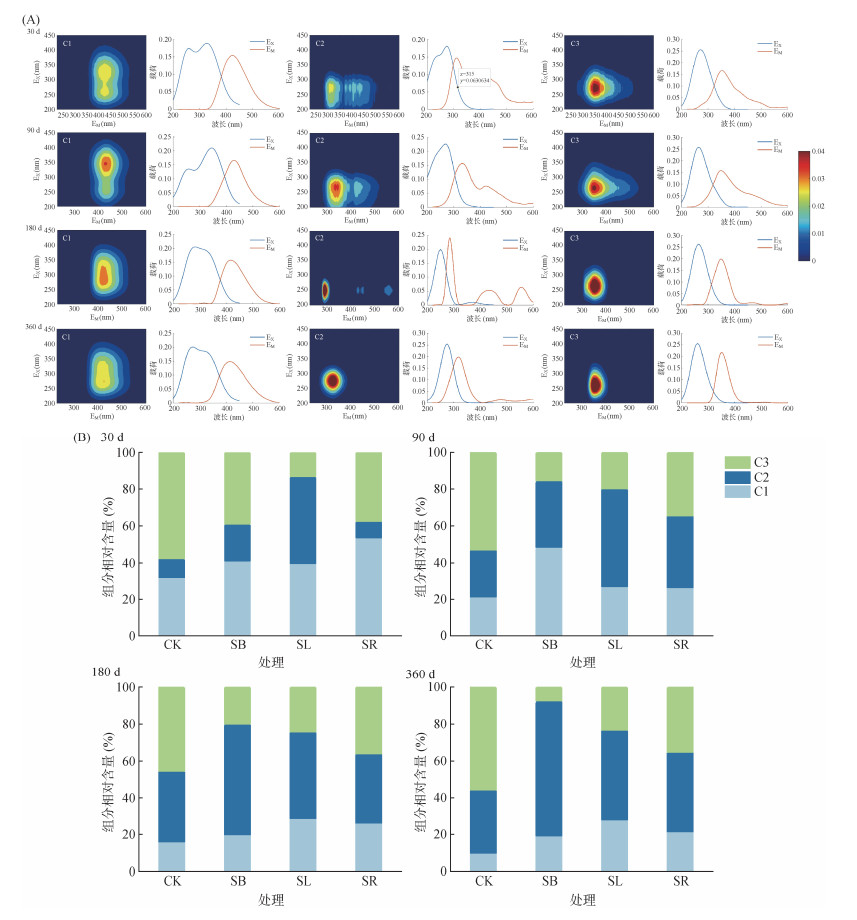
平行因子分析结果表明,土壤DOM由3个组分组成(C1、C2和C3;图 3)。C1的激发波长/发射波长(EX/EM)为250~320/410,代表类富里酸物质;C2的EX/EM为280/310,代表类酪氨酸物质,是微生物代谢产物;C3的EX/EM为280/350,代表类色氨酸物质。CK中C3组分始终占主导(45.52%~57.81%),C1组分相对含量随培养时间从32.03% 降至9.96%,C2组分相对含量从10.16% 提升至34.28%。SB处理C2组分相对含量持续增加,由19.94% 升至73.31%;而C1和C3组分相对含量随培养时间逐渐降低。SL处理C2组分占主导(47.16%~53.27%),C3组分在180 d时升至24.41%,在360 d时各组分趋于稳定。SR处理C1组分相对含量在360 d降至21.33%,C2组分相对含量随培养时间从9.07% 升至43.28%,C3组分保持相对稳定(34.58%~37.61%)。
|
图 3 基于平行因子分析的土壤DOM荧光组分(A)及其相对含量(B) Fig. 3 Fluorescence components (A) and relative contents (B) of soil DOM based on EEM-PARAFAC |
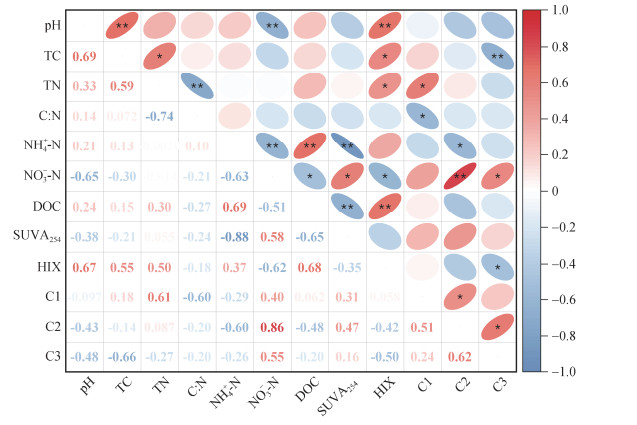
Pearson相关性分析表明(图 4),土壤DOC含量与NH4+-N含量、HIX值呈极显著正相关(P < 0.01),与NO3–-N及SUVA254值呈显著负相关(P < 0.05);SUVA254值与NO3–-N含量呈显著正相关(P < 0.05),与NH4+-N含量呈极显著负相关(P < 0.01);HIX值与TC、TN含量及pH呈显著正相关,与NO3–-N含量呈显著负相关(P < 0.05)。荧光组分中,C1组分相对含量与TN含量呈显著正相关,与土壤C: N呈显著负相关(P < 0.05);C2组分相对含量与NH4+-N含量呈显著负相关(P < 0.05);C3组分相对含量与NO3–-N含量呈显著正相关,与HIX值、TC含量呈显著负相关(P < 0.05)。
|
(*、** 分别表示相关性达P < 0.05和P < 0.01显著水平) 图 4 DOM含量、组成和荧光特性与土壤基本性质的皮尔逊相关关系 Fig. 4 Pearson correlations between soil properties with contents and fluorescence characteristics of DOM and its components |
本研究通过360 d培养试验揭示土壤DOC含量的动态变化:30 d时各处理土壤DOC含量显著升高,90 d时大幅度降低,180 d和360 d时变化幅度趋于平缓。这反映了DOC含量短期升高后随培养时间降低的趋势。Wang等[30]将13C标记光叶水青冈凋落叶衍生的DOC添加到土壤中,发现DOC含量随培养时间降低。Yoshida等[31]通过170 d培养试验发现针叶林和阔叶林土壤DOC含量在55 d达到峰值后急剧下降,本研究结果与此吻合。土壤DOC含量初期显著升高,随后急剧下降,归因于微生物对易分解碳源(如可溶性糖、氨基酸)的快速分解与释放,导致DOC含量短期激增[32]。随着易分解碳源耗尽,微生物转向分解木质素、多酚等复杂有机质,其降解速率显著低于初期。本研究结果表明,30、90及180 d时SL和SR处理显著提高土壤DOC含量,而SB处理无显著影响,这是由于凋落叶和细根中富含可溶性糖、有机酸及半纤维素等易分解物质,在微生物分泌的胞外酶作用下分解[33],导致DOC含量升高。而添加生物质炭带入的DOC含量远小于凋落叶和细根,且高温热解制备的生物质炭具有高度芳香化结构和抗分解特性,其难溶性碳组分占比 > 90%,矿化释放可溶性组分的能力有限[21],这是SB处理DOM含量较低的原因。
3.2 不同碳源添加对土壤DOM组成的影响SUVA254值可表征DOM中芳香族化合物含量及共轭程度。30 d时各处理SUVA254值较低,这是由于初期DOM以低芳香性的脂肪族、碳水化合物为主[34],其共轭结构少,芳香化程度较低。90 d时,SUVA254值显著增加且处理间无显著差异,归因于随着易分解组分快速消耗,残留的DOM中高芳香性组分(如木质素、多酚)比例升高。SUVA254值与土壤DOC含量的负相关性也佐证了这一观点。Wang等[35]研究发现,在生物降解过程中,DOM中易分解有机物被消耗,而芳香族化合物相对保留,本研究结果与此一致。SUVA254值在360 d时降低,是芳香族化合物被进一步分解矿化的结果。此外,SL和SR处理SUVA254值显著高于CK,这是因为杉木叶和根凋落物中含有较多木质素和多酚类化合物[36],通过淋溶作用释放大量芳香性DOM,直接提升SUVA254值。同时,真菌(如白腐真菌)分泌木质素过氧化物酶,将大分子芳香化合物分解为低分子量腐殖质[37],维持较高的SUVA254值。而SB处理与CK相比无显著差异。Liu等[38]发现,生物质炭中不稳定碳(如脂类、糖类)被微生物优先分解,而其芳香族骨架会降低微生物代谢商,抑制其对复杂芳香结构的分解,导致SUVA254值无显著变化。
HIX值是衡量DOM腐殖化程度的重要指标。研究表明,除180 d外,HIX值整体呈下降趋势,反映DOM腐殖化程度逐渐降低。这是由于培养过程中随可利用底物减少,微生物转向分解木质素和芳香族化合物,导致HIX值下降[39]。此外,SL、SR及SB处理HIX值显著高于CK。Jin等[40]发现,有机物料(秸秆、粪便)处理的多酚、氨基酸等腐殖质前体物质含量较对照组增加15%~25%,与腐殖酸含量呈正相关,且有机物料处理提高了过氧化氢酶和漆酶活性,这可能是碳源添加下土壤HIX值高于对照的原因。HIX值与TC、TN呈正相关性,表明碳源添加下TC和TN含量的增加为腐殖质合成提供物质基础,促进土壤DOM腐殖化。
本研究中,土壤DOM共识别出类富里酸(C1)、类酪氨酸(C2)和类色氨酸(C3) 3种荧光组分,这与Ye等[34]对热带人工林土壤DOM的研究结果相似。C1组分为低分子量腐殖质,其结构复杂,具有较高芳香性和丰富的官能团,而C2和C3组分归属于微生物源类蛋白质组分。整体而言,C1相对含量在30 d时较高,后随培养时间逐渐降低,而C2相对含量随培养时间逐渐增加。初期土壤中木质素、多酚等植物源大分子通过氧化缩合形成类富里酸物质[41],在缺乏外源有机物输入时,土壤微生物通过分泌胞外酶降解部分类富里酸转化为类蛋白质物质[39],导致C2组分的积累。不同处理土壤DOM荧光组分相对含量存在差异。SB处理C2组分相对含量从19.94% 升至73.31%,而C1和C3组分相对含量持续降低。陈丽铭等[42]通过为期45 d培养试验发现,生物质炭添加提高了与微生物转化有关组分的相对含量,降低了类富里酸组分的相对含量,本研究结果与此相似。这是由于生物质炭的特性(如多孔结构、芳香族化合物及功能基团)通过改变土壤微生物,特别是真菌群落组成和多样性,驱动土壤DOM从植物源类腐殖质向微生物源类蛋白质组分的转化。阎海涛等[43]发现,生物质炭添加显著改变了真菌群落结构,使担子菌门和子囊菌门的丰度增加,其分泌的氧化酶加速类色氨酸物质的分解。本研究中,SL处理C2组分相对含量始终较高(47.16%~53.27%),C3组分相对含量在180 d时升至24.41%,之后趋于稳定。此动态特征反映了凋落叶分解的两个阶段性过程,初期凋落叶富含的可溶性糖、有机酸及半纤维素等易分解组分通过微生物代谢途径转化为类蛋白质[12],后期真菌(如白腐真菌)通过分泌木质素过氧化物酶逐步降解大分子有机物[37],维持了C2和C3组分相对含量的稳定。而SR处理C2组分相对含量从9.07% 升至43.28%,C3组分相对含量保持稳定。与凋落叶相比,细根较高的木质素含量延缓了分解,更有利于长期碳固存[44]。细根分解产生的植物源DOM优先被土壤微生物消耗,并转化为微生物来源的DOM分子[45],引起C2组分相对含量升高。而Kalbitz等[46]通过为期1年的培养试验发现,pH为4.2的森林土壤中DOM类色氨酸组分通过铁铝氧化物的配体交换被吸附,吸附态DOM的矿化率仅为游离态的1/6,表明类色氨酸组分因与矿物表面结合(如铁铝氧化物的配位键)而被选择性保留,维持了C3组分的相对稳定。
4 结论添加凋落叶和细根显著提高了土壤DOM含量和芳香性,而添加生物质炭无显著影响。添加凋落叶、细根和生物质炭显著提高了土壤DOM腐殖化程度,且添加凋落叶对土壤DOM腐殖化的促进作用强于细根和生物质炭。类富里酸(C1)组分相对含量在各处理中持续降低;添加生物质炭提升了类酪氨酸(C2)组分相对含量,但抑制了类色氨酸(C3)组分的积累;添加细根促进C2组分相对含量升高,而C3组分维持相对稳定;凋落叶添加下C2和C3组分保持相对稳定,反映了土壤中植物源DOM经微生物降解逐步转化为类蛋白质组分的过程。
本研究通过控制单一碳源输入的方式,探讨了凋落叶、细根(地上、地下植物碳源)及生物质炭(人工碳源)对土壤DOM影响的差异。然而,自然生态系统中各类外源碳输入是并存的,本研究未考虑多种碳源输入及其交互作用对土壤DOM的影响,在后续研究中可考虑结合傅里叶变换离子回旋共振质谱(FT-ICRMS)分析技术,深入开展凋落叶、细根及其生物质炭混合添加对土壤DOM分子组成的影响研究。
| [1] |
Kaiser K, Kalbitz K. Cycling downwards–dissolved organic matter in soils[J]. Soil Biology and Biochemistry, 2012, 52: 29-32 DOI:10.1016/j.soilbio.2012.04.002 (  0) 0) |
| [2] |
Wang Z, Zhang C X, Pan S L, et al. Responses of molecular composition and biodegradation of dissolved organic matter to erosion in topsoil versus subsoil in a Mollisol agricultural ecosystem[J]. Agriculture, Ecosystems & Environment, 2023, 354: 108569 (  0) 0) |
| [3] |
Man M L, Simpson M J. Dissolved organic matter molecular composition controls potential biodegradability[J]. Organic Geochemistry, 2025, 200: 104924 DOI:10.1016/j.orggeochem.2024.104924 (  0) 0) |
| [4] |
Zhou P, Tian L, Graham N, et al. Spatial patterns and environmental functions of dissolved organic matter in grassland soils of China[J]. Nature Communications, 2024, 15: 6356 (  0) 0) |
| [5] |
D'Andrilli J, Junker J R, Smith H J, et al. DOM composition alters ecosystem function during microbial processing of isolated sources[J]. Biogeochemistry, 2019, 142(2): 281-298 DOI:10.1007/s10533-018-00534-5 (  0) 0) |
| [6] |
Li T, Li P F, Qin W, et al. Fertilization weakens the ecological succession of dissolved organic matter in paddy rice rhizosphere soil at the molecular level[J]. Environmental Science & Technology, 2023, 57(48): 19782-19792 (  0) 0) |
| [7] |
Wang J, Qu L R, Osterholz H, et al. Effects of DOM chemodiversity on microbial diversity in forest soils on a continental scale[J]. Global Change Biology, 2025, 31(3): e70131 (  0) 0) |
| [8] |
Zhang Y L, Heal K V, Shi M J, et al. Decreasing molecular diversity of soil dissolved organic matter related to microbial community along an Alpine elevation gradient[J]. Science of the Total Environment, 2022, 818: 151823 (  0) 0) |
| [9] |
Cao X H, Li S G, Huang H, et al. Wildfire impacts on molecular changes of dissolved organic matter during its passage through soil[J]. Environmental Science & Technology, 2024 DOI:10.1021/acs.est.3c11056 (  0) 0) |
| [10] |
Koukol O, Novák F, Hrabal R, et al. Saprotrophic fungi transform organic phosphorus from spruce needle litter[J]. Soil Biology and Biochemistry, 2006, 38(12): 3372-3379 (  0) 0) |
| [11] |
Kalbitz K, Solinger S, Park J H, et al. Controls on the dynamics of dissolved organic matter in soils: A review[J]. Soil Science, 2000, 165(4): 277-304 (  0) 0) |
| [12] |
Cui Y, Luo F L, Chen Y H, et al. Rhizodeposition and litter decomposition of Phragmites australis play important roles in composition and properties of soil dissolved organic matter[J]. Ecological Indicators, 2022, 142: 109275 (  0) 0) |
| [13] |
黄煖, 王海珍, 杨智杰, 等. 种植米槠、杉木土壤DOM浓度和光谱特征差异及其对短期增温的响应[J]. 土壤, 2025, 57(1): 47-57 DOI:10.13758/j.cnki.tr.2025.01.006 (  0) 0) |
| [14] |
Zhao L, Du C C, Zhang Q, et al. The ultraviolet–visible absorbance and fluorescence characterization of dissolved organic matter derived from the leaf litter of Populus simonii, Artemisia desertorum, Salix cheilophila, and Populus tomentosa[J]. Environmental Science and Pollution Research, 2020, 27(29): 36439-36449 (  0) 0) |
| [15] |
Ma H Z, Mo L D, Crowther T W, et al. The global distribution and environmental drivers of aboveground versus belowground plant biomass[J]. Nature Ecology & Evolution, 2021, 5(8): 1110-1122 (  0) 0) |
| [16] |
Guo L L, Deng M F, Yang S, et al. The coordination between leaf and fine root litter decomposition and the difference in their controlling factors[J]. Global Ecology and Biogeography, 2021, 30(11): 2286-2296 (  0) 0) |
| [17] |
Lai S T, Dai W T, Wu F Z, et al. Labile carbon release from plant litter and its effect on soil organic matter formation in a subtropical forest[J]. Plant and Soil, 2025, 511(1): 151-161 (  0) 0) |
| [18] |
方婧, 金亮, 程磊磊, 等. 环境中生物质炭稳定性研究进展[J]. 土壤学报, 2019, 56(5): 1034-1047 (  0) 0) |
| [19] |
Lehmann J, Rillig M C, Thies J, et al. Biochar effects on soil biota–A review[J]. Soil Biology and Biochemistry, 2011, 43(9): 1812-1836 (  0) 0) |
| [20] |
Pei J M, Li J Q, Mia S, et al. Biochar aging increased microbial carbon use efficiency but decreased biomass turnover time[J]. Geoderma, 2021, 382: 114710 (  0) 0) |
| [21] |
Sun Y Q, Xiong X N, He M J, et al. Roles of biochar-derived dissolved organic matter in soil amendment and environmental remediation: A critical review[J]. Chemical Engineering Journal, 2021, 424: 130387 (  0) 0) |
| [22] |
Si D F, Wu S, Wu H T, et al. Activated carbon application simultaneously alleviates paddy soil arsenic mobilization and carbon emission by decreasing porewater dissolved organic matter[J]. Environmental Science & Technology, 2024, 58(18): 7880-7890 (  0) 0) |
| [23] |
Smebye A, Alling V, Vogt R D, et al. Biochar amendment to soil changes dissolved organic matter content and composition[J]. Chemosphere, 2016, 142: 100-105 (  0) 0) |
| [24] |
Eykelbosh A J, Johnson M S, Couto E G. Biochar decreases dissolved organic carbon but not nitrate leaching in relation to vinasse application in a Brazilian sugarcane soil[J]. Journal of Environmental Management, 2015, 149: 9-16 (  0) 0) |
| [25] |
Yang Y, Sun K, Liu J, et al. Changes in soil properties and CO2 emissions after biochar addition: Role of pyrolysis temperature and aging[J]. Science of the Total Environment, 2022, 839: 156333 (  0) 0) |
| [26] |
Zhang H, Zhou G M, Wang Y X, et al. Clear-cut and forest regeneration increase soil N2O emission in Cunninghamia lanceolata plantations[J]. Geoderma, 2021, 401: 115238 (  0) 0) |
| [27] |
Guo J H, Feng H L, Roberge G, et al. The negative effect of Chinese fir (Cunninghamia lanceolata) monoculture plantations on soil physicochemical properties, microbial biomass, fungal communities, and enzymatic activities[J]. Forest Ecology and Management, 2022, 519: 120297 (  0) 0) |
| [28] |
Wu P P, Ding Y D, Li S L, et al. Carbon, nitrogen and phosphorus stoichiometry controls interspecific patterns of leaf litter-derived dissolved organic matter biodegradation in subtropical plantations of China[J]. IForest - Biogeosciences and Forestry, 2021, 14(1): 80-85 (  0) 0) |
| [29] |
张厚喜, 林丛, 程浩, 等. 武夷山不同海拔梯度毛竹林土壤有机碳特征及影响因素[J]. 土壤, 2019, 51(4): 821-828 DOI:10.13758/j.cnki.tr.2019.04.025 (  0) 0) |
| [30] |
Wang M, Tian Q X, Liao C, et al. The fate of litter-derived dissolved organic carbon in forest soils: Results from an incubation experiment[J]. Biogeochemistry, 2019, 144(2): 133-147 (  0) 0) |
| [31] |
Yoshida H, Sazawa K, Wada N Y, et al. Changes in the chemical composition of soil organic matter including water-soluble component during incubation: A case study of coniferous and broadleaf forest soils[J]. Catena, 2018, 171: 22-28 (  0) 0) |
| [32] |
Hu A, Jang K S, Meng F F, et al. Microbial and environmental processes shape the link between organic matter functional traits and composition[J]. Environmental Science & Technology, 2022, 56(14): 10504-10516 (  0) 0) |
| [33] |
Yin L M, Zhang T S, Dijkstra F A, et al. Priming effect varies with root order: A case of Cunninghamia lanceolata[J]. Soil Biology and Biochemistry, 2021, 160: 108354 (  0) 0) |
| [34] |
Ye Q H, Wang Y H, Zhang Z T, et al. Dissolved organic matter characteristics in soils of tropical legume and non-legume tree plantations[J]. Soil Biology and Biochemistry, 2020, 148: 107880 (  0) 0) |
| [35] |
Wang Y H, Wang Y S, Han L L, et al. Concentration and compositional controls on degradation of permafrost- derived dissolved organic matter on the Qinghai–Tibetan Plateau[J]. Limnology and Oceanography Letters, 2024, 9(5): 563-572 (  0) 0) |
| [36] |
马志良, 杨万勤, 吴福忠, 等. 四川盆地亚热带常绿阔叶林凋落叶多酚类物质在不同降雨期间的降解特征[J]. 生态学报, 2018, 38(9): 3078-3085 (  0) 0) |
| [37] |
郭嘉龙, 张丽仙, 杨丽, 等. 不同发育阶段杉木凋落物分解过程中难分解物质的动态特征[J]. 江西农业大学学报, 2024, 46(6): 1488-1497 (  0) 0) |
| [38] |
Liu H T, Wang X, Song X Q, et al. Generalists and specialists decomposing labile and aromatic biochar compounds and sequestering carbon in soil[J]. Geoderma, 2022, 428: 116176 (  0) 0) |
| [39] |
Liu J X, Liu S G, Li Y Y, et al. Warming effects on the decomposition of two litter species in model subtropical forests[J]. Plant and Soil, 2017, 420(1): 277-287 (  0) 0) |
| [40] |
Jin S G, Ma H B, Jia L, et al. Organic material additions have stronger effects on humic substances and enzyme activities than soil types[J]. Land Degradation & Development, 2022, 33(15): 2783-2794 (  0) 0) |
| [41] |
Qin X Q, Yao B, Jin L, et al. Characterizing soil dissolved organic matter in typical soils from China using fluorescence EEM–PARAFAC and UV–visible absorption[J]. Aquatic Geochemistry, 2020, 26(1): 71-88 (  0) 0) |
| [42] |
陈丽铭, 吴月颖, 李财生, 等. 土壤溶解性有机质分子特征对不同来源有机肥分解的响应[J]. 土壤学报, 2023, 60(4): 1101-1112 (  0) 0) |
| [43] |
阎海涛, 殷全玉, 丁松爽, 等. 生物炭对褐土理化特性及真菌群落结构的影响[J]. 环境科学, 2018, 39(5): 2412-2419 (  0) 0) |
| [44] |
郑琳敏, 熊小玲, 姜永孟, 等. 武夷山不同海拔杉木凋落叶和细根分解规律以及驱动因素的差异[J]. 植物生态学报, 2025, 49(2): 244-255 (  0) 0) |
| [45] |
Roth V N, Lange M, Simon C, et al. Persistence of dissolved organic matter explained by molecular changes during its passage through soil[J]. Nature Geoscience, 2019, 12(9): 755-761 (  0) 0) |
| [46] |
Kalbitz K, Schwesig D, Rethemeyer J, et al. Stabilization of dissolved organic matter by sorption to the mineral soil[J]. Soil Biology and Biochemistry, 2005, 37(7): 1319-1331 (  0) 0) |
2. Fujian Provincial Key Laboratory for Plant Eco-physiology, Fujian Normal University, Fuzhou 350007, China
 2026, Vol. 58
2026, Vol. 58


