2. 江南大学环境过程与污染控制研究所, 江苏无锡 214122
腐殖酸(Humic acid,HA)是土壤有机质中结构复杂、活性较高的天然有机大分子聚合物,由动植物残体在微生物群落及地球物理化学作用下,经过数百年至千年的生物化学过程形成,广泛分布于土壤、泥炭等环境[1-2]。在农业生产中,腐殖酸对耕地质量改善与作物提质增效发挥着关键作用[3-4]。
在土壤改良方面,腐殖酸通过含氧官能团(如羧基、酚羟基等)与多种金属离子(如Fe³+、Al³+、Ca2+等)形成稳定络合物[5],显著增强土壤吸附性能和离子交换能力,使土壤pH维持相对稳定,平衡土壤酸化和盐碱化效应[6];凭借其表面活性特性,腐殖酸可以对农药制剂产生乳化分散作用,增强农药溶解性,降低有效成分的分解速率[7],提高农药利用率;此外,其胶黏性可以促进土壤团粒结构形成,增强土壤通气性和透水性,改善保水保肥性能[8];通过竞争性结合脲酶活性位点,抑制尿素水解,延长尿素肥效[9];同时,腐殖酸能够促进土壤颗粒对磷的解吸,增加土壤中生物可利用的有效磷含量,提高磷有效性[10]。在植物生长调控方面,腐殖酸所含的醌氢醌结构具有类植物生长素活性基团[11],能够刺激植物根细胞的分裂和生长[12];其较强的氧化还原特性,有助于增强生物体的光能捕获和电子转移[13],同时通过提供营养增加叶绿素合成,提高光系统II(PSII)过程的光能转换效率,促进植物光合作用[14],最终实现糖类、维生素C(VC)等营养物质的合成积累与生物量的增长[15]。腐殖酸对土壤–植物系统的双重调控效应,奠定了其在现代农业生产中不可替代的地位。
在农业绿色转型和“双碳”战略背景下,天然腐殖酸资源面临储量有限及提取成本高的瓶颈[16-17],利用农业废弃物合成的人工腐殖酸的需求日益增长[18]。我国每年产生约9亿吨农业秸秆废弃物,为人工腐殖酸的合成提供充足原料[6]。值得注意的是,不同原料组分合成的人工腐殖酸性质存在差异,纤维素类物质、木质素衍生物等含量直接影响腐殖酸的功能特性[19],这些差异可能导致腐殖酸对“土壤–植物”系统产生特异性调控作用。本研究聚焦以玉米秸秆、香樟树叶、花生壳和蓝藻4种具有不同碳结构和木质纤维素含量的废弃生物质为原料合成的人工腐殖酸,通过土培–盆栽试验体系,系统探究不同人工腐殖酸对土壤理化性质(有机碳组分、有效磷、pH等)的影响规律,以及对植物(生菜)生物量、光合参数及VC含量的差异化作用机制,为人工腐殖酸的农用功能化开发提供了靶向选择策略。
1 材料与方法 1.1 试验材料供试土壤采自江苏省无锡市(120°16′E,31°28′N)旱地土,按五点混合采样法采集0~20 cm土层土样,去除可见根系以及石砾,风干备用。土壤基础理化性质为:pH 8.3,电导率(EC)2.78 mS/cm,全氮含量23.15 g/kg,硝态氮含量0.12 g/kg,有效磷含量206.60 mg/kg。供试生菜品种为四季生菜(Lactuca sativa)。
以无锡当地收集的玉米秸秆(CS)、香樟树叶(CL)、花生壳(PS)和太湖收集的混合蓝藻(MC)为原料,合成人工腐殖酸。水热腐殖化合成人工腐殖酸在100 mL反应釜中进行,加入3 g原料固体、0.6 g KOH和60 mL去离子水,KOH使反应体系为碱性环境(pH=13),200 ℃下反应24 h。反应结束后,用0.22 μm聚醚砜过滤器(Titan,上海)过滤得到的液体样品为最终的人工腐殖酸产物。由原料玉米秸秆、香樟树叶、花生壳、蓝藻合成的人工腐殖酸分别命名为HACS、HACL、HAPS、HAMC。本文所用人工腐殖酸的基本理化性质已在先前研究中系统表征,包括pH、总养分含量、氧化还原活性及官能团组成等[3]。
1.2 试验设计室内培养试验于2022年3月至5月进行,采用上口外边长10.5 cm、下口外边长7 cm、高9.5 cm的花盆进行盆栽试验,每盆装干土2.5 kg。试验共设置7个处理,包括空白对照(CK)、施用秸秆(CS,3.2 g/kg土,拌土)、施用等量秸秆合成的腐殖酸(HACS,64 mL/kg土)、1/2量秸秆腐殖酸(1/2HACS,32 mL/kg)、1/2量香樟树叶腐殖酸(1/2HACL,32 mL/kg)、1/2量花生壳腐殖酸(1/2HAPS,32 mL/kg)和1/2量蓝藻腐殖酸(1/2HAMC,32 mL/kg)处理,每处理3个重复。生菜种子用10% 的H2O2灭菌10 min,然后用去离子水反复冲洗,将无菌种子在25 ℃、平均湿度60% 的避光处孵育3 d后,每个花盆移栽一株发芽均匀的幼苗。在生菜“露心”后第1个叶环的5~6片叶全部展开时施用人工腐殖酸,按照处理施用量平均分为4 d施用,对照处理用同样的方法灌溉去离子水。试验过程中,土壤含水率保持在土壤最大持水量的70%,除草、浇水等日常管理措施均保持一致。从移栽到收获累计58 d,生长周期符合四季生菜的生长规律。生菜收获时,进行破坏性取样,将土壤样品混合后分为两部分,一部分鲜土置于–20 ℃冰箱,另一部分经自然风干处理后研磨过筛,用于指标测定。
1.3 测定指标及方法土壤理化性质及植物生理指标的测定参照《土壤农业化学分析方法》[20]。土壤pH采用电位法测定,以水为浸提剂,水土质量比为2.5∶1,恒温振荡均匀后静置30 min,采用精密pH计(S210,METTLER TOLEDO,中国)测定;土壤全碳、全氮含量使用元素分析仪(Unicube,Elementar,德国)通过高温燃烧法(900 ℃)测定,检测精度为±0.1%;土壤硝态氮含量采用紫外分光光度计(UV1800,Shimadzu,日本)测定;土壤有效磷含量采用0.5 mol/L碳酸氢钠浸提–钼锑抗比色法测定;土壤溶解性有机碳含量采用总有机碳分析仪(Vario TOC Select,Elementar,德国)测定。人工腐殖酸施加完成后的第7天,使用便携式光合仪(CIRAS-3,PP SYSTEMS,美国)测定植物光合参数,同步获取植物净光合速率和蒸腾速率;收获后,生菜叶片VC含量采用钼蓝比色法测定。
1.4 数据统计分析采用Excel 2019进行数据整理,利用SPSS Statistics v23.0对数据进行统计分析,采用单因素方差分析和邓肯比较法进行处理间差异显著性检验(P < 0.05);图表绘制通过Origin 2018软件完成。
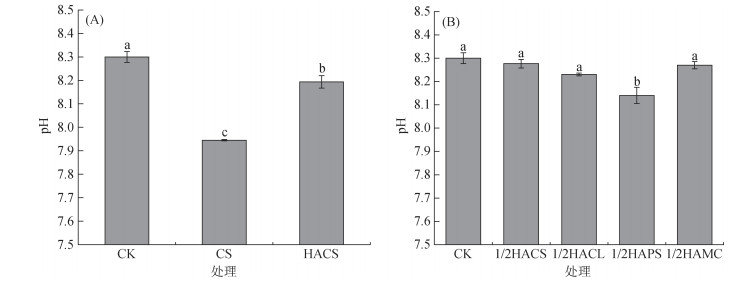
2 结果与分析 2.1 不同源人工腐殖酸对土壤理化性质的影响 2.1.1 土壤pH土壤酸碱度对土壤中的生物化学反应具有重要影响[21]。图 1A展示了秸秆直接还田和施加等量秸秆源腐殖酸对土壤pH的影响,CK、CS和HACS处理的pH分别为8.30、7.94和8.19,与CK相比,CS和HACS处理均能有效降低碱性土壤的pH,其中CS处理对土壤pH的降低更显著。结果表明,秸秆直接还田对碱性土壤的酸化效应强于其衍生的腐殖酸,而后者因腐殖化过程形成的缓冲体系,表现出更为温和的pH调节能力。施加32 mL/kg不同源腐殖酸后的pH响应如图 1B所示,仅1/2HAPS处理使土壤pH显著下降了0.16,其余处理均未表现出显著变化。这可能是由于花生壳本身含氮量高,花生壳腐殖酸中羧基、酚羟基等官能团促进土壤胶体盐基离子淋湿,降低土壤缓冲能力;此外,高碳氮比(C/N)腐殖酸的加入可激发土壤硝化反应,成为土壤酸化的主要驱动力[3]。
|
(CK:对照;CS:秸秆;HACS:秸秆源腐殖酸;HACL:香樟叶源腐殖酸;HAPS:花生壳源腐殖酸;HAMC:蓝藻源腐殖酸。图柱上方不同小写字母表示处理间差异显著(P < 0.05),下图同) 图 1 不同处理条件下土壤pH Fig. 1 Soil pH under different treatments |
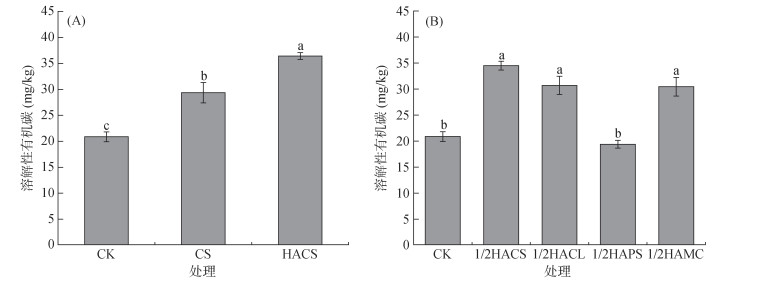
溶解性有机碳作为土壤有机碳的重要组成部分[22],因其具有溶解性强、稳定性低、易被分解和氧化等特性,对土壤中化学物质的溶解、吸附与迁移过程具有显著影响;同时,溶解性有机碳易于被植物和微生物利用,是维持土壤生态功能的重要物质基础[23]。秸秆直接还田和施加秸秆源腐殖酸后土壤溶解性有机碳含量如图 2A所示,相比CK处理(20.88 mg/kg),CS和HACS处理的溶解性有机碳含量分别为29.37和36.41 mg/kg,分别增加了40.66% 和74.37%。这表明向土壤中添加秸秆或以等量秸秆合成的腐殖酸,均能显著提高土壤中溶解性有机碳的含量,秸秆腐殖化处理比直接还田提升效果更为显著。进一步分析施加32 mL/kg不同源腐殖酸对土壤溶解性有机碳含量的影响,结果如图 2B所示。1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的溶解性有机碳含量分别为34.49、30.70、19.39和30.44 mg/kg,其中,1/2HACS、1/2HACL和1/2HAMC处理均能显著提高土壤溶解性有机碳含量,增幅分别为65.19%、47.05% 和45.82%;而1/2HAPS处理下溶解性有机碳含量未发生变化,说明花生壳源腐殖酸对土壤溶解性有机碳含量无显著影响。
|
图 2 不同处理条件下土壤溶解性有机碳含量 Fig. 2 Soil dissolved organic carbon contents under different treatments |
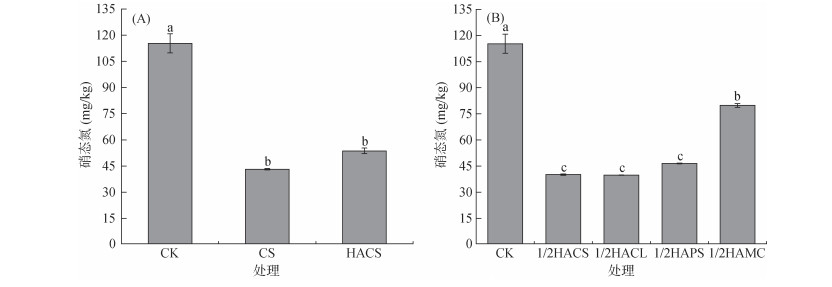
硝态氮作为潜在环境风险因子,其过量累积不仅会破坏土壤结构,还可能造成植物生理胁迫[24]。秸秆直接还田和施加秸秆源腐殖酸对土壤硝态氮的调控效应如图 3A所示,CK、CS和HACS处理的硝态氮含量分别为115.25、43.15和53.68 mg/kg。与CK相比,CS和HACS处理均显著降低土壤的硝态氮累积,降幅分别为62.56% 和53.42%;CS与HACS处理之间的硝态氮含量差异较小,表明秸秆及其等量合成的腐殖酸在降低土壤硝态氮方面具有相似效果,腐殖化过程并未削弱秸秆直接还田的硝态氮消减能力。施加32 mL/kg不同源人工腐殖酸后的土壤硝态氮含量如图 3B所示,1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的土壤硝态氮含量分别为40.15、39.79、46.57和79.82 mg/kg,相较于CK,4种不同源人工腐殖酸处理的硝态氮含量分别降低了65.16%、65.48%、59.59% 和30.74%。结果表明,人工腐殖酸的加入能够有效平衡土壤中的硝态氮含量,从而降低其环境健康风险。
|
图 3 不同处理条件下土壤硝态氮含量 Fig. 3 Soil nitrate nitrogen contents under different treatments |
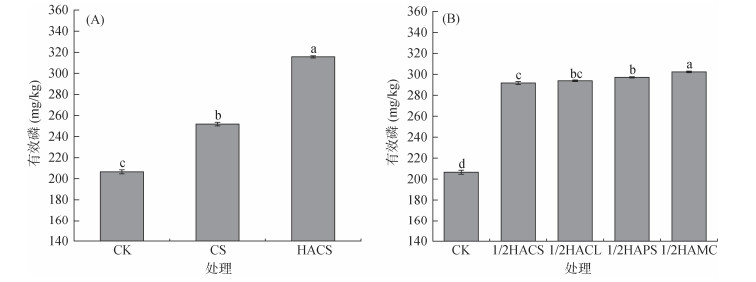
土壤有效磷作为植物根系可直接吸收的磷形态,是评价土壤磷素供应能力的关键指标[25]。图 4A展示了秸秆直接还田和施加秸秆源腐殖酸对土壤有效磷含量的影响,CK、CS和HACS处理的土壤有效磷含量分别为206.58、251.9和315.66 mg/kg。CS和HACS处理相比于CK,均显著提高了土壤中的有效磷含量,增幅分别达到了21.93% 和52.80%,腐殖化处理比秸秆直接还田多提升30.9%,表明腐殖化过程更能有效提升土壤有效磷含量。向土壤中施加不同原料合成的32 mL/kg腐殖酸均能显著提高土壤有效磷含量(图 4B),1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的土壤有效磷含量分别为291.68、293.91、297.13和302.34 mg/kg。相较于CK,4种不同源人工腐殖酸处理的土壤有效磷含量增幅依次升高,分别为41.19%、42.22%、43.83%、46.35%,表明不同源人工腐殖酸对土壤有效磷含量的影响存在差异,其中蓝藻源腐殖酸处理对土壤有效磷含量的提升效果最为显著。
|
图 4 不同处理条件下土壤有效磷含量 Fig. 4 Soil available phosphorus contents under different treatments |
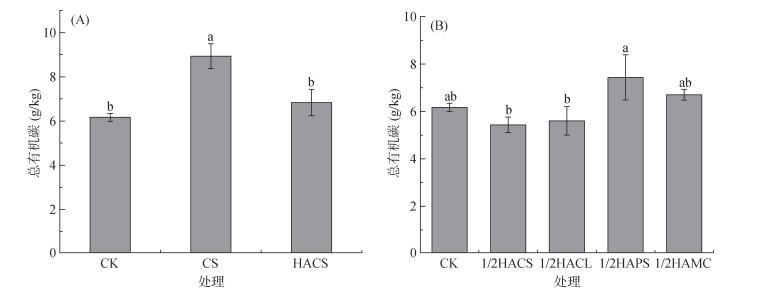
土壤总有机碳是土壤、植物及其他有机物流失后残留的碳汇,其含量易受生态环境因素显著影响,能够反映土壤肥力和有机质累积状态[26]。秸秆直接还田和施加秸秆源腐殖酸对土壤总有机碳的调控效应如图 5A所示,CK、CS和HACS处理的土壤总有机碳含量分别为6.17、8.93和6.83 g/kg。与CK相比,CS处理显著提高了土壤总有机碳含量,增幅达44.73%,而HACS处理则未表现出显著变化。施加32 mL/kg不同源腐殖酸后的土壤总有机碳含量如图 5B所示,1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的土壤总有机碳含量分别为5.43、5.60、7.43和6.70 g/kg,4种不同源人工腐殖酸处理的土壤总有机碳含量与CK均无显著差异,表明人工腐殖酸提升土壤有机碳含量的作用并不显著。
|
图 5 不同处理条件下土壤总有机碳含量 Fig. 5 Total soil organic carbon contents under different treatments |
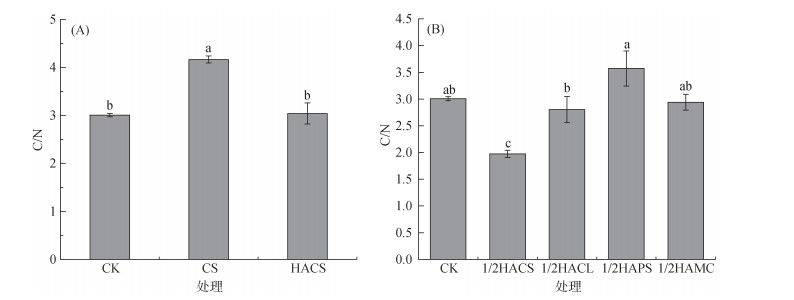
土壤C/N是指土壤中碳元素与氮元素总含量的比值,该比值是衡量土壤健康状况的重要指标之一[27]。C/N过低时,植物根系难以有效吸收水溶性有机碳而导致早衰,C/N过高则会抑制微生物分解矿化作用,同时消耗土壤中的有效氮素。因此,维持适宜的C/N对土壤肥力和植物生长具有重要意义。秸秆直接还田和施加4种不同源人工腐殖酸对土壤C/N的调控效应如图 6A和6B所示,CS处理显著提高土壤C/N,而秸秆源腐殖酸的施用对土壤C/N的影响相对较小。另外,花生壳源腐殖酸处理的C/N相较于其他3种不同源人工腐殖酸处理显著提高。
|
图 6 不同处理条件下土壤碳氮比 Fig. 6 Soil carbon to nitrogen ratios (C/N) under different treatments |
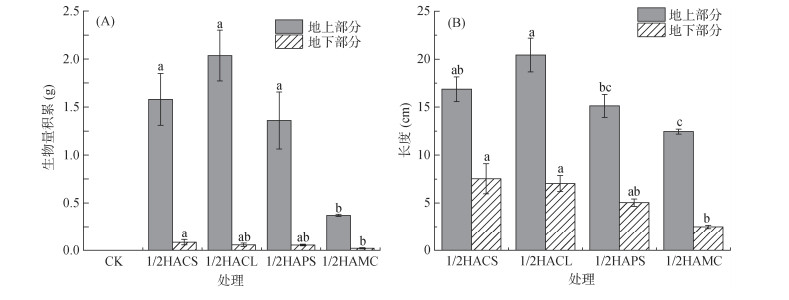
人工腐殖酸对生菜生长指标的调控效应如图 7A和7B所示。CK未表现出生菜的生长,而施加4种不同源人工腐殖酸后,各处理均成功萌发出生菜,表明人工腐殖酸在一定程度上能够刺激生菜的生长。其中,1/2HACL处理在生菜地上部和根部的生物量及长度方面表现最优,而1/2HAMC处理由于其硝态氮含量显著高于其他人工腐殖酸处理,出现明显生物量抑制。结果表明,人工腐殖酸的施加对土壤肥力具有一定改善作用,但不同来源的人工腐殖酸对土壤肥力改善和植物生长效果存在显著差异。
|
图 7 不同处理对生菜生物量(A)及长度(B)的影响 Fig. 7 Lettuce biomass (A) and lengths (B) under different treatments |
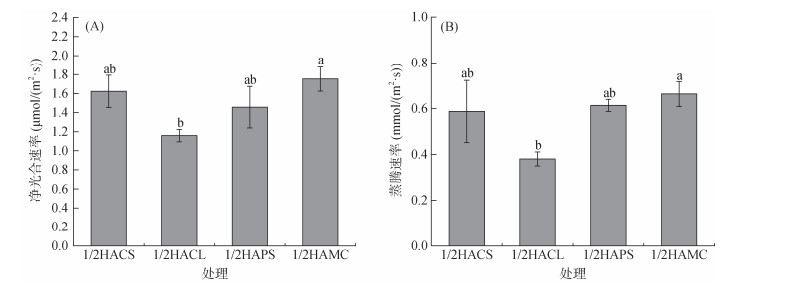
光合作用作为植物生长的基础生理代谢过程,驱动糖类物质的合成进而增加作物生物量的累积[22]。光合作用通过吸收光能将二氧化碳和水转化为有机物并释放氧气,期间会产生大量热量使植物体表温度升高,促进水分的蒸发,蒸腾速率是衡量植物蒸腾过程的重要参数[28],可以反映植物在水分吸收和运输方面的效率。施加4种不同源人工腐殖酸对生菜净光合速率和蒸腾速率的调控规律如图 8A和8B所示。光合作用与蒸腾作用之间呈显著的正相关,表明两者在植物生长过程中相互作用。1/2HAMC处理展现出最强的光合性能,生菜净光合速率和蒸腾速率分别高达1.75 μmol/(m2·s)和0.66 mmol/(m2·s),1/2HACS和1/2HAPS处理的光合和蒸腾参数次之,1/2HACL处理最低。值得注意的是,1/2HACL处理在生菜地上部和根部的生物量和长度最大(图 7),但净光合速率最低,说明净光合速率与生物量及生菜大小之间并非绝对正相关,这表明光合作用不仅影响植物的产量,还与作物的品质密切相关。
|
图 8 不同源人工腐殖酸对生菜的净光合速率(A)和蒸腾速率(B)的影响 Fig. 8 Lettuce net photosynthetic rates (A) and transpiration rates (B) under different treatments |
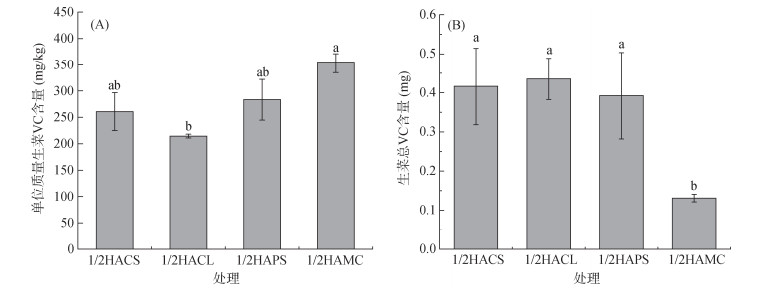
由于人体无法自行合成VC,VC成为人类日常生活必须要摄入的物质,对提高身体免疫力、抵御疾病风险等起着至关重要的作用,作物的VC含量是评价其品质的重要指标[29]。施加4种不同源人工腐殖酸对单位质量生菜地上部VC含量的调控规律如图 9A所示,1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的单位VC含量分别为260.96、214.48、283.47和353.12 mg/kg,表现为1/2HAMC > 1/2HAPS≈1/2HACS > 1/2HACL,该排序与生菜的净光合速率和蒸腾速率呈显著正相关,证实光合作用水平的提高可以促进VC的生物合成。如图 9B所示,1/2HACS、1/2HACL、1/2HAPS和1/2HAMC处理的地上部总VC累积量分别为0.42、0.44、0.39和0.13 mg,表现为1/2HACL≈1/2HACS≈1/2HAPS > 1/2HAMC,不同处理的总VC含量排序与单位VC含量的排序并不一致,源于总VC含量是由单位VC含量与生物量乘积决定的。施加蓝藻源腐殖酸对单位VC含量的提升效果最佳,但其对生物量的促进作用有限,导致生菜总VC含量最低,说明不同来源的人工腐殖酸对作物VC含量的影响不仅与其光合特性相关,还受到植物生长状态和人工腐殖酸种类的综合影响。
|
图 9 不同处理对单位质量生菜VC含量(A)和总VC含量(B)的影响 Fig. 9 Lettuce unit (A) and total (B) VC contents under different treatments |
与直接秸秆还田相比,秸秆源腐殖酸对土壤有效养分的提升和溶解性有机碳含量的提升效果更显著,且对土壤pH的调节更温和。秸秆中可溶性糖、蛋白质的释放可直接增加土壤溶解性有机碳。而人工腐殖酸中不仅含有腐殖质碳等稳定性有机碳组分,还能够提供未完全腐殖化的活性分子作为快速补剂激活土壤微生物活性,直接提高土壤溶解性有机碳含量[30]。秸秆腐殖化过程中大量活性官能团的生成有助于提升土壤缓冲能力和减少有效养分的流失。人工腐殖酸通过螯合土壤中不可利用的营养物质,从而维持土壤酸碱平衡。通常,人工腐殖酸作为带负电的阴离子,能够与土壤中的钙、镁等金属阳离子发生吸附作用,形成腐殖酸盐缓冲体系,从而抑制土壤盐分的上升,起到隔盐、吸盐的作用,有效防治盐碱化问题。此外,人工腐殖酸因其含有丰富的官能团(如羧基、酚羟基和氨基),有较强的离子交换能力,可以有效地平衡硝态氮含量,同时抑制土壤对水溶性磷的固定,减缓磷从速效态向迟效态或无效态的转化,还可以增强对土壤中钾元素、微量元素等养分的吸附和固定能力,减少养分的淋溶损失,从而提高氮磷钾等养分的有效性[31]。人工腐殖酸对土壤微生物的激活作用可显著增加真菌、细菌和放线菌的菌落数量和代谢活性,提升其对土壤元素循环的周转性能,提高土壤肥力[32]。然而,不同原料制备的人工腐殖酸性质差异导致其对土壤理化性质的改良效果不同。例如,与花生壳和蓝藻源腐殖酸相比,秸秆源和香樟叶源腐殖酸中营养物质含量较高且官能团结构丰富,而花生壳和蓝藻源腐殖酸具有更强的电子传输能力和丰富的可生物降解物质[3]。人工腐殖酸的两亲性聚合物组分可提高土壤中活性有机碳组分,蓝藻源腐殖酸可通过氧化还原反应和土壤矿物磷的溶解作用促进土壤有效磷的释放[13]。人工腐殖酸对土壤性质的改良很可能有助于土壤环境可持续发展和作物生长。
3.2 人工腐殖酸对生菜生长和品质的影响人工腐殖酸对生菜生长和品质具有显著的调控作用,但促生效果因原料类型而异。香樟叶源腐殖酸具有最佳的促生效果,但蓝藻源腐殖酸对生菜光合作用和品质的提升效果更显著。这主要是由于前者的直接养分供给能力和对土壤有效养分的活化,人工腐殖酸具有较强的离子交换能力,可以起到固氮、解磷等作用,提高土壤中有效养分含量。此外,人工腐殖酸还能促进植物体内吲哚乙酸的合成,增强根系活力和新陈代谢,从而提升生物量的累积[33]。而蓝藻源腐殖酸中高含量的镁可以作为叶绿素合成中间体,促进叶片的光能捕获和电子传递,最终提升植物光合作用[3]。另外,人工腐殖酸对光反应能量合成的促进和Rubisco酶活性的提高,加速叶片中糖和氨基酸的合成,进一步增强光合作用效率[34]。光合作用对碳水化合物的补充可进一步为VC的合成提供前体物质,从而提高单位生菜叶片中VC的含量。此外,人工腐殖酸中的微量元素如铁、锌等可作为VC合成的关键酶辅助因子,提升植物根系活力和养分利用效率等,进而提升生菜的营养品质。前期研究结果表明,蓝藻源腐殖酸中含有丰富的植物生长因子和还原性小分子酸,这些物质一方面可以激发植物抗氧化防御系统,另一方面,作为酶调因子可促进VC的合成与再生[33, 35]。
4 结论1) 秸秆直接还田与秸秆源腐殖酸均能有效降低碱性土壤pH,因腐殖化过程形成的缓冲体系,人工腐殖酸表现出更温和的调节能力。秸秆源人工腐殖酸在提升碳、磷有效性方面优于秸秆直接还田。
2) 不同农业废弃物原料制备的人工腐殖酸功能差异显著。秸秆源腐殖酸在提升土壤溶解性有机碳和降低硝态氮方面效果突出;香樟叶源腐殖酸促进生菜生物量增长最显著;花生壳源腐殖酸在土壤改良和作物生长方面调控效果不显著;蓝藻源腐殖酸提升有效磷幅度最大,光合作用提升最强,单位VC含量最高。
3) 人工腐殖酸通过理化调控与生物调控的协同作用影响土壤–植物系统,其综合效应受原料特性主导,不同来源人工腐殖酸在土壤肥力提升、作物生长与品质调控方面表现出差异化优势。
| [1] |
Shan J, Brune A, Ji R. Selective digestion of the proteinaceous component of humic substances by the geophagous earthworms Metaphire guillelmi and Amynthas corrugatus[J]. Soil Biology and Biochemistry, 2010, 42(9): 1455-1462 DOI:10.1016/j.soilbio.2010.05.008 (  0) 0) |
| [2] |
Almendros G, Guadalix M E, González-Vila F J, et al. Preservation of aliphatic macromolecules in soil humins[J]. Organic Geochemistry, 1996, 24(6/7): 651-659 (  0) 0) |
| [3] |
Li X N, Zhi Y C, Jia M H, et al. Properties and photosynthetic promotion mechanisms of artificial humic acid are feedstock-dependent[J]. Carbon Research, 2024, 3(1): 4 DOI:10.1007/s44246-023-00085-x (  0) 0) |
| [4] |
Yang F, Tang C Y, Antonietti M. Natural and artificial humic substances to manage minerals, ions, water, and soil microorganisms[J]. Chemical Society Reviews, 2021, 50(10): 6221-6239 DOI:10.1039/D0CS01363C (  0) 0) |
| [5] |
Yang F, Antonietti M. The sleeping giant: A polymer view on humic matter in synthesis and applications[J]. Progress in Polymer Science, 2020, 100: 101182 DOI:10.1016/j.progpolymsci.2019.101182 (  0) 0) |
| [6] |
Boguta P, Sokołowska Z. Influence of phosphate ions on buffer capacity of soil humic acids[J]. International Agrophysics, 2012, 26(1): 7-14 DOI:10.2478/v10247-012-0002-1 (  0) 0) |
| [7] |
袁瑞江, 姚银娟, 王丽乔, 等. 生物腐植酸(黄腐酸)及其在农业中的应用[J]. 河北农业科学, 2009, 13(7): 36–38, 133 (  0) 0) |
| [8] |
Wang L Q, Zhao Y, Liu H L, et al. The action difference of metabolic regulators on carbon conversion during different agricultural organic wastes composting[J]. Bioresource Technology, 2021, 329: 124902 DOI:10.1016/j.biortech.2021.124902 (  0) 0) |
| [9] |
Dong L H, Yang J S, Yuan H L, et al. Chemical characteristics and influences of two fractions of Chinese lignite humic acids on urease[J]. European Journal of Soil Biology, 2008, 44(2): 166-171 DOI:10.1016/j.ejsobi.2007.07.002 (  0) 0) |
| [10] |
Yang F, Zhang S S, Song J P, et al. Synthetic humic acids solubilize otherwise insoluble phosphates to improve soil fertility[J]. Angewandte Chemie International Edition, 2019, 58(52): 18813-18816 DOI:10.1002/anie.201911060 (  0) 0) |
| [11] |
García A C, de Souza L G A, Pereira M G, et al. Structure- property-function relationship in humic substances to explain the biological activity in plants[J]. Scientific Reports, 2016, 6: 20798 DOI:10.1038/srep20798 (  0) 0) |
| [12] |
Zanin L, Tomasi N, Zamboni A, et al. Water-extractable humic substances speed up transcriptional response of maize roots to nitrate[J]. Environmental and Experimental Botany, 2018, 147: 167-178 DOI:10.1016/j.envexpbot.2017.12.014 (  0) 0) |
| [13] |
Dermastia M. Plant hormones in phytoplasma infected plants[J]. Frontiers in Plant Science, 2019, 10: 477 DOI:10.3389/fpls.2019.00477 (  0) 0) |
| [14] |
李兴杰, 胡笑涛, 杨鑫, 等. 腐植酸对水培生菜生长和品质的影响[J]. 西北农业学报, 2016, 25(11): 1679-1685 (  0) 0) |
| [15] |
El-Shabrawi H M, Bakry B A, Ahmed M A, et al. Humic and oxalic acid stimulates grain yield and induces accumulation of plastidial carbohydrate metabolism enzymes in wheat grown under sandy soil conditions[J]. Agricultural Sciences, 2015, 6(1): 175-185 DOI:10.4236/as.2015.61016 (  0) 0) |
| [16] |
Dargie G C, Lewis S L, Lawson I T, et al. Age, extent and carbon storage of the central Congo Basin peatland complex[J]. Nature, 2017, 542(7639): 86-90 DOI:10.1038/nature21048 (  0) 0) |
| [17] |
Yang F, Fu Q, Antonietti M. Anthropogenic, carbon- reinforced soil as a living engineered material[J]. Chemical Reviews, 2023, 123(5): 2420-2435 DOI:10.1021/acs.chemrev.2c00399 (  0) 0) |
| [18] |
Zhou X, Zeng Y, Lv F T, et al. Organic semiconductor– organism interfaces for augmenting natural and artificial photosynthesis[J]. Accounts of Chemical Research, 2022, 55(2): 156-170 DOI:10.1021/acs.accounts.1c00580 (  0) 0) |
| [19] |
Smolyakov B S, Sagidullin A K, Bychkov A L, et al. Humic-modified natural and synthetic carbon adsorbents for the removal of Cd(II) from aqueous solutions[J]. Journal of Environmental Chemical Engineering, 2015, 3(3): 1939-1946 DOI:10.1016/j.jece.2015.07.005 (  0) 0) |
| [20] |
鲁如坤. 土壤农业化学分析方法[M].
中国农业科技出版社, 北京, 2002
(  0) 0) |
| [21] |
徐仁扣. 土壤酸化及其调控研究进展[J]. 土壤, 2015, 47(2): 238-244 (  0) 0) |
| [22] |
Bolan N S, Adriano D C, Kunhikrishnan A, et al. Dissolved organic matter[M]//Advances in Agronomy. Amsterdam: Elsevier, 2011: 1–75.
(  0) 0) |
| [23] |
Chen Z K, Liu F D, Cai G Y, et al. Responses of soil carbon pools and carbon management index to nitrogen substitution treatments in a sweet maize farmland in South China[J]. Plants, 2022, 11(17): 2194 DOI:10.3390/plants11172194 (  0) 0) |
| [24] |
Zhang H Q, Zhao X Q, Shi Y, et al. Changes in soil bacterial communities with increasing distance from maize roots affected by ammonium and nitrate additions[J]. Geoderma, 2021, 398: 115102 DOI:10.1016/j.geoderma.2021.115102 (  0) 0) |
| [25] |
Jindo K, Audette Y, Olivares F L, et al. Biotic and abiotic effects of soil organic matter on the phytoavailable phosphorus in soils: A review[J]. Chemical and Biological Technologies in Agriculture, 2023, 10(1): 29 (  0) 0) |
| [26] |
Doran J W, Jones A J, Arshad M A, et al. Determinants of soil quality and health[M]. Soil quality and soil erosion. Boca Raton: CRC Press, 1999: 17-36.
(  0) 0) |
| [27] |
杨志远, 徐灵颖, 续勇波, 等. 土壤pH和有机物料碳氮比对强还原处理去除设施土壤硝酸盐效果和途径的影响[J]. 土壤, 2025, 57(1): 24-34 DOI:10.13758/j.cnki.tr.2025.01.004 (  0) 0) |
| [28] |
Tan Y Q, Yang Y, Shen X, et al. Multiple cyclic nucleotide-gated channels function as ABA-activated Ca2+ channels required for ABA-induced stomatal closure in Arabidopsis[J]. The Plant Cell, 2023, 35(1): 239-259 DOI:10.1093/plcell/koac274 (  0) 0) |
| [29] |
Terzaghi M, De Tullio M C. The perils of planning strategies to increase vitamin C content in plants: Beyond the hype[J]. Frontiers in Plant Science, 2022, 13: 1096549 DOI:10.3389/fpls.2022.1096549 (  0) 0) |
| [30] |
张睿含, 智燕彩, 贾明昊, 等. 生物质废弃物类型和水热pH对人工腐殖酸性能影响[J]. 生态环境学报, 2023, 32(8): 1496-1506 (  0) 0) |
| [31] |
Nebbioso A, Piccolo A. Advances in humeomics: Enhanced structural identification of humic molecules after size fractionation of a soil humic acid[J]. Analytica Chimica Acta, 2012, 720: 77-90 (  0) 0) |
| [32] |
魏世平, 吴萌, 李朋发, 等. 腐殖酸对花生连作地土壤真菌群落结构的影响[J]. 土壤学报, 2023, 60(3): 846-856 (  0) 0) |
| [33] |
Trevisan S, Pizzeghello D, Ruperti B, et al. Humic substances induce lateral root formation and expression of the early auxin-responsive IAA19 gene and DR5 synthetic element in Arabidopsis[J]. Plant Biology, 2010, 12(4): 604-614 (  0) 0) |
| [34] |
Muscolo A, Panuccio M R, Sidari M, et al. Alteration of amino acid metabolism by humic substances during germination of Pinus laricio seeds[J]. Seed Science and Technology, 2002, 30: 205-210 (  0) 0) |
| [35] |
Zhi Y C, Li X N, Wang X W, et al. Photosynthesis promotion mechanisms of artificial humic acid depend on plant types: A hydroponic study on C3 and C4 plants[J]. Science of the Total Environment, 2024, 917: 170404 DOI:10.1016/j.scitotenv.2024.170404 (  0) 0) |
2. Institute of Environmental Processes and Pollution Control, Jiangnan University, Wuxi, Jiangsu 214122, China
 2026, Vol. 58
2026, Vol. 58


