2. 湿润亚热带生态地理过程教育部重点实验室, 福州 350117
在全球范围内,森林生态系统储存了约60% 的陆地碳[1],其土壤碳库约占全球土壤碳储量的45%[2]。森林土壤有机碳的存储、稳定与矿化过程对全球碳平衡具有重要影响,是生态系统碳循环的关键环节;同时,有机质分解释放的CO2和养分[3]也与全球气候变化及土壤肥力密切相关。土壤同样是森林生态系统中重要的氮库[4],其中有机氮占土壤全氮90% 以上[5],在氮循环中发挥核心作用,经矿化后可被植物吸收利用[5-6]。因此,维持并提高森林土壤碳、氮储量对生态系统的可持续性具有重要意义。
森林凋落物包括地上部分(如枝叶、花果和粗木质残体)和地下部分(如根系残体、根系分泌物、土壤动物及微生物残体与分泌物)[7]。凋落物分解是土壤碳、氮及其他养分归还的重要途径[8-9],实现了养分从地上向地下的转移[10-11],是连接植物与土壤物质循环和能量流动的纽带[12]。叶凋落物与根凋落物在化学组成上存在明显差异:叶凋落物通常碳氮比较低,分解较快[13];而根凋落物则含有较多酸不溶物、缩合单宁等难降解有机成分[14]。已有研究表明,去除凋落叶和根系会降低土壤有机碳(SOC)含量[15-16],而添加凋落物则提高SOC含量[16]。添加根系分泌物可显著提升土壤可溶性有机氮(DON)含量[17],其分泌的酸性化合物还能刺激微生物活性,间接促进碳矿化[18]。此外,根系分泌物的输入增强土壤氮矿化过程[17],去除根系一年后可能导致土壤有机质损失24%、全氮损失14%[19]。添加凋落叶(如马尾松、火力楠和枫香)虽可提高SOC矿化量和累积矿化量[20],但也可能对SOC积累产生负效应[21]。目前,关于叶与根凋落物对SOC贡献的研究结论尚不一致,有学者认为根系凋落物对SOC积累贡献更大[22],也有研究显示叶凋落物的贡献更为显著[15]。因此,需从输入动态和稳定性机制两方面深入探讨凋落物对森林土壤碳、氮的影响。
不同林型凋落物质量存在显著差异[8],叶与根的作用也因林型而异。研究表明,在阔叶林中去除凋落叶对SOC含量的降低效应大于去除活根,而在针叶林中去除活根的影响更显著[16]。与阔叶林相比,针叶林凋落叶具有更高的碳、木质素、纤维素、总酚和缩合单宁含量[23],导致其分解和养分归还效率较低。阔叶林凋落物通常分解更快,养分释放率更高[24]。林型差异还体现在根系分泌物组成上,针叶林(如云杉、冷杉)根系分泌物中醇类含量较高,而有机酸、糖醇等化合物含量低于阔叶林(如白桦、红桦)[25]。凋落物分解不同阶段输入土壤的物质也存在差异,前期以易分解的低分子化合物为主,后期则以木质素、酚类等难降解物质为主[26]。然而,现有研究多聚焦于凋落物整体隔离或添加对土壤的影响,较少关注不同分解时期输入对土壤碳、氮动态的具体作用。
基于此,本研究以福建建瓯万木林保护区的针叶林与阔叶林为研究对象,通过野外控制试验探讨隔离新鲜凋落叶与根系对土壤碳、氮含量及组分的影响,并结合室内培养试验分析叶、根凋落物在土壤碳、氮稳定性方面的作用,以深化对森林生态系统土壤碳、氮转化机制的理解,并为相关研究提供理论依据。
1 材料与方法 1.1 研究区域概况研究区位于福建省建瓯市房道镇万木林保护区(27°03′N,118°09′E)。该地区属于中亚热带季风气候,年均气温18.8 ℃,年均降水量1 673 mm。地貌类型为东南低山丘陵,地带性土壤为红壤和黄壤。
样地概况:①阔叶林(天然浙江桂林),坡向330°,坡度20°,海拔390 m,林龄166 a,胸径36.4 cm,树高26 m。乔木层中浙江天竺桂(Cinnamomum chekiangense)占绝对优势,假蚊母树(Distyliopsis dunnii)次之。灌木层较稀疏,草本层不发达。②针叶林(人工杉木林),坡向300°,坡度11°~15°,海拔390 m,林龄27 a,胸径18.3 cm,树高18 m,为杉木(Cunninghamia lanceolata)幼苗造林形成的人工林,树种单一,林分结构简单。灌木层以杜茎山(Maesa japonica)、狗骨柴(Woodwardia japonica)为主。草本有狗脊蕨(Woodwardia japonicd)、草珊瑚(Sarcandra glabra)等。
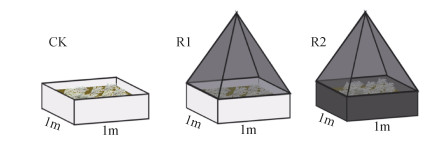
1.2 样地布置样地布置时间为2018年7月20日,在天然阔叶林(浙江天竺桂)和人工针叶林(杉木)中分别设置9个样方(3种处理,每个处理3个重复),每个样方由PVC板围成,大小为1 m × 1 m。对照(CK)不采取任何隔离凋落物措施;R1为去除新鲜凋落叶,用60目尼龙网将地上凋落物与样地土壤隔离,确保没有凋落叶进入样方内,每年5月份将样方外处于分解后期的凋落叶洒入样方内,且每年选取样方外不同方位的凋落叶,确保没有新鲜凋落叶进入样方内;R2为去除新鲜凋落叶和根系,在R1的基础上将400目尼龙网沿着PVC板打入土中,深度为60 cm,阻止外界根系进入。样地具体布置见图 1。
|
图 1 样地示意图 Fig. 1 Sample plot diagram |
采样时间为2024年7月24日,采样时将土壤表面的凋落物轻轻扫开,用小铲子挖取样方内表层土壤(0~15 cm),共采集2(林型)×3(处理)×3(重复)=18个土样。土样带回后进行挑除石头、根系及凋落物处理,取一部分过4 mm筛进行室内培养试验,其余风干后过2 mm及100目筛,待测。
1.4 室内培养试验对野外试验土样进行室内培养,研究处理对土壤碳、氮稳定性的影响。将过筛的18个土样进行称重装瓶,每个土样称取5份,每份50 g (以干质量计),分别装入250 mL培养瓶,并用去离子水调节土壤水分含量为饱和持水量(WHC) 的60%,再用锡纸封口,在锡纸上钻5个小孔(以保证氧气供应),置于25 ℃恒温箱黑暗培养。培养期间每3 d称重,用去离子水补充水分,保持土壤含水量相对稳定。
在培养后第0、15、60、120、240天进行破坏性取样,测定土壤可溶性氮和可溶性有机碳;在培养后第0、2、4、6、8、12、16、20、24、30、36、42、48、63、78、93、123、153、183、240天进行气体取样。气体取样步骤:在每次取样前3 h,将培养瓶取出置于空旷场地通风(为帮助空气充分混入,同时用50 mL注射器向瓶内注射3次新鲜空气,使瓶内原有气体排出),用注射器抽取3个20 mL的新鲜空气样本作为空白值对照后,拧紧瓶盖,放入培养箱继续避光培养3 h。3 h后拿出培养瓶进行顶空取样抽气,取20 mL气体装入提前抽真空的气瓶中,待测CO2、N2O浓度。抽气结束后把密闭的培养瓶打开,继续放入培养箱培养。
1.5 测定项目与方法 1.5.1 土壤基本理化性质土壤含水量采用烘干法测定;土壤pH采用玻璃电极法(水土质量比为2.5∶1)测定;土壤全碳(TC)、全氮(TN)采用过100目筛的土样直接元素分析仪(Elementar Vario MAX CN,德国)测定;土壤总酚采用NaOH溶液浸提–福林酚比色法测定[27];土壤易氧化有机碳(Easily- oxidized organic carbon,EOC)采用高锰酸钾氧化–比色法[28]测定。
土壤可溶性氮和可溶性有机碳浸提:称取8 g土样置于50 mL离心管中,加入40 mL 0.5 mol/L K2SO4溶液,经1 h充分振荡(250 r/min),离心10 min(4 000 r/min),0.45 μm滤膜过滤得到浸提液。浸提液土壤可溶性氮(可溶性总氮(TDN)、NH4+-N、NO3–-N)采用连续流动分析仪(SKALAR San Classic,荷兰)测定;可溶性有机碳(DOC)采用总有机碳分析仪(岛津/TOC–L CPH,日本)测定;芳香性指数(Aromatic index,AI)采用紫外分光光度计测吸光度进行计算[29]。
| $ \text { 土壤矿质氮含量 }=\mathrm{NO}_3^{-}-\mathrm{N} \text { 含量 }+\mathrm{NH}_4^{+}-\mathrm{N} \text { 含量 } $ | (1) |
| $ \quad可溶性有机氮({\rm{DON}})=可溶性总氮({\rm{TDN}})–矿质氮 \\ 矿质氮 $ | (2) |
| $ \quad净氮硝化速率 =(培养后 \mathrm{NO}_3^{-}-\mathrm{N} 含量-培养前 \\ \mathrm{NO}_3^{-}-\mathrm{N} 含量)/培养时间 $ | (3) |
| $ \quad净氮矿化速率 =(培养后矿质氮含量 - 培养前矿质\\ 氮含量)/培养时间 $ | (4) |
| $ \text { 芳香性指数 } \mathrm{AI}(\mathrm{~L} /(\mathrm{m} \cdot \mathrm{mg}))=\left(\mathrm{UV}_{254} / C_{\mathrm{DOC}}\right) \times 100 $ | (5) |
式中:UV254为紫外分光光度计254 nm处的吸光度值(cm–1);CDOC为DOC溶液的浓度值(mg/L)。
| $ \text { 土壤易氧化有机碳 } \mathrm{EOC}=\frac{C \times V \times 250 \times 9}{M \times 1000}$ | (6) |
式中:C为KMnO4浓度变化值(mmol/L);V为KMnO4用量(mL);250为稀释倍数;9为每消耗1 mmol KMnO4溶液相当于氧化9 mg碳;M为烘干土的质量(g)。
| $ 叶前期\text{EOC}占比=\frac{{\text{EOC}}_{\text{CK}}-{\text{EOC}}_{\text{R}1}}{{\text{EOC}}_{\text{CK}}} $ | (7) |
| $ 根\text{EOC}占比=\frac{{\text{EOC}}_{\text{R}1}-{\text{EOC}}_{\text{R}2}}{{\text{EOC}}_{\text{CK}}} $ | (8) |
| $ 叶后期\text{EOC}占比=\frac{{\text{EOC}}_{\text{R}2}}{{\text{EOC}}_{\text{CK}}} $ | (9) |
气体CO2、N2O浓度采用气相色谱仪(岛津,SHIMADZ GC2010 Pro,日本)测定。
气体排放速率计算公式[30]:
| $ F = k \times \frac{V}{m} \times \frac{{{\text{d}}c}}{{{\text{d}}t}} \times \frac{{273}}{{273 + T}} $ | (10) |
式中:F表示气体产生速率(mg/(kg·d));k为常数,N2O取1.964 μg/μL,CO2取1.977 μg/μL;V是培养瓶体积(L);m为干土重(kg);dc/dt为气体在观测时间内浓度随时间变化的直线斜率(μL/(L·d));T为培养温度(℃)。
气体累积排放量计算公式[30]:
| $ CE =\mathop \sum \limits_{i = 1}^n F \times \Delta t $ | (11) |
式中:CE为气体累积排放量(mg/kg);F为气体排放速率(mg/(kg·d));
数据采用SPSS 16.0和Excel软件进行分析。采用单因素方差分析(ANOVA)检验不同林型和凋落物处理之间的差异显著性,所有数据均为3个重复的平均值±标准误。使用Origin 2021软件绘图。
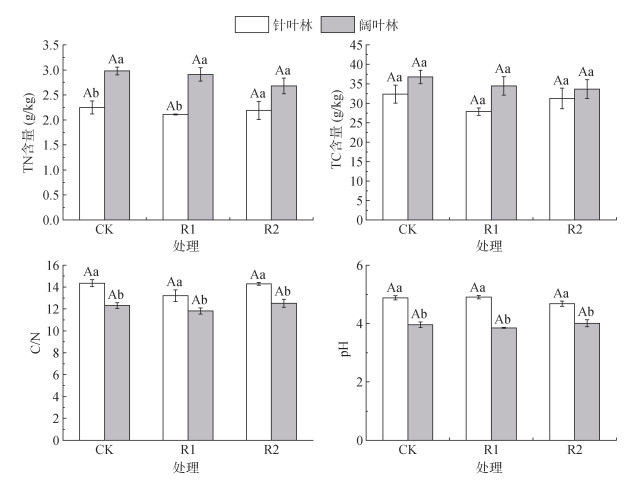
2 结果与分析 2.1 叶和根凋落物处理对针阔叶林碳氮的影响不同凋落物处理对土壤全碳(TC)、全氮(TN)、碳氮比(C/N)及pH均无显著影响,但林型间各项指标差异显著(图 2)。在针叶林中,TC与TN含量均表现为CK > R2 > R1,其中R1处理较CK分别下降13.96% 和6.36%,R2处理降幅分别为3.49% 和2.96%。而在阔叶林中,TC与TN表现为CK > R1 > R2,R1处理较CK降幅分别为6.31% 和2.35%,R2处理降幅为8.55% 和10.06%。林型间比较显示,针叶林CK和R1处理的TN含量分别比阔叶林显著降低24.47% 和27.57%(P < 0.05);阔叶林各处理的C/N均显著低于针叶林,CK、R1、R2处理降幅分别为16.59%、11.87% 和14.10%;其pH也显著低于针叶林,降幅分别为23.04%、27.16% 和16.89%。
|
(柱图上方大写字母不同表示同一林型不同处理间差异显著(P < 0.05),小写字母不同表示同一处理不同林型间差异显著(P < 0.05),下同) 图 2 不同凋落物处理下针阔叶林土壤基本理化性质 Fig. 2 Soil basic physicochemical properties of coniferous and broad-leaved forests under different litter treatments |
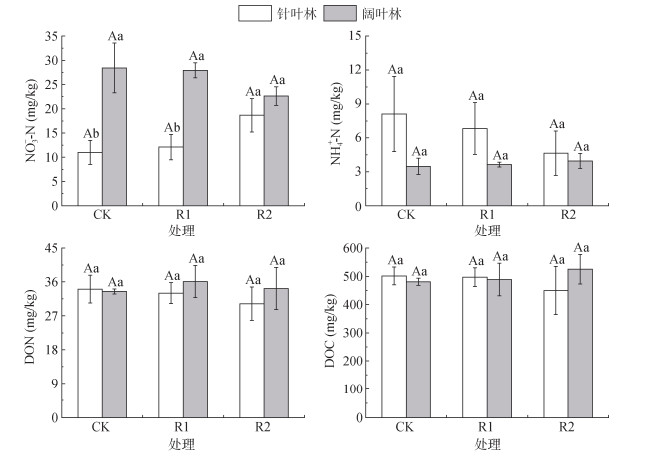
尽管处理间土壤可溶性组分无显著差异,但仍存在一定的变化趋势(图 3)。针叶林中,NH4+-N、可溶性有机氮(DON)和可溶性有机碳(DOC)含量均为CK > R1 > R2,其中R1和R2处理的NH4+-N较CK分别下降15.80% 和42.75%,DON下降3.14% 和11.37%,DOC下降0.83% 和10.30%;相反,NO3–-N在R2和R1处理中分别较CK提高69.63% 和10.08%。阔叶林中NO3–-N表现为CK > R1 > R2,R1和R2较CK分别下降1.75% 和20.46%;而NH4+-N和DOC表现为R2 > R1 > CK,与CK相比,R2和R1处理NH4+-N增幅分别为13.70% 和4.37%,DOC增幅为9.29% 和1.74%;DON则表现为R1 > R2 > CK,在R1和R2中分别较CK提高7.80% 和2.23%。林型间比较显示,阔叶林各处理的NO3–-高于针叶林,CK、R1、R2处理增幅分别为61.29%、56.62% 和17.43%;CK、R1、R2处理下,针叶林NH4+-N含量分别比阔叶林高132.87%、87.87% 和17.26%;DON含量则表现为针叶林CK处理略高于阔叶林(1.84%),而R1和R2处理则分别比阔叶林低8.49% 和11.71%;针叶林DOC含量在CK和R1处理中分别比阔叶林高4.32% 和1.68%,而R2处理则比阔叶林降低14.38%。
|
图 3 不同凋落物处理下针阔叶林土壤可溶性氮和可溶性有机碳含量 Fig. 3 Soil soluble nitrogen and soluble organic carbon contents in coniferous and broad-leaved forests under different litter treatments |
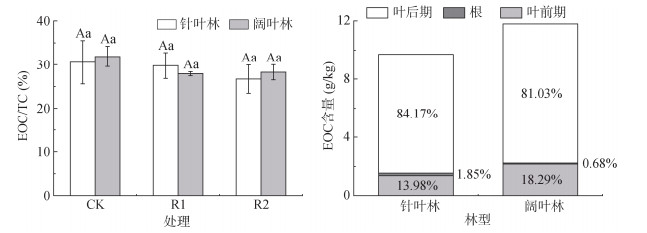
易氧化有机碳(EOC)与TC比值(EOC/TC) 在处理间变化较小(图 4)。针叶林中,R1处理的EOC/TC略低于CK (0.74%),R2则比CK降低3.83%;阔叶林中,R1和R2处理分别较CK降低3.99% 和3.65%。针阔叶林中的EOC均主要来源于凋落叶分解后期,其在针叶林和阔叶林中的贡献率分别为84.17% 和81.03%,而凋落叶前期的贡献率分别为13.98% 和18.29%。
|
图 4 不同凋落物处理下针阔叶林土壤易氧化有机碳含量及占比 Fig. 4 Soil easily-oxidized organic carbon contents and proportions in coniferous and broad-leaved forests under different litter treatments |
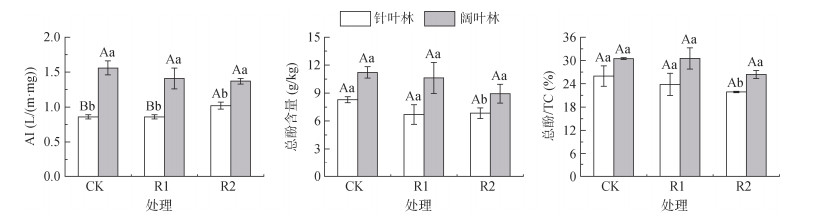
芳香性指数(AI)和总酚含量在处理和林型间表现不同(图 5)。针叶林中,R2处理的AI较CK显著提高19.27%,R1与CK接近;阔叶林中R1和R2的AI分别下降10.00% 和12.56%。针叶林各处理的AI均显著低于阔叶林,CK、R1、R2降幅分别为45.27%、39.22% 和25.38%。总酚含量在针叶林中表现为R1和R2处理分别较CK降低19.28% 和17.45%,阔叶林中R1和R2分别降低5.29% 和20.47%。针叶林总酚含量均低于阔叶林,CK、R1、R2降幅分别为26.17%、37.08% 和23.36%。总酚占TC的比例在针叶林CK、R1、R2处理中分别为25.97%、23.81% 和21.90%,阔叶林中分别为30.49%、30.51% 和26.39%。
|
图 5 不同凋落物处理下针阔叶林土壤芳香性指数、总酚含量和总酚占全碳比 Fig. 5 Soil aromatic indexes, total phenolic contents and total phenol to total carbon ratios in coniferous and broad-leaved forests under different litter treatments |
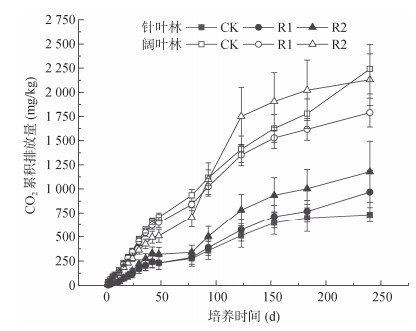
培养期间土壤CO2累积排放量持续上升(图 6)。0~50 d各处理排放量迅速增加,针叶林中表现为R2 > R1 > CK,阔叶林中为CK > R1 > R2;50~75 d增速减缓;75~125 d针叶林所有处理排放量再次显著上升直至培养结束,阔叶林中R2处理排放量超过R1和CK,且在175~240 d CK处理排放重新加快。培养240 d后,针叶林R1和R2处理排放量较CK分别提高32.42% 和46.46%,阔叶林R1和R2处理则分别下降20.08% 和6.11%;阔叶林整体的累积排放量均高于针叶林。
|
图 6 不同凋落物处理下针阔叶林土壤CO2累积排放量 Fig. 6 Soil cumulative emissions of CO2 in coniferous and broad-leaved forests under different litter treatments |
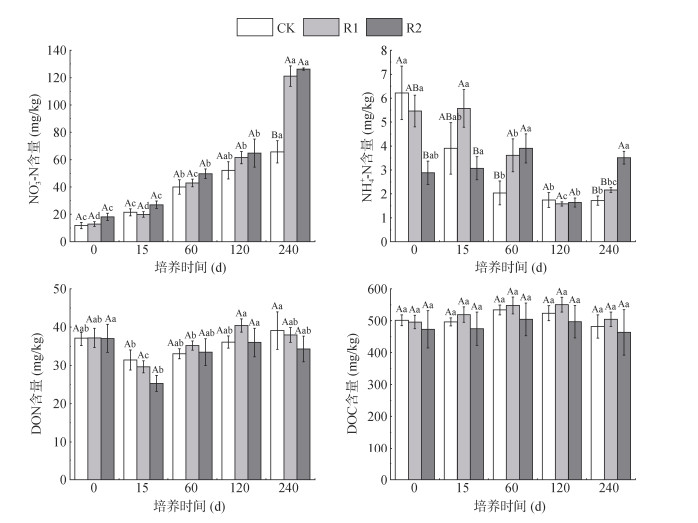
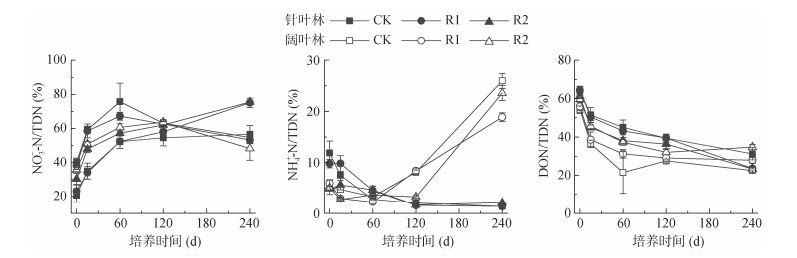
可溶性氮组分在培养过程中发生显著动态变化(图 7~图 9)。初始阶段DON占TDN约60%,其后比例逐渐下降。针叶林NO3–-N自第60天起持续上升,至第240天时,R1和R2处理含量显著高于CK,增幅分别为84.24% 和91.99%,NO3–-N占比也达到最高。NH4+-N在第60天时CK和R1较初始显著下降67.22% 和33.75%,第120天时R1继续下降66.14%,R2下降40.57%,其占比持续降低。尽管初始时R2处理NH4+-N含量显著低于CK和R1,但第240天时R1和R2反超CK,分别高出26.09% 和104.43%。DON在第15天降至最低(降幅15.30%~31.75%),后期回升,至第240天时与初始时无显著差异。
|
(柱图上方大写字母不同表示同一培养时间不同处理间差异显著(P < 0.05),小写字母不同表示同一处理不同培养时间差异显著(P < 0.05)。下同) 图 7 不同凋落物处理下针叶林土壤可溶性氮和可溶性有机碳含量 Fig. 7 Soil soluble nitrogen and soluble organic carbon contents in coniferous forests under different litter treatments |
|
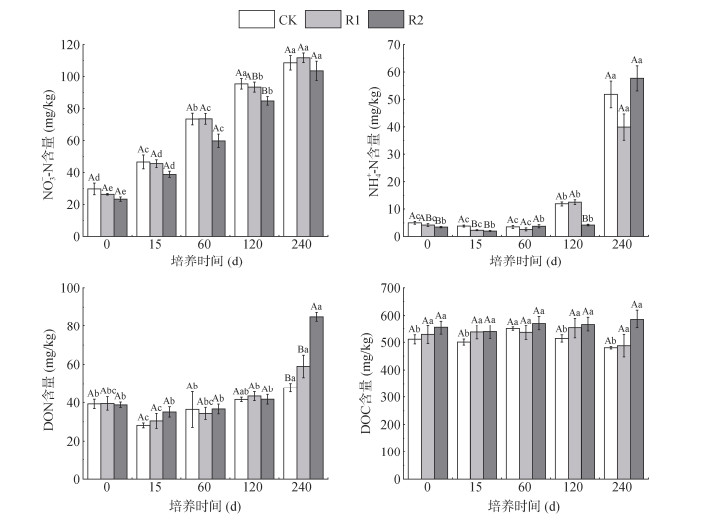
图 8 不同凋落物处理下阔叶林土壤可溶性氮和可溶性有机碳含量 Fig. 8 Soil soluble nitrogen and soluble organic carbon contents in broad-leaved forests under different litter treatments |
|
图 9 不同凋落物处理下针阔叶林土壤NH4+-N、NO3–-N和DON在可溶性总氮中的占比 Fig. 9 Proportions of NH4+-N, NO3–-N and DON in total dissolved nitrogen in coniferous and broad-leaved forests under different litter treatments |
阔叶林NO3–-N自第15天起持续上升;NH4+-N在第120天时CK和R1显著上升(139.20% 和198.65%),第240天时大幅增加,其占比在第120天后突增,NO3–-N占比则下降。DON在第15天显著下降(如CK下降28.31%),后期回升,第240天时所有处理DON含量均显著高于初始,R1和R2处理分别较CK高23.36% 和78.07%。整个培养过程中土壤DOC含量无显著变化,针阔叶林间也无差异,均维持在500 mg/kg左右。
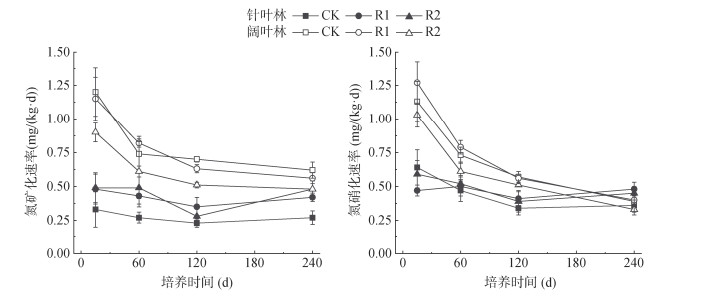
净氮矿化速率与硝化速率因林型而异(图 10)。针叶林两者均呈先降后升趋势,除第60天R2处理矿化速率显著高于CK(80.26%)外,处理间无显著差异;R1和R2处理氮矿化速率总体高于CK,增幅为22.87%~80.26%。阔叶林两者在0~15 d最高,之后持续下降,处理间无显著差异,120~240 d进一步下降45.98%~51.34%(矿化)和65.38%~68.84%(硝化)。
|
图 10 不同凋落物处理下针阔叶林土壤净氮矿化和净硝化速率 Fig. 10 Soil net nitrogen mineralization and nitrification rates in coniferous and broad-leaved forests under different litter treatments |
凋落物是土壤碳、氮的重要来源,其自然输入是维持土壤TC、TN储量的关键[23, 31]。本研究中,去除凋落物处理降低了针叶林与阔叶林的土壤TC和TN含量,这与在杉木[15]、米槠[32]和针阔叶林[33]中的研究发现一致。但也有研究表明,短期(如1年)去除凋落物可能改变土壤水热条件,加速表层原有有机质分解,反而短期内增加土壤TC含量[31],这凸显了研究时长对结果的重要影响。
通常,针叶林凋落物质量较低、C/N较高、分解缓慢,易在表层积累[34];而阔叶林凋落物质量较高、C/N较低、分解较快,更利于土壤碳、氮积累[34]。因此,阔叶林土壤具有比针叶林更高的碳、氮含量[35],本研究结果(阔叶林 > 针叶林)符合这一规律。值得注意的是,不同处理对两种林型的影响程度存在差异。本研究发现,针叶林中去除新鲜凋落叶(R1处理)对TC的降低效应最大,而阔叶林中去除新鲜凋落叶和根系(R2处理)对TN的降低程度最为显著。彭思瑞等[15]的长期试验也发现,杉木凋落叶去除对TC的负效应大于根系去除;Wu等[16]报道,阔叶林去除凋落叶对TC的降低幅度大于去除活性根系。
在活性有机碳、氮组分方面,3种处理间的DOC和DON含量无显著差异。这可能意味着,在试验期间,凋落叶分解前期的物质输入与根系输入对DOC和DON的贡献差异不显著,或根系的贡献小于凋落叶分解后期释放的物质。EOC易被微生物利用[36],土壤EOC/TC比值越高,表明土壤中碳活性越高,稳定性越差[37],本研究中针阔叶林中去除凋落物均降低了EOC/TC的比值。针叶林R2处理的土壤EOC/TC比值低,表明其土壤中的碳活性最低,稳定性最高。根组织有较高的化学抗性[14],而木栓质作为根的生物标志物[38],其含量与EOC/TC呈正相关,去除根系使得EOC/TC比值降低,对土壤有机碳的稳定性有积极影响[39]。研究表明,根系排除会降低针叶林土壤稳定有机碳含量[40],但R2处理在隔绝根系分泌物输入的同时,仅保留了凋落物分解后期的物质,可能导致土壤活性碳输入也减少,促使微生物转而分解土壤中原有的、更稳定的有机质[41],导致矿化量上升,并因养分有效性降低而抑制了对芳香类化合物的分解,可能提高了有机质的芳香性指数。
相比之下,阔叶林凋落物更易分解、养分含量高[34],因此去除凋落物处理对降低土壤DOC的效果较弱。阔叶林R1处理的EOC/TC比值最低,表明土壤碳稳定性最高,其可溶性有机质矿化较慢,有利于DOC和DON的积累。微生物通常优先分解高质量的凋落物[42],这可能降低了EOC的含量。此外,阔叶林土壤细菌多样性更高,更能有效分解易分解有机质[43]。
根系对土壤碳、氮循环的影响尤为关键。研究表明,与凋落叶相比,根系对土壤酶活性的影响更为显著[44],并具有促进碳、氮矿化的作用[17, 45]。这一机制很好地解释了为何在针叶林中,R2处理的TC和TN含量反而高于R1处理:因为隔离根系消除了其促进矿化的作用,减缓了有机质的分解损耗,从而导致测得的碳、氮含量相对偏高。同时,菌根真菌也被隔离,而菌丝碳输入对土壤氮矿化有重要贡献[46]。此外,两种林型根系的分布策略不同[47]及其分泌物的差异(如阔叶林根系分泌物更利于固氮菌活动)[48],共同导致R2处理对阔叶林土壤TN的影响尤为突出。
3.2 针阔叶林不同凋落物处理对土壤矿化的影响本研究中,针叶林去除凋落物处理增加了土壤有机碳的累积矿化量,这与杨轶晗等[49]在樟子松林中的研究发现一致。移除凋落叶和根系等易利用碳源,会降低微生物的碳利用效率[50],迫使微生物转而分解土壤中原本更难分解的有机质,从而促进CO2排放[51]。特别是对于针叶林,其低质量凋落物能诱导更强的正激发效应[52],因此去除新鲜凋落叶(R1处理)对土壤碳库的激发潜力更大,这可能是导致其土壤TC降低的主要原因。去除新鲜凋落叶和根系(R2处理)DOC的芳香性指数显著高于CK和R1(图 5),可能会抑制碳矿化[53],但是由于缺少根系的影响[54],土壤总酚含量及其在TC中所占比例在R2处理最低,有利于碳矿化。因此,综合表现为室内培养试验中R2的CO2累积排放量最高(图 6)。培养试验表明,在缺乏凋落物碳氮输入的情况下,土壤碳矿化有增加的潜力,不利于土壤碳保存,这与Zhu等[55]2年试验研究结果相似,凸显针叶林凋落物归还对维持土壤TC储量的重要性。
与碳矿化相比,不同处理对土壤氮矿化的净影响在培养试验中并不显著。培养过程中针叶林土壤NH4+-N一直处于较低水平,说明以硝化作用为主;随着培养时间延长,NO3–-N/TDN持续上升、DON/ TDN持续降低(图 9),表明针叶林土壤净氮硝化维持很长时间(图 10)。但这可能源于培养试验本身的条件:作为一个封闭系统,硝化作用产生的NO3–-N无法通过植物吸收或淋溶损失,导致其持续积累,掩盖了真实的矿化速率。结合野外取样数据(R2处理NO3–-N含量最高)分析,可能在原位环境下,R2处理对土壤氮库的影响小于对碳库的影响。培养试验中R2处理土壤CO2累积排放量最高,表明其碳消耗增加,活性碳含量减少,而活性碳能促进土壤氮固定[56],因此在缺少碳输入条件下,不利于土壤NO3–-N固定。然而,在野外一旦植物根系对氮的吸收降低,土壤NO3–-N就存在淋溶损失的风险。
阔叶林土壤有机碳的累积矿化量总体高于针叶林,这与徐天懂等[57]的发现一致,通常归因于其更高的酶活性(如酸性磷酸酶、脲酶、过氧化物酶),这些酶能有效驱动有机质分解和氮素转化。本研究还观察到处理间矿化过程的动态差异:在培养前期(50 d内),阔叶林R1和R2处理的CO2累积排放量均低于CK,其中R2最低,这与其较低的EOC/TC比值所指示的惰性碳库特征相符,短期内土壤中可被微生物利用的活性碳较少,使得矿化受到抑制;然而在后期(75~125 d),R2处理的矿化量快速上升并超过其他处理。这表明隔绝根系输入后,土壤有机质的分解过程发生了显著改变,即土壤碳的稳定性不会持久,微生物会通过调整代谢策略分解稳定碳库,使得矿化量补偿上升。Men等[44]的研究为这一现象提供了机理解释:凋落物去除显著提高了碳氧化酶活性,这可能增加了DOC的产生但暂时抑制了其矿化;而根系去除则可能通过改变微生物群落和酶活性,延迟了土壤碳的矿化过程。
尽管野外取样表明R2处理对阔叶林TN的降低效应最大,但其室内培养的氮矿化速率却最低。凋落物去除更可能是通过改变土壤微环境(温度、湿度、pH)来影响氨氧化微生物的活性,进而调控硝化–反硝化过程[58]。此外,阔叶林根际富集固氮菌,固氮菌在分解有机氮产生NH4+-N后,会优先将其同化到自身生物量中,转化为微生物生物量氮,而不是直接释放到环境中。这种“固持作用”在短期内降低了可直接检测的无机氮含量,形成抑制氮矿化的“假象”,但长期可通过微生物残体分解缓慢释放氮,维持稳定的氮矿化,避免无机氮因淋溶或反硝化损失[59],同时也促进了有机无机复合体的形成,增强了碳的稳定性。室内培养试验后期大量NH4+-N和DON的累积,且氮矿化速率降低并趋于平缓,可能抑制了氮矿化,主要是抑制了净氮硝化,而在野外可能不存在这种抑制作用,导致TN降低。
综上所述,凋落物处理对氮矿化的影响因林型和处理方式而异,其核心机制在于改变了“微生物–酶–底物”之间的互作关系。凋落叶作为关键的有机氮输入源,其去除直接减少了氮矿化的底物供应[60-61]。根系则通过分泌物(如有机酸、萜类)和根际酶活性(如脲酶)深刻调控微生物活性和氮转化过程[59, 62],根系去除削弱了这一调控能力。凋落叶和根系的化学组成(如C/N)决定了矿化的方向。针叶林凋落叶C/N高,去除后对氮矿化底物影响较小,且其根系分泌物可能抑制硝化菌[62],因此,根去除后反而可能因解除抑制而增加净硝化速率。相反,阔叶林凋落叶C/N低,是土壤氮的主要来源,其去除直接削减了氮底物库。同时,阔叶林丰富的根系分泌物和细根生物量[59]能促进固氮和矿化相关的微生物活动,其去除对氮库的负面影响更大。值得注意的是,根系在加速碳矿化的同时,其输入的多酚等物质(如单宁)也可通过与有机氮或矿物质结合,形成稳定的复合物[19],从而在长期尺度上增强碳、氮的稳定性,形成一个复杂的“分解–稳定”动态平衡。因此,根系去除的净效应是打破这一平衡的关键,对土壤碳、氮的稳定性有重要影响。
4 结论本研究揭示了凋落物输入对维持森林土壤碳、氮库的关键作用,并阐明了叶和根在不同林型中的独特功能。去除新鲜凋落叶和根系降低了土壤全碳和全氮含量,但其影响程度因林型和处理方式而异:针叶林土壤碳库对凋落叶去除更敏感,而阔叶林土壤氮库对根系去除响应更为显著。本研究强调了在森林管理中,对于针叶林需重点关注凋落叶归还,而对于阔叶林则需重视根系功能的保护,以实现土壤碳、氮库的长期固存。
| [1] |
McKinley D C, Ryan M G, Birdsey R A, et al. A synthesis of current knowledge on forests and carbon storage in the United States[J]. Ecological Applications, 2011, 21(6): 1902-1924 DOI:10.1890/10-0697.1 (  0) 0) |
| [2] |
Schimel. Ecological controls over global soil carbon storage[J]. Bulletin of the Ecological Society of America, 1995, 76: 384-385 (  0) 0) |
| [3] |
曹亚鑫, 程曼, 文永莉. 芦芽山不同植被类型下土壤有机碳矿化特征及其对铁添加的响应[J]. 应用与环境生物学报, 2024, 30(1): 18-25 (  0) 0) |
| [4] |
Gurmesa G A, Lu X K, Gundersen P, et al. High retention of 15N-labeled nitrogen deposition in a nitrogen saturated old-growth tropical forest[J]. Global Change Biology, 2016, 22(11): 3608-3620 DOI:10.1111/gcb.13327 (  0) 0) |
| [5] |
Bingham A H, Cotrufo M F. Organic nitrogen storage in mineral soil: Implications for policy and management[J]. Science of the Total Environment, 2016, 551/552: 116-126 DOI:10.1016/j.scitotenv.2016.02.020 (  0) 0) |
| [6] |
Hurisso T T, Moebius-Clune D J, Culman S W, et al. Soil protein as a rapid soil health indicator of potentially available organic nitrogen[J]. Agricultural & Environmental Letters, 2018, 3(1): 180006 (  0) 0) |
| [7] |
洪小敏, 魏强, 李梦娇, 等. 亚热带典型森林地上和地下凋落物输入对土壤新老有机碳动态平衡的影响[J]. 应用生态学报, 2021, 32(3): 825-835 (  0) 0) |
| [8] |
郭剑芬, 杨玉盛, 陈光水, 等. 森林凋落物分解研究进展[J]. 林业科学, 2006, 42(4): 93-100 (  0) 0) |
| [9] |
张悦, 张艺凡, 马怡波, 等. 森林生态系统凋落物分解影响因素研究进展[J]. 环境生态学, 2023, 5(4): 45-56 (  0) 0) |
| [10] |
Çakır M, Makineci E. Litter decomposition in pure and mixed Quercus and Fagus stands as influenced by arthropods in Belgrad Forest, Turkey[J]. Journal of Forestry Research, 2020, 31(4): 1123-1137 DOI:10.1007/s11676-019-00915-y (  0) 0) |
| [11] |
Farooq T H, Yan W D, Chen X Y, et al. Dynamics of canopy development of Cunninghamia lanceolata mid-age plantation in relation to foliar nitrogen and soil quality influenced by stand density[J]. Global Ecology and Conservation, 2020, 24: e01209 DOI:10.1016/j.gecco.2020.e01209 (  0) 0) |
| [12] |
Wang H, Liu S R, Wang J X, et al. Mixed-species plantation with Pinus massoniana and Castanopsis hystrix accelerates C loss in recalcitrant coniferous litter but slows C loss in labile broadleaf litter in Southern China[J]. Forest Ecology and Management, 2018, 422: 207-213 DOI:10.1016/j.foreco.2018.04.024 (  0) 0) |
| [13] |
Sun T, Hobbie S E, Berg B, et al. Contrasting dynamics and trait controls in first-order root compared with leaf litter decomposition[J]. Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(41): 10392-10397 (  0) 0) |
| [14] |
Xia M X, Talhelm A F, Pregitzer K S. Fine roots are the dominant source of recalcitrant plant litter in sugar maple-dominated northern hardwood forests[J]. New Phytologist, 2015, 208(3): 715-726 DOI:10.1111/nph.13494 (  0) 0) |
| [15] |
彭思瑞, 张慧玲, 孙兆林, 等. 长期凋落物去除对亚热带杉木林土壤有机碳及其组分的影响[J]. 植物生态学报, 2024, 48(8): 1078-1088 (  0) 0) |
| [16] |
Wu Q X, Wu F Z, Zhu J J, et al. Leaf and root inputs additively contribute to soil organic carbon formation in various forest types[J]. Journal of Soils and Sediments, 2023, 23(3): 1135-1145 DOI:10.1007/s11368-022-03403-9 (  0) 0) |
| [17] |
Liu Y, Evans S E, Friesen M L, et al. Root exudates shift how N mineralization and N fixation contribute to the plant-available N supply in low fertility soils[J]. Soil Biology and Biochemistry, 2022, 165: 108541 DOI:10.1016/j.soilbio.2021.108541 (  0) 0) |
| [18] |
Liu Y H, Shahbaz M, Ge T D, et al. Effects of root exudate stoichiometry on CO2 emission from paddy soil[J]. European Journal of Soil Biology, 2020, 101: 103247 DOI:10.1016/j.ejsobi.2020.103247 (  0) 0) |
| [19] |
Adamczyk B, Sietiö O M, Straková P, et al. Plant roots increase both decomposition and stable organic matter formation in boreal forest soil[J]. Nature Communications, 2019, 10: 3982 DOI:10.1038/s41467-019-11993-1 (  0) 0) |
| [20] |
梅孔灿, 陈岳民, 范跃新, 等. 凋落叶和磷添加对马尾松林土壤碳激发效应的影响[J]. 土壤学报, 2022, 59(4): 1089-1099 (  0) 0) |
| [21] |
Wu J J, Zhang Q, Zhang D D, et al. The ratio of ligninase to cellulase increased with the reduction of plant detritus input in a coniferous forest in subtropical China[J]. Applied Soil Ecology, 2022, 170: 104269 DOI:10.1016/j.apsoil.2021.104269 (  0) 0) |
| [22] |
Mambelli S, Bird J A, Gleixner G, et al. Relative contribution of foliar and fine root pine litter to the molecular composition of soil organic matter after in situ degradation[J]. Organic Geochemistry, 2011, 42(9): 1099-1108 (  0) 0) |
| [23] |
Zhang X X, Wang B Y, Liu Z W. Impacts of plant secondary metabolites from conifer litter on the decomposition of Populus purdomii litter[J]. Journal of Forestry Research, 2019, 30(6): 2237-2245 DOI:10.1007/s11676-018-0766-7 (  0) 0) |
| [24] |
Farooq T H, Li Z W, Yan W D, et al. Variations in litterfall dynamics, C: N: P stoichiometry and associated nutrient return in pure and mixed stands of camphor tree and Masson pine forests[J]. Frontiers in Environmental Science, 2022, 10: 903039 DOI:10.3389/fenvs.2022.903039 (  0) 0) |
| [25] |
夏瑞雪, 刘佳, 赵文强, 等. 川西亚高山森林优势针阔树种根系分泌物的化学组分与含量差异[J]. 应用与环境生物学报, 2024, 30(1): 26-34 (  0) 0) |
| [26] |
Berg B, McClaugherty C. Plant litter: Decomposition, humus formation, carbon sequestration[M]. Berlin, Heidelberg: Springer, 2014.
(  0) 0) |
| [27] |
王米兰, 胡荣桂. 湖北省几种农业土壤中酚含量及其与碳氮的关系[J]. 农业环境科学学报, 2014, 33(4): 702-707 (  0) 0) |
| [28] |
Blair G J, Lefroy R, Lisle L. Soil carbon fractions based on their degree of oxidation, and the development of a carbon management index for agricultural systems[J]. Australian Journal of Agricultural Research, 1995, 46(7): 1459-1466 DOI:10.1071/AR9951459 (  0) 0) |
| [29] |
Weishaar J L, Aiken G R, Bergamaschi B A, et al. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J]. Environmental Science & Technology, 2003, 37(20): 4702-4708 (  0) 0) |
| [30] |
Cheng Y, Cai Z C, Chang S X, et al. Effects of soil pH and salt on N2O production in adjacent forest and grassland soils in central Alberta, Canada[J]. Journal of Soils and Sediments, 2013, 13(5): 863-868 DOI:10.1007/s11368-013-0663-9 (  0) 0) |
| [31] |
孙轲, 黎建强, 杨关吕, 等. 滇中高原云南松林枯落物输入对土壤碳氮储量及其分布格局的影响[J]. 生态学报, 2021, 41(8): 3100-3110 (  0) 0) |
| [32] |
张锦新, 涂凤兰, 许恩兰, 等. 凋落物输入量对米槠天然林土壤氮矿化的影响[J]. 生态学杂志, 2022, 41(10): 1916-1922 (  0) 0) |
| [33] |
Feng J G, He K Y, Zhang Q F, et al. Changes in plant inputs alter soil carbon and microbial communities in forest ecosystems[J]. Global Change Biology, 2022, 28(10): 3426-3440 DOI:10.1111/gcb.16107 (  0) 0) |
| [34] |
Chakravarty S, Rai P, Vineeta, et al. Litter production and decomposition in tropical forest[J]. Practice, Progress, and Proficiency in Sustainability, 2020, 193-212 (  0) 0) |
| [35] |
Wei C H, Wang Q, Ren M L, et al. Soil aggregation accounts for the mineral soil organic carbon and nitrogen accrual in broadleaved forests as compared to that of coniferous forests in Northeast China: Cross-sites and multiple species comparisons[J]. Land Degradation & Development, 2021, 32(1): 296-309 (  0) 0) |
| [36] |
漆良华, 杜满义, 范少辉, 等. 湘中丘陵区毛竹纯林、竹杉混交林土壤有机碳库动态[J]. 生态学杂志, 2012, 31(12): 3038-3043 (  0) 0) |
| [37] |
Yang Y, Liu S, Schindlbacher A, et al. Topsoil organic carbon increases but its stability declines after five years of reduced throughfall[J]. Soil Biology and Biochemistry, 2021, 156: 108221 DOI:10.1016/j.soilbio.2021.108221 (  0) 0) |
| [38] |
Feng X J, Simpson A J, Wilson K P, et al. Increased cuticular carbon sequestration and lignin oxidation in response to soil warming[J]. Nature Geoscience, 2008, 1(12): 836-839 DOI:10.1038/ngeo361 (  0) 0) |
| [39] |
叶晓丹, 刘世荣, 栾军伟, 等. 树种丰富度和组成对南亚热带人工林土壤植物源碳保存及有机碳稳定性的影响[J]. 生态学报, 2023, 43(12): 4974-4983 (  0) 0) |
| [40] |
Sun D S, Qiu X L, Feng J Y, et al. Forest types control the contribution of litter and roots to labile and persistent soil organic carbon[J]. Biogeochemistry, 2024, 167(12): 1609-1617 DOI:10.1007/s10533-024-01185-5 (  0) 0) |
| [41] |
Hao Z Z, Li P, Le Q L, et al. Litter and root removal modulates soil organic carbon and labile carbon dynamics in larch plantation ecosystems[J]. Forests, 2024, 15(11): 1958 DOI:10.3390/f15111958 (  0) 0) |
| [42] |
Hättenschwiler S, Tiunov A V, Scheu S. Biodiversity and litter decomposition in terrestrial ecosystems[J]. Annual Review of Ecology, Evolution, and Systematics, 2005, 36(2005): 191-218 (  0) 0) |
| [43] |
Yang B, Qi K B, Bhusal D R, et al. Soil microbial community and enzymatic activity in soil particle-size fractions of spruce plantation and secondary birch forest[J]. European Journal of Soil Biology, 2020, 99: 103196 DOI:10.1016/j.ejsobi.2020.103196 (  0) 0) |
| [44] |
Men X X, Bao Y, Wu M H, et al. Soil enzyme activities responded differently to short-term litter input manipulation under coniferous and broad-leaved forests in the subalpine area of Southwest China[J]. Forest Ecology and Management, 2023, 546: 121360 DOI:10.1016/j.foreco.2023.121360 (  0) 0) |
| [45] |
李彦林, 陈杨洋, 杨霜溶, 等. 植物根系分泌的有机酸对土壤碳氮矿化的影响[J]. 生态环境学报, 2024, 33(9): 1362-1371 (  0) 0) |
| [46] |
Zhang Z L, Phillips R P, Zhao W Q, et al. Mycelia-derived C contributes more to nitrogen cycling than root-derived C in ectomycorrhizal alpine forests[J]. Functional Ecology, 2019, 33(2): 346-359 DOI:10.1111/1365-2435.13236 (  0) 0) |
| [47] |
郭钰, 姚佳峰, 董媛, 等. 油松和刺槐纯林及混交林根系分布特征[J]. 应用生态学报, 2023, 34(11): 2881-2888 (  0) 0) |
| [48] |
Li X G, Zi H Y, Carrion V J, et al. Conifer and broadleaf trees show a strong co-evolution with rhizosphere diazotrophic microbiome[J]. Plant and Soil, 2023, 484(1): 487-501 (  0) 0) |
| [49] |
杨轶晗, 王彤, 常宇飞, 等. 凋落物去除对城市公园樟子松林土壤有机碳矿化及其温度敏感性的影响[J]. 土壤与作物, 2022, 11(3): 298-306 (  0) 0) |
| [50] |
Deng C, Lyu M K, Xiong X L, et al. Understory ferns removal downregulates microbial carbon use efficiency and carbon accrual in previously degraded lands[J]. Agricultural and Forest Meteorology, 2023, 340: 109631 DOI:10.1016/j.agrformet.2023.109631 (  0) 0) |
| [51] |
Ma S L, Zhu W Z, Wang W W, et al. Increased microbial carbon use efficiency and turnover rate drive soil organic carbon storage in old-aged forest on the southeastern Tibetan Plateau[J]. Biology and Fertility of Soils, 2025, 61(1): 163-176 DOI:10.1007/s00374-024-01877-y (  0) 0) |
| [52] |
Li S T, Jiang Y M, Lyu M K, et al. High-quality litter exerts a greater effect on soil carbon gain in unrestored than restored pine plantations[J]. Science of the Total Environment, 2024, 952: 175975 (  0) 0) |
| [53] |
Straathof A L, Chincarini R, Comans R N J, et al. Dynamics of soil dissolved organic carbon pools reveal both hydrophobic and hydrophilic compounds sustain microbial respiration[J]. Soil Biology and Biochemistry, 2014, 79: 109-116 DOI:10.1016/j.soilbio.2014.09.004 (  0) 0) |
| [54] |
Crow S E, Lajtha K, Filley T R, et al. Sources of plant-derived carbon and stability of organic matter in soil: Implications for global change[J]. Global Change Biology, 2009, 15(8): 2003-2019 DOI:10.1111/j.1365-2486.2009.01850.x (  0) 0) |
| [55] |
Zhu H Q, Gong L, Ding Z L, et al. Effects of litter and root manipulations on soil carbon and nitrogen in a Schrenk's spruce (Picea schrenkiana) forest[J]. PLoS One, 2021, 16(2): e0247725 DOI:10.1371/journal.pone.0247725 (  0) 0) |
| [56] |
Ma H L, Yin Y F, Gao R, et al. Response of nitrogen transformation to glucose additions in soils at two subtropical forest types subjected to simulated nitrogen deposition[J]. Journal of Soils and Sediments, 2019, 19(5): 2166-2175 DOI:10.1007/s11368-018-02237-8 (  0) 0) |
| [57] |
徐天懂, 史珑燕, 谷雨晴, 等. 2种林分类型土壤有机碳矿化及生物活性[J]. 东北林业大学学报, 2024, 52(12): 140-148 (  0) 0) |
| [58] |
Teng Q M, Lu X N, Zhang Q Q, et al. Litterfall quality modulates soil ammonium and nitrate supply through altering microbial function in bamboo encroachment of broadleaf forests[J]. Geoderma, 2023, 437: 116592 DOI:10.1016/j.geoderma.2023.116592 (  0) 0) |
| [59] |
Wang W B, Chen D S, Zhang Q, et al. Effects of mixed coniferous and broad-leaved litter on bacterial and fungal nitrogen metabolism pathway during litter decomposition[J]. Plant and Soil, 2020, 451(1): 307-323 (  0) 0) |
| [60] |
Sayer E J, Tanner E V J. Experimental investigation of the importance of litterfall in lowland semi-evergreen tropical forest nutrient cycling[J]. Journal of Ecology, 2010, 98(5): 1052-1062 DOI:10.1111/j.1365-2745.2010.01680.x (  0) 0) |
| [61] |
Xiong Y M, Zeng H, Xia H P, et al. Interactions between leaf litter and soil organic matter on carbon and nitrogen mineralization in six forest litter-soil systems[J]. Plant and Soil, 2014, 379(1): 217-229 (  0) 0) |
| [62] |
Zhang C F, Zhao Q X, Cai Y M, et al. Effect of litter removal and addition on root exudation and associated microbial N transformation in a Pinus massoniana plantation[J]. Forests, 2023, 14(7): 1305 DOI:10.3390/f14071305 (  0) 0) |
2. Key Laboratory for Humid Subtropical Ecogeographical Processes of the Ministry of Education, Fujian Normal University, Fuzhou 350117, China
 2026, Vol. 58
2026, Vol. 58


