2. 广东省生态环境技术研究所, 广州 510650
土壤养分主要来源于土壤腐殖质,土壤腐殖质对土壤的物理、化学、生物学性质都有重要影响,是土壤肥力指标之一[1]。腐殖质是土壤有机质的主体[2],其组成和性质随生物气候条件不同而存在显著差异[3-4]。一般来说,土壤腐殖质主要由胡敏酸、富啡酸和胡敏素所组成,其中胡敏酸和富啡酸总称为腐殖酸(HA)。腐殖酸(HA)的流失是土壤侵蚀导致土壤养分流失和土壤肥力下降的关键问题。减少腐殖酸(HA)流失,对保障土壤肥力至关重要。近年来,生物质炭(Biochar)在国内外关注度广泛提高,它是秸秆、稻壳、木屑等农业废料或生活垃圾在低氧或缺氧条件下,经热解炭化产生的一类高度芳香化的难溶性固态物质[5]。生物质炭是一种新型吸附剂[6],对腐殖酸有较好的吸附作用。经研究表明,生物质炭有较大的比表面积,孔隙结构发达且有较高的电荷密度[7],可以提高土壤孔隙度和土壤保土保肥能力[8-9],还能提高对养分的吸附能力[10]。
到目前为止生物质炭对氮、磷等营养组分吸附和解吸研究较多[11-14],但对于生物质炭中腐殖酸(HA)吸附-解吸的研究还较少。在龙川江流域地带牛粪大量堆积,如何处置牛粪,对去资源化和再利用有待解决。因此,本文以牛粪为原料制备生物质炭,研究不同的背景电解质(NaCl、Na2SO4和Na3PO4)对牛粪生物质炭中腐殖酸(HA)吸附-解吸的影响,为提高腐殖酸(HA)利用率提供理论依据。
1 材料与方法 1.1 供试材料本试验以牛粪为生物质炭的制备原料,供试牛粪来自云南省楚雄州牟定县龙丰村旱地。生物质炭制备方法:牛粪经风干,破碎至2 ~ 4 cm,装入铝盒中,放入可编辑气氛保护箱式炉(SRJX-4-13,北京市永光明医疗仪器有限公司),在通入氮气保护的情况下,以8 ℃/min的速率升温,热解温度为600 ℃,慢速热解2.5 h。随炉自然冷却至室温后取出,研钵研磨,过100目筛,贮存。
1.2 腐殖酸溶液的配制称取1 g的商品HA(生化试剂),加入一定量的去离子水和NaOH溶液使其逐渐溶解,配制成1 L的HA溶液,放置24 h,再用HCl调节pH为7,过0.45 μm滤膜后待用。取10 ml储备液,进行总有机碳(TOC)含量的测定,并以TOC含量表示HA含量,配制成HA储备液,于冰箱中冷藏备用。
1.3 试验方法 1.3.1 等温吸附试验称取过0.2 mm的牛粪生物质炭0.5 g于离心管中并称重(W1),按照1︰25的样液比分别将含腐殖酸为0、10、20、40、60、80、100、120、140 mg/L的溶液25 ml(分别以0.01 mol/L的NaCl、Na2SO4、Na3PO4作背景电解质,再加几滴氯仿以防止微生物繁殖),用HCl和NaOH调节溶液pH为7,放于25 ℃恒温箱中持续振荡24 h,于8 000 r/min条件下离心10 min并过滤,测定滤液中的腐殖酸浓度并计算含量,每个处理3次重复,在UV254下测其吸光度[15]。
1.3.2 等温解吸试验取浓度为10、20、40、60、80、100、120、140 mg/L的上述样品,将含有分离出上清液的离心管称重(W2),计算残留液中含腐殖酸量(W2-W1),然后分别加入0.01 mol/L的NaCl、Na2SO4、Na3PO4溶液25 ml,放置于25 ℃恒温箱中持续振荡24 h,于8 000 r/min条件下离心10 min,倾倒上清液并过滤,测定上清液腐殖酸浓度。根据吸附平衡后的浓度、残留液体积计算腐殖酸的解吸量。每个处理3次重复。
1.4 测定方法生物质炭表面形态结构采用扫描电子显微镜(SSX-550,日本岛津)进行观察测定;生物质炭元素含量采用元素分析仪(Vario Macro cube,德国Elementar)及EDS元素分析仪分别对C、N、O和Ca、K、Fe等元素测定;生物质炭比表面积和孔隙度/孔径分别采用BET单点法用004A型BET氮吸附比表仪进行测定和全自动快速中孔/微孔分析仪(ASAP2020,天津港东科技股份有限公司)进行测定;腐殖酸浓度采用紫外可见分光光度计进行测定。
1.5 数据分析按下列公式计算吸附量、解吸量和解吸率:
| $ 吸附量\left( {\rm mg/g} \right) = \left( {初始浓度 - 平衡浓度} \right) \times 溶液体积/称样质量 $ |
| $ 解吸量\left( {\rm mg/g} \right) = 解吸液浓度 \times 解吸液体积/称样质量 $ |
| $ 解吸率\left( \% \right) = 解吸量/吸附量 \times 100\% $ |
数据经Excel 2010整理,用SPSS19.0软件进行统计分析。
2 结果与分析 2.1 牛粪生物质炭结构表征 2.1.1 扫描电镜和元素含量分析本试验设定的600 ℃热解温度条件下烧制成牛粪生物质炭,生物质炭材料吸附腐殖酸与其本身的结构和元素组成相关,为此本试验对牛粪生物质炭进行SEM元素分析及EDS元素组成分析,并和牛粪进行了对比分析(表 1)。从表 1可以看出,牛粪生物质炭和牛粪的几种元素进行对比,牛粪生物质炭中Fe比牛粪增加了7.28%,可促进腐殖酸在土壤中吸附,减少其流失。牛粪生物质炭中的盐基离子Ca2+和K+分别比牛粪增加了10.77%和96.35%,这些盐基离子的增加有助于改善土壤肥力[16]。
|
|
表 1 元素分析及EDS元素组成分析表(%) Table 1 The element analysis and analysis of EDS elemental composition |
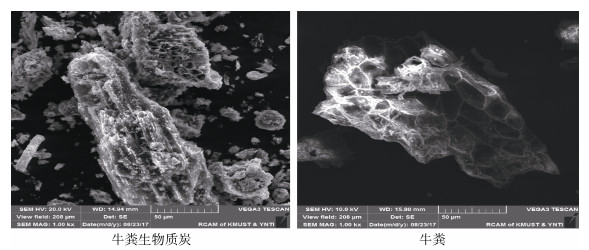
从图 1牛粪生物质炭的扫描电镜图可以看出:热解温度升高,生物质炭孔隙结构增加,且生物质炭表面的粗糙、分层程度越明显,这是由于牛粪在热解过程中,有机质不断分解、消耗,因此在生物质炭表面结构上留下了较多的孔,从而使得生物质炭整体疏松多孔;生物质各组分的热解所需温度不一样,导致生物质炭表面孔隙结构各异且排列不规则,热解温度越高,损失的组分越多,表面就越粗糙[17]。相对而言牛粪管状结构非常少,并且管状结构容易被其他的物体所堵塞,孔径比较小,孔洞也比较少,不利于吸附。
|
图 1 牛粪生物质炭与牛粪的SEM结构扫描图(5 000倍) Fig. 1 The SEM structure scan of dairy manure biochar and dairy manure |
比表面积和孔容/孔径是影响生物质炭吸附性能的关键因素。生物质炭的比表面积与生物质原料和制备条件相关,研究表明大多数生物质炭的比表面积在0.1 ~ 410 m2/g之间。表 2中的数据是本实验制备的牛粪生物质炭比表面积等结构表征数据。结果表明,牛粪生物质炭BET比表面积约为13.168 m2/g,单点吸附总体积约为2.28 ×10-2 cm3/g,t-Plot微孔比表面积4.369 m2/g,t-Plot微孔体积1.82×10-3 cm3/g,平均孔径6.628 nm。BET比表面积和单点吸附总孔体积可以表征生物质炭孔隙结构的发达程度,t-Plot微孔比表面积和t-Plot微孔体积表征生物质炭微孔结构的分布状况即微孔吸附的性能。上述数据与相关文献数据无明显差异[18],结合电镜图片,牛粪生物质炭具有发达的孔隙结构、吸附性能,可以满足吸附腐殖酸的需要,有利于土壤肥力的提高。
|
|
表 2 牛粪生物质炭的孔隙结构、比表面积参数 Table 2 Pore structure、specific surface area parameters of the dairy manure biochar |
在不同背景电解质条件下,牛粪生物质炭对腐殖酸的吸附呈现不同的特征,从表 3可以看出:NaCl、Na2SO4、Na3PO4 3种背景电解质对牛粪生物质炭中腐殖酸都有较大的吸附量;对同种背景溶液而言,随着加入液中腐殖酸浓度增加,牛粪生物质炭对腐殖酸的吸附量逐渐增加,吸附率从刚开始的快速增加,到后面缓慢增加,直至达到饱和吸附量。3种背景溶液的化学组成不同,导致背景电解质中的离子不同,因此牛粪生物质炭对腐殖酸的吸附作用存在差异。在加入液为低浓度(10 ~ 20 mg/L)时,Na2SO4中牛粪生物质炭对腐殖酸的吸附量和吸附率最大,分别为0.17 ~ 0.62 mg/g、35.20% ~ 62.00%;NaCl中牛粪生物质炭对腐殖酸的吸附量和吸附率其次,分别为0.13 ~ 0.60 mg/g、25.4% ~ 60.00%;Na3PO4中牛粪生物质炭对腐殖酸的吸附量和吸附率最小,分别为0.12 ~ 0.37 mg/g、12.00% ~ 37.00%。在加入液浓度为中高浓度(40 ~ 120 mg/L)时,3种背景电解质相比,NaCl中牛粪生物炭质对腐殖酸的吸附量和吸附率最大,其次是Na2SO4,最后是Na3PO4。在加入液为高浓度(140 mg/L)时,NaCl、Na2SO4、Na3PO4中牛粪生物质炭对腐殖酸吸附量达到最大,吸附率也达到最大,吸附量范围为4.36 ~ 6.10 mg/g,吸附率范围为62.28% ~ 87.14%。3种背景电解质相比,牛粪生物质炭对腐殖酸最大吸附量和吸附率存在显著的差异,NaCl中牛粪生物质炭对腐殖酸的吸附量和吸附率最大,分别为6.10 mg/g、87.14%,均为Na3PO4中牛粪生物质炭对腐殖酸吸附的1.40倍;Na2SO4中牛粪生物质炭对腐殖酸的吸附量和吸附率其次,分别为5.89 mg/g、84.14%,均为Na3PO4中牛粪生物质炭对腐殖酸吸附的1.35倍;Na3PO4中牛粪生物质炭对腐殖酸的吸附量和吸附率最小。
|
|
表 3 不同电解质对腐殖酸的吸附特征 Table 3 Adsorption characteristics of humic acid by different electrolytes |
将3种背景电解质对腐殖酸的解吸量与加入腐殖酸浓度作等温解吸曲线,牛粪生物质炭吸附的腐殖酸只有部分被解吸下来,而且随着加入腐殖酸浓度的增加,解吸量也随之增加。由表 4可知,在腐殖酸浓度为10 ~ 60 mg/L时,牛粪生物质炭对腐殖酸的解吸量增加迅速,有可能Cl-、SO42-、PO43-与腐殖酸竞争牛粪生物质炭的吸附位点,Cl-、SO42-、PO43-能把吸附在牛粪生物质炭的腐殖酸给替换出来,3种背景电解质相比,牛粪生物质炭对腐殖酸的解吸量的大小顺序为SO42- > PO43- > Cl-,最大的SO42-是最小的Cl-的1.56倍。在腐殖酸浓度大于60 mg/L时,3种背景电解质对牛粪生物质炭中腐殖酸的解吸量增加放缓;在腐殖酸浓度为80 ~ 100 mg/L时,在SO42-和PO43-中牛粪生物质炭对腐殖酸的解吸量相近,变化范围分别为0.67 ~ 0.70 mg/g,0.59 ~ 0.66 mg/g,在Cl-中牛粪生物质炭对腐殖酸的解吸量为0.37 ~ 0.43 mg/g;在腐殖酸浓度为120 ~ 140 mg/L时,牛粪生物质炭对腐殖酸的解吸量的大小顺序为SO42- > PO43- > Cl-,这3种离子中牛粪生物质炭吸附的腐殖酸的解吸量达到最大值。
|
|
表 4 不同电解质对腐殖酸的解吸特征 Table 4 Desorption characteristics of humic acid by different electrolytes |
腐殖酸的解吸率能反映Cl-、SO42-、PO43-对牛粪生物质炭中腐殖酸解吸的活性,更能反映出腐殖酸的解吸特征。由表 4可知,随着加入腐殖酸浓度增加,在Cl-、SO42-、PO43-中牛粪生物质炭吸附的腐殖酸的解吸率从一个较大值逐渐减小并趋于稳定。在腐殖酸浓度为10 ~ 80 mg/L时,下降幅度较大,其中在PO43-中,下降幅度达到67.02%。总体而言,在低中腐殖酸浓度时,SO42-和PO43-中牛粪生物质炭吸附的腐殖酸的解吸率较大,而Cl-中牛粪生物质炭吸附腐殖酸的解吸率相对偏小。在腐殖酸浓度大于80 mg/L时,在Cl-、SO42-、PO43-中牛粪生物质炭吸附的腐殖酸的解吸率逐渐减小并趋向于稳定。一般来说,解吸率的大小由吸附强度的高低所决定的,吸附强度越大,解吸率越小,吸附强度越小,解吸率越大,吸附强度的大小顺序为Cl- > SO42- > PO43-。在低中高腐殖酸浓度下,Cl-、SO42-、PO43-对牛粪生物质炭的吸附态腐殖酸具有较好的有效性,其中Cl-对牛粪生物质炭中的吸附态腐殖酸有效性最高。3种离子中牛粪生物质炭吸附的腐殖酸的最高解吸率和最低解吸率的大小顺序都为PO43- > SO42- > Cl-,其极差值分别为73.31%、73.59%、45.32%。通过上述证明了在低中高腐殖酸浓度中SO42-、PO43-对牛粪生物质炭吸附腐殖酸的解吸率影响较大,相对而言Cl-的影响较小,Cl-相对于SO42-、PO43-作用下牛粪生物质炭对腐殖酸有较大的吸附性。
2.4 牛粪生物质炭对腐殖酸的等温吸附解吸方程以牛粪生物质炭在不同浓度下所得的平衡液浓度为横坐标,平衡液浓度与吸附量、解吸量的比值分别为纵坐标做Langmuir和Freundlich方程拟合的等温吸附和等温解吸结果见表 5。拟合度R2(Langmuir) > R2(Freundlich) > 0.937,由此可见,牛粪生物质炭对腐殖酸的吸附以单层分子不均匀吸附模式为主,同时也存在着多层分子吸附。根据方程计算牛粪生物质炭吸附腐殖酸的平衡参数RL均小于1 (0.194 ~ 0.984),说明牛粪生物质炭对腐殖酸的吸附为有利吸附,而且随着初始浓度的增加,平衡参数减小,说明提高初始浓度有利于牛粪生物质炭对腐殖酸的吸附。
|
|
表 5 不同电解质对腐殖酸的等温吸附方程拟合参数 Table 5 Isotherm constants for humic acid adsorption by different electrolytes |
将拟合的结果和所得的表征吸附和解吸特性的参数列表 6,可见Langmuir方程能很好地拟合3种背景电解质对牛粪生物质炭中腐殖酸吸附和解吸的过程,其相关系数分别为0.948 ~ 0.991,0.892 ~ 0.970,均达到显著水平。在Langmuir吸附方程参数中,Qm为最大吸附量,反映了不同背景电解质对牛粪生物质炭中腐殖酸吸附的差异以及吸附潜力,Qm值的大小顺序为NaCl > Na2SO4 > Na3PO4,NaCl的最大,为25.814 mg/g;Na3PO4的最小,为9.852 mg/g,两者相差2.62倍。KL则反映的是与吸附结合能有关的常数,具有吸附强度的意义。假如KL值越大,说明固体对腐殖酸的吸附速率相对最大,解吸速率相对较小。最大缓冲容量(MBC)为KL与Qm的乘积,能综合吸附量与强度因子的综合参数,表示固体对养分的吸附特性。MBC越大,吸附能力越强;MBC越小,吸附能力越弱。不同背景电解质的MBC值在0.158 ~ 0.490之间,大小顺序为NaCl > Na2SO4 > Na3PO4。
|
|
表 6 不同电解质对腐殖酸的等温解吸方程拟合参数 Table 6 Isotherm constants for humic acid desorption by different electrolytes |
在Langmuir解吸方程中,Xm为最大解吸量,反映了牛粪生物质炭在一定温度、电解质等试验条件下,对吸附的腐殖酸的解吸量达到最大限值,与最大吸附量(Qm)值相近,大小顺序为Na3PO4 > Na2SO4 > NaCl,Na3PO4的Xm最大,为0.992 mg/g,NaCl的Xm最小,为0.593 mg/g。KL值为解吸平衡常数,其大小能在某种程度上反映生物质炭对吸附的腐殖酸解吸能力的强弱。Na2SO4的KL值最大,为0.037,Na3PO4的KL值最小,为0.021。最大缓冲容量(MBC)为KL与Xm的乘积,可以用来表征电解质对解吸能力的影响。通过Langmuir解吸方程拟合表明,3种背景电解质对腐殖酸的解吸能力不同,即使Na3PO4的解吸量最大,但是解吸能力不如Na2SO4。因为解吸量大并不代表电解质对腐殖酸的解吸能力强,最大解吸量(Xm)仅仅是电解质对腐殖酸的容量因子,而最大缓冲容量(MBC)是综合了强度和容量因子,能更好地反映电解质对腐殖酸的解吸能力。
3 讨论由结果分析可知,牛粪生物质炭吸附符合Langmuir吸附曲线,这与朱志平等[19]研究碳纳米管吸附腐植酸的动力学、热力学及机理研究相似,以单层分子吸附为主,多层分子为辅,平衡参数RL < 1,为有利吸附。NaCl、Na2SO4和Na3PO4 3种背景电解质对牛粪生物质炭中腐殖酸的吸附和解吸影响不同。随着腐殖酸的浓度增加,牛粪生物质炭对腐殖酸的吸附量和解吸量增加,解吸率降低,这与黄容等[20]研究不同生物质灰渣对磷的吸附和解吸动力学特征相似;但是吸附率是增加的,这与黄容研究的结果又不一致。同时也与Maghsoodloo等[21]研究壳聚糖处理对活性炭吸附腐殖酸的影响相似,其吸附量和吸附率随着腐殖酸浓度增加而增加。在Na2SO4和Na3PO4体系生物质炭对腐殖酸的吸附量和吸附率小于NaCl体系,主要因为牛粪生物质炭含有较高的Ca,SO42-、PO43-和腐殖酸均易与Ca形成沉淀,存在竞争作用;而CaCl2是可溶盐,不会与腐殖酸竞争Ca,所以在NaCl中牛粪生物质炭对腐殖酸的吸附量和吸附率最高,这与Li等[22]用Ca改性碳纳米管去除水中腐殖酸的结果相似,腐殖酸的吸附量和吸附率得到提高。PO43-与牛粪生物质炭中的Ca形成Ca3(PO4)2沉淀,占据牛粪生物质炭的吸附位点,导致牛粪生物质炭无法正常吸附到腐殖酸,所以在Na3PO4中牛粪生物质炭对腐殖酸的吸附量和吸附率最低;SO42-与牛粪生物质炭中的Ca形成CaSO4沉淀,但其溶解度比Ca3(PO4)2高,所以在Na2SO4中牛粪生物质炭对腐殖酸的吸附量和吸附率位于NaCl和Na3PO4之间。而在解吸试验中,腐殖酸已经先行吸附完成,Cl-对牛粪生物质炭中腐殖酸进行解吸时,HA与牛粪生物质炭中Ca形成沉淀,占据牛粪生物质炭的吸附位点,导致HA的解吸量和解吸率较低;SO42-对牛粪生物质炭中腐殖酸进行解吸时,SO42-与牛粪生物质炭中Ca形成沉淀,但其溶解度比Ca3(PO4)2高,其在一定程度上能将腐殖酸解吸出来;PO43-对腐殖酸进行解吸时,PO43-与牛粪生物质炭中Ca形成沉淀,同时又占据牛粪生物质炭的吸附位点,导致PO43-能将大部分腐殖酸从牛粪生物质炭中替换出来,PO43-与牛粪生物质炭的吸附能要大于腐殖酸与牛粪生物质炭的吸附能,因此PO43-对牛粪生物质炭中腐殖酸的解吸率最高。Guan和Qin等[23-24]也得到类似的结论,即PO43-与金属氧化物的吸附能大于腐殖酸与金属氧化物的吸附能。MBC是KL与Qm的乘积,反映吸附能力的大小,吸附能力的大小顺序为NaCl > Na2SO4 > Na3 PO4,可能是吸附强度越大吸附能力也就越大。同时MBC也是KL与Xm的乘积,反映解吸能力的大小,解吸能力的大小顺序为Na2SO4 > Na3PO4 > NaCl,但是解吸量最大的Na3PO4解吸能力不如Na2SO4,可能是Na3PO4解吸强度不如Na2SO4。通过上述分析可知,背景电解质NaCl中腐殖酸的吸附量和吸附率最大,解吸量和解吸率最小,有利于牛粪生物质炭更好地吸附腐殖酸,减少腐殖酸的流失。
4 结论1) 在NaCl,Na2SO4和Na3PO4 3种背景电解质作用下,随着腐殖酸浓度的增加,牛粪生物质炭对腐殖酸的吸附量和解吸量也是增加的,吸附量的大小顺序为NaCl > Na2SO4 > Na3PO4,解吸量的大小顺序为Na2SO4 > Na3PO4 > NaCl;随着腐殖酸浓度的增加,牛粪生物质炭对腐殖酸的吸附率也是增加的,而腐殖酸的解吸率是降低的。吸附率的大小顺序为NaCl > Na2SO4 > Na3PO4,解吸率的大小顺序为Na3PO4 > Na2SO4 > NaCl。
2) 牛粪生物质炭吸附腐殖酸符合Langmuir吸附曲线,以单层分子不均匀吸附模式为主,同时也存在着多层分子吸附,平衡参数RL均小于1 (0.194 ~ 0.984),说明牛粪生物质炭吸附腐殖酸为有利吸附。
3) 最大缓冲容量(MBC)用来描述吸附能力和解吸能力参数,吸附能力的大小顺序为NaCl > Na2SO4 > Na3PO4,解吸能力的大小顺序为Na2SO4 > Na3PO4 > NaCl。
4) 背景电解质NaCl可以更好用于牛粪生物质炭吸附和解吸腐殖酸,有利于更大程度上吸附腐殖酸,减少腐殖酸的流失,有利于保土保肥
| [1] |
Shindo H, Yoshida M, Yamamoto A, et al. 13C values of organic constituents in Japanese volcanic ash soils[J]. Soil Science, 2005, 170(3): 175-182 DOI:10.1097/00010694-200503000-00003 (  0) 0) |
| [2] |
吴景贵, 王明辉, 万忠梅, 等. 玉米秸秆腐解过程中形成胡敏酸的组成和结构研究[J]. 土壤学报, 2006, 43(3): 443-451 DOI:10.3321/j.issn:0564-3929.2006.03.013 (  0) 0) |
| [3] |
Yang J S, Jun bao Y U, Liu J S, et al. Humus distribution and fraction of typical marsh soil depth profiles in the Sanjiang Plain[J]. Chinese Journal of Soil Science, 2006, 37(5): 865-868 (  0) 0) |
| [4] |
Zhang J J, Dou S, Cui-Lan L I, et al. Studies on fractionation of soil humus[J]. Chinese Journal of Soil Science, 2004, 35(6): 706-709 (  0) 0) |
| [5] |
张阿凤, 潘根兴, 李恋卿. 生物黑炭及其增汇减排与改良土壤意义[J]. 农业环境科学学报, 2009, 28(12): 2459-2463 DOI:10.3321/j.issn:1672-2043.2009.12.004 (  0) 0) |
| [6] |
Chang M P, Han J, Chu K H, et al. Influence of solution pH, ionic strength, and humic acid on cadmium adsorption onto activated biochar: Experiment and modeling[J]. Journal of Industrial & Engineering Chemistry, 2017, 48(2): 186-193 (  0) 0) |
| [7] |
Amonette J E, Joseph S. Characteristics of biochar: Microchemical properties[J]. Journal of the Party School of Shengli Oilfield, 2009, 7(6): 1649-1654 (  0) 0) |
| [8] |
巢军委, 王建国, 戴敏, 等. 生物炭对水稻土Olsen-P的影响[J]. 土壤, 2015, 47(4): 670-674 (  0) 0) |
| [9] |
王光飞, 马艳, 郭德杰, 等. 不同用量秸秆生物炭对辣椒疫病防控效果及土壤性状的影响[J]. 土壤学报, 2017, 54(1): 204-215 (  0) 0) |
| [10] |
Kolb S E, Fermanich K J, Dornbush M E. Effect of charcoal quantity on microbial biomass and activity in temperate soils[J]. Soil Science Society of America Journal, 2009, 73(73): 1173-1181 (  0) 0) |
| [11] |
王冰, 赵闪闪, 秦治家, 等. 生物质炭对黑土吸附-解吸硝态氮性能的影响[J]. 农业环境科学学报, 2016, 35(1): 115-121 (  0) 0) |
| [12] |
王荣萍, 余炜敏, 梁嘉伟, 等. 改性生物炭对菜地土壤磷素形态转化的影响[J]. 生态环境科学学报, 2016, 25(5): 872-876 (  0) 0) |
| [13] |
Liu N, Sun Z T, Wu Z C, et al. Adsorption characteristics of ammonium nitrogen by biochar from diverse origins in water[J]. Advanced Materials Research, 2013, 664(4): 305-312 (  0) 0) |
| [14] |
Xu G, Sun J N, Shao H B, et al. Biochar had effects on phosphorus sorption and desorption in three soils with differing acidity[J]. Ecological Engineering, 2014, 62(1): 54-60 (  0) 0) |
| [15] |
余晨, 何盈盈, 杨立. 活性炭吸附腐殖酸的分段等温吸附模拟及热力学研究[J]. 水处理技术, 2014, 40(1): 29-32 (  0) 0) |
| [16] |
徐仁扣. 秸秆生物质炭对红壤酸度的改良作用:回顾与展望[J]. 农业资源与环境学报, 2016, 33(4): 303-309 (  0) 0) |
| [17] |
Janus A, Pelfrêne A, Heymans S, et al. Elaboration, characteristics and advantages of biochars for the management of contaminated soils with a specific overview on Miscanthus biochars[J]. Journal of Environmental Management, 2015, 162(4): 275-289 (  0) 0) |
| [18] |
张鹏, 武健羽, 李力, 等. 猪粪制备的生物炭对西维因的吸附与催化水解作用[J]. 农业环境科学学报, 2012, 31(2): 416-421 (  0) 0) |
| [19] |
朱志平, 黄可龙, 周艺. 碳纳米管吸附腐植酸的动力学、热力学及机理研究[J]. 无机材料学报, 2011, 26(2): 170-174 (  0) 0) |
| [20] |
黄容, 高明, 廖燕妮. 不同生物质灰渣对磷的吸附解吸动力学特征[J]. 水土保持学报, 2014, 28(1): 156-160 DOI:10.3969/j.issn.1009-2242.2014.01.030 (  0) 0) |
| [21] |
Maghsoodloo S, Noroozi B, Haghi A K, et al. Consequence of chitosan treating on the adsorption of humic acid by granular activated carbon[J]. Journal of Hazardous Materials, 2011, 191(1/2/3): 380-387 (  0) 0) |
| [22] |
Li S, He M, Li Z, et al. Removal of humic acid from aqueous solution by magnetic multi-walled carbon nanotubes decorated with calcium[J]. Journal of Molecular Liquids, 2017, 230(3): 520-528 (  0) 0) |
| [23] |
Guan X H, Shang C, Chen G H. Competitive adsorption of organic matter with phosphate on aluminum hydroxide[J]. Journal of Colloid & Interface Science, 2006, 296(1): 51-58 (  0) 0) |
| [24] |
Qin X, Liu F, Wang G. Fractionation and kinetic processes of humic acid upon adsorption on colloidal hematite in aqueous solution with phosphate[J]. Chemical Engineering Journal, 2012, 209(41): 458-463 (  0) 0) |
2. Guangdong Institute of Eco-environment and Soil Sciences, Guangzhou 510650, China
 2019, Vol. 51
2019, Vol. 51


