2. 南京市蔬菜科学研究所, 南京 210042
土壤生态系统是连接大气圈、水圈、岩石圈和生物圈的纽带,与地上生态系统之间紧密联系、相互依存,共同决定着陆地生态系统的特征、过程和功能[1]。土壤微生物作为土壤生态系统的主要组成部分,不仅在元素的生物地球化学循环中起着重要作用,也在作物健康生长和可持续生产中起着关键作用[2]。尽管植物与微生物的互作关系是土传病害发生的重要决定因子[3],但目前对于根际微生物区系组成与生态系统功能之间的关联仍有待深入研究。
近年来农用化学品的大量投入是作物持续高产的重要支撑之一,但同时也给土壤及环境的健康带来了挑战[4]。高强度集约化农业生产一定程度上破坏了土壤微生物群落结构的稳态平衡,削弱了土壤生态系统的功能。尤以抑制土传病害发生的能力(抑病能力)下降为甚,导致作物根腐病、枯萎病、全蚀病、立枯病等土传病害频繁爆发[5]。番茄是全世界栽培最为普遍的果菜之一,设施番茄产业已成为农民增收的重要产业之一。然而,因青枯菌(Ralstonia solanacearum)侵染导致的番茄青枯病严重威胁着世界番茄种植产业的发展[6]。因此,土传青枯病的有效防控仍是关系到世界番茄产业可持续发展的重大理论及技术问题。
土壤微生物群落结构及组成对于番茄抵御青枯菌的侵染有着重要影响[7],因此,研究同一连作田块中健康与罹患青枯病的番茄土壤微生物群落结构及组成差异对于番茄土传青枯病的防控极其重要。然而,尽管已有大量研究表明调控土壤微生物区系可有效防控番茄青枯病的发生[6, 8-9],但对于同一连作条件下健康与患病番茄土壤微生物群落结构与组成差异的研究仍相对缺乏。杨尚东等[10]利用传统的分子生态学手段(PCR-DGGE)初步比较了番茄青枯病罹病植株和健康植株根际土壤细菌群落结构及多样性特征,但该研究手段不能揭示群落的组成差异;Li等[5]利用454焦磷酸测序技术研究比较了健康与患病番茄根际土壤及根内细菌群落结构和组成特征,但未揭示与根际细菌装配密切相关的土体土壤细菌群落差异。
因此,为全面揭示连作条件下健康与患病番茄的土体及根际细菌群落结构和组成差异及探究土体细菌群落的差异与根际细菌群落组成差异之间的关系,本研究拟采集设施大棚内长期连作番茄田块中感染土传青枯病植株的土体及根际土壤和健康植株的土体及根际土壤,利用荧光定量PCR和MiSeq高通量测序技术比较设施大棚内健康番茄与感染土传青枯病番茄的土体及根际土壤中细菌群落结构和组成差异,为番茄青枯病土壤的微生物区系调控提供理论依据和方向支撑。
1 材料与方法 1.1 供试材料 1.1.1 供试种子供试番茄种子为世纪红冠(Solanum lycopersicum Mill., CV. Shijihongguan),由南京市蔬菜花卉科学研究所提供。
1.1.2 试验点基本信息试验点设在江苏省南京市蔬菜花卉科学研究所(31°43' N,118°46' E)。试验区域为典型亚热带季风气候,年平均温度为15.4 ℃,年均降雨量达1 106 mm。试验设施土壤的基本性状如下:供试土壤为黄岗土,pH 6.33、有机质23.56 g/kg、全氮1.89 g/kg、有效磷138 mg/kg、速效钾464 mg/kg。
1.2 试验设计 1.2.1 番茄育苗将供试番茄种子用2% 次氯酸钠表面消毒3 min,再用无菌蒸馏水洗涤3次后在合适的温度和水分环境下发芽。种子发芽后,播入育苗基质中于育苗车间进行培育。当幼苗长出3~4片真叶时,选取长势一致的幼苗进行田间移植。
1.2.2 田间试验供试设施大棚自2013年2月开始于每年春夏及秋冬两季连续种植番茄。本试验于2015年2-6月在此设施大棚开展,此前已连续种植4季番茄,部分蕃茄植株已呈现出感染青枯病的症状。试验设4个小区,每个小区面积为10 m2(长×宽=2 m×5 m)。种植前施用7 kg商品鸡粪有机肥(N + P2O5+ K2O> 5%)及0.5 kg复合肥(N-P2O5-K2O,15-15-15)作为基肥,视长势追施尿素及氯化钾。所用商品鸡粪有机肥、复合肥、尿素及氯化钾均为市售常见肥料。基肥施入7 d后,每个小区移栽32棵番茄种苗,种植密度为0.6 m × 0.6 m(株距×行距)。移栽定植番茄种苗20 d后,每周监测番茄青枯病发生状况。为尽量避免土壤过于湿润所导致的潜在的细菌过度交叉污染,除定植移苗后一次性浇透以外,日常水分管理采取“少量多次”的策略,利用滴灌设施向番茄茎基部补充水分。
1.2.3 番茄土壤样品采集及DNA提取于番茄收获期每小区分别随机选定5株青枯病感病或健康(未明显感病)植株,用铁铲将距番茄茎部10 cm以内且0~20 cm深的土壤和根系一起挖取,将5株样品混匀后带回实验室进行后续处理。轻抖根系,将附着根上的土壤抖落,连同土体土壤利用四分法保留约200 g土壤作为感病(DB)及健康(HB)土体土壤样品。将去除轻松附着根系上的番茄根置入预先装有150 ml无菌水的500 ml三角烧瓶中,室温下以170 r/min震荡30 min,震荡后4 000 × g离心5 min,离心后沉淀即为根际土壤,将收集到的根际土壤混匀保存于-70 ℃备用。称取0.4 g土壤样品,用土壤DNA提取试剂盒(Mo Bio Laboratories, Inc., Carlsbad, CA, USA)按操作说明提取土壤DNA并用核酸定量仪(NanoDrop 2000, USA)测定提取的土壤DNA核酸浓度。
1.3 测定方法 1.3.1 土壤理化性质的测定土壤理化性质测定参照《土壤农化分析》[10]。利用玻璃电极酸度计测定土壤pH(w(土): V(水)=25:1);利用电导率仪测定土壤电导率(EC)(w(土): V(水)=5:1);利用元素分析仪(Vario EL, Germany)通过干烧法测定土壤的全碳(TOC)和全氮(TON)含量;0.01 mol/L氯化钙溶液浸提,流动分析仪(Auto Analyzer 3, Germany)测定土壤悬液的NH4+-N和NO3--N含量;利用醋酸铵浸提,火焰分光光度计测定土壤有效钾(AK)含量;碳酸氢钠浸提,钼锑抗比色法测定土壤有效磷(AP)含量。
1.3.2 土壤细菌和青枯菌数量的测定土壤细菌和青枯菌的数量采用实时荧光定量PCR法测定[12-13]。细菌扩增采用引物Eub338/Eub518 (5′-ACTCCTACGGGAGGCAGCAG-3′/5′-ATTACCGCG GCTGCTGG-3′),青枯菌扩增采用flicF/flicR (5′-GAACGCCAACGGTGCGAACT-3′/5′-GGCGGCCTTCAGGGAGGTC-3′)。将含大肠杆菌16 S全长及青枯菌flic基因的质粒进行梯度稀释,采用ABI 7500荧光定量PCR仪,按照标准程序制成标准曲线。扩增条件为:10 μl SYBR®Premix Ex Taq,0.4 μl上游引物和下游引物,0.4 μl ROX Reference Dye,2 μl模板DNA和6.8 μl无菌水。PCR扩增程序为:95 ℃预变性30 s;95 ℃预变性5 s,60 ℃延伸34 s,循环40次。所有样品进行3次重复,用无菌超纯水代替DNA模板设置为阴性对照。根据各样品Ct值计算每克土壤所含的拷贝数,并换算成每克干土形成的拷贝数,取对数值,以log (copies/g干土) 表示。
1.3.3 细菌测序文库构建参照Caporaso等[14]发表的方法构建细菌测序文库。细菌16S rRNA扩增采用引物520F (5′-AYTGGGYDTAAAGNG-3′)/802R (5′-TACNVGGGTATCTAATCC-3′)。细菌16S rRNA扩增体系为(25 μl):5.0 μl 5 × Reaction Buffer、5.0 μl 5 × GC high Enhancer、2.0 μl dNTP (2.5 mmol/L)、1.0 μl上下游引物(10 μmol/L)、0.25 μl TaKaRa Polymerase (5 U/μl)、2 μl模板DNA及9.0 μl无菌水。PCR扩增条件为:98 ℃预变性5 min;98 ℃变性30 s,50 ℃退火30 s,72 ℃延伸30 s,25个循环;最终72 ℃延伸5 min。对PCR产物进行割胶回收后利用BioTek酶标仪对纯化产物进行定量。将纯化的扩增子等摩尔浓度合并,然后用NEB Next® UltraTM DNA Library Prep Kit for Illumina(New England Biolabs, UK)建库,使用Agilent 2100 Bioanalyzer Instruments、Pico green和荧光分光光度计对文库进行质量和浓度的检测。多样品测序文库均一化至10 nmol/L后等体积混合,逐步稀释定量至4~5 pmol/L后进行上机测序。所有PCR扩增、文库准备及上机测序均在上海派森诺生物科技股份有限公司完成。
1.3.4 高通量数据分析利用QIIME软件对下机后的原始序列根据相应的barcode信息进行各样品序列分配并去除接头和引物序列;去除低质量序列后,利用Usearch软件对正反向序列进行拼接;拼接后的序列参照UPARSE的标准流程分析,生成操作分类单元(OTU)表格并挑选出各OTU代表性序列;利用RDP classifier[16]将代表性序列与RDP 16S rRNA数据库比对获取各OTU分类组成信息[15];最后,对去除所有样品中相对丰度均小于0.01% 的OTU的数据进行后续多样性分析。在Mothur软件[17]内基于Bray-Curtis参数计算各样品主成分分析(principal co-ordinates analysis,PCoA)比较各处理细菌群落结构差异;各样品取平后,基于97% 相似度水平利用Mothur计算细菌群落丰富度Chao值及多样性Shannon值;利用韦恩图探究样品之间组成上的差异性;各物种的相对丰度用该物种序列数除以该样品总序列数的百分比表示。
1.4 数据统计分析生物数据统计分析在IBM SPSS 20.0(SPSS Inc., Chicago, USA)及R语言中完成。采用多因素方差分析、多重比较及独立样本t检验分析比较处理间的显著性差异。
2 结果与分析 2.1 健康与感病番茄土壤基本理化性状即使在同一设施大棚小区内,健康与感病番茄植株土体土壤的部分基本理化性质差异明显(表 1)。健康与感病番茄土壤中电导率、NH4+-N、NO3--N、有效磷和全氮含量无显著差异,但健康植株土壤中pH和全碳含量显著高于感病植株土壤,速效钾的含量显著低于感病植株土壤。
|
|
表 1 健康与感病番茄土体土壤基本理化性质 Table 1 Basic chemical properties for bulk soils of healthy and diseased tomato-planting fields |
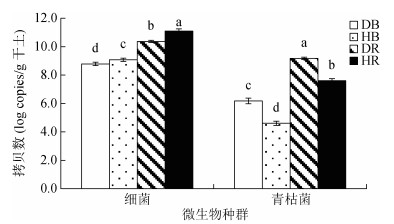
荧光定量PCR结果表明,根际土壤中细菌和青枯菌的数量显著高于土体土壤(P < 0.05),根际青枯菌的数量比土体青枯菌的数量高出3个数量级。健康番茄植株土体及根际土壤中细菌的数量分别显著高于感病番茄植株土体及根际土壤,而健康番茄植株土体及根际土壤青枯菌数量显著低于感病番茄植株土体及根际土壤(图 1)。
|
(DB. 感病番茄土体土壤;HB,健康番茄土体土壤;DR. 感病番茄根际土;HR. 健康番茄根际土。图中小写字母不同表示不同土壤间差异显著(P < 0.05),下同) 图 1 健康与感病番茄土体及根际土壤中细菌和青枯菌的数量 Fig. 1 Populations of bacteria and R. solanacearum in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
高通量原始序列经过基本质控过滤并去除古菌及低丰度序列后,16个土壤样品共有856 374条优质16S rRNA序列,其中最少的样品有38 449条序列,而最多的样品有74 009条序列。在97% 相似度水平下,856 374条序列共划分为3 452个OTU,其中最少的样品有1 168个OTU,而最多的样品有3 079个OTU。与RDP数据库比对后,856 374条序列可归类于38个细菌门,其中酸杆菌门、放线菌门、拟杆菌门、厚壁菌门及变形菌门为相对丰度最高的前5个门,占序列总数的86.7%。
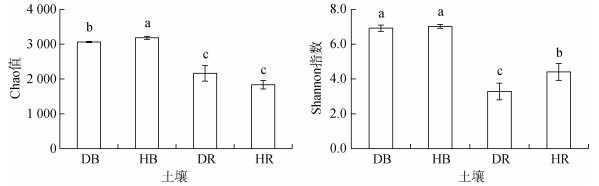
2.4 健康与感病番茄土壤细菌群落alpha多样性如图 2所示,根际土壤中细菌群落的alpha多样性指标,如Chao及Shannon指数均显著低于土体土壤(t检验,P < 0.05)。尽管健康番茄土体土壤丰富度Chao值显著高于感病土壤,但健康及感病番茄根际土壤中Chao值无显著差异。与之相反,尽管健康与感病番茄土体土壤多样性Shannon指数无显著差异,但健康番茄根际土壤中Shanon指数显著高于感病番茄根际土壤。
|
图 2 健康与感病番茄土体及根际土壤细菌群落Chao和Shannon多样性指标 Fig. 2 Chao and Shannon indices for bacterial communities in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
健康及感病番茄根际土壤细菌群落主坐标成分在一轴上明显区分于其土体土壤(图 3)。健康番茄根际土壤细菌群落主成分在二轴上明显区分于感病番茄根际土壤,尽管健康与感病番茄土体土壤细菌主成分差异不如根际土壤差异明显,但健康番茄土体土壤细菌群落主成分仍明显不同于感病番茄土体土壤。进一步的PerMANOVA分析,也表明土壤类型(土体与根际)及土壤健康(健康与感病)均是细菌群落差异的显著性驱动因素(Adonis检验,F土体vs根际 = 40.8,P土体vs根际= 0.001;F健康vs感病 = 6.7,P健康vs感病= 0.009)。

|
图 3 健康与感病番茄土体及根际土壤细菌群落主成分图 Fig. 3 Principal coordinate analysis (PCoA) for bacterial communities in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
如图 4所示,与土体土壤相比,番茄根际土壤在细菌门水平上的组成类似,但门的相对丰度有所差异,如变形菌门的相对丰度显著增高,而酸杆菌门、放线菌门、芽单胞菌门及疣微菌门的相对丰度显著降低低(t检验,P < 0.05)。尽管健康与感病番茄土体土壤细菌主要门的相对丰度无显著差异,但健康番茄根际土壤中拟杆菌门及疣微菌门的相对丰度显著高于感病番茄根际土壤,而厚壁菌门、芽单胞菌门及变形菌门的相对丰度显著低于感病番茄根际土壤(P < 0.05)。

|
图 4 健康与感病番茄土体及根际土壤细菌群落门的相对丰度 Fig. 4 Relative abundances of dominate phyla for bacterial communities in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
在属水平上健康与感病番茄土体及根际土壤的组成较为类似。在土体土壤中共鉴定出691个属,其中有657个属(95.1%)共同存在于健康及感病番茄土体土壤中;在根际土壤中共鉴定出615个属,其中有476个属(77.5%)共同存在于健康及感病番茄根际土壤中。健康及感病番茄土壤中共有属相对丰度的t检验结果表明:在健康与感病番茄土体土壤共有的657个属中,健康番茄土体土壤中有83个属的相对丰度显著高于感病番茄土体土壤,而有60个属的相对丰度显著低于感病番茄土体土壤;在健康与感病番茄根际土壤共有的476个属中,健康番茄根际土壤中有32个属的相对丰度显著高于感病番茄根际土壤,而有60个属的相对丰度显著低于感病番茄根际土壤(图 5)。

|
(纵坐标P指显著性P值) 图 5 健康与感病番茄土体及根际土壤细菌群落属的曼哈顿图 Fig. 5 Manhattan diagrams at genus level for bacterial communities in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
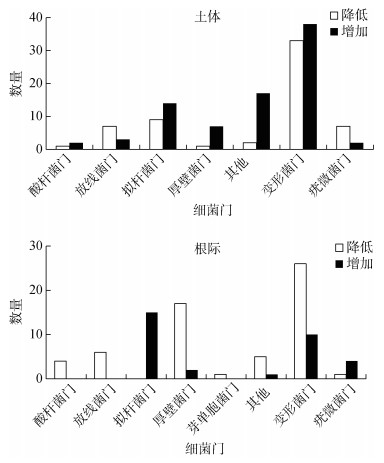
健康番茄土体土壤中相对丰度显著增加的83个属及显著降低的60个属均归类于酸杆菌门、放线菌门、拟杆菌门、厚壁菌门、变形菌门、疣微菌门及部分低丰度门;而健康番茄根际土壤中相对丰度显著降低的60个属归类于酸杆菌门、放线菌门、芽单胞菌门、厚壁菌门、变形菌门、疣微菌门及部分低丰度门,相对丰度显著增加的32个属归类于拟杆菌门、厚壁菌门、变形菌门、疣微菌门及部分低丰度门(图 6)。其中,健康番茄根际显著增加和降低的属分别多属于拟杆菌门和变形菌门。
|
图 6 健康番茄土体及根际土壤细菌群落中差异属所在的门及属的数量 Fig. 6 Numbers and affiliations of significant genera at phylum level for bacterial communities in bulk and rhizosphere soils of healthy tomato-planting fields |
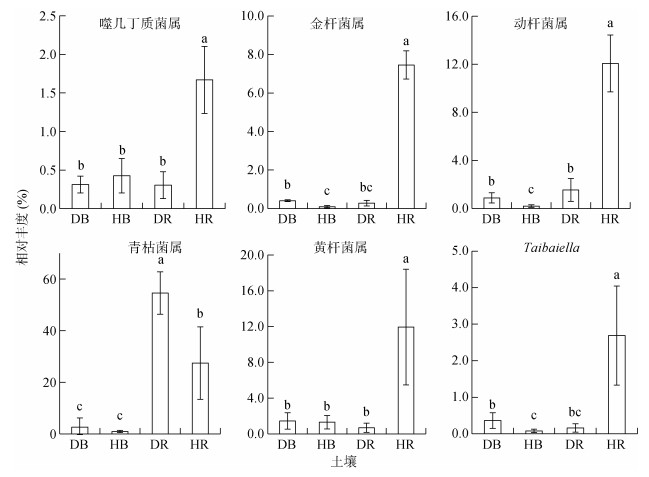
如图 7所示,在健康番茄根际土壤中相对丰度显著降低的变形菌门中,青枯病致病菌所在的青枯菌属的相对丰度仅为27.4%,显著低于感病番茄根际土壤中青枯菌属的相对丰度(54.6%),而土体土壤之间无显著差异。在健康番茄根际土壤中相对丰度显著增加的拟杆菌门中,噬几丁质菌属、金杆菌属、动杆菌属、黄杆菌属及Taibaiella的相对丰度大于1%,为优势菌属,而土体土壤之间也无显著差异。
|
图 7 健康和感病番茄土体及根际土壤部分细菌关键属的相对丰度 Fig. 7 Relative abundances of some key bacterial genera in bulk and rhizosphere soils of healthy and diseased tomato-planting fields |
根际土壤中细菌群落的多样性及稳定性决定着土壤和植物的健康以及生态系统的可持续性[18]。抑病型土壤指的是病原菌不能定殖,或能定殖但危害很小或没有危害,或者能定殖并一时造成危害随后即使在病原菌存在的情况下发病也很轻的土壤;而容易感病的土壤即为导病型土壤[19]。土著微生物群落或者特定种群具有抑制病原菌侵染植物的能力是抑病型土壤的关键因素[20-21]。本研究通过比较连作番茄田块中健康番茄土壤(抑病型土壤)及感病番茄土壤(导病型土壤)细菌组成差异,利用高通量测序技术深入揭示了抑制土传青枯病发生的土壤细菌群落结构及组成特征。
与Li等[5]的研究结果类似,本研究中健康番茄土体及根际土壤细菌群落明显不同于感病番茄土体及根际土壤,表明抑制土传青枯病发生的土壤细菌群落确与感病土壤细菌群落不同。Garbeva等[22]研究表明,根际土壤细菌多样性高能抑制土传病害的发生,与之类似,本研究中健康番茄根际土壤细菌群落的Shannon多样性指数更高,证实了细菌多样性与生态系统生产力之间存在的正相关关系。
Li等[5]利用454焦磷酸测序技术研究番茄根际土壤细菌群落组成时发现番茄根际土壤细菌群落中变形菌门的相对丰度最高。本研究中根际细菌群落中变形菌门的相对丰度也占优势地位,可能是因为其相对较快的生长速率[23]。本研究结果表明,抑制番茄土传青枯病发生的根际土壤中拟杆菌门的相对丰度显著高于感病土壤。拟杆菌门通常栖居于土体土壤中,而且是微生态系统中相对稳定的组分[24]。尽管拟杆菌门的相对丰度很少受土壤养分状况的影响,但近年来越来越多的研究表明拟杆菌门可能与土壤抑病能力相关[25]。本研究中拟杆菌门所包含的噬几丁质菌属、金杆菌属、动杆菌属、黄杆菌属及Taibaiella均为抑制土传青枯病发生的根际土壤中的优势菌属(相对丰度>1%),且与抑病能力密切相关。Liu等[26]研究表明噬几丁质菌属与番茄青枯病之间呈负相关关系,而Inderbitzin等[27]研究发现西兰花和几丁质混合物中接种噬几丁质菌属可提升土壤抑制轮枝菌侵染诱发的黄萎病的能力。金杆菌属已被成功分离并应用于辣椒疫病的生物防治[28]。Kwak等[25]研究表明,黄杆菌属在番茄根际土壤抵御青枯病侵染的过程中发挥重要作用。尽管尚未有直接证据表明其具有生防功能,但近年来的研究表明动杆菌属及Taibaiella在健康土壤中的相对丰度较高,可能也与抑病相关[29]。此外,本研究中健康番茄根际土壤中无论是青枯菌属的相对丰度还是绝对数量虽显著低于感病根际土壤,但仍属于较高水平,说明健康根际的整体细菌群落对于提升土壤抑病能力也具有一定的作用。
土壤微生物的装配受植物基因型和土壤状况等共同影响[30]。尽管感病与健康样品在同一设施大棚内采集,但可能因土壤的异质性、施肥的不均匀、灌溉不均匀以及与作物互作关系不一致等原因,导致健康与感病土壤样品的部分理化性状有显著差异。本研究中,抑制土传青枯病发生的土壤拥有较高的pH及全碳含量。Deltour等[31]研究发现高土壤pH能增强土壤抑镰刀菌枯萎病能力。土壤pH不仅能通过作用于病原菌或其他微生物直接影响土壤抑病型能力,还能通过影响土壤速效养分间接影响土壤抑病型能力[32]。此外,土壤全碳含量高通常预示着土壤有机质含量较高,而有机质含量较高的土壤中通常微生物生物量及活力也较高,也能在抑病过程中发挥重要作用[22]。Satoh和Toyota[33]研究证实提升土壤中有机质含量可降低土壤中青枯菌的数量,进而提升土壤抑制青枯病的能力。总而言之,提升土壤pH及全碳(有机质)含量,不仅可直接降低土壤中青枯菌,还可通过调控土体土壤微生物组成,进而影响根际微生物群落装配,并最终决定群落整体的抑病能力。
微生物、土壤及植物之间的互作关系非常复杂,影响了植物地下部微生物组成及生态系统功能,进而决定了地上部植物的生长与健康。本研究借助MiSeq高通量测序技术利用全面的分析比较了同一连作田块中健康与患病番茄土体及根际土壤细菌群落的组成特征,结果表明,相较于感病土壤,健康土壤中pH及有机质含量较高,其栖居的细菌群落组成特异,所种植的番茄从土壤中招募微生物装配形成的根际细菌群落多样性高,且富集了噬几丁质菌属、金杆菌属、动杆菌属、黄杆菌属及Taibaiella等土著有益微生物,不仅有效降低了根际土壤中青枯病的相对丰度,还提升了群落整体抑病能力。但番茄如何招募这些有益微生物在根际进行装配将是未来研究的热点与难点。
| [1] |
贺纪正, 李晶, 郑袁明. 土壤生态系统微生物多样性-稳定性关系的思考[J]. 生物多样性, 2013, 21(4): 411-420 (  0) 0) |
| [2] |
Berendsen R L, Pieterse C M J, Bakker P A H M. The rhizosphere microbiome and plant health[J]. Trends in Plant Science, 2012, 17(8): 478-486 DOI:10.1016/j.tplants.2012.04.001 (  0) 0) |
| [3] |
Hassani M A, Durán P, Hacquard S. Microbial interactions within the plant holobiont[J]. Microbiome, 2018, 6: 58 DOI:10.1186/s40168-018-0445-0 (  0) 0) |
| [4] |
Khan S, Hanjra M A, Mu J X. Water management and crop production for food security in China: a review[J]. Agricultural Water Management, 2009, 96(3): 349-360 DOI:10.1016/j.agwat.2008.09.022 (  0) 0) |
| [5] |
Li J G, Ren G D, Jia Z J, et al. Composition and activity of rhizosphere microbial communities associated with healthy and diseased greenhouse tomatoes[J]. Plant and Soil, 2014, 380(1/2): 337-347 DOI:10.1007/s11104-014-2097-6 (  0) 0) |
| [6] |
韦中. 生物有机肥防控土传番茄青枯病的效果及其机制研究[D]. 南京: 南京农业大学, 2012
(  0) 0) |
| [7] |
Raaijmakers J M, Paulitz T C, Steinberg C, et al. The rhizosphere: A playground and battlefield for soilborne pathogens and beneficial microorganisms[J]. Plant and Soil, 2009, 321(1/2): 341-361 (  0) 0) |
| [8] |
张鹏, 韦中, 朱震, 等. 生物有机肥对连作番茄和辣椒根际土壤微生物区系及茄科雷尔氏菌的影响[J]. 南京农业大学学报, 2013, 36(4): 77-82 (  0) 0) |
| [9] |
Wei Z, Yang X M, Yin S X, et al. Efficacy of Bacillus-fortified organic fertiliser in controlling bacterial wilt of tomato in the field[J]. Applied Soil Ecology, 2011, 48(2): 152-159 DOI:10.1016/j.apsoil.2011.03.013 (  0) 0) |
| [10] |
鲍士旦. 土壤农化分析(第3版)[M].
中国农业出版社, 北京, 2000
(  0) 0) |
| [11] |
杨尚东, 赵久成, 郭伊娟, 等. 番茄青枯病罹病植株和健康植株根际土壤细菌群落结构的初步分析[J]. 中国蔬菜, 2014(8): 25-29 (  0) 0) |
| [12] |
Fierer N, Jackson J A, Vilgalys R, et al. Assessment of soil microbial community structure by use of taxon-specific quantitative PCR assays[J]. Applied and Environmental Microbiology, 2005, 71(7): 4117-4120 DOI:10.1128/AEM.71.7.4117-4120.2005 (  0) 0) |
| [13] |
Schönfeld J, Heuer H, van Elsas J D, et al. Specific and sensitive detection of Ralstonia solanacearum in soil on the basis of PCR amplification of fliC fragments[J]. Applied and Environmental Microbiology, 2003, 69(12): 7248-7256 DOI:10.1128/AEM.69.12.7248-7256.2003 (  0) 0) |
| [14] |
Caporaso J G, Lauber C L, Walters W A, et al. Global patterns of 16S rRNA diversity at a depth of millions of sequences per sample[J]. PNAS, 2011, 108(Supplement_1): 4516-4522 DOI:10.1073/pnas.1000080107 (  0) 0) |
| [15] |
Edgar R C. UPARSE: Highly accurate OTU sequences from microbial amplicon reads[J]. Nature Methods, 2013, 10(10): 996-998 DOI:10.1038/nmeth.2604 (  0) 0) |
| [16] |
Wang Q, Garrity G M, Tiedje J M, et al. Na ve Bayesian ï classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy[J]. Applied and Environmental Microbiology, 2007, 73(16): 5261-5267 DOI:10.1128/AEM.00062-07 (  0) 0) |
| [17] |
Schloss P D, Westcott S L, Ryabin T, et al. Introducing mothur: Open-source, platform-independent, communitysupported software for describing and comparing microbial communities[J]. Applied and Environmental Microbiology, 2009, 75(23): 7537-7541 DOI:10.1128/AEM.01541-09 (  0) 0) |
| [18] |
Trivedi P, He Z L, van Nostrand J D, et al. Huanglongbing alters the structure and functional diversity of microbial communities associated with citrus rhizosphere[J]. The ISME Journal, 2012, 6(2): 363-383 DOI:10.1038/ismej.2011.100 (  0) 0) |
| [19] |
张瑞福, 沈其荣. 抑病型土壤的微生物区系特征及调控[J]. 南京农业大学学报, 2012, 35(5): 125-132 (  0) 0) |
| [20] |
Weller D M, Raaijmakers J M, Gardener B B M, et al. Microbial populations responsible for specific soil suppressiveness to plant pathogens[J]. Annual Review of Phytopathology, 2002, 40(1): 309-348 DOI:10.1146/annurev.phyto.40.030402.110010 (  0) 0) |
| [21] |
Mendes R, Kruijt M, de Bruijn I, et al. Deciphering the rhizosphere microbiome for disease-suppressive bacteria[J]. Science, 2011, 332(6033): 1097-1100 DOI:10.1126/science.1203980 (  0) 0) |
| [22] |
Garbeva P, van Veen J A, van Elsas J D. Microbial diversity in soil: Selection of microbial populations by plant and soil type and implications for disease suppressiveness[J]. Annual Review of Phytopathology, 2004, 42(1): 243-270 DOI:10.1146/annurev.phyto.42.012604.135455 (  0) 0) |
| [23] |
Fierer N, Bradford M A, Jackson R B. Toward an ecological classification of soil bacteria[J]. Ecology, 2007, 88(6): 1354-1364 DOI:10.1890/05-1839 (  0) 0) |
| [24] |
Yergeau E, Schoondermark-Stolk S A, Brodie E L, et al. Environmental microarray analyses of Antarctic soil microbial communities[J]. The ISME Journal, 2009, 3(3): 340-351 DOI:10.1038/ismej.2008.111 (  0) 0) |
| [25] |
Kwak M J, Kong H G, Choi K, et al. Rhizosphere microbiome structure alters to enable wilt resistance in tomato[J]. Nature Biotechnology, 2018, 36(11): 1100-1109 DOI:10.1038/nbt.4232 (  0) 0) |
| [26] |
Liu H J, Xiong W, Zhang R F, et al. Continuous application of different organic additives can suppress tomato disease by inducing the healthy rhizospheric microbiota through alterations to the bulk soil microflora[J]. Plant and Soil, 2018, 423(1/2): 229-240 DOI:10.1007/s11104-017-3504-6 (  0) 0) |
| [27] |
Inderbitzin P, Ward J, Barbella A, et al. Soil microbiomes associated with verticillium wilt-suppressive broccoli and chitin amendments are enriched with potential biocontrol agents[J]. Phytopathology, 2018, 108(1): 31-43 DOI:10.1094/PHYTO-07-17-0242-R (  0) 0) |
| [28] |
Kim H S, Sang M K, Jung H W, et al. Identification and characterization of Chryseobacterium wanjuense strain KJ9C8 as a biocontrol agent of Phytophthora blight of pepper[J]. Crop Protection, 2012, 32: 129-137 DOI:10.1016/j.cropro.2011.10.018 (  0) 0) |
| [29] |
Fu L, Penton C R, Ruan Y Z, et al. Inducing the rhizosphere microbiome by biofertilizer application to suppress banana Fusarium wilt disease[J]. Soil Biology and Biochemistry, 2017, 104: 39-48 DOI:10.1016/j.soilbio.2016.10.008 (  0) 0) |
| [30] |
Lundberg D S, Lebeis S L, Paredes S H, et al. Defining the core Arabidopsis thaliana root microbiome[J]. Nature, 2012, 488(7409): 86-90 DOI:10.1038/nature11237 (  0) 0) |
| [31] |
Deltour P, C França S, Liparini Pereira O, et al. Disease suppressiveness to Fusarium wilt of banana in an agroforestry system: Influence of soil characteristics and plant community[J]. Agriculture, Ecosystems & Environment, 2017, 239: 173-181 (  0) 0) |
| [32] |
彭双, 王一明, 叶旭红, 等. 土壤环境因素对致病性尖孢镰刀菌生长的影响[J]. 土壤, 2014, 46(5): 845-850 (  0) 0) |
| [33] |
Satoh K, Toyota K. Comparison of disease suppressiveness of different soils with or without repeated application of organic matters toward bacterial wilt of tomato caused by ralstonia solanacearum[J]. Microbes and Environments, 2004, 19(4): 310-314 DOI:10.1264/jsme2.19.310 (  0) 0) |
2. Nanjing Institute of Vegetable Science, Nanjing 210042, China
 2021, Vol. 53
2021, Vol. 53


