2. 农业部华北耕地保育重点开放实验室, 北京 100193
可溶性有机质(DOM,dissolved organic matter)指经溶液浸提后,能透过0.45 µm滤膜的有机分子混合体,包含小分子量的有机酸、碳水化合物和大分子量的腐殖质、氨基酸、多酚等[1]。土壤DOM的主要来源有植物凋落物、土壤腐殖质、降雨淋溶物等[2]。DOM作为土壤有机质库中最活跃的组成部分,虽然只占土壤有机质库的极小部分,却参与了土壤中有机质腐殖化、吸附–解吸、微生物代谢活动等一系列生物地球化学过程,对调节土壤养分循环和稳定土壤微生态起着重要的桥梁作用[3]。DOM具有比固相有机质更多的吸附位点,可通过静电吸附、配位体交换、络合反应、疏水作用、氢键作用和阳离子键桥等方式与土壤矿物结合而被固定[4],并在一定条件下解吸和重新释放,这对土壤有机碳固存、土壤养分储存和释放、土壤成土过程及重金属元素有效性有着重要的意义[5]。因此,提高土壤中DOM含量将具有重要意义。但土壤DOM却一直未受重视,直到20世纪70年代末,特别是20世纪80年代以后,随着全球碳循环问题受到广泛关注,土壤DOM才逐渐引起人们的重视[6]。土壤DOM由于其本身组分复杂,测定过程中易于改变其固有性质,采用传统的化学分析方法难以有效确定DOM的结构特征[7]。紫外–可见光谱分析技术具有灵敏度高、成本低、耗时短、操作简单快捷、结果可靠并且不会破坏样品等优点[8]。荧光光谱技术可以获得有机物质的大量有效信息[9],进而可以精确地阐明不同环境中有机物的组分和结构特征[10]。近年来,紫外–可见光谱和荧光光谱逐渐应用于研究土壤DOM的组分和结构特征及其变化规律。李帅东等[11]采用紫外–可见光谱和三维荧光光谱技术相结合的方法,研究了昆明松华坝库区表层土壤中DOM的组成结构和来源,结果表明,荧光光谱参数可以表征土壤DOM的组分来源。王玉涛等[12]研究表明方面,紫外–可见光谱和荧光光谱技术对黄土丘陵区不同植被下土壤DOM的组成和结构具有很好的表征效果。但上述研究主要集中在某一土壤类型或作物种植下土壤DOM的数量和光谱特征,对不同土壤DOM的数量和结构特征差异的研究比较少见。
黑土、潮土和红壤是我国3种比较典型的土壤类型,分布范围广,代表性强。因此,本研究选择黑土、潮土和红壤3种典型农田土壤,进行土壤DOM浸提试验,分析不同类型土壤DOM的数量变化,并采用紫外–可见光光度计和荧光光谱仪分析其光谱特征,以为制定合理的土壤培肥方案,提高土壤有机质和DOM含量提供理论依据。
1 材料与方法 1.1 供试土壤试验所用土样采样点概况如表 1所示。采用“S”布点法采样,每个采样点采集5个样品,土样均为0 ~ 20 cm表层土壤。土样采集后,带回实验室将较明显的植物残体捡出后,过2 mm筛,用于提取DOM,及pH、电导率和机械组成测定。部分土壤风干并研磨过0.149 mm(或100目)筛用于测定土壤有机碳(SOC)含量。
|
|
表 1 采样点和土样概况 Table 1 Information of sampling sites and soil samples |
土壤电导率使用DDS-11A电导仪测定(土水质量比1∶5),pH使用雷磁PHS-3D型pH计测定,有机碳(SOC)采用重铬酸钾外加热法测定,机械组成采用吸管法测定。土壤的基本理化性质如表 2所示。
|
|
表 2 供试土壤的基本理化性质 Table 2 Basic physiochemical properties of tested soils |
土壤DOM采用水浸提法,取5.00 g土样于100 ml离心管中,加入去离子水50 ml(土水质量比1∶10),在水平恒温振荡机上振荡120 min(25℃,200 r/min)后,4 000 r/min离心10 min,上清液过0.45 μm滤膜,滤液中有机质即为DOM[12]。提取的DOM样品保存在4℃冰箱中,3 d之内进行紫外–可见光谱和荧光光谱分析。采用Eelementar Vario TOC有机碳分析仪测定DOM样品DOC含量(cDOC)。
使用紫外–可见分光光度计(JINGHUA UV- 1800PC) 测定样品紫外–可见光吸光度值。通过检测待测液在波长254 nm处的吸光度值(SUVA254)来计算其芳香化系数,计算公式:SUVA254=(A254/cDOC)× 100 [13]。
荧光光谱使用HORIBA FluoroMaxⓇ-4仪器进行测定,激发和发射光栅狭缝宽度都为10 nm,扫描速度1 200 nm/min,激发波长254 nm,荧光发射光谱波长范围300 ~ 480 nm,荧光同步光谱波长范围250 ~ 500 nm。荧光发射光谱435~480nm区域与300~345nm区域的峰面积比值被称为荧光发射光谱腐殖化指数(HIXem)。荧光同步光谱波长460 nm与345 nm处荧光强度的比值为荧光同步光谱腐殖化指数(HIXsyn)[14];荧光效率(Feff)计算方法为样品荧光发射光谱的最大荧光强度(Fmax)与其SUVA254的比值,为提高灵敏度,荧光光谱测定前使用2 mol/L盐酸将所有待测液的pH调为2[12, 14]。
1.3 数据处理与分析用Excel 2019进行试验数据汇总和表格制作,用Origin 2018进行图形制作。采用SPSS 18.0软件中单因素方差分析方法进行3种土壤DOM数量和光谱参数的差异分析,用LSD多重比较对不同土壤进行差异显著性检验,显著性水平设定为P < 0.05。
2 结果与讨论 2.1 三种土壤中SOC和DOC的数量特征土壤DOM含量通常采用DOC含量来表示。由表 3可知,3种土壤SOC含量变化范围为2.64 ~ 20.24 g/kg,不同类型土壤间存在显著差异(P < 0.05)。土壤中DOC含量与SOC含量的变化规律一致,均为黑土 > 红壤 > 潮土。
|
|
表 3 三种土壤的有机质含量和组分特征 Table 3 Contents of soil organic matter and its components |
SOC/DOC值可以表示土壤DOM的提取比例。本研究中,SOC/DOC值大小为红壤 > 黑土 > 潮土(P < 0.05),红壤SOC/DOC值为145.58,黑土和潮土的SOC/DOC值为119.33、82.39,说明潮土DOM的提取比例高于黑土和红壤。红壤比黑土的黏粒含量高30 g/kg,但SOC/DOC值却显著高于黑土(表 3),这表明土壤类型会影响土壤DOM的提取比例[15],可能是红壤含有更多的铁铝氧化物,具有更多吸附位点,对DOM吸附固定能力更强[16]。由此可以说明,土壤类型及黏粒含量明显影响土壤中DOM的提取比例。
2.2 三种土壤中DOM的光谱特征不同类型土壤中DOM的分子量大小不同,其组成结构也存在差异。紫外–可见光谱和荧光光谱技术是解析有机质结构特征的重要手段。其中,A254值可以表征DOM的芳香化程度,A254值越大,芳香性结构物质含量越高[17]。E4/E6值可以表征腐殖质的腐殖化程度,E4/E6比值越大,腐殖化程度越低。SUVA254值可表征DOM芳香性构化程度,其值越大,芳香性构化程度越高,分子量越大[18]。本研究中,红壤的A254、SUVA254值最低,这表明红壤DOM中芳香性结构物质含量和芳香性构化程度均比黑土和潮土DOM低。这可能是因为红壤含有更多的铁铝氧化物,对芳香性结构物质的吸附能力比黑土和潮土强[16],导致DOM溶液中芳香性结构物质含量较少。
此外,pH也是影响DOM中芳香性结构物质含量的因素之一。本研究中3种土壤pH大小为:潮土 > 黑土 > 红壤,SUVA254值大小为:潮土 > 黑土 > 红壤,pH越高,土壤DOM中芳香性构化程度高的物质含量越高。有研究[16]表明,土壤吸附试验中吸附平衡液的SUVA254值与pH呈显著正相关。这表明土壤pH越高,土壤颗粒对DOM中芳香性构化程度低的物质的吸附能力越弱,即土壤吸附的芳香性构化程度低的物质更容易解吸进入DOM溶液中。
|
|
表 4 三种土壤DOM的E4/E6值和紫外特征吸光值 Table 4 Values of E4/E6 and UV absorbances of DOM in three tested soils |
荧光指数(FI)可以表征DOM的来源。一般认为,植物来源和微生物代谢产物源的2个端源FI值分别是1.4和1.9,FI < 1.4时,DOM以植物源输入为主;FI介于1.4 ~ 1.9时,表示既有植物源又有微生物代谢产物源输入;FI > 1.9时,DOM以微生物代谢产物源为主[19]。本研究中,红壤FI值为1.70(表 5),介于1.4 ~ 1.9,表明红壤DOM既有植物源也有微生物代谢产物源;黑土和潮土DOM的FI值均小于1.4(表 5),说明黑土和潮土DOM主要为植物源,微生物源贡献较小。
|
|
表 5 三种土壤DOM的荧光光谱参数 Table 5 Fluorescence parameters of DOM in three tested soils |
此外,荧光发射光谱给出的腐殖化指数(HIXem) 可以用来表征DOM的腐殖化程度,高HIXem值往往意味着含有更多的微生物代谢产物[20]。本研究中,红壤DOM的腐殖化指数(HIXem、HIXsyn)比黑土和潮土DOM高(表 5),这表明红壤DOM的腐殖化程度比黑土和潮土DOM高。这可能是因为红壤所处气候区的湿热条件有利于土壤微生物活动和有机物周转[21]。相关研究[22-23]也表明,土壤有机质在分解过程中,温度升高和土壤水分含量增加可以增强土壤微生物代谢活动,提高有机质周转次数,加速有机质的腐殖化过程。
荧光效率值(Feff)与DOM分子的结构有关,π电子共轭基团含量越多,荧光效率值越高[13]。一般情况下,绝大多数π电子共轭基团含芳环、不饱和键或杂环结构[24]。如表 5所示,红壤DOM的Feff显著高于黑土和潮土DOM,这表明红壤DOM含有更多π电子共轭基团,这些基团很可能是微生物代谢的产物(FI=1.7)[25]。
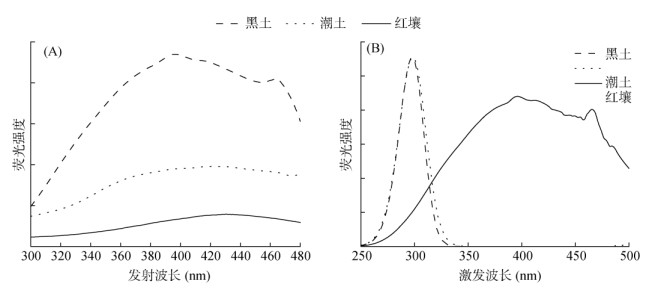
荧光发射光谱图(图 1A)显示,3种土壤的发射光谱波形相似,波峰主要集中在380 ~ 440 nm,相对峰面积大小为黑土 > 潮土 > 红壤,这与A254、E4/E6值的变化趋势一致。荧光同步光谱图(图 1B)显示,DOM的同步光谱特征峰主要有以下3类:①激发波长λex =285 ~ 290 nm,代表类蛋白质基团,如芳香氨基酸等;②λex= 349 ~ 381 nm,代表芳香性脂肪族基团;③λex =450 ~ 453 nm,代表木质素类基团[26]。本研究中,黑土和潮土的特征峰相似,只有一个特征峰(λex= 285 ~ 290 nm,代表类蛋白质基团),红壤的特征峰为λex = 390 ~ 410 nm,这说明黑土和潮土的DOM组分以含类蛋白质基团的物质为主,红壤DOM组分倾向于以含木质素类基团物质为主,可能是因为在南方土壤中,水热条件良好,类蛋白质基团物质易被降解而不易积累[21-22]。
|
图 1 三种土壤中DOM的荧光发射光谱(A)、荧光同步光谱(B) Fig. 1 Spectra of fluorescence emission(A) and synchronous(B) fluorescence of DOM in three tested soils |
综上所述,土壤中有机物的解吸和释放是土壤DOM的重要来源之一。SOC/DOC值可作为评价土壤DOM提取难易的一个参数,光谱方法可以用来解析土壤DOM的结构和来源特征[27]。本研究中,黑土DOM含量高于潮土和红壤,SOC/DOC值比潮土高,但比红壤低。黑土和潮土DOM腐殖化程度低,植物源特征强,红壤DOM腐殖化程度高,植物源特征弱,微生物源特征强。因此,就农业生产中促进土壤有机质积累,提高DOM含量措施而言,对于黑土和潮土,施用腐殖化程度低的有机肥和秸秆还田可能效果较好;而对于红壤,施用腐殖化程度高,抗分解能力强的有机肥可能更为合适。此外,今后还需要进一步研究SOC/DOC值在不同区域、不同类型土壤间的可比性,特别是深入探讨SOC/DOC值与土壤总有机碳含量、土壤矿物类型及土壤黏粒含量的关系。
3 结论本研究对3种不同类型土壤中DOM的数量和光谱特征进行研究,得出以下结论:不同类型土壤DOM的提取比例不同,红壤的SOC/DOC值大于黑土和潮土,红壤DOM的提取比例比黑土和潮土低;不同类型土壤的DOM结构特征不同,红壤DOM腐殖化程度比黑土和潮土高,但芳香性物质含量和芳香性构化程度比黑土和潮土低;红壤DOM成分主要是相对分子质量较大的木质素类基团物质,黑土和潮土DOM主要是含类蛋白质基团的芳香性结构物质;潮土DOM的芳香性结构物质含量低于黑土,但芳香性构化程度高于黑土和红壤。
| [1] |
Kalbitz K, Solinger S, Park J H, et al. Controls on the dynamics of dissolved organic matter in soils: A review[J]. Soil Science, 2000, 165(4): 277-304 DOI:10.1097/00010694-200004000-00001 (  0) 0) |
| [2] |
侯翠翠, 宋长春, 李英臣, 等. 不同水分条件下小叶章湿地表土有机碳及活性有机碳组分季节动态[J]. 环境科学, 2011, 32(1): 290-297 (  0) 0) |
| [3] |
郭剑芬, 杨玉盛, 陈光水, 等. 不同营林措施对森林土壤DOM的影响研究进展[J]. 福建师范大学学报(自然科学版), 2008, 24(4): 102-108 (  0) 0) |
| [4] |
McDowell W H. Dissolved organic matter in soils-future directions and unanswered questions[J]. Geoderma, 2003, 113(3-4): 179-186 DOI:10.1016/S0016-7061(02)00360-9 (  0) 0) |
| [5] |
黄泽春, 陈同斌, 雷梅. 陆地生态系统中水溶性有机质的环境效应[J]. 生态学报, 2002, 22(2): 259-269 (  0) 0) |
| [6] |
Chefetz B, Hader Y, Chen Y. Dissolved organic carbon fractions formed during composting of municipal solid waste: properties and significance[J]. Acta Hydrochimica et Hydrobiologica, 1998, 26(3): 172-179 DOI:10.1002/(SICI)1521-401X(199805)26:3<172::AID-AHEH172>3.0.CO;2-5 (  0) 0) |
| [7] |
周江敏, 代静玉, 潘根兴. 应用光谱分析技术研究土壤水溶性有机质的分组及其结构特征[J]. 光谱学与光谱分析, 2004, 24(9): 1060-1065 (  0) 0) |
| [8] |
谢军, 赵亚南, 陈轩敬, 等. 长期不同施肥对土壤溶解性有机质含量及其结构特征的影响[J]. 光谱学与光谱分析, 2018, 38(7): 2250-2255 (  0) 0) |
| [9] |
周石磊, 张艺冉, 黄廷林, 等. 基于UV-vis及EEMs解析周村水库夏秋季降雨不同相对分子质量DOM的光谱特征及来源[J]. 环境科学, 2019, 40(1): 172-184 (  0) 0) |
| [10] |
Lu Y Y, Shan G C, Huang J H, et al. Insights into characteristics of Dissolved organic matter fractions in Co-composted dairy manure and Chinese herbal residues[J]. Waste and Biomass Valorization, 2018, 9(5): 777-782 DOI:10.1007/s12649-017-9842-z (  0) 0) |
| [11] |
李帅东, 张明礼, 杨浩, 等. 昆明松华坝库区表层土壤溶解性有机质(DOM)的光谱特性[J]. 光谱学与光谱分析, 2017, 37(4): 1183-1188 (  0) 0) |
| [12] |
王玉涛, 石辉, 刘雄飞, 等. 黄土丘陵区不同植被下土壤可溶性有机物的荧光特征研究[J]. 植物营养与肥料学报, 2016, 22(1): 171-179 (  0) 0) |
| [13] |
靳世蕊. 利用方式对土壤水溶性有机物紫外光谱特性影响评价[D]. 哈尔滨: 东北农业大学, 2014.
(  0) 0) |
| [14] |
刘翥, 杨玉盛, 朱锦懋, 等. 中亚热带2种经济林土壤可溶性有机质数量与光谱学特征比较[J]. 水土保持学报, 2014, 28(5): 170-175 (  0) 0) |
| [15] |
Seifert A G, Roth V N, Dittmar T, et al. Comparing molecular composition of dissolved organic matter in soil and stream water: Influence of land use and chemical characteristics[J]. The Science of the Total Environment, 2016, 571: 142-152 DOI:10.1016/j.scitotenv.2016.07.033 (  0) 0) |
| [16] |
徐基胜, 赵炳梓. 可溶性有机碳在典型土壤上的吸附行为及机理[J]. 土壤, 2017, 49(2): 314-320 (  0) 0) |
| [17] |
方芳, 刘国强, 郭劲松, 等. 渗滤液中DOM的表征及特性研究[J]. 环境科学, 2009, 30(3): 834-839 (  0) 0) |
| [18] |
胡春明, 张远, 于涛, 等. 太湖典型湖区水体溶解有机质的光谱学特征[J]. 光谱学与光谱分析, 2011, 31(11): 3022-3025 (  0) 0) |
| [19] |
元晓春, 陈岳民, 袁硕, 等. 氮沉降对杉木人工幼林土壤溶液可溶性有机物质浓度及光谱学特征的影响[J]. 应用生态学报, 2017, 28(1): 1-11 (  0) 0) |
| [20] |
Miano T M, Senesi N. Synchronous excitation fluorescence spectroscopy applied to soil humic substances chemistry[J]. Science of the Total Environment, 1992, 117/118: 41-51 DOI:10.1016/0048-9697(92)90071-Y (  0) 0) |
| [21] |
Marschner B, Kalbitz K. Controls of bioavailability and biodegradability of Dissolved organic matter in soils[J]. Geoderma, 2003, 113(3/4): 211-235 (  0) 0) |
| [22] |
汪景宽, 徐英德, 丁凡, 等. 植物残体向土壤有机质转化过程及其稳定机制的研究进展[J]. 土壤学报, 2019, 56(3): 528-540 (  0) 0) |
| [23] |
陈晓芬, 吴萌, 江春玉, 等. 不同培养温度下长期施肥红壤水稻土有机碳矿化特征研究[J]. 土壤, 2019, 51(5): 864-870 (  0) 0) |
| [24] |
高颖, 鲍勇, 胡伟芳, 等. 亚热带地区3种典型林分土壤DOM数量及光谱特征[J]. 亚热带资源与环境学报, 2018, 13(1): 26-35 (  0) 0) |
| [25] |
董珊珊, 窦森, 邵满娇, 等. 秸秆深还不同年限对黑土腐殖质组成和胡敏酸结构特征的影响[J]. 土壤学报, 2017, 54(1): 150-159 (  0) 0) |
| [26] |
马莹玲, 邢帅虎, 朱思佳, 等. 中亚热带森林土壤淋滤液DOM浓度与光谱学特征[J]. 亚热带资源与环境学报, 2018, 13(3): 17-26 (  0) 0) |
| [27] |
郑小东, 陈香碧, 胡亚军, 等. 亚热带典型地貌下旱地和水田可溶性有机物化学组成特征[J]. 土壤, 2019, 51(6): 1114-1121 (  0) 0) |
2. Key Laboratory of Arable Land Conservation(North China), Ministry of Agriculture, Beijing 100193, China
 2021, Vol. 53
2021, Vol. 53


