2. 中国科学院大学, 北京 100049
自工业革命以来,大气CO2浓度([CO2])已由约280 μmol/mol上升到410 μmol/mol左右,预计21世纪末将达到700 μmol/mol[1]。CO2作为光合作用的底物,[CO2]升高势必会增加C3作物叶片的光合速率[2],从而促进生长,提高产量[3]。氮(N)作为植物生长过程中必需的矿质元素,参与核酸、蛋白质等物质的组成,能够通过影响植物体内的蛋白质,来影响光合作用[4]。植物从土壤中吸收的氮主要是无机态氮,包括硝态氮(NO3–-N)和铵态氮(NH4+-N)[5]。植物对无机态氮的吸收与它们各自的喜好[6]以及土壤环境中氮的可利用性有关[7]。硝态氮和铵态氮作为不同形态的氮素营养对植物的生理生化过程影响是不同的[8]。有研究发现,植物在供铵态氮条件下由于表现出较高的核酮糖-1, 5-二磷酸羧化酶(Rubisco)含量和活性、1, 5-二磷酸核酮糖(RuBP)再生速率以及较少的能量消耗,导致供铵态氮植物的光合速率高于供硝态氮植物[8]。Raab和Terry[9]的研究也发现,植物在铵态氮营养条件下有着更高的光合速率。而植物对高[CO2]的响应与氮的可利用性[10]以及氮的供给形态有关[11-12]。
水稻是世界主要粮食作物之一[13]。未来高[CO2]会显著增加水稻叶片的光合作用,从而增加其生长和产量[14]。然而,由于水稻田长期处于淹水状态,使得稻田土壤中的无机氮以铵态氮为主;但在水稻实际生产中常用的烤田措施,又会使稻田土壤无机氮在特定时间以硝态氮为主。因而不同的氮素供给形态是否会影响水稻叶片光合作用对高[CO2]的响应,值得进一步研究。此外,前人研究发现,籼稻和杂交稻比粳稻更能高效地利用高[CO2],因而籼稻和杂交稻产量在高[CO2]下增加的幅度要高于粳稻[15],故不同氮素供给形态下水稻叶片光合作用对高[CO2]的响应是否在品种间存在差异也需要进行研究。因此,本研究利用人工气候生长箱精准控制大气[CO2],以粳稻(武运粳23和淮稻5号)、籼稻(扬稻6号)和杂交稻(Y-两优6号)为试验材料,研究不同氮素供给形态下水稻叶片光合作用对高[CO2]的响应,以期为未来高[CO2]下水稻高效生长的肥料管理策略提供理论依据。
1 材料与方法 1.1 供试水稻品种供试水稻(Oryza sativa L)为:武运粳23号(WYJ)、淮稻5号(HD)、扬稻6号(YD)和Y-两优6号(Y-LY),其中WYJ和HD为粳稻品种,YD为籼稻品种,Y-LY为杂交稻品种。
1.2 试验设计试验分别设计两种氮素形态和两种[CO2]处理。供氮形态分别为1 mmol/L NH4+-N((NH4)2SO4))和1 mmol/L NO3–-N(KNO3),分别以NH4+、NO3–表示。此外,添加0.59 g/L的双氰胺(DCD)作为硝化抑制剂,5 mmol/L MES作为pH缓冲剂。[CO2]处理分别为大气[CO2] (400 μmol/mol)处理、高[CO2](600 μmol/mol)处理。本试验共4个处理,即NH4++大气[CO2]、NH4++高[CO2]、NO3–+大气[CO2]、NO3–+高[CO2]。
水稻种子经10% H2O2消毒30 min后,用蒸馏水清洗,清洗后均匀地铺于育秧盘中,使其在34℃的恒温避光条件下露芽,露芽后的种子接着在0.5 mmol/L CaCl2溶液中暗培养3 d后使水稻幼苗在改进的木村B完全营养液[16]中培养,调节营养液pH为5.5左右,并将水稻幼苗放置在生长箱中。改进的木村B完全营养液配方为:0.25 mmol/L(NH4)2SO4,0.5 mmol/L KNO3,0.18 mmol/L NaH2PO4·2H2O,0.18 mmol/L KCl,0.36 mmol/L CaCl2·2H2O,0.6 mmol/LMgSO4·7H2O,9 μmol/L MnCl2·4H2O,0.1 μmol/L (NH4)2MoO4,10 μmol/L H3BO3,0.7 μmol/L ZnSO4·7H2O,0.3 μmol/L CuSO4·5H2O,20 μmol/L FeSO4·7H2O-EDTA。生长箱光周期设置为14 h/10 h(白天/夜晚),相对湿度为70%,昼夜温度分别为30℃和22℃,光合有效辐射(PAR)为800 μmol/(m2·s)。7 d后选取长势一致的幼苗移栽至不透光的容器中进行氮素形态处理和[CO2]处理,NO3–、NH4+处理的营养液组成见表 1。每个处理重复4次,营养液每3 d更换1次,待处理28 d后,对水稻叶片进行光合测定。
|
|
表 1 不同氮素供给形态下营养液中大量和微量元素含量 Table 1 Macroelement and microelement contents in nutrient solutions under different N supply forms |
叶绿素色度比值:采用叶绿素仪(型号SPAD-502)测定新展开完全叶SPAD值,每个重复测定1片叶,每片叶测定8次,取平均值。
叶片光合作用测定:采用Li-Cor6800便携式光合系统分析仪测定水稻新展开完全叶的净光合速率(Pn)、胞间CO2浓度(Ci)、气孔导度(gs)和蒸腾速率(Tr),按照公式计算水分利用效率(WUE):WUE=Pn/Tr。测定时大气[CO2]和高[CO2]所选的参比CO2浓度分别是400和600 μmol/mol,光强设定为1 500 μmol/(m2·s),流速设定为500 m/s,叶温设定为30℃,相对湿度设定在50% ~ 60%。每一叶片测定3次取平均值,每个处理测定4次。
1.4 数据处理利用SPSS Statistics 23进行数据分析,Origin 2018作图,采用最小显著差异法(LSD)进行处理间的差异显著性分析。
2 结果与分析 2.1 高[CO2]对不同氮素供给形态下水稻叶片SPAD值的影响由图 1可知,无论在何种氮素供给形态下,高[CO2]对WYJ、HD和Y-LY叶片的SPAD值都无显著影响;高[CO2]虽然显著降低了NH4+处理下YD叶片的SPAD值,但降幅仅3.7%。因而,总体而言,高[CO2]对水稻叶片SPAD值影响不大。

|
(图心图 6中数据为平均值±标准差;*、**和***分别表示同一水稻品种不同CO2处理间差异在P < 0.05、P < 0.01、P < 0.001水平显著) 图 1 高[CO2]对不同氮素供给形态下水稻叶片SPAD值的影响 Fig. 1 Effects of elevated [CO2] on SPAD values of rice leaves under different N supply forms |
由图 2可知,高[CO2]促进了NO3–处理下水稻叶片Pn,使NO3–处理下WYJ、YD和Y-LY叶片Pn分别增加24.1%、43.2% 和30.9%,差异达到显著水平;但对HD叶片Pn无显著影响。相比NO3–处理,高[CO2]对NH4+处理水稻叶片Pn影响不大,仅显著地促进了WYJ叶片Pn,使其增加22.2%;对其他水稻叶片无显著影响。相比NO3–处理,NH4+处理水稻叶片Pn高于NO3–处理。[CO2]和氮素形态对Pn有着显著的交互作用,品种、[CO2]和氮素形态对Pn也有显著的交互作用(表 2)。

|
图 2 高[CO2]对不同氮素供给形态下水稻叶片Pn的影响 Fig. 2 Effects of elevated [CO2] on Pnof rice leaves under different N supply forms |
|
|
表 2 高[CO2]、氮素供给形态及品种对水稻叶片光合参数影响的方差分析 Table 2 Variance analysis of effects of elevated [CO2], N supply forms and varieties on photosynthetic parameters of rice leaves |
由图 3可知,高[CO2]极显著地提高了各氮素供给形态下水稻叶片Ci,在NO3–处理下,WYJ、HD、YD和Y-LY分别增加45.5%、45.3%、42.1% 和39.1%;在NH4+处理下WYJ、HD、YD和Y-LY分别增加57.8%、44.8%、65% 和37.7%。而且,从图 3可知,NO3–处理下的水稻叶片Ci值普遍高于NH4+处理。

|
图 3 高[CO2]对不同氮素供给形态下水稻叶片Ci的影响 Fig. 3 Effects of elevated [CO2] on Ciof rice leaves under different N supply forms |
由图 4可知,高[CO2]不同程度地降低了水稻叶片gs,在NO3–处理下,WYJ、HD、YD和Y-LY叶片的gs分别降低26%、37.6%、21.7% 和25.9%,差异达到显著水平;在NH4+处理下,HD、YD和Y-LY叶片的gs分别降低41.5%、25.1% 和45.4%,差异达到显著水平,但对WYJ降幅不显著。由此可知,粳稻(WYJ和HD)叶片gs在NO3–处理下对高[CO2]的响应大于籼稻(YD),杂交稻(Y-LY)叶片gs在NH4+处理下对高[CO2]的响应大于粳稻和籼稻。

|
图 4 高[CO2]对不同氮素供给形态下水稻叶片gs的影响 Fig. 4 Effects of elevated [CO2] on gsof rice leaves under different N supply forms |
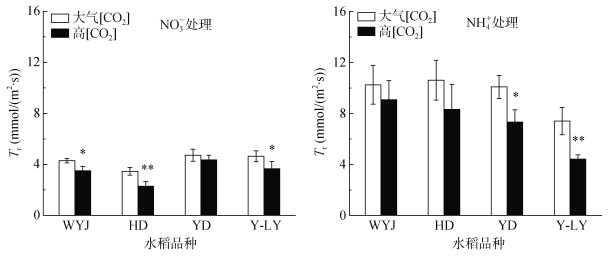
由图 5可知,高[CO2]会降低水稻叶片蒸腾速率Tr,使NO3–处理下WYJ、HD和Y-LY叶片的Tr分别降低18.4%、33.6% 和21.1%,差异达到显著水平,但对YD降幅不显著;使NH4+处理下YD和Y-LY叶片的Tr降低27.3% 和40.4%,差异达到显著水平,但对WYJ和HD降幅不显著。可见,粳稻叶片Tr在NO3–处理下对高[CO2]的响应大于籼稻,而杂交稻叶片Tr在NH4+处理下对高[CO2]的响应大于粳稻和籼稻。
|
图 5 高[CO2]对不同氮素供给形态下水稻叶片Tr的影响 Fig. 5 Effects of elevated CO2on Trof rice leaves under different N supply forms |
由图 6可知,无论是NO3–处理还是NH4+处理,高[CO2]都能促进水稻叶片WUE。在NO3–处理下,高[CO2]使WYJ、HD、YD和Y-LY叶片的WUE分别增加52.2%、55.5%、54.7% 和66.6%,差异达到显著水平。在NH4+处理下,高[CO2]使WYJ、YD和Y-LY叶片的WUE分别增加37.6%、28.7% 和70.8%,差异达到显著水平,但对HD的增幅无显著影响。因而,相比NH4+处理下,高[CO2]更能促进NO3–处理下水稻叶片WUE。

|
图 6 高[CO2]对不同氮素供给形态下水稻叶片WUE的影响 Fig. 6 Effects of elevated [CO2] on WUE of rice leaves under different N supply forms |
本研究表明,[CO2]及氮素供给形态对水稻叶片Pn会产生显著的交互作用,其具体表现为高[CO2]显著或极显著地增加了NO3–处理下的WYJ、YD和Y-LY水稻叶片的Pn,增幅为24% ~ 43%;但在NH4+处理下,高[CO2]对水稻叶片的Pn影响不大(图 2)。这一结果与Li等[17]的研究结果相同,但不同于Cruz等[18]的研究结果。这些研究结果表明植物叶片光合作用对高[CO2]的响应与氮素供给形态有关,但由于目前高[CO2]对不同氮素供给形态下水稻光合作用的研究还是空白,对其他植物还只是初步的研究,故水稻叶片光合作用对高[CO2]的响应为何偏向于硝态氮或铵态氮,还有待于进一步研究。另外,本研究发现,水稻品种响应差异明显,粳稻(WYJ和HD)叶片的Pn在NH4+处理下要明显高于籼稻(YD)和杂交稻(Y-LY);高[CO2]明显促进了NH4+处理下WYJ叶片的Pn,对其他水稻却无显著影响(图 2)。NH4+处理下WYJ和HD叶片的Pn明显高于YD和Y-LY可能与WYJ和HD叶片的SPAD值(图 1)比YD和Y-LY更高有关。因为SPAD值标示着叶片中叶绿素含量,能近似反映叶片中氮素积累量[19]。当叶片氮素累积量低时,叶片的Pn值也会低[20]。高[CO2]对NH4+处理下C3作物叶片Pn的影响还存在种间和种内的差异[17-18, 21],因而除WYJ外其他水稻叶片Pn在高[CO2]下无显著差异的原因还有待进一步研究。此外,与NO3–处理相比,NH4+处理下水稻叶片的Pn值更高(图 2),这与孙园园等[22]的研究结果相一致。有研究显示,NH4+处理下叶片更高的Pn值可能与Rubisco含量有关[9]。根据Raab和Terry[9]的研究,供以铵态氮营养的植物有着更高的Rubisco含量;由于Rubisco含量会影响植物的光合作用,因而,在NH4+处理下高含量的Rubisco会导致叶片的Pn值更高。植物叶片的光合作用除了受Rubisco含量影响外,还可能受气孔导度的影响[23]。Farquhar和Sharkey[24]认为,当Pn、gs和Ci值同时下降时,Pn的下降可认为与gs有关。而本研究发现,虽然水稻叶片在NH4+处理下有着更高的Pn和gs,但水稻叶片在NO3–处理下的Ci值普遍高于NH4+处理,因而推测NH4+处理下水稻叶片有着更高的Pn与gs无关。这一点不同于Raab和Terry[9]的研究结果,其可能是研究的植物种类以及环境条件存在差异所致。
气孔是植物与外界环境进行气体交换的门户,其开闭活动控制着CO2和水汽进出叶片,从而影响叶片的光合作用和蒸腾作用[25]。本研究结果表明,高[CO2]显著降低水稻叶片的gs,使NO3–处理下水稻叶片的gs降低22% ~ 38%,使NH4+处理下水稻叶片的gs降低12% ~ 45%。有研究显示,叶片气孔导度的降低可能与植物为保持细胞间分压的稳定性有关[26];植物在高[CO2]条件下通过调节气孔开闭程度来降低胞间[CO2],由于气孔对胞间[CO2]很敏感,胞间[CO2]过高会引起气孔的关闭,进而降低气孔导度[26],这一结果与邵在胜等[27]和周宁等[28]的研究结果相一致。另外,相对NO3–处理,NH4+处理条件下水稻叶片gs值更高,究其原因可能与NO3–处理下营养液pH增加有关。因为增加的pH可能会通过改变保卫细胞膜离子通量而影响保卫细胞的活性以及气孔孔径,导致气孔关闭,气孔导度降低[29]。并且,本研究发现,不同氮素供给形态下水稻叶片的gs和Tr对高[CO2]的响应在品种间存在很大的差异,具体表现为:NO3–处理下粳稻叶片的gs和Tr对高[CO2]的响应大于籼稻,但是NH4+处理下杂交稻叶片的gs和Tr对高[CO2]的响应大于粳稻和籼稻。然而,不同氮素供给形态下水稻叶片的gs和Tr对高[CO2]的响应在品种间差异的原因尚未明确,有待进一步的研究。此外,本研究还发现,与叶片gs的结果类似,高[CO2]会降低水稻叶片的Tr,使NO3–处理下水稻叶片的Tr降低8% ~ 34%,NH4+处理下降低11% ~ 40%。这是因为高[CO2]会导致叶片gs下降,气孔阻力增加,从而减少了叶片内水分的逸出量,使蒸腾作用也相应减弱[3],这与Meng等[30]的研究结果一致。
本研究表明,高[CO2]显著增加了水稻叶片WUE,这与Pn和gs有关。因为高[CO2]会增加水稻叶片的Pn,降低叶片的gs,引起Tr下降;又因WUE为Pn与Tr的比值,因而增加的Pn和降低的Tr会共同导致水稻WUE的增加,这与Seibt等[31]利用同位素技术研究高[CO2]对植物WUE影响的结果相一致。此外,本研究结果显示,水稻叶片的WUE在NO3–处理下对高[CO2]的响应要高于NH4+处理,其原因可能是在NO3–处理下高[CO2]对Pn的促进作用要高于NH4+处理。Li等[17]在研究高[CO2]对不同NH4+/ NO3–比率下植物WUE影响时也发现,无论在单位叶片水平上还是单位植株水平上,植物WUE在NO3–处理下(NH4+/ NO3–为0/100)对高[CO2]的响应要高于NH4+处理(NH4+/ NO3–为100/0),并且这种更高的响应与其在NO3–处理下有着更高的Pn有关。此外,本研究还发现,水稻品种响应存在差异;在NH4+处理下杂交稻叶片的WUE对高[CO2]的响应要明显高于粳稻和籼稻,这与上述原因类似,主要是因为杂交稻的Tr对高[CO2]的响应要高于粳稻和籼稻。通常,植物WUE越高,抵御干旱胁迫的能力越强,越有利于适应干旱胁迫的环境[32]。因而,在未来高[CO2]条件下,NO3–处理的水稻以及NH4+处理的杂交稻有更高的WUE,表明其有更强的抵御干旱胁迫的能力。
4 结论本研究利用人工气候箱首次探究不同氮素供给形态下水稻叶片光合作用、对高[CO2]的响应,结果表明,水稻叶片的光合作用和水分利用效率对高[CO2]的响应与氮素供给形态有关,且不同氮素供给形态下水稻叶片的气孔导度和蒸腾速率对高[CO2]的响应在不同基因型品种间存在很大的差异。本试验说明了合理选择不同基因型的水稻品种来高效利用不同氮素形态及抵御未来可能的干旱胁迫的必要性。
| [1] |
Change Intergovernmental Panel on Climate. Evaluation of climate models pages 801 to 866[M]//Climate Change 2013-The Physical Science Basis. Cambridge: Cambridge University Press, 2013: 801-866.
(  0) 0) |
| [2] |
Wang J Y, Wang C, Chen N N, et al. Response of rice production to elevated[CO2] and its interaction with rising temperature or nitrogen supply: a meta-analysis[J]. Climatic Change, 2015, 130(4): 529-543 DOI:10.1007/s10584-015-1374-6 (  0) 0) |
| [3] |
(  0) 0) |
| [4] |
Evans J R. Photosynthesis and nitrogen relationships in leaves of C3 plants[J]. Oecologia, 1989, 78(1): 9-19 DOI:10.1007/BF00377192 (  0) 0) |
| [5] |
Epstein E, Bloom A J. Mineral nutrition of plants: principles and perspectives[M].
Sinauer Associates, Sunderland, MA, 2005
(  0) 0) |
| [6] |
Zhang J B, Wang J, Müller C, et al. Ecological and practical significances of crop species preferential N uptake matching with soil N dynamics[J]. Soil Biology and Biochemistry, 2016, 103: 63-70 DOI:10.1016/j.soilbio.2016.08.009 (  0) 0) |
| [7] |
Hasegawa S, MacDonald C A, Power S A. Elevated carbon dioxide increases soil nitrogen and phosphorus availability in a phosphorus-limited Eucalyptus woodland[J]. Global Change Biology, 2016, 22(4): 1628-1643 DOI:10.1111/gcb.13147 (  0) 0) |
| [8] |
Guo S, Zhou Y, Shen Q, et al. Effect of ammonium and nitrate nutrition on some physiological processes in higher plants-growth, photosynthesis, photorespiration, and water relations[J]. Plant Biology (Stuttgart, Germany), 2007, 9(1): 21-29 DOI:10.1055/s-2006-924541 (  0) 0) |
| [9] |
Raab T K, Terry N. Nitrogen source regulation of growth and photosynthesis in beta vulgaris L[J]. Plant Physiology, 1994, 105(4): 1159-1166 DOI:10.1104/pp.105.4.1159 (  0) 0) |
| [10] |
吴晶晶, 施卫明. 高低应答CO2水稻品种苗期根系对高碳环境的响应[J]. 土壤, 2019, 51(6): 1057-1064 (  0) 0) |
| [11] |
Bloom A J. The increasing importance of distinguishing among plant nitrogen sources[J]. Current Opinion in Plant Biology, 2015, 25: 10-16 DOI:10.1016/j.pbi.2015.03.002 (  0) 0) |
| [12] |
Asensio J S R, Rachmilevitch S, Bloom A J. Responses of Arabidopsis and wheat to rising CO2 depend on nitrogen source and nighttime CO2 levels[J]. Plant Physiology, 2015, 168(1): 156-163 DOI:10.1104/pp.15.00110 (  0) 0) |
| [13] |
R RI. 1993-1995 IRRI rice almanac[M].
International Rice Research Institute, Manila, 1993
(  0) 0) |
| [14] |
景立权, 赵新勇, 周宁, 等. 高CO2浓度对杂交水稻光合作用日变化的影响——FACE研究[J]. 生态学报, 2017, 37(6): 2033-2044 (  0) 0) |
| [15] |
Zhu C W, Xu X, Wang D, et al. An indica rice genotype showed a similar yield enhancement to that of hybrid rice under free air carbon dioxide enrichment[J]. Scientific Reports, 2015, 5: 12719 DOI:10.1038/srep12719 (  0) 0) |
| [16] |
Cao X C, Zhong C, Zhu C Q, et al. Ammonium uptake and metabolism alleviate PEG-induced water stress in rice seedlings[J]. Plant Physiology and Biochemistry, 2018, 132: 128-137 DOI:10.1016/j.plaphy.2018.08.041 (  0) 0) |
| [17] |
Li J, Zhou J M, Duan Z Q. Effects of elevated CO2 concentration on growth and water usage of tomato seedlings under different ammonium/nitrate ratios[J]. Journal of Environmental Sciences, 2007, 19(9): 1100-1107 DOI:10.1016/S1001-0742(07)60179-X (  0) 0) |
| [18] |
Cruz J L, Alves A A C, LeCain D R, et al. Effect of elevated CO2 concentration and nitrate: ammonium ratios on gas exchange and growth of cassava (Manihot esculenta Crantz)[J]. Plant and Soil, 2014, 374(1/2): 33-43 (  0) 0) |
| [19] |
Peng S B, Laza M R C, Garcia F V, et al. Chlorophyll meter estimates leaf area-based nitrogen concentration of rice[J]. Communications in Soil Science and Plant Analysis, 1995, 26(5/6): 927-935 (  0) 0) |
| [20] |
Nakano H, Makino A, Mae T. The effect of elevated partial pressures of CO2 on the relationship between photosynthetic capacity and N content in rice leaves[J]. Plant Physiology, 1997, 115(1): 191-198 DOI:10.1104/pp.115.1.191 (  0) 0) |
| [21] |
Vega-Mas I, Marino D, Sánchez-Zabala J, et al. CO2 enrichment modulates ammonium nutrition in tomato adjusting carbon and nitrogen metabolism to stomatal conductance[J]. Plant Science, 2015, 241: 32-44 DOI:10.1016/j.plantsci.2015.09.021 (  0) 0) |
| [22] |
孙园园, 孙永健, 秦俭, 等. 适度水分胁迫下增硝对不同基因型水稻苗期生长及生理特性的影响[J]. 干旱地区农业研究, 2013, 31(4): 144-151 DOI:10.3969/j.issn.1000-7601.2013.04.027 (  0) 0) |
| [23] |
Sharkey T D. O(2)-insensitive photosynthesis in c(3) plants: Its occurrence and a possible explanation[J]. Plant Physiology, 1985, 78(1): 71-75 DOI:10.1104/pp.78.1.71 (  0) 0) |
| [24] |
Farquhar G D, Sharkey T D. Stomatal conductance and photosynthesis[J]. Annual Review of Plant Physiology, 1982, 33(1): 317-345 DOI:10.1146/annurev.pp.33.060182.001533 (  0) 0) |
| [25] |
Hetherington A M, Woodward F I. The role of stomata in sensing and driving environmental change[J]. Nature, 2003, 424(6951): 901-908 DOI:10.1038/nature01843 (  0) 0) |
| [26] |
Bunce J A. Responses of stomatal conductance to light, humidity and temperature in winter wheat and barley grown at three concentrations of carbon dioxide in the field[J]. Global Change Biology, 2000, 6(4): 371-382 DOI:10.1046/j.1365-2486.2000.00314.x (  0) 0) |
| [27] |
邵在胜, 赵轶鹏, 宋琪玲, 等. 大气CO2和O3浓度升高对水稻'汕优63'叶片光合作用的影响[J]. 中国生态农业学报, 2014, 22(4): 422-429 (  0) 0) |
| [28] |
周宁, 景立权, 朱建国, 等. 杂交水稻光合和荧光特性对高CO2浓度的动态响应[J]. 核农学报, 2019, 33(4): 772-780 (  0) 0) |
| [29] |
Wilkinson S. pH as a stress signal[J]. Plant Growth Regulation, 1999, 29(1/2): 87-99 DOI:10.1023/A:1006203715640 (  0) 0) |
| [30] |
Meng F C, Zhang J H, Yao F M, et al. Interactive effects of elevated CO2 concentration and irrigation on photosynthetic parameters and yield of maize in Northeast China[J]. PLoS One, 2014, 9(5): e98318 DOI:10.1371/journal.pone.0098318 (  0) 0) |
| [31] |
Seibt U, Rajabi A, Griffiths H, et al. Carbon isotopes and water use efficiency: Sense and sensitivity[J]. Oecologia, 2008, 155(3): 441-454 DOI:10.1007/s00442-007-0932-7 (  0) 0) |
| [32] |
Jensen B, Christensen B T. Interactions between elevated CO2 and added N: effects on water use, biomass, and soil 15N uptake in wheat[J]. Acta Agriculturae Scandinavica, Section B—Soil & Plant Science, 2004, 54(3): 175-184 (  0) 0) |
2. University of Chinese Academy of Sciences, Beijing 100049, China
 2021, Vol. 53
2021, Vol. 53


